Глава 3 Антиаритмические препараты I класса
Блокада быстрых натриевых каналов — главное свойство, определяющее принадлежность препарата к I классу. Однако вследствие различных эффектов на натриевые и калиевые каналы препараты, относящиеся к I классу, проявляют себя не одинаково. Исходя из их натрий- и калийблокирующего действия, препараты I класса подразделяются на группы IA, IB и 1C. Основные клинические характеристики, электрофизиологические свойства и побочные эффекты антиаритмических препаратов I класса суммированы в соответствующих таблицах.
Класс IA
Антиаритмические препараты класса IA — это препараты для любых целей, потому что они имеют умеренную эффективность при лечении большинства типов тахиаритмий. К сожалению, они также умеренно эффективны в вызывании побочных эффектов, принадлежащих к обеим основным группам — воздействие на периферические органы и проаритмические эффекты.
Как показано на рис. 3.1, препараты класса IA блокируют быстрые натриевые каналы (замедляя фазу 0 потенциала действия и скорость проведения) и калиевые каналы (удлиняя потенциал действия и рефрактерность). Эти электрофизиологические эффекты проявляются как в предсердной, так и в желудочковой тканях, поэтому препараты класса IA имеют потенциальную эффективность и при предсердных, и при желудочковых тахиаритмиях. Основные клинические характеристики антиаритмических препаратов класса IA приведены в табл. 3.1, а основные электрофизиологические свойства — в табл. 3.2.
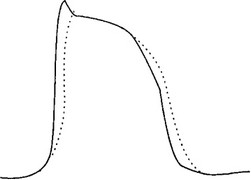
Рис. 3.1. Эффект препаратов класса IA на сердечный потенциал действия. Исходный потенциал действия изображен сплошной линией; пунктирная линия показывает действие препаратов класса IA
Хинидин
Хинидин — это D-изомер антималярийного препарата хинина, который, как было замечено еще в XVIII в., успешно применялся для лечения сердцебиений. Антиаритмический эффект самого хинидина обнаружен в начале XX в.
Клиническая фармакология
Хинидин назначают внутрь в форме одной из трех солей — сульфата, глюконата или полигалактуроната,— в зависимости от того, какую из них пациент переносит лучше. Примерно 80—90 % сульфата хинидина абсорбируется после приема внутрь; пик концентрации препарата в плазме достигается в течение 2 ч. Глюконат и полигалактуронат хинидина абсорбируются медленнее и в меньшей степени, чем сульфат. Хинидин на 80—90 % связывается с белками плазмы и имеет большой объем распределения. Концентрация препарата в 4—10 раз выше в сердце, печени и почках, чем в циркуляторном русле. Хинидин выводится в основном посредством печеночного метаболизма. Период полувыведения препарата составляет 5-8 ч, но может удлиняться у пациентов с застойной сердечной недостаточностью или у пожилых.
Клиническая фармакология препаратов класса IA
Таблица 3.1
|
|
Хинидин |
Прокаинамид |
Дизопирамид | |
|
Всасывание в ЖКТ |
80-90% |
70-90 % |
80-90% |
|
Связывание с белками |
80-90% |
Слабое (меньше при более высоких концентрациях препарата) |
Вариабельное |
|
Выведение |
Печень |
Метабол изиру- ется в печени до N-АПА; ПА и N-АПА экскре- тируются почками |
60 % — почки 40 % — печень |
|
Период полувы веден ИЯ |
5-8 ч |
3-5 ч |
8-9 ч |
|
Терапевтический уровень |
2-5 мг/л |
4-2 мг/л (ПА) 9-20 мг/л (N-АПА) |
2-5 мг/л |
|
Доза |
300-600 мг 4 раза в день (сульфат) 324-972 мг 3-4 раза в день (глюконат) |
15 мг/кг в/в, затем 1-6 мг/мин в/в; или 500-1250 мг внутрь 4 раза в день |
100-200 мг 4 раза в день |
N-АПА — N-ацетилпрокаинамид; ПА — прокаинамид; ЖКТ — желудочно-кишечный тракт; в/в — внутривенно.
Электрофизиологические свойства
Хинидин блокирует натриевые каналы и замедляет скорость деполяризации потенциала действия. Как и все препараты класса IA, хинидин связывается и разъединяется с натриевыми каналами медленнее лидокаина, но быстрее препаратов класса 1C. Поэтому выраженность его эффекта на скорость проведения занимает промежуточную позицию между препаратами групп IB и 1C. Его эффект на калиевые каналы приводит к удлинению
Таблица 3.2
Электрофизиологические эффекты препаратов класса IA
|
|
Хинидин |
Прокаинамид |
Дизопирамид |
|
Скорость проведения |
Уменьшает ++ |
Уменьшает ++ |
Уменьшает ++ |
|
Рефрактерные периоды |
Увеличивает ++ |
Увеличивает ++ |
Увеличивает ++ |
|
Автоматизм |
Подавляет + |
Подавляет + |
Подавляет I + |
|
I Следовые | деполяризации |
Может вызывать РСД |
Может вызывать РСД |
Может вызывать РСД |
|
| Эффективность |
|||
|
I ФПДП |
++ |
++ |
++ |
|
1 АВУ-риентри |
+ |
+ |
+ |
|
1 Макрориентри |
+ |
+ |
+ |
|
ЖЭС |
++ |
++ |
++ |
|
1 ЖТ/ФЖ |
++ |
++ |
++ |
АВУ — атриовентрикулярный узел; РСД — ранние следовые деполяризации; ФП — фибрилляция предсердий; ТП — трепетание предсердий; ЖЭС— желудочковая экстрасистолия; ЖГ — желудочковая тахикардия; ФЖ — фибрилляция желудочков.
потенциала действия и, соответственно, рефрактерного периода. Электрофизиологические эффекты препарата проявляются как в предсердной, так и в желудочковой тканях. Хинидин способен подавлять автоматизм в волокнах Пуркинье и, подобно всем препаратам, удлиняющим рефрактерность, — вызывать ранние следовые деполяризации (и следовательно, тахикардию типа torsades de pointes) у склонных к данной патологии пациентов.
Гемодинамические эффекты
Хинидин блокирует а-адренергические рецепторы, что иногда приводит к периферической вазодилатации и рефлекторной синусовой тахикардии. Эти эффекты обычно выражены минимально при приеме внутрь, но могут быть значительными при внутривенном введении препарата. Поэтому внутривенная форма хинидина используется очень редко. Хинидин также оказьшает ваголитическое действие, что проявляется улучшением проводимости в АВ-узле. Наличие ваголитического эффекта особенно важно при лечении фибрилляции или трепетания предсердий — увеличенное АВ-узловое проведение может привести к учащению желудочкового ритма, если только одновременно не назначены препараты, блокирующие АВ-узел. При лечении хинидином депрессия миокарда не наблюдается.
Терапевтическое применение
Хинидин умеренно эффективен как при предсердных, так и желудочковых тахиаритмиях. Примерно у 50 % пациентов, принимающих хинидин по поводу фибрилляции предсердий, сохраняется синусовый ритм более 1 года. Хинидин действует на дополнительный путь у пациентов с синдромом WPW и на быстрый путь у пациентов с АВ-узловой реципрокной тахикардией. Вот почему хинидин используется в лечении всех типов реципрокных суправентрикулярных тахиаритмий.
Препарат эффективен для подавления желудочковых экстрасистол и неустойчивой желудочковой тахикардии. Однако в силу того что хинидин (и большинство других анти- аритмических препаратов) обладает проаритмическим потенциалом, эти нарушения сердечного ритма не следует лечить, за исключением тех случаев, когда наблюдается выраженная симптоматика. По этой же причине хинидин не применяют для лечения устойчивой желудочковой тахикардии без защиты имплантируемым дефибриллятором.
Побочные реакции и взаимодействие с другими препаратами
Симптоматичные побочные эффекты наблюдаются у 30—50 % пациентов, принимающих хинидин, и в 20—30 % случаев препарат приходится отменять вследствие его токсичности. К наиболее типичным побочным эффектам относятся желудочно-кишечные расстройства, в основном диарея. Как правило, при возникновении диареи препарат отменяют, поскольку диарея в данной ситуации обычно не корригируется адекватным образом посредством приема соответствующих медикаментов, что приводит к электролитному дисбалансу, который усугубляет аритмию. Хинидин способен также вызывать головокружение, головную боль или интоксикацию (шум в ушах, нечеткость зрения, нарушения слуха). Сыпь отмечается довольно часто, не исключены выраженные реакции гиперчувствительности, например гемолитическая анемия и тром- боцитопения. Сообщалось о случаях волчанки и гепатита.
При назначении хинидина, как и всех других препаратов класса IA, основной проблемой является проаритмия. Прием любого препарата, удлиняющего потенциал действия, чреват возникновением тахикардии типа torsades de pointes у предрасположенных к ней индивидуумов, а любой препарат, изменяющий скорость проведения или рефрактерность, может усугублять реципрокные аритмии. Поэтому хинидин способен вызывать (и вызывает) желудочковые аритмии по обоим механизмам. Хинидиновые обмороки были описаны еще несколько десятилетий назад, но только относительно недавно установлено, что этот клинический синдром обусловлен желудочковыми тахиаритмиями. Индуцированные хинидином желудочковые аритмии обычно появляются рано, чаще всего через 3—5 дней после начала терапии, однако могут наблюдаться в любое время. Хотя встречаемость вызванной хинидином про- аритмии трудно определить количественно, мета-анализ в рандомизированных исследованиях при лечении хинидином фибрилляции предсердий показал, что общая смертность у пациентов, получавших хинидин, составила 2,9 %, а при приеме плацебо — 0,8 %. Увеличение смертности может быть опосредовано проаритмическим действием. Наличие таких данных настоятельно требует мониторирования сердечного ритма в течение нескольких дней после начала терапии хинидином.
Сообщается о взаимодействии хинидина с некоторыми другими препаратами. Так, хинидин потенцирует эффект ан- тихолинергических средств, варфарина и фенотиазинов. При назначении хинидина пациентам, получающим дигоксин, обычно наблюдается возрастание уровня последнего в сыворотке. Концентрация хинидина снижается под действием фенобарбитала, рифампина и фенитоина и повышается в комбинации с амиодароном.
Прокаинамид
Прокаинамид используется в клинической практике с 1951 г. Наличие двух форм прокаинамида — для внутреннего и внутривенного применения — обеспечило его широкое распространение при лечении острых и хронических тахиаритмий.
Клиническая фармакология
При внутривенном введении прокаинамид начинает действовать почти немедленно, при приеме внутрь — примерно через 1 ч. Абсорбция при пероральном употреблении составляет 70-90 %, связь с белками слабая. С мочой выводится 50 % препарата, вариабельное количество прокаинамида метаболизи- руется в печени с образованием N-ацетилпрокаинамида (N-АПА) — активного метаболита с антиаритмическими свойствами III класса. Количество N-АПА в плазме зависит от функции печени и фенотипа ацетилирования (до 50 % популяции относится к «медленным ацетиляторам», и эти индивидуумы могут быть предрасположены к индуцированной про- каинамидом волчанке). Прокаинамид и N-АПА экскретиру- ются почками. Период полувыведения составляет 3—5 ч у нормальных субъектов. В настоящее время существуют методы измерения концентрации прокаинамида и N-АПА.
Дозировка
Скорость внутривенного введения прокаинамида не должна превышать 50 мг/мин для минимизации гемодинамических побочных эффектов до общей дозы 15 мг/кг. Введение препарата замедляют при развитии гипотензии и прекращают при расширении QRS более чем на 50 % или при появлении сердечной блокады. Поддерживающая инфузия со скоростью 1—6 мг/мин используется для сохранения терапевтического уровня препарата. Внутрь обычно назначают 3—6 г/день. Сегодня выпускаются пролонгированные формы препарата, которые можно принимать 2—4 раза в день. Вследствие короткого периода полувыведения стандартной формы прокаинамида его применяют каждые 3—4 ч.
Электрофизиологические свойства
Электрофизиологические свойства прокаинамида сходны с таковыми у хинидина.
Гемодинамические эффекты
Как и хинидин, прокаинамид вызывает артериолярную вазодилатацию; этот эффект наблюдается почти исключительно при внутривенном введении. Этот побочный эффект прокаинамида путем титрования скорости инфузии контролировать легче, чем таковой у хинидина. Препарат имеет антихолинерги- ческий эффект, но менее выраженный по сравнению с таковым у хинидина. Отрицательный инотропный эффект незначительный, за исключением токсических уровней прокаинамида, особенно когда концентрация N-АПА превьппает 30 мг/л.
Терапевтическое применение
Терапевтическое использование прокаинамида аналогично таковому у хинидина. Прокаинамид применяют при всех ре- ципрокных предсердных и желудочковых тахиаритмиях; при этом его общая эффективность сходна с таковой у хинидина. Поскольку прокаинамид выпускается и в форме для относительно быстрого внутривенного введения, его часто используют при лечении фибрилляции предсердий с быстрым проведением по дополнительному пути. Прокаинамид также широко используется для острого купирования фибрилляции и трепетания предсердий и для подавления или замедления постоянной желудочковой тахикардии.
Побочные реакции и взаимодействие с другими препаратами
К побочным эффектам, которые развиваютя вскоре после начала лечения прокаинамидом, относятся гипотензия (при внутривенном введении) и желудочно-кишечные расстройства (преимущественно тошнота, рвота и диарея) у 25 % леченых пациентов. При длительной терапии прокаинамидом самой серьезной, но редкой проблемой является агранулоцитоз. От него погибают 25 % пациентов, у которых он развился. Агранулоцитоз обычно обнаруживается в первые 3 месяца лечения. Индуцированный прокаинамидом волчаночный синдром наблюдается у 20 % пациентов, получающих препарат постоянно, и нередко проявляется лихорадкой, сыпью, артритом, плевритом или перикардитом. Симптоматика обычно исчезает в течение нескольких недель после прекращения приема препарата. При приеме прокаинамида может также наблюдаться постоянная высокая температура без других проявлений волчаночного синдрома. Сообщалось также о случаях индуцированного прокаинамидом психоза.
Уровень прокаинамида может возрастать при его применении совместно с амиодароном, триметопримом и, в особенности, циметидином (но не ранитидином). Алкоголь способен снижать уровень прокаинамида за счет "увеличения печеночного метаболизма.
Предосторожности, предпринимаемые с целью избежания проаритмии, те же, что и для хинидина.
Источник: Фогорос Р.Н., «Антиаритмические средства. Изд. 2-е.» 2009
А так же в разделе «Глава 3 Антиаритмические препараты I класса »
- Дизопирамид
- Класс IB
- Класс 1C
- Флекаинид
- Этмозин(морицизин)
- Глава 4 Антиаритмические препараты II класса: 3-блокаторы
- (3 -Блокаторы в лечении аритмий Суправентрикулярные аритмии
- Желудочковые аритмии
- Побочные реакции и взаимодействие с другими препаратами
- Глава 5 Антиаритмические препараты III класса
- Амиодарон
- Электрофизиологические свойства
- Соталол
- Ибутилид
- Глава 6 Препараты IV класса: кальцийблокирующие средства
- Клиническое использование кальцийблокирующих препаратов
- Глава 7 Неклассифицированные антиаритмические средства
- Магний
- Глава 8 Исследуемые антиаритмические препараты
- Азимилид
- Дронедарон
- Тедисамил
- Глава 9 Типичные побочные эффекты антиаритмических препаратов
- Усугубление реципрокных аритмий
- Тахиаритмия torsades de pointes