АМИНОГЛИКОЗИДЫ
Это очень большой класс антибиотиков, образуемых некоторыми штаммами Streptomyces, Micromonospora и Bacillus. Все антибиотики этого класса очень близки по своим химическим и биологическим свойствам и по механизму действия. По химической структуре это аминоциклитолы (циклогексан с гидроксильными и амино- или гуанидино-заместителями) с глико- зильными заместителями по одной или нескольким гидроксильным группам. Благодаря такой структуре аминогликозиды имеют основные свойства, хорошо растворимы в воде и плохо растворимы в липидах. Отсюда ясно, почему аминогликозидные антибиотики плохо всасываются при приеме внутрь, и их транспорт через бактериальную мембрану, по-®идимому, осуществ-
Таблица 5.1..Основные амииоциклитолсодержащие антибиотики
|
Аминоциклитол |
Основные антибиотики |
|
|
Название |
Структура |
|
|
Стрептидин БлюЭнзидин 2-дезоксистре пт- амин Актин амин |
4Н^с=™- NH yl Ho\i__ \ NH НО II 1ш~с-ын2 HjN'-C=NH ^он Н nh2 Но\ \ но H3CHN L _/nHCH3 |
Стрептомицин Блюэнзомицин Неомицин Паромомицин Ливидомиции Канамицин Геитамицин Сизомицин Рибостамицин Бутирозин Тобрамицин Селдомиции Спектиномиции |
ляется за счет специфического активного механизма* а не в результате простой пассивной диффузии. Аминогликозидные антибиотики можно разделить на несколько групп в соответствии с природой аминоциклитола (табл. 5.1).
А. СТРЕПТОМИЦИН
- СВОЙСТВА
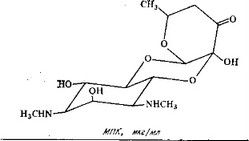
Стрептомицин (рис. 5.19) был открыт в 1944 г. благодаря тщательно спланированной программе поиска антибиотиков, активных в отношении грамотрицательных бактерий. Помимо того
что он обладает высокой активностью в отношении грамотрицательных бактерий (за исключением некоторых штаммов Proteus и некоторых малочувствительных видов Pseudomonas), стрептомицин в низких концентрациях подавляет рост Mycobacterium tuberculosis. Это первый эффективный препарат для лечения туберкулеза. Он активен также в отношении стафилококков, но
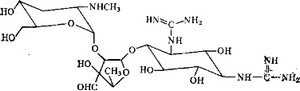
Рис. 5.19. Стрептомицин.
стрептококки к нему не очень чувствительны. Спектр действия стрептомицина представлен в гл. 2. Как отмечалось выше, он не всасывается при лриеме внутрь. При парэнтеральном введении стрептомицин выводится главным образом с мочой и поэтому, как и другие аминогликозидные антибиотики, является ценным препаратом для лечения инфекционных заболеваний мочевых путей.
Отрицательные особенности, сильно ограничивающие в настоящее время применение стрептомицина, состоят в следующем: 1) специфическая токсичность в отношении восьмого черепномозгового нерва, что приводит к нарушениям со стороны вестибулярного аппарата, а иногда к глухоте, 2) довольно высокая частота аллергических реакций и 3) высокая частота появления устойчивых мутантов и их широкое распространение.
Имеются различные классы мутантов, устойчивых к стрептомицину. Первый класс составляют мутанты с измененной ЗОБ-субчастицей рибосом, которая, как известно, является мишенью этого антибиотика. Эти мутанты не обладают устойчивостью к другим аминогликозидным антибиотикам. У другого класса мутантов устойчивость обусловлена пониженной проницаемостью клеточной мембраны для антибиотика. Эти мутанты обладают перекрестной устойчивостью к другим аминогликози- дам. Оба этих типа мутантов присутствуют в популяции восприимчивых бактерий с разной частотой и могут отбираться при лечении больных. Наиболее широко распространенный механизм устойчивости состоит, однако, в ферментативной инактивации антибиотика в результате аденилирования или фосфорилирова- ния гидроксильной группы в положении 3 метилглюкозамина и определяется трансмиссивным R-фактором.
^ МОДИФИКАЦИИ СТРУКТУРЫ
- Отщепление амидиногрупп, замещение аминогрупп и восстановительное аминирование альдегидных групп полностью инак- ивирует стрептомицин. Напротив, удаление метильной группы юетиламина, замещение одной амидиногруппы на карбамид (как у блюэнзомицина) и каталитическое восстановление альдегидной группы в гидроксильную не вызывают значительного изменения активности. В результате последней реакции получается дигидрострептомицин — соединение, которое было также выделено из культуры Streptomyces. Дигидрострептомицин одно время использовался в клинике, но позднее от него отказались, поскольку он, хотя и обладает меньшей по сравнению со стрептомицином токсичностью в отношении вестибулярного аппарата, чаще вызывает потерю слуха. Интересно отметить, что восстановление альдегидной группы снижает частоту аллергических реакций.
Б. АМИНОГЛИКОЗИДНЫЕ АНТИБИОТИКИ,
СОДЕРЖАЩИЕ 2-ДЕЗОКСИСТРЕПТАМИН
К этой группе принадлежат многие антибиотики, и часть из них используется в медицинской практике.
2-дезоксистрептамин сам по себе не обладает биологической активностью. При введении остатков различных аминосахаров в положении 6 также получаются неактивные соединения. Но если сахарные остатки ввести в положение 5 или 4, появляется слабая антимикробная активность. Достаточно высокая активность наблюдается в том случае, когда производится одновременно замещение по положениям 4 и 5 или 4 и 6.
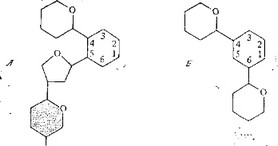
Таким образом, есть две группы 2-дезоксистрептаминсодер- жащих антибиотиков, используемых в клинике. У представителей первой группы у аминоциклитола замещены две соседние гидроксильные группы в положениях 5 и 4, у представителей второй — гидроксильные группы в положениях 4 и 6 (рис. 5.20). У антибиотиков первой группы сахарный остаток в положении 5 почти всегда представлен рибозой, и, когда к нему присоединен еще остаток аминосахара, активность увеличивается. В обеих группах на активность антибиотика влияет наличие аминогрупп у остатка сахара в положении 4. Максимальная активность имеет место 'при наличии двух аминогрупп — в положениях 2' и 6', а когда аминогруппа присутствует только в одном из этих положений, наблюдается меньшая активность. Другой особенностью структуры, существенной для сохранения активности, является наличие двух аминогрупп в положениях 1 и 3 остатка дезоксистрептамина. Обычно любые замещения этих двух групп
уменьшают активность, однако в особых случаях, описанных ниже, замещение аминогруппы при С-1 сообщает антибиотику весьма ценные свойства.
R
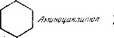 о
о
 и
и
Рис. 5.20. Схематическое представление двух классов 2-дезоксистрептамиисо- держащнх антибиотиков. А. Производное, замещенное по положениям 4 и 5. Затененный остаток сахара у рибостамицииов отсутствует. У ливидомицииов в положении R имеется еще одни остаток сахара. Б. Производное, замещенное по положениям 4 и 6. Антибиотики обоих классов различаются наличием у сахарных остатков амиио-, гидроксильных и метильиых групп.
- ПРОИЗВОДНЫЕ ДЕЗОКСИСТРЕПТАМИНА,
ЗАМЕЩЕННОГО ПО ПОЛОЖЕНИЯМ 4 И 5
Наиболее известные представители этой группы — неомици- ны, главным из которых является неомицин В, полученный в
- г. из культуры Streptomyces fradiae (рис. 5.21). Их спектр действия близок спектру действия стрептомицина, включая умеренную активность в отношении Streptococcus и Pseudomonas. Неомицин применяют только местно из-за ототоксичности и нефротоксичности. Паромомицин (аминозидин) напоминает неомицин по структуре и по биологическим свойствам. Он используется для стерилизации кишечника, поскольку не поступает в кровь при приеме внутрь. Паромомицин используют для лечения кишечных амебиазов, а также кишечных инфекций, вызываемых бактериями. Недавно в Японии были получены два антибиотика для системного применения, рибостамицин и ливидо-
мицин А. Первый из них менее активен, чем второй (поскольку у него не замещен остаток рибозы), но и менее токсичен. Ливи- домицин А имеет хороший спектр действия (он активен даже в отношении Pseudomonas) и менее токсичен, чем неомицин.
- ПРОИЗВОДНЫЕ ДЕЗОКСИСТРЕПТАМИНА,
ЗАМЕЩЕННОГО ПО ПОЛОЖЕНИЯМ 4 И 6
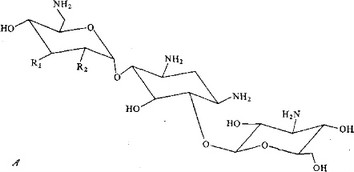
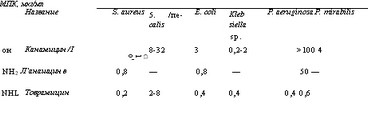
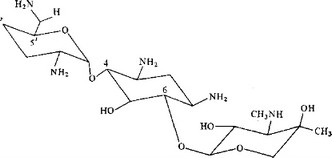
Эта группа антибиотиков (рис. 5.22) была открыта сравнительно поздно и получила широкое распространение благодаря высокой активности природных антибиотиков этого класса и некоторых недавно полученных полусинтетических производных. Первым представителем этой группы, используемым в медицине, был канамицин А, полученный в 1957 г. из культуры Streptomyces kanamyceticus вместе с компонентами В и С. Спектр его действия близок спектру действия стрептомицина, но он обладает меньшей ототоксичностью, хотя и не менее токсичен для почек, чем стрептомицин. Канамицин А используется в Японии для лечения заболеваний, вызываемых грамотрицательными бактериями, а также для лечения туберкулеза. Недавно внедрен в медицинскую практику канамицин В, или беканамицин, биологические свойства которого близки свойствам канами- цина А.
В 1963 г. из культуры Micromonospora purpurea был выделен гентамициновый комплекс, содержащий много компонентов. Название «гентамицин» обычно относят к смеси компонентов, используемой в медицине и содержащей гентамицины Ci, Cia и С2, отличающиеся друг от друга по степени метилирования 6-го углеродного атома сахарного остатка в положении 4. Гентамицин очень активен в отношении S. aureus и грамотрицательных бактерий. Очень высокая активность гентамицина в отношении Pseudomonas и некоторых видов Proteus имеет важное практическое значение, и поэтому он широко используется в клинике, но из-за высокой токсичности в отношении вестибулярного аппарата и почек его применяют только для лечения тяжелых заболеваний.
Позже в медицинскую практику были внедрены тобрамицин и сизомицин. Первый из них образуется культурой Streptomyces tenebrarius и по структуре близок канамицину (он представляет собой З'-дезоксиканамицин В), а по спектру действия — гентамицину. Тобрамицин активнее гентамицина в отношении Pseudomonas и несколько менее активен в отношении других грамотрицательных бактерий. Сизомицин образуется культурой Micromonospora inyoensis и по структуре и биологическим свойствам близок гентамицину, отличаясь более высокой активностью в отношении Pseudomonas.
.
- СВЯЗЬ МЕЖДУ СТРУКТУРОЙ И ФЕРМЕНТАТИВНОЙ
ИНАКТИВАЦИЕЙ И ПОЛУСИНТЕТИЧЕСКИЕ ПРОИЗВОДНЫЕ
Чтобы понять связь между структурой производных 2-дезок- систрептамина и их активностью в отношении определенных штаммов бактерий, необходимо исследовать механизмы устойчивости некоторых штаммов или видов бактерий к этим антибиотикам.
В отличие от стрептомицина в этом 'случае устойчивость не связана с изменением мишени — рибосомных белков, возможно,
Присоединение
нуклеотида
‘Росроримирование динение
„ а ииклеотида
//метилирование 3
nh2
Присоединение нуклеотида -"NH2"* Ацегпимиро$акие
Фосфорилирование Н2М
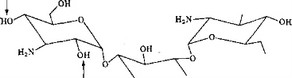
Рис. 5.23. Модификации канамицина ферментами бактерий, приводящие к потери активности.
потому, что эти антибиотики могут связываться с несколькими участками на рибосоме. Устойчивость, обусловленная непроницаемостью клеточной мембраны для антибиотиков, также встречается редко, за исключением некоторых штаммов Pseudomonas. Однако часто выделяют штаммы, образующие ферменты, которые инактивируют антибиотики. Пример такого рода представлен на рис. 5.23, где схематически показаны модификации, вызываемые бактериальными ферментами в структуре канамицина В.
Очевидно, не все эти модификации важны с практической точки зрения. Присоединение ацетильной группы к атому азота в положении 6' происходит редко и не имеет практического значения. Присоединение остатка адениловой кислоты к атому кислорода в положении 4' и фосфатной группы к атому кислорода в положении 2" осуществляется только при инфекции S. aureus, при которой аминогликозиды следует прописывать лишь в исключительных случаях. С другой стороны, .присоединение фосфатной группы к атому кислорода в положении Ъ' встречается очень часто, особенно в случае штаммов Pseudomonas. Двумя другими важными реакциями является ацетилиро- вание аминогруппы в положении 3 дезоксистрептамина и присоединение нуклеотида к кислороду в положении 2'. Отсюда по-
нятно, почему тобрамицин (З'-дезоксиканамицин В) активен в отношении Pseudomonas: этот антибиотик не несет гидроксильной группы в положении 3' и, следовательно, не может подвергаться инактивации путем фосфорилирования соответствующим ферментом Pseudomonas. Аналогично этому гентамицин не может подвергаться фосфорилированию в положении 3' или присоединять нуклеотид в положении 4', поскольку ни один из этих атомов углерода не содержит в качестве заместителя гидроксильной группы.
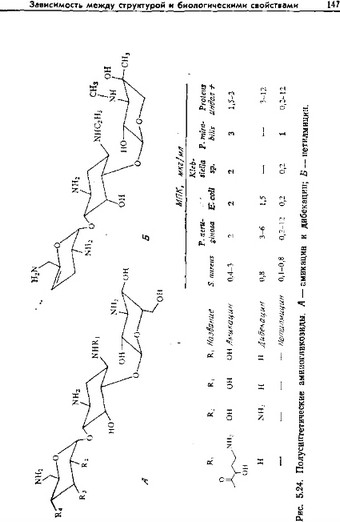
Эти данные служат основой для рационального планирования программы синтеза химически модифицированных производных. Среди таких производных в клинике используются ди- бекацин (3',4'-дезоксиканамицин В) и амикацин (Ы-окси-у-ами- нобутирилканамицин А) (рис. 5.24). Дибекацин, конечно, нечувствителен к ферментам, атакующим гидроксильные группы в положениях 3' и 4', и поэтому его активность сравнима с активностью гентамицина. Основанием для синтеза амикацина послужил тот факт, что антибиотик, образуемый В. circulans, бутиро- зин В, который отличается от рибостамицина только наличием заместителя, а-окси-у-аминомасляной кислоты, при аминогруппе в положении С-1 в отличие от рибостамицина активен в отношении Pseudomonas и других штаммов, образующих инактивирующие ферменты.
Когда различные аминогликозиды были ацилированы а-ок- си-у-аминомасляной кислотой, оказалось, что полученные производные нечувствительны к ферментам, катализирующим присоединение фосфатной группы через кислород в положении 3', к ферментам, катализирующим присоединение ацетильной группы через азот в положении 3, и нуклеотидилтрансферазам, атакующим кислород в положении 2".
Амикацин — производное, полученное путем присоединения ацильной группы к атому азота при С-1 канамицина А, — представляет собой аминогликозид с наиболее широким спектром действия. Его используют в основном при заболеваниях, вызываемых бактериями, которые устойчивы к другим производным, поскольку активность амикацина в отношении чувствительных штаммов ниже активности гентамицина.
Недавно получено еще одно полусинтетическое производное— нетилмицин, или l-N-этилсизомицин (рис. 5.24). Нетил- мицин обладает несколько более широким спектром действия, чем гентамицин. Его главным преимуществом является меньшая токсичность в опытах на лабораторных животных.
В. АМИНОГЛИКОЗИДНЫЕ АНТИБИОТИКИ,
СОДЕРЖАЩИЕ РАЗЛИЧНЫЕ АМИНОЦИКЛИТОЛЫ
Помимо аминогликозидов, описанных выше, только один аминогликозидный антибиотик используется в клинике. Это
спектиномицин (рис. 5.25), образуемый культурой Streptomy- ces spectabilis и содержащий аминоциклитол актинамин. Он отличается от других аминогликозидов тем, что обладает не бактерицидным, а бактериостатическим действием. Его используют для лечения гонореи.
Некоторые аминогликозидные антибиотики используют в сельском хозяйстве. По-видимому, наиболее денным из них яв-
Название S. pyogenes S. pneumoniae Neisseria gonorrhoeae E. coli Спектиномицин 6 12 8 12
Рис. 5.25. Спектиномицин.
ляется касугамицин, применяющийся в Японии для борьбы с болезнью риса, вызываемой Piricularia oryzae. При аскаридозе у животных применяют гигромидин В, образуемый S. hygrosco- picus, и дестомицин, образуемый S. rimofaciens. Наконец, для борьбы с некоторыми болезнями растений, вызываемыми грибами, используют валидомицин.
Г. АМИНОГЛИКОЗИДЫ, ПОЛУЧЕННЫЕ ПУТЕМ БИОСИНТЕЗА С ИСПОЛЬЗОВАНИЕМ СИНТЕТИЧЕСКИХ ПРЕДШЕСТВЕННИКОВ
При обработке мутагенами штаммов, образующих аминогликозидные антибиотики, можно получить мутанты, утратившие способность синтезировать дезоксистрептамин. Эти мутанты легко идентифицировать, поскольку они образуют антибиотики только при выращивании в среде с 2-дезоксистрептамином. Если вместо него в среду добавить другой аминоциклитол, некоторые мутанты используют его и синтезируют соответствующие аналоги природных антибиотиков. Этот метод получения новых
антибиотиков называют мутасинтезом или мутационным биосинтезом.
Первыми продуктами, полученными таким путем, были гиб- римицины (2-оксинеомицины), образуемые мутантным штаммом
S. fradiae в присутствии стрептамина. Позднее для синтеза новых аналогов стрептомицина, паромомицина, канамицина, рибостамицина, бутирозина и, наконец, сизомицина были использованы другие микроорганизмы. По-видимому, этот метод является весьма перспективным. Полученные продукты, многие из которых обладали антимикробной активностью, помогли выяснить связь между структурой и активностью у аминогликози- дов, а некоторые из них могут представить интерес для медицинской практики.
Главный недостаток этого метода, по крайней мере на сегодняшний день, состоит в том, что выход антибиотиков слишком мал для их промышленного производства.
Д. НЕРЕШЕННЫЕ ПРОБЛЕМЫ
Спектр действия аминогликозидов обсуждался при описании отдельных антибиотиков. Необходимо отметить, что в целом антибиотики этого класса неактивны в отношении анаэробных бактерий или аэробных бактерий, растущих в анаэробных условиях.
Мы уже останавливались на проблеме устойчивости к антибиотикам и на попытках ее решения путем направленного синтеза новых продуктов. Несомненно, новые производные имеют важное значение для химиотерапии, и есть основания полагать, что интенсивные исследования, ведущиеся в этой области в настоящее время, принесут свои плоды.
Исходя из общих свойств этого класса антибиотиков, можно сделать вывод, что получить производные, способные всасываться при приеме внутрь, вряд ли удастся.
Наиболее важный вопрос, касающийся аминогликозидов, состоит в том, можно ли путем биосинтеза или в результате химического синтеза получить менее токсичные аминогликозидные антибиотики, чем те, которые используются сегодня. Мы не можем с уверенностью ответить на этот вопрос, пока не установим на биохимическом уровне причины токсического действия аминогликозидов на восьмой черепномозговой нерв и на почки. Вообще говоря, анализ влияния различных заместителей на токсичность и сравнение активности и токсичности десятков соединений, по-видимому, свидетельствуют о том, что активность и токсичность изменяются параллельно. Если данные о меньшей токсичности нетилмицина, полученные в опытах на животных, подтвердятся при клинических испытаниях, это в значительной мере стимулирует поиски новых нетоксичных аминогликозидов.
Источник: Ланчини Д., Паренти Ф., «Антибиотики. Пер. с англ. — М.: Мир. — 272 с., ил.» 1985