МЕНИНГОКОККОВАЯ ИНФЕКЦИЯ
Менингококковая инфекция — заболевание, проявляющееся различными клиническими формами и вызываемое менингококком (Neisseria meningitidis). Основной формой инфекции является носительство. У части зараженных людей размножение бактерий в носоглотке приводит к местным воспалительным реакциям (назофарингит). У другой части зараженных наблюдаются генерализованные формы менингококковой инфекции (ГФМИ). При этом возбудитель гематогенно проникает в различные органы. Чаще он проникает в ЦНС, вызывая поражение мозговых оболочек (цереброспинальный менингит) и реже — мозговой ткани (энцефалит). Встречаются общетоксические формы, сопровождающиеся поражением многих тканей и циркуляцией менингококка в крови (менингококкцемия). Инкубационный период при ГФМИ 2 — 6, максимум 10—11 дней.
Механизм развития эпидемического процесса. Менингококк по антигенной структуре очень сложен, имеются компоненты, объединяющие все менингококки, но есть и отличающие их — по поверхностному полисахариду различается ряд групп: А, В, С, D, Е (29Е), I, К, X, Y, W (W135) и Z. Не все менингококки равноценны по патогенности — наиболее опасны так называемые эпидемические — А, В, С. D-менингококк встречается крайне редко и практического значения не имеет. Все остальные группы могут вызывать заболевания, но чаще всего в виде незначительного числа спорадических случаев. Наряду с этим было замечено учащение тяжелых форм болезни, вызванных менингококком группы W135. Внутри отдельных групп имеются типовые различия. Менингококки, кроме того, имеют общие, главным образом белковые, антигенные компоненты с многими непатогенными нейссериями, постоянно обнаруживаемыми в носоглотке, в том числе с N. laqtamica, которая часто вегетирует в носоглотке детей раннего возраста (грудных).
Имеются косвенные данные о возможности изменения вирулентности возбудителей: так, в СССР в длительные годы благополучия (50 —60-е годы) от редких больных выделялись менингококки группы А, а затем этот же менингококк вызвал эпидемию. Типовая дифференциация менингококков В, С, Y и некоторых других групп также указывает на возможность различия вирулентности штаммов. В последние годы при вспышках и эпидемиях, как правило, выделяются культуры возбудителя, резистентного к сульфаниламидам.
Циркуляция различных групп менингококков и непатогенных нейссерий создает среди населения целую гамму устойчивости у людей к различным агентам и определяет ряд особенностей развития эпидемического процесса.
Имеются данные об опасности больных в конце инкубации. Больной генерализованной формой менингококковой инфекции (ГФМИ) заразен в течение всей болезни, считается, что возбудитель в носоглотке сохраняется до трех недель (максимум). Больные назофарингитом оказываются опасными для окружающих примерно до трех недель. В настоящее время в крупных городах на 1 больного ГФМИ приходится в год 45000 — 50000 носителей. Носительство имеет решающую эпидемиологическую роль. Большинство случаев заражений, в том числе ведущих к ГФМИ, есть результат заражения от носителей (однако отнюдь не все носители несут равную эпидемиологическую функцию). У большинства носителей (примерно 70%) вегетация менингококка в носоглотке кратковременна (повторные анализы через 7—10 дней отрица-
Рис. 84. Длительно существующий очаг ме- нингококковой инфекции в организованном коллективе.
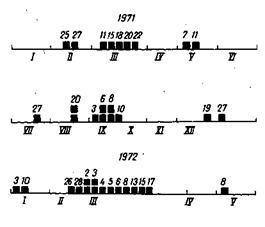 Черным квадратом обозначен случай ГфМИ, цифрой над квадратом — дата заболевания.
Черным квадратом обозначен случай ГфМИ, цифрой над квадратом — дата заболевания.
тельны) и не сопровождается обильным размножением (выявляются единичные, максимум 10—20 колоний при посеве мазка). Такие носители либо не дают последующих заражений, либо из-за малого количества выделяемого возбудителя могут вызвать такое же кратковременное носительство. Остальные носители выделяют культуру какое-то время,~ но большая часть из них освобождается от менингококка через 3 — 6 мес. Лишь около 5 % носителей выделяют культуру более 6 мес, причем некоторые из них в течение нескольких лет. У таких людей заселенность носоглотки значительна (при посевах одного мазка обнаруживается свыше 30 колоний, нередко чистая культура). Если учесть, что длительное и массивное носительство характерно в основном для эпидемических штаммов (А, В, С), то понятна их ведущая роль в распространении менингококковой инфекции, в частности ГФМИ. Именно за счет таких резидентных, «злостных» носителей формируются в закрытых организованных коллективах длительно существующие очаги, когда в течение нескольких лет возникают периодически с интервалами времени, существенно превышающими инкубационный период, ГФМИ, причем чаще всего по несколько случаев сразу. На рис. 84 показан очаг такого типа в одном организованном коллективе. Прекратить заболеваемость удалось после выявления и изоляции «злостного» носителя. И вне организованных коллективов роль «злостных» носителей ведущая, однако, поскольку они, эпизодически общаясь с множеством людей в различных местах, вызывают разрозненные случаи ГФМИ и поэтому не обнаруживают себя, борьбу с ними вести очень трудно. Такие «злостные» носители чаще всего встречаются среди взрослых.
Неоднородность циркулирующих среди населения менингококков особенно отчетливо проявляется при изучении этиологической структуры заболеваний. Если ГФМИ вызываются чаще всего одним'ведущим эпидемическим вариантом мейингококка (например, А), роль других эпидемических групп хотя и проявляется, но уступает значению ведущей группы, то носительство всегда полиэтиологично. Иначе говоря, для эпидемических штаммов характерны и ГФМИ, и носительство, для неэпидемических штаммов — практически только носительство.
Передача возбудителя осуществляется воздушно-капельным путем. В последние годы появились данные о некоторых генетических различиях восприимчивости. г и
При'менингококковой инфекции вырабатывается иммунитет, напряженность и продолжительность которого пока не определены. Носительство, которое в таких крупных административных центрах, как Москва, Ленинград и другие, достигает при моментном обследовании 5 — 8%, имеет большое значение в пррэпидемичцвании населения. На рис. 85 показана иммунологическая характеристика здорового населения Ленинграда в возрастном аспекте по отношению к менингококку группы А в очагах ГФМИ, вызванных этим возбудителем, и вне одагов. Здесь важно подчеркнуть то, что, с одной стороны, на-
Prie. 85. Титры антител к менингококку группы À у здоровых людей разного возраста в очагах (заштриховано красным) и вне очагов (не заштриховано). Линиями на вершине столбиков обозначены границы доверительного интервала, в пределах которого различия недостоверны.
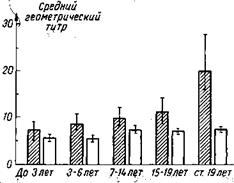 селение города с возрастом становится более иммунным, а с другой — в очагах (т. е. в условиях свежего инфицирования) титры заметно выше, чем вне очагов. С возрастом из-за Многократных предшествующих встреч с возбудителем иммунитет более напряжен, и потому при свежем инфицировании иммунологическая реакция весьма значительна (бустер-эффект). При менингококковой инфекции необходимо различать защиту от ГФМИ и местный иммунитет. Опыт показывает, что защита от ГФМИ при частых заражениях, которые сопровождаются носительством, вырабатывается надежная, а местный иммунитет тканей носоглотки оказывается нестойким, поэтому и возможны случаи повторного и многократного носительства. Важнейшее значение имеет то, что в популяции встречаются лица, которые, имея иммунитет против генерализации инфекционного процесса, практически не в состоянии выработать местную невосприимчивость — из таких людей формируются «злостные», резидентные носители. 1
селение города с возрастом становится более иммунным, а с другой — в очагах (т. е. в условиях свежего инфицирования) титры заметно выше, чем вне очагов. С возрастом из-за Многократных предшествующих встреч с возбудителем иммунитет более напряжен, и потому при свежем инфицировании иммунологическая реакция весьма значительна (бустер-эффект). При менингококковой инфекции необходимо различать защиту от ГФМИ и местный иммунитет. Опыт показывает, что защита от ГФМИ при частых заражениях, которые сопровождаются носительством, вырабатывается надежная, а местный иммунитет тканей носоглотки оказывается нестойким, поэтому и возможны случаи повторного и многократного носительства. Важнейшее значение имеет то, что в популяции встречаются лица, которые, имея иммунитет против генерализации инфекционного процесса, практически не в состоянии выработать местную невосприимчивость — из таких людей формируются «злостные», резидентные носители. 1
Механизмы внутренней регуляции эпидемического процесса иллюстрируют данные рис. 12.
Проявления эпидемического процесса. Заболеваемость менингококковой инфекцией в большинстве стран умеренных широт невысока и колеблется от ничтожных цифр (0,01 — 0,02 на 100 тыс.) до 8—12 на 100 тыс. в годы эпидемического неблагополучия. Однако, учитывая тяжесть ГФМИ, частую инвалидность после перенесения болезни (глухота, умственная неполноценность и др.), высокую летальность (при цереброспинальном менингите она иногда достигает 10 — 20%, при энцефалите — 90 %), даже эта невысокая заболеваемость представляет важную медицинскую и социальную проблему. С другой стороны, в тропической зоне Африканского континента менингококковая инфекция вызывает очень высокую годовую заболеваемость, Достигающую 300—500—700 на 100 тыс. населения. Указанное своеобразное распределение заболеваемости менингококковой инфекцией принципиально отличает ее от других воздушно-капельных инфекций. Но нужно отметить, что в любых местах (широтах)'- может возникнуть локальная высокая заболеваемость.
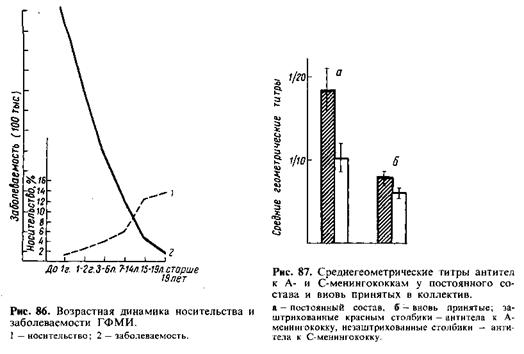
Максимальные уровни заболеваемости ГФМИ регистрируются у детей до 1 г. ; с Возрастом заболеваемость постепенно снижается. Возрастное распределение носительства имеет по сравнению с возрастной структурой заболеваем моей*П^ЬтйврпбйбМЦую* 1еййеШЩЩ» (рис! 86). В начале последнего циклического подъема > заболеваемости имели место вспышки и соответственно повышенная заболеваемость среди молодых людей, находящихся в различных организованных коллективах. В таких коллективах ГФМИ возникает после формирования коллектива, причем заболевают вновь влившиеся в коллектив неиммунные лйца (рис. 87).
Дети 3 — 6 лет (организованные и неорганизованные) болеют с равной частотой, а дети раннего возраста — больше неорганизованные.
 |
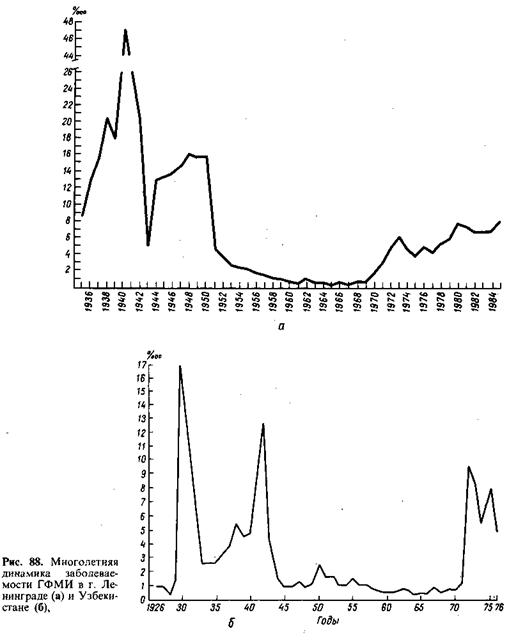
Многолетняя динамика при менингококковой инфекции характеризуется большими циклами (рис. 88). Возрастная структура заболеваемости при этом существенно не меняется: на подъеме возрастают показатели заболеваемости во всех возрастных группах.
Циклические подъемы заболеваемости происходят достаточно синхронно на больших территориях — в разных странах и даже континентах, причем часто за счет менингококков разных групп. Так, последний подъем конца 60-х — начала 70-х годов был вызван в СССР и странах Восточной Европы менингококком группы А, в Западной и частично Центральной Европе — менингококком группы В. Поражение в самом начале циклического подъема детей до 1 года и приезжих в организованные коллективы и только затем остальной части населения свидетельствует о первоначальной еще недостаточной вирулентности менингококка, которая затем возрастает.
Сезонность при менингококковой инфекции достаточно характерна — максимальный уровень заболеваемости достигается в январе — мае, хотя подъем начинается в осенние месяцы. Как и при других воздушно-капельных инфекциях, в годы неблагополучия сезонный подъем выражен резче.
Характерно, что сначала вовлекается в циклический подъем население нескольких крупных и крупнейших городов страны, вслед за тем (иногда через 1—2 г.) поражается население других административных центров, причем — судя по последней волне — чем выше широты, тем вовлечение в эпидемический процесс происходит позже и интенсивность его меньше. Затем города, особенно крупные, становятся своеобразным «эпицентром» распространения заболеваемости на окружающей территории — сначала в прйгородах, затем и в отдаленных небольших городах и рабочих поселках, связанных коммуникациями с центральным городом. Жители сел вовлекаются в эпидемический процесс редко. Последовательность вовлечения населенных пунктов в циклический подъем показана на рис. 21.
 |
Противоэпидемические мероприятия. При угрозе роста заболеваемости не- • обходимо усилить разъяснительную работу среди родителей детей до 1 года с целью обеспечить максимальную изоляцию последних. Родители и другие родственники, ухаживающие за детьми, должны при обслуживании детей носить ватно-марлевые маски, которые прикрывают рот и нос.
Вопрос о вакцинации решается пока непросто. В ряде стран, в том числе в СССР* создана вакцина против менингококков групп А и С, которая содержит очищенный поверхностный групповой полисахарид. Вакцина проверялась
в сложных эпидемических ситуациях и дала хорошие результаты. Однако наиболее уязвимый контингент — детей до 1 г. — прививать не решаются, поскольку их иммунологическая реактивность еще недостаточна, а реактогед- ность препарата для них, как показал опыт Финляндии, значительна.
Учитывая общую невысокую заболеваемость и редкие подъемы, вводить в стране плановые прививки нецелесообразно, они проводятся только по эпидемическим показаниям.
При возникновении заболеваний ГФМИ необходима немедленная изоляция и срочная, от которой зависит эффект лечения, госпитализация больных. Дезинфекционные мероприятия в очагах не нужны — микроб очень нестойкий, кроме того, опасная с точки зрения развития ГФМИ доза может быть получена только в результате тесного непосредственного общения с источником инфекции. Больные выписываются с учетом бактериологических данных, но даже без бактериологических исследований возможна выписка через 3 недели.
Спорным является вопрос об обследовании на носительство в очагах. В большинстве стран такую работу не ведут, считая ее нецелесообразной. Мо- ментное обследование может дать очень высокие положительные результаты, причем абсолютное большинство выявленных носителей эпидемиологической опасности не представляет.
Обследование на носительство показано в очагах, где заболеваемость формируется за счет резидентных, «злостных» носителей. Но бактериологическое обследование при этом должно быть целенаправленным: материал забирается только от постоянно работающих в коллективе (постоянного состава), а не от влившейся молодежи. Изолируются только носители эпидемического штамма. Санация показана в отношении людей, у которых культура выделяется неоднократно.
Эпидемиологический надзор. Целью эпидемиологического надзора за ме- нингококковой инфекцией является предупреждение смертельных исходов и снижение показателей заболеваемости в группах риска на основе оценки тенденций развития эпидемического процесса. При проведении ретроспективного и оперативного эпидемиологического анализа учитываются следующие обстоятельства.
1. Подъем заболеваемости начинается всегда с поражения детей первого года жизни, в некоторых случаях, особенно в самом начале эпидемии, с поражения также молодежи, прибывшей в организованные коллективы в городах (ПТУ, вузы и др.).
В связи с этим на всех территориях определяется ежегодно темп роста заболеваемости среди детей до 1 г. (или до 2 лет, если численность населения невелика); заметное возрастание темпов роста является неблагоприятным прогностическим признаком. Точно так же определяются темпы роста среди лиц 15 лет и старше, при этом учитывается приезд в город, включение в организованные коллективы.
2. Пораженность ГФМИ населения в следующем году определяется краткостью роста заболеваемости в ноябре — декабре по сравнению с сентябрем (индексом роста), т. е. четвертый квартал является «базисным» для следующего года, точнее, для следующих января — августа.
Длительные (многолетние) наблюдения позволяют определить индекс, который не вызывает беспокойства, и индекс, свидетельствующий о развивающемся неблагополучии.
3. Для слежения за эпидемическим процессом целесообразно в^сти постоянное изучение носительства в выбранных, достаточно репрезентативных индикаторных группах населения (учащиеся ПТУ, техникумов и др.). Материал следует забирать дважды — в сентябре и в ноябре — декабре. Степень роста уровня носительства, особенно актуального штамма (ведущего возбудителя ГФМИ), дозволяет предвидеть ситуацию в будущем году. Очень хорошие результаты дает постоянное наблюдение за иммунологическими показателями в сыворотках доноров, которые сдают кровь в августе и в декабре. Индекс роста уровня антител (особенно против актуального штамма) позволяет оттенить будущую эпидемическую ситуацию.
На основе оценки обстановки принимаются перспективные и текущие управленческие решения в отношений проведения тех или иных противо-. эпидемических мероприятий.
Источник: Беляков В. Д., Яфаев Р. X., «Эпидемиология: Учебник» 1989