Характеристика макроорганизма (хозяина)
Организм (макроорганизм) становится хозяином для того вида постороннего живого агента, который находит условия для питания и размножения. В том случае, если организм не может стать средой обитания для микроорганизма (из-за отсутствия необходимых условий не включаются его метаболические процессы), последний отмирает или (и) механически удаляется как инородное тело.
Речь, таким образом, идет о видовой восприимчивости к тому или иному паразиту или, наоборот, невосприимчивости. В прошлом это последнее явление называлось видовым иммунитетом, хотя к иммунитету оно не имеет никакого отношения. Так, человек страдает от вируса кори, но не болеет чумой собак, вызываемой вирусом, сходным с вирусом кори; болеет брюшным тифом, но безразличен к внедрению Salmonellapullorum, которая вызывает тяжелую смертельную инфекцию у кур, хотя возбудители этих заболеваний очень близки между собой (по современным представлениям относятся к одному виду).
Организм хозяина, участвующий во взаимодействии с паразитом, который проник внутрь его тела или осел на коже или слизистых покровах, в эволюционном развитии приобрел лишь оборонительные средства защиты. Это механическая защита внутренней среды организма, свойственная коже и слизистым оболочкам (особенно эффективна защитная функция кожных покровов), а также лимфатическим узлам; различные иеспецифические гуморальные (комплемент, глобулины, лизоцим и т. д.) и клеточные (микро- и макрофаги) факторы зашиты, участвующие в воспалительной реакции, а также специфическая защита —- иммунитет.
Надо отметить, что эти факторы (за исключением механических барьеров) в естественных условиях включаются в защиту практически только против тех агентов, которые могут паразитировать, т. е. активно существовать, поскольку первоначальная доза (до размножения) весьма незначительна (как бы незаметна для организма). В искусственных условиях, когда возможно введение сразу больших доз микроорганизма, картина может быть иной — защитные механизмы, в том числе иммунная система, активно включаются в борьбу с посторонним агентом. Так, например, для получения диагностических иммунных сывороток с высокими титрами антител против возбудителей дизентерии используется внутривенная иммунизация кроликов большими дозами живых или убитых дизентерийных палочек, хотя кролики к этим микроорганизмам не обладают восприимчивостью. Этот пример показывает, что именно дозировка часто определяет складывающуюся ситуацию в повседневной жизни.
При наличии видовой восприимчивости наблюдаются индивидуальные различия в этой реакции на внедрение возбудителя. Как видно из табл. 8.2, при одинаковых заражающих дозах последствия были различными: одни заболевали брюшным тифом, другие переносили инфекцию бессимптомно, третьи — вообще не заражались. Из табл. 8.1 и 8.2 видно, что восприимчивость к паразиту или к отдельным его штаммам можно определить по заражающей дозе, которая ведет к развитию инфекционного процесса, в том числе ведущего к патологии. Если учесть, что в данном опыте группа добровольцев была достаточно однородна (мужчины одного возраста, тождественные по всем параметрам социальные условия), то можно представить значение определенных тонких генетических различий, которые не удалось выявить. По-видимому, для однородной группы характерен разброс восприимчивости в соответствии с кривой нормального распределения Гаусса (рис 8.2): наибольшее число людей заражается (или заболевает) от средних инфицирующих доз, но есть

|
высоко восприимчивые люди, которые заражаются (заболевают) при малых инфицирующих дозах (чем выше доза, тем число их становится большим). С другой стороны, некоторое число лиц обладает повышенной резистентностью разной степени - чем выше устойчивость, тем меньше таких людей в популяции.
Надо также обратить внимание на то, что если инфекционный процесс может протекать в двух вариантах: бессимптомно и в виде патологии, то инфицирующие дозы для одного и того же человека будут различными: доза, вызывающая патологию, будет выше.
Наряду с генетическими характеристиками, включая половые особенности, расовые и, возможно, какие-то другие (например, различие по группам крови), имеют значение и фенотипные характеристики — возраст, характер питания, стрессовые состояния, сопутствующие заболевания и т. п. Необходимо отметить, что очень часто без должных оснований утверждается, что восприимчивость детей к многим возбудителям выше, чем взрослых; предполагается, что к паразитам велика восприимчивость
4 Ы 48-46
пожилых людей. Между тем известно, что взрослые, которые по каким- либо причинам избежали заражения в детстве вирусами кори и ветряной оспы, переносят названные инфекции очень тяжело, несопоставимо тяжелее, чем большинство детей. Исследования в лаборатории М. Р. Сапина показали, что мощность лимфоидной системы в стенке тонкой и толстой кишок (относительный размер и число бляшек) у детей выше, чем у взрослых (рис. 8.3).
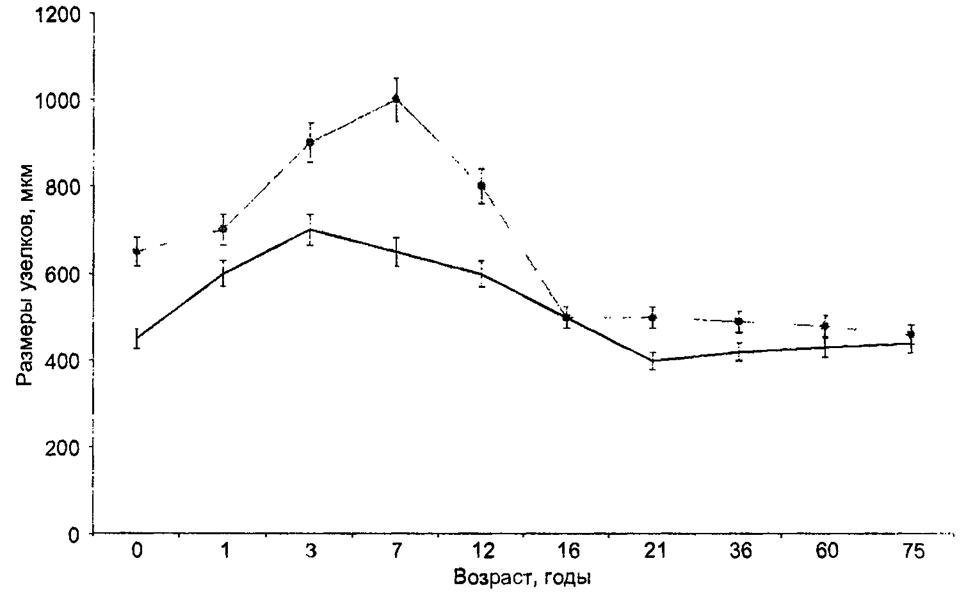
Рис. 8.3. Графическое изображение средних размеров (высоты) лимфоидных узелков, входящих в состав лимфоидных бляшек тощей (сплошная линия) и подвздошной (пунктирная линия) кишок человека в постнатальном онтогенезе (М. Р. Сапин) |
По-видимому, представление о большей уязвимости детей основано на высокой заболеваемости детей первых дней и месяцев жизни (они действительно очень восприимчивы ко многим паразитам) и существовании так называемых «детских» инфекций, хотя взрослые болеют ими редко из-за наличия иммунитета после перенесения болезни в детстве. В отношении пожилых людей также требуется более тщательное эпидемиологическое исследование с применением современных методик. По нашим сравнительно немногочисленным наблюдениям (145 пациентов) было установлено, что частота послеоперационных гнойных осложнений после аппендэктомии у лиц активного возраста и у пожилых людей была одинакова — различия оказались статистически недостоверными. Аналогичные данные были получены при изучении вероятности развития гнойно-септических инфекций (ГСП) у пациентов травматологического стационара (табл. 8 3).
Таблица 8.3
| Частота развития ГСИ в зависимости от возраста у пациентов
травматологического стационара
Пр имечание Различия везде недостоверны (р>0,05) |
Неспецифические факторы защиты: механические (кожа, слизистые покровы, лимфатические узлы), клеточные (макро- и микрофаги), гуморальные (комплемент, лизоцим, бета-лизин, интерферон и др.) — обладают ограниченными возможностями (за исключением кожных покровов). Поэтому в эволюционном развитии постепенно сформировалась дополнительная, новая система, обеспечивающая борьбу с помощью механизмов, направленных строго специфично против внедрившегося паразита. Речь идет об уже упомянутой иммунной системе. Эта система, по-видимому, включается сразу (немедленно) по достижении в результате размножения такого количества паразита, которое необходимо для раздражения лимфоцитов. Однако эффект ее действия сказывается далеко не сразу, чаще всего через несколько дней или даже недель. Это связано с необходимостью накопления соответствующего, ответственного за борьбу с конкретным возбудителем инфекции, клона лимфоцитов. Возможности иммунной системы, как правило, несопоставимо выше, чем неспецифических факторов защиты; так, выздоровление при острых инфекционных заболеваниях обеспечивается сформировавшимся иммунитетом.
К сожалению, хронические инфекции свидетельствуют о том, что иногда иммунная система не в состоянии обеспечить надежную защиту (например, при сифилисе, проказе и т. д.); сомнительна защитная роль иммунной системы при гельминтозах.
Надо также отметить иногда как бы парадоксальную реакцию иммунной системы. Имеется в виду аллергизация организма, которая развивается при некоторых нозоформах весьма отчетливо (туберкулез, бруцеллез, туляремия, сап и др.), при других выражена заметно слабее (сибирская язва, дизентерия и др.). Очевидной целесообразности — с точки зрения защиты организма от паразита — здесь усмотреть не удается.
Иммунитет может быть общим, который формируется чаще всего при проникновении возбудителя в кровь (образование антител — IgM и IgG, активизация специфичных против данного паразита лимфоцитов с разной функциональной направленностью, выполняющих клеточную защиту).
Кроме того, в слизистых оболочках, а также в некоторых секреторных органах (слюнные, молочные железы) имеются скопления лимфоидной
вз
ткани, предназначенные для местной гуморальной (IgA, IgG) и клеточной зашиты. Особенно мощно лимфоидная ткань представлена в слизистой оболочке кишечника, гораздо меньше ее в слизистой оболочке дыхательного тракта.
Необходимо отметить, что напряженность иммунитета возрастает при повторных, особенно многократных встречах с паразитом. При повторных встречах с возбудителем по сравнению с первичным иммунным ответом растет как напряженность иммунитета, так и скорость иммунной реакции (так называемый бустер-эффект). Это связывают с накоплением после первичного иммунного ответа специфичных для каждого паразита В- и Т- лимфоцитов памяти. Активность иммунной системы, так же как и факторов неспецифической защиты, у отдельных индивидуумов колеблется в зависимости от генотипных и фенотипных особенностей.
Наряду с иммунитетом, который вырабатывается организмом хозяина при встрече с посторонним агентом, возможен и так называемый пассивный иммунитет. В естественных условиях он наблюдается у новорожденных, получающих готовые антитела от иммунной матери. Такой иммунитет держится у детей сравнительно короткий срок, поскольку введенные извне иммуноглобулины недолговечны. Между тем известно, что дети, рожденные от иммунных матерей, не заболевают соответствующими болезнями 3“6 месяцев. Подобный феномен требует оценки после тщательно спланированных эпидемиологических исследований, поскольку вероятность заболеть для детей нескольких месяцев отроду в общем не велика из-за защищающих изоляционных мероприятий, которые осуществляют родители. Известно, что вероятность заболеть в самом раннем возрасте зависит, в частности, от того, в каких вариантах у людей вообще может протекать инфекционный процесс. Так, менингококковой инфекцией, при которой высок уровень носительства среди населения, чаще всего заболевают дети раннего возраста (возможности встречи с возбудителем становятся реальными уже вскоре после рождения). С другой стороны, корью заболевают обычно дети старше 6-месячного возраста, поскольку вероятность встречи с больным корью (заразиться можно только от больного) существенно меньше. Защитная роль молока матери, содержащей IgA против какого-либо возбудителя кишечных инфекций, нуждается в очень серьезной проверке и оценке.
Схематично возможности макроорганизма в защите от паразита показаны на рис. 8.4.
Итак, взаимодействие макроорганизма и паразита на организменном уровне может привести к развитию инфекционного процесса, который в зависимости от заражающей дозы и свойств паразита (видовая генетическая характеристика, вирулентность), а также от состояния защитных возможностей хозяина (неспецифическая защита, иммунитет) развивается по-разному: в виде здорового носительства или патологии разной степени выраженности. Все формы инфекционного процесса имеют значение, хотя и неравнозначное, в сохранении и поддержании вида патогенного агента юо
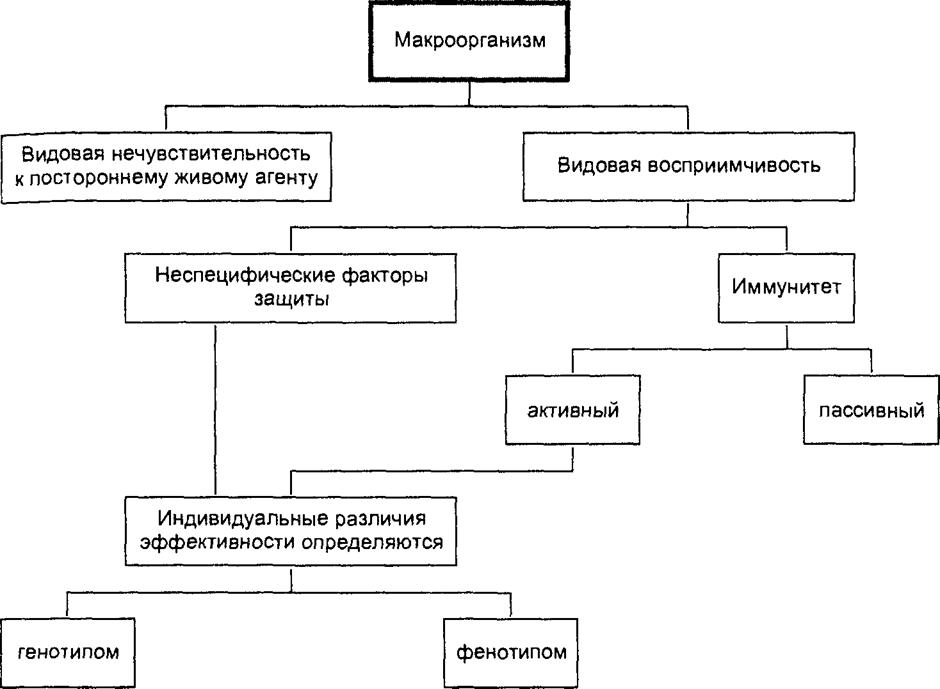
Рис. 8.4. Характеристика восприимчивости человека |
Человек восприимчив к паразитам, которые адаптированы строго к его организму. Заболевания, вызванные такими паразитами, именуют антропонозами. Но в связи с определенным биологическим сходством с животными, человек оказывается восприимчив к некоторым паразитам последних (это так называемые зоонозы). Наряду с этим иногда возникают заболевания человека при заражении упомянутыми факультативными паразитами. Иначе говоря, человек может быть восприимчив к некоторым свободно живущим микроорганизмам. В таких случаях заболевания относят к сапронозам.
Надо, однако, заметить, что взаимодействие на организменном уровне, как бы оно ни было благоприятным для паразита, не в состоянии обеспечить сохранение вида. Это объясняется тем, что организм хозяина смертен. Он может умереть естественной смертью, может погибнуть при разных, нередко случайных обстоятельствах, в частности в результате инфекционного процесса. Только при появлении возможности перемещаться из одной особи хозяина в другую создаются условия для сохранения паразитического вида Иначе говоря, в эволюционном развитии паразита сформировалась не только способность жить в организме хозяина, но и менять одну особь хозяина на другую. В основе появления такой возможности лежит уже упомянутая быстрота смены поколений у паразита, несопоставимая с более замедленной у хозяина. По предложению Л В Громашевского, эволюционно сложившаяся способность к перемещению пара-
0 си
зита из организма одной особи хозяина в другую называется механизмом передачи.
Учение Л. В. Громашевского о механизме передачи вскрыло одну важнейшую эволюционную особенность формирования паразитического вида: адаптация живого постороннего агента была возможна только к тем тканям, которые могли обеспечить выход паразита за пределы организма хозяина. Более того, адаптационные возможности в эволюционном развитии были ограничены необходимостью попадания (проникновения) паразита в аналогичные ткани другой особи хозяина (в ткани, к которым он адаптирован).
Таким образом, миссия механизма передачи не ограничивается только обеспечением выхода паразита за пределы организма хозяина, он выполняет еще одну специфическую функцию, а именно доставляет паразита в такую же ткань, из какой он был выделен. Например, если паразит вегетировал в слизистой оболочке кишечника, то за счет соответствующего механизма передачи он должен попасть в слизистую оболочку кишечника другой особи хозяина. В обобщенном варианте механизм передачи можно представить в виде схемы (рис. 8.5).
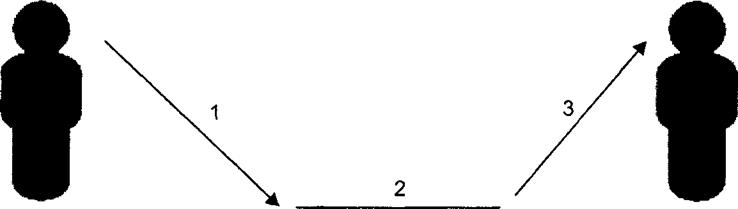
Рис. 8.5. Механизм передачи: 1 — фаза выведения возбудителя из зараженного организма, 2 — фаза пребывания возбудителя во внешней среде, 3 — фаза внедрения возбудителя в восприимчивый организм |
Все три фазы механизма передачи носят четкий специфический характер: фаза выведения зависит от локализации возбудителя в организме, вторая фаза — это попадание и нахождение паразита только в тех объектах внешней среды, которые могли быть контаминированы материалом первой фазы и, наконец, третья фаза определяется спецификой объектов внешней среды, обеспечивающих проникновение паразита в ткани, к которым он адаптирован.
Фаза выведения возбудителя из зараженного организма (1-я фаза) и фаза внедрения (3-я фаза) непродолжительны и соответствуют времени выброса тех или иных субстратов из организма (капелек слизи из дыхательного тракта при кашле или чихании, фекальных масс при дефекации и т. д.) и восприятия этих выделений (при вдохе, при питье зараженной воды или приеме контаминированной пищи и т. д.).
С другой стороны, вторая фаза при различных механизмах передачи имеет различную продолжительность. Например, при заражении непосредственным контактом, в частности при венерических заболеваниях,
она может вообще отсутствовать, при других способах заражения возбудитель во внешней среде должен иногда находиться длительное время, поскольку быстрое совмещение 1-й и 3-й фаз отнюдь не всегда возможно. Именно в этих случаях в эволюции у паразита за счет мутаций (возможно, обмена генетическим материалом) и селекции сформировалась способность сохраняться (переживать) в объектах внешней среды достаточно длительное время — такое, которое при соответствующем механизме передачи обеспечивает успешное его перемещение из одной особи хозяина в другую.
Необходимо отметить, что для облигатных паразитов внешняя среда, ее различные объекты не являются средой обитания, поэтому речь идет только о сохранении жизнеспособности. При этом, конечно, надо иметь в виду, что за счет неблагоприятных для паразита различных физических (ультрафиолетовая часть солнечных лучей, аномалии влажности и т. д.), химических (кислород воздуха, обладающий сильной окисляющей функцией, и т. д.), а иногда и биологических (антагонизм постоянных обитателей внешней среды) факторов с удлинением экспозиции происходит отмирание части паразитов, и, соответственно, опасность заражения восприимчивых людей снижается.
Лишь в редких случаях во внешней среде возможно размножение облигатных паразитов. Так, иногда при случайном благоприятном для паразита стечении обстоятельств наблюдается размножение различных представителей семейства кишечных бактерий в пищевых продуктах, богатых белковыми веществами или сахарами (мясные, молочные продукты, кондитерские изделия), что создает угрозу развития пищевых вспышек. Однако такие редкие эпизоды для сохранения паразитического вида практического значения не имеют.
Правда, есть некоторое исключение из общего правила о значимости внешней среды для облигатных паразитов, как среды неблагоприятной, в которой может иметь место только сохранение, переживание: у геогельминтов созревание в яйцах личинок до инвазионной стадии происходит в почве (этот процесс реализуется при более низких температурах, чем температура организма человека, и других физико-химических характеристиках окружающей среды).
Во второй фазе возбудитель в зависимости от вида механизма передачи попадает, как уже говорилось, на (в) какие-то специфичные для данного механизма передачи объекты внешней среды (воздух при воздушнокапельных, почва, вода, пищевые продукты — при инфекциях пищеварительного тракта и т. д.), в которых он может сохраняться и с помощью которых обеспечивается реализация третьей фазы. Такие объекты внешней среды называются факторами передачи. Во второй фазе возможно участие одного или эстафеты факторов передачи. В некоторых случаях в рамках одного и того же механизма передачи возможно участие не одного, а нескольких факторов передачи, которые действуют независимо, как бы параллельно. Например, дизентерией можно заразиться через воду или пищевые продукты. В подобных случаях говорят о конкретной реализации механизма передачи различными путями, при этом, если наблюдает
ся участие эстафеты факторов передачи, то путь обычно обозначают по конечному фактору (водный путь, пищевой путь и т. д.). В эпидемиологической диагностической работе выявление конкретных факторов и путей передачи имеет большое значение, поскольку позволяет затем провести эффективные целенаправленные мероприятия.
Итак, локализация паразита в организме хозяина и механизм передачи образуют специфическую систему: каждой локализации соответствует свой механизм передача (и наоборот).
С учетом необходимости непременного перемещения паразита из одной особи хозяина в другую сформировалось всего 4 такие системы (табл. 8.4)
| Таблица 8.4
Эволюционно сформировавшиеся системы соответствия основной локализации возбудителя в организме и механизма передачи
|
В некоторых случаях при развитии инфекционного процесса возможно через какое-то время проникновение паразита в ткани, находящиеся за пределами основной (первичной) локализации. Подобное имеет место при следующих обстоятельствах:
1. При усложненном патогенезе, отражающем особенности приспособления паразита в процессе эволюции к жизни в организме хозяина. Так, например, при брюшном тифе после заражения и первичного размножения возбудителя в слизистой оболочке тонкой кишки он через лимфатическую систему проникает в кровь, в которой продолжает размножаться, затем, фиксируясь в купферовских клетках печени, начинает выделяться через желчные ходы вновь в кишечник
При аскаридозе высвободившиеся в просвете кишечника из заглоченных яиц инвазионные личинки проходят сложный миграционный процесс (стенка кишки, кровь, альвеолы, дыхательные пути, глотка, кишечник, где, наконец, происходит созревание половозрелых гельминтов).
Во всех случаях такого усложненного патогенеза паразит в заключительной фазе должен обязательно достичь первичной (основной) локализации. Только в этом случае реализуется механизм передачи.
1 При осложнении течения инфекционного процесса Если в организм попадают высоковирулентные расы паразита, или существенно ослабляются защитные возможности хозяина (снижение общей резистентности, иммунодефицит), или совмещаются оба эти фактора, возможен, хотя в общем не очень часто, выход паразита за пределы первичной (основной) локализации. Среди тканей, в которые случайно попадает паразит, могут быть такие, в которых возбудитель находит весьма благоприятные условия для вегетирования. При этом возможно серьезное поражение тканей вторичной локализации. Так, при менингококковой инфекции изредка возможно развитие генерализованных форм — цереброспинального менингита, энцефалита, менингококкемии (основная локализация возбудителя — слизистая оболочка носоглотки). При полиомиелите возможно необратимое поражение серого вещества спинного мозга, хотя основная (первичная), причем, как правило, безобидная, локализация — клетки слизистой оболочки тонкой кишки. Важно отметить, что подобная вторичная локализация для сохранения паразитического вида не имеет никакого значения, поскольку она не обеспечивает выход паразита во внешнюю среду (вторичная локализация тупиковая, а возбудитель, оказавшийся в ней, — смертник, «камикадзе»). Но, к сожалению, эта вторичная локализация часто определяет тяжесть болезни, поэтому при таких нозоформах у клиницистов объектом внимания, как правило, оказывается не первичная, а вторичная локализация.
Итак, за счет эеолюционно сложившейся системы—локализация возбудителя в организме и соответствующий ей механизм передачи, — которая отражает популяционные взаимоотношения паразита и хозяина, обеспечивается сохранение (существование) паразитического вида. Эти популяционные взаимоотношения реализуются (проявляются) в виде эпидемического процесса.
В настоящее время зарегистрирован еще один способ заражения за счет, как говорят, вертикальной передачи, т. е. заражения плода матерью. При этом в одних случаях имеют в виду только внутриутробное заражение, в других — внутриутробное и заражение в процессе родов при прохождении родовых путей.
По-видимому, вторая точка зрения менее оправдана, поскольку заражение ребенка при родах происходит в результате контакта со слизистой оболочкой родовых путей и может быть отнесено к заражению с контактным механизмом передачи.
Внутриутробное заражение, к сожалению, сейчас фиксируется достаточно часто (краснуха, ВИЧ-инфекция, вирусный гепатит В и др.), однако вряд ли это можно рассматривать как механизм передачи, обеспечивающий сохранение возбудителя как вида. Внутриутробное заражение имеет, скорее всего, второстепенное (хотя, конечно, отнюдь не безобидное) значение, которое надо всегда учитывать и как-то предотвращать.
По-видимому, правомерно говорить о вертикальном механизме передачи (именно механизме, а не случайном эпизодическом заражении) только при генетических (наследственных) заболеваниях.
Источник: Л. П. Зуева, Р. X. Яфаев, «ЭПИДЕМИОЛОГИЯ» 2005
А так же в разделе «Характеристика макроорганизма (хозяина) »
- Глава 8 ОПРЕДЕЛЕНИЕ ЭПИДЕМИЧЕСКОГО ПРОЦЕСС
- 8.1. Характеристика паразитов
- Глава 9 СОСТАВНЫЕ ЧАСТИ (ВНУТРЕННЯЯ СТРУКТУРА) ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
- 9.1. Источник инфекции
- 9.2. Механизм передачи
- 9.2. Восприимчивый организм
- Глава 10 ПОПУЛЯЦИОННЫЙ ИММУНИТЕТ И ТЕОРИЯ САМОРЕГУЛЯЦИИ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
- Теория саморегуляции эпидемического процесса
- Глава 11 КЛАССИФИКАЦИЯ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ
- Глава 19 ХАРАКТЕРИСТИКА ПРОЯВЛЕНИЙ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
- Глава 13 ФАКТОРЫ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
- Глава 14 ЭПИДЕМИОЛОГИЧЕСКИЙ НАДЗОР
- 14,1. Оперативный анализ
- 14.2. Ретроспективный анализ
- Глава 15 ПРОФИЛАКТИЧЕСКИЕ И ПРОТИВОЭПИДЕМИЧЕСКИЕ МЕРОПРИЯТИЯ
- 1.5.1. Общая структура профилактических и противоэпидемических мероприятий
- Дезинфекция 15,2. Дезинфекция (обеззараживание)
- 15.2.2, Дезинсекция
- 15.2.3. Дератизация
- 15.3. Специфическая профилактика инфекционных заболеваний