Результаты лазерной терапии при осложненных формах деструктивной пневмонии
Роль лазерной терапии в лечении ГСЗ в последние годы значительно возросла. Этому способствовала ее несомненная эффективность в борьбе с гаойно-воспалительными процессами различных локализаций. Многочисленные публикации, освещающие как физико-химические, так и медико-биологические аспекты действия лазерного излучения, во многом противоречивы и не отражают стройной концепции ни в теоретическом плане, ни в прикладном отношении.
За 17 лет нами накоплен опыт применения НИЛ И в лечении более 250 детей с гнойно-септическими заболеваниями. Внутриполостная лазеротерапия проведена 165 детям с осложненными формами ОГДП. Из них 137 детей (83 %) были с пиопневмотораксом с бронхоплевральными свищами и 28 (17 %) — с постдеструктивными полостными внутрилегочными образованиями (абсцессы, напряженные буллы). У 85 детей с осложнениями разлитого гнойного перитонита, острым панкреатитом и острым гематогенным остеомиелитом использовался инфракрасный лазер для чрескожного облучения крови и воздействия на очаг. Средний возраст детей составил 3 года
- мес. Новорожденных было 5, остальные дети — в возрасте от
- мес до 14 лет. В последние 5 лет уменьшилось число детей до 1 года (15 %), но увеличилось количество детей старшего возраста.
В МОНИКИ дети поступали из ЦРБ области в крайне тяжелом состоянии на 18±2,6-й день от начала заболевания и 2—3-й день от возникновения плевролегочных осложнений. Процесс чаще локализовался справа (69,3 %), слева — у 21 % детей и двусторонняя деструктивная пневмония отмечена у
- %. У детей с двусторонней деструктивной пневмонией выявлялись гнойные очаги — острый гематогенный остеомиелит, медиастинит, гепатоспленомегалия, миокардит. Проведение интенсивной терапии в условиях детского реанимационного отделения потребовалось у 23 % поступивших детей.
Все дети в ЦРБ и в МОНИКИ получали комплексное интенсивное лечение, которое включало: антибиотики, детоксикацию, иммунотерапию, физиотерапию и дренирование плевральной полости. Чрескожное дренирование плевральной полости или полости абсцесса проводилось с учетом рентгенологических данных и ультразвукового исследования. С этой целью использовались дренажи из силиконизированной резины или троакар-катетеры, которые применялись и для дренирования легочных абсцессов. В первые 3—5 дней поступления в клинику полость эмпиемы активно санировалась различными антисептиками, проводилось чрескожное облучение крови инфракрасным лазером. После этого подключалось лечение гелий-неоновым лазером с доставкой лазерного света в полость эмпиемы или внутрилегочного абсцесса через дренаж по кварц-полимерному световоду. Разовая доза облучения в среднем составляла от 0,15 до 0,52 Дж/см2, суммарная — от 2,1 до 5,2 Дж/см2.
Микробная флора гнойных полостей до лазерной терапии представлена преимущественно гемолитическим стафилококком в концентрации 105— 106 у 62,3%; в 11,6% случаев — синегнойной палочкой; в 9,3 % — стрептококком и E.coli, клебсиелой — по 2,3 %. Отрицательные результаты получены у
- % детей. Нередко выявлялась смешанная флора — недифференцируемые грамотрицательные бактерии, дрожжеподобные грибы, сапрофитная флора. До лазерной терапии выявлена высокая устойчивость выделенных микроорганизмов к антибиотикам широкого спектра действия.
За время лазеротерапии в 4 раза увеличилось количество анализов, в которых не было выявлено роста аэробной микрофлоры и отмечено расширение спектра чувствительности флоры к антибиотикам: гентамицину, полимиксину, левоми- цетину, карбенициллину, хотя у большинства больных характер флоры практически не менялся. Полученные данные, отмеченные и другими авторами, свидетельствуют о том, что гелий-неоновый лазер бактерицидным действием на микрофлору не обладает. Что же касается инфракрасного лазерного излучения, то оно, по данным литературы, обладает антимикробной активностью и его рекомендуют использовать в целях борьбы с микрофлорой. Однако это положение требует дальнейшего клинического подтверждения.
Наш опыт применения лазерного излучения в лечении ГСЗ у детей показал, что НИЛИ даже при местном воздействии вызывает общую реакцию организма комплексным ответом всех систем гомеостаза.
Более чем у половины больных после первых двух сеансов лазерной терапии обнаружено повышение температуры тела до 37,2—37,3 °С при отсутствии ухудшения общего состояния и самочувствия. При этом у детей уменьшалась эндогенная интоксикация, увеличилась экскурсия грудной клетки, менее выраженным стал рефлекторный сколиоз грудного отдела позвоночника, исчезал болевой синдром в местах стояния дренажей.
Как правило, после 2—3 сеансов лазерной терапии наблюдалось увеличение количества гнойного или серозно-гнойного экссудата из плевральной полости. С 4-го сеанса количество отделяемого из плевральной полости уменьшалось в 2—3 раза, становилось по характеру серозным; к 8—10-му сеансу отмечалось сокращение остаточной полости до 2—3 мл, рассасывание инфильтрации легочной ткани с облитерацией бронхиального свища и ликвидацией полости эмпиемы или абсцесса легкого в среднем на 7 дней раньше, чем при лечении без применения лазеротерапии. В большинстве случаев для облитерации бронхоплеврального свища было достаточно 4—10 сеансов лазеротерапии и только у 4 больных с эмпиемой плевры, существовавшей более 1,5 мес, которым до лазеротерапии безуспешно проводилась временная окклюзия бронхов, потребовалось для облитерации свищей провести от 12 до 16 сеансов. Примером могут служить два наших наблюдения.
- Больная К., 9 лет, поступила в ДХО МОНИКИ на 13-е сутки от начала заболевания двусторонней острой гнойной деструктивной пневмонией и на 3-й — после дренирования плевральной полости слева в связи с развившимся пиопневмотораксом, повторных пункций плевральной полости справа с эвакуацией до 500 мл геморрагического выпота. При поступлении в клинику состояние ребенка очень тяжелое (рис. 7.9, а). Кожные покровы бледные, выраженный цианоз носогубного треугольника, значительная подкожная эмфизема левой половины грудной клетки. Одышка до 60 дыханий в 1 мин с участием вспомогательной мускулатуры. Дыхание слева выслушивается во всех отделах, жесткое. Справа перкуторно в области верхушки — коробочный звук, в аксиллярной и задненижних областях отмечается притупление, дыхание резко ослаблено. Пульс — 160 уд/мин, тоны сердца приглушены. АД 138/72 мм рт.ст. На рентгенограммах грудной клетки (рис. 7.9, б) при поступлении левое легкое расправлено, в нижних отделах — понижение прозрачности за счет наличия жидкости; справа — картина пиопневмоторакса, легочная ткань практически не определяется. Органы средостения несколько смещены влево. Произведено дренирование плевральной полости справа и смена дренажа слева. Назначена комплексная интенсивная терапия в условиях детского реанимационного отделения. Состояние оставалось тяжелым. Отмечалось отхождение гнойного содержимого из правой плевральной полости до 300 мл и левой — до 120 мл; имелось сильное продувание справа, слева — при кашле. Температура тела сохранялась высокой — до 38 °С; в легких выслушивались разнокалиберные влажные хрипы. Местно проводилась санация плевральных полостей антисептиками и чрескожное облучение крови инфракрасным лазером ("Узор") числом 6. Продувание по дренажу из левой плевральной полости прекратилось. В связи с сохраняющимся бронхиальным свищом справа на 8-е сутки поступления произведена бронхоскопия с временной окклюзией бронха поролоновой губкой, удаленной через
- сут. Свищ не закрылся, сформировалась остаточная полость до 30 мл (рис. 7.9, в). Начато облучение остаточной полости гелий-неоновым лазером через дренаж (суммарная доза 5,68 Дж/см2). Продувание исчезло после 6-го сеанса лазеротерапии; остаточная полость
- мл. После 9-го сеанса дренаж удален, легкое расправилось полностью; инфильтрация легочной ткани постепенно исчезла (рис. 7.9, г).
- Больной П., 12 лет, поступил в ДХО МОНИКИ на 9-й день заболевания пневмонией справа и 2-й день после дренирования плевральной полости в связи с возникшим пиопневмотораксом. Состояние ребенка очень тяжелое. Одышка до 60 в 1 мин, пульс 150 уд/мин. Дыхание справа резко ослаблено, в области верхушки выслушивались влажные мелкопузырчатые хрипы. На рентгенограммах грудной клетки — правое легкое коллабировано, определялся тотальный пиопнев- моторакс с наличием осумкованной жидкости (рис. 7.10, а, б). По дренажу из плевральной полости — гнойное отделяемое до 50 мл, отмечалось сильное продувание через дренаж. Проводилось интенсивное комплексное лечение. Состояние улучшилось, но ребенок высоко лихорадил, не уменьшалась остаточная полость эмпиемы, сохранялось сильное продувание. При фистулографии верографином на 18-й день лечения (рис. 7.10, в) выявлена полость с попаданием контрастного вещества в правое трахеобронхиальное дерево, что подтвердило наличие бронхиального свища. Начато ежедневное облучение полости гелий-неоновым лазером с разовой дозой 0,48 Дж/см2. Температура тела нормализовалась после 3-го сеанса, после 5-го сеанса ребенок переведен на короткий дренаж, свищ закрылся. После 7-го сеанса (суммарная доза 3,36 Дж/см2) дренаж удален, и через 2 дня ребенок выписан домой. На контрольной рентгенограмме грудной клетки (рис. 7.10, г, д) правое легочное поле без очагово-инфильтративных теней.
Общее воздействие лазерной терапии выражалось также достоверным увеличением количества лейкоцитов в периферической крови, которое сохранялось до конца курса лечения. Если средний исходный показатель числа лейкоцитов в основной группе и группе сравнения был 9,0±0,3109/л, то после первого сеанса облучения он составил соответственно 10,5+0,4 • 10-/л и 9,0±0,4 • 107л (t=2,5), а после окончания курса — 9,3+0,4^ 109/л и 8,1±0,5 • 10 /л (t=2,0). Достоверно повышенным после первого сеанса было и содержание сегментоядерных нейтрофилов, но к концу курса их число значительно ниже, чем в группе сравнения (44,6+2,2 • 109/л и 50,1+1,4 Ю9/л соответственно; t=2,l). Отмечен также достоверный рост СОЭ.
Следовательно, изменение показателей лейкограммы под влиянием лазерного излучения связано с некоторой активацией воспалительного процесса, на что указывает кратковременное повышение температуры тела, увеличение лейкоцитоза, нейтрофилеза и повышение СОЭ. Механизм так называемого обострения клинических проявлений заболевания после
- 2 сеансов лазерной терапии, по мнению В.И. Елисеенко (1997), связан с преимущественной активацией лишь артериального звена микроциркуляции, что приводит к усилению экссудативных процессов с развитием периваскулярного отека. При последующих сеансах лазерной терапии наступает активация венозного и лимфатического дренажа, что сопровождается разрешением экссудативной фазы воспаления и включением процессов клеточной пролиферации.
Нами также изучено влияние НИЛИ на состояние факторов АИР и калликреин-кининовой системы крови, являющейся одной из важных гуморальных систем, регулирующей гомеостаз и осуществляющей адаптационно-защитные реакции организма.
Реакцию организма на воспалительный процесс оценивали на основании следующих факторов системы АИР: уровня иммуноглобулинов классов А, М, G, содержания Т-лимфоцитов (Е-РОК) и Т-активных лимфоцитов (АЕ-РОК), ФА клеток
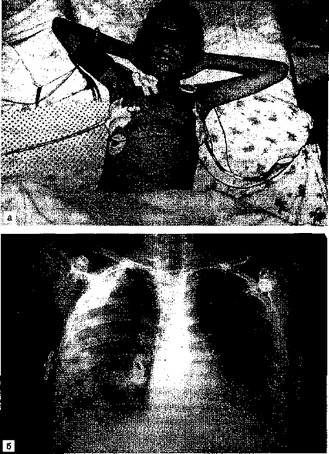
Рис. 7.9. Больная К., 9 лет. Двусторонняя деструктивная пневмония, пиопневмоторакс слева.
а — общий вид; б — обзорная рентгенография грудной клетки. Справа тотальное затенение всего легочного поля, слева картина пиопневмоторакса.
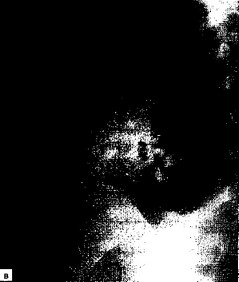
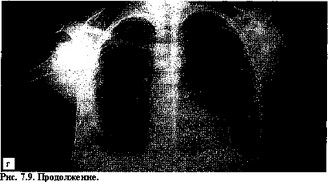 в — рентгенограмма грудной клетки с фистулофаммой (боковая проекция) на 18-й день лечения эмпиемы плевры до облучения остаточной полости гелий- неоновым лазером. Полость до 30 мл, бронхоплевральный свищ не закрылся; г — рентгенограмма грудной клетки после 9 сеансов внутриполостной лазерной терапии (перед выпиской). Правое легкое расправлено, небольшие плеврокостальные наложения в области латерального синуса.
в — рентгенограмма грудной клетки с фистулофаммой (боковая проекция) на 18-й день лечения эмпиемы плевры до облучения остаточной полости гелий- неоновым лазером. Полость до 30 мл, бронхоплевральный свищ не закрылся; г — рентгенограмма грудной клетки после 9 сеансов внутриполостной лазерной терапии (перед выпиской). Правое легкое расправлено, небольшие плеврокостальные наложения в области латерального синуса.
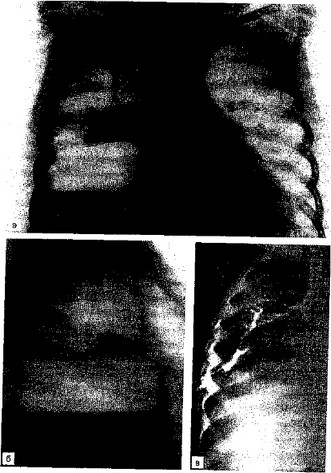
Рис. 7.10. Рентгенограммы грудной клетки. Тотальный пиопневмото- ракс справа и колабирование легкого у больного П.
а — прямая проекция; б — боковая проекция; в — фистулография. Попадание контрастного вещества в бронхиальное дерево.
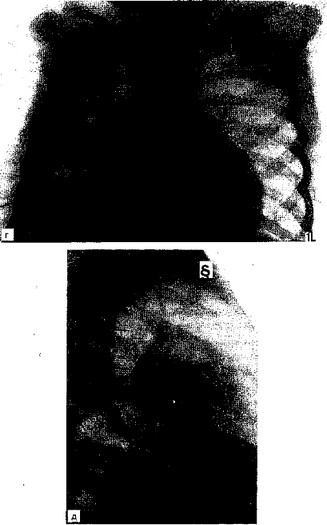
Рис. 7.10. Продолжение.
г, д — результат лазеротерапии. Полное расправление легкого перед удалением дренажа.
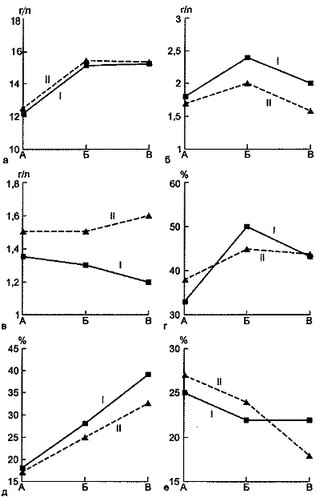
Рис. 7.11. Динамика некоторых показателей системы АИР под влиянием лазерной терапии у детей с острой гнойной деструктивной пневмонией.
крови с помощью латекс-теста и НСТ-теста. Интенсивность кининогенеза устанавливали с помощью колориметрического метода определения БАЭЭ-эстеразной активности трех форм кининобразующего фермента — калликреина (общего, связанного с ингибиторами, прекалликреина) и процента адсорбции калликреина на каолине (ПАКЛ).
Исследование показателей иммунитета, кининов и уровня МСМ проводили до лечения, через 7—10 дней, 3—4 нед, а в некоторых случаях — через 1—1,5 мес после лечения.
В зависимости от вида лечения выделены две группы больных: основная — 42 ребенка, получавших лазерную терапию, и группа сравнения — 40 детей, которые были идентичны по возрасту, исходному состоянию и объему комплексного лечения. Исследование иммунного статуса больных до лазерной терапии выявило нарушение во всех звеньях иммунной системы. Особенно отмечены снижение активности клеточного иммунитета, нарушение баланса иммуноглобулинов сыворотки крови, блокада фагоцитарной системы.
Более выраженным было влияние лазерной терапии на Т-систему иммунитета (рис. 7.11). Количество Т-РОК повышалось с 35 до 46 %, а Т-РОК-акт. с 18 до 39 %; в группе же сравнения содержание Т-РОК и Т-РОК-акт. было соответственно 34 и 33 %. Число В-лимфоцитов существенно не различалось в исследуемых группах. Под влиянием лазерной терапии происходила нормализация концентрации сывороточного IgG, что проявлялось снижением его количества с 20,1±3,0 до 12,4±2,5 г/л у 20 % детей, а у 30 % больных с исходно пониженным уровнем наблюдалось повышение до нормальных значений. Низкое у большинства больных содержание IgA под влиянием лазерной терапии нормализовалось лишь у 25 %, а повышенные (в 2—2,5 раза) показатели IgM снижались незначительно. Под действием лазерной терапии выявлена активация нейтрофильных гранулоцитов. Так, при проведении теста на восстановление нитросинего тетразолия отмечено резкое увеличение количества формазанположительных нейтрофилов с 2,3±0,7 % перед лазерной терапией до 25,3±0,6 % после 10-го сеанса ее (при норме 7,7±0,6 %), что определяет повышение окислительно-восстановительного потенциала фагоцитирующих клеток. Полученные данные позволяют заключить, что НИЛИ является фактором, преимущественно стимулирующим Т-систему иммунитета и фагоцитоз.
Результаты исследования калликреин-кининовой системы у больных с ГСЗ представлены в табл. 7.3.
а—динамика IgG; б — динамика IgM; в — динамика IgA; г — динамика гемолитического комплемента; д — динамика Т-РОК-акт.; е — динамика В-РОК: I — первая группа, II — вторая группа, А — до лазеротерапии, Б — после сеанса лазеротерапии, В — после курса лазеротерапии.
Таблица 7.3
Показатели кининогенеза при гнойно-септических заболеваниях у де
|
Кининоге- нез |
Лечение |
Гнойно септические заболевания |
Калликреин, моль/(сл) |
||
|
|
|
общий* |
|
||
|
|
|
|
1 |
2 |
3 |
|
Усилен |
Лазеро |
Остеомиелит |
25 787 |
33 834 |
41 167 |
|
(п=7) |
терапия |
(п=1) |
|
|
|
|
|
(п=4) |
Деструктив |
31 000± |
34 834± |
35 834± |
|
|
|
ная пневмо |
±1600 |
±1800 |
±1750 |
|
|
|
ния (п=3) |
|
|
|
|
|
Общепри |
Остеомиелит |
31 000± |
37 834± |
- |
|
|
нятое |
(п=3) |
±1650 |
±1900 |
|
|
|
(п=3) |
|
|
|
|
|
Ослаблен |
Лазероте |
Остеомиелит |
8000± |
16 000+ |
23 000± |
|
(п=7 5) |
рапия |
(п=16) |
±450 |
±820 |
±1300 |
|
|
(п=38) |
Перитонит |
11 2 0 0± |
18 600± |
24 000± |
|
|
|
(п=11) |
±670 |
±1100 |
±1300 |
|
|
|
Деструктив |
11 4 8 0 ± |
19 100± |
23 7 0 0± |
|
|
|
ная пневмо |
±620 |
±980 |
±1150 |
|
|
|
ния (п=11) |
|
|
|
|
|
Общепри |
Остеомиелит |
11 000± |
11 300± |
15 000± |
|
|
нятое |
(п=10) |
±570 |
±680 |
±780 |
|
|
(п=37) |
Перитонит |
10 000± |
16 000± |
21 000± |
|
|
|
(п=13) |
±590 |
±890 |
±1200 |
|
|
|
Деструктив |
11 580± |
15 0 5 0± |
19 100± |
|
|
|
ная пневмо |
±610 |
±770 |
±980 |
|
|
|
ния (п=14) |
|
|
|
|
Не изме |
- |
Практически |
24 000± |
- |
- |
|
нен (п=30) |
|
здоровые |
±1200 |
|
|
Примечание. ПАКЛ — показатель адсорбции калликреина на каолине; лазеротерапии. * Изменения статистически достоверны: рlt;0,05—0,01.
Из табл. 7.3 видно, что у 9—13 % обследованных больных ГСЗ протекали на фоне усиленного кининогенеза (повышения активности общего калликреина плазмы на 10—13 %, обусловленного значительным — больше 213—283 % — повышением содержания калликреина, связанного с ингибиторами, компенсирующим снижение на 45—68 % уровня прекалликреина).
В 87—92 % случаев ГСЗ протекали на фоне ослабленного на 48—58 % кининогенеза, обусловленного снижением на 64— 73 % уровня предшественника калликреина — прекалликреина — и на 20—48 % — калликреина, связанного с ингибиторами (р lt;0,05—0,01). Ослабление кининогенеза сопровождалось изменением его пространственной структуры, на что указывает 2,5—3,5-кратное повышение величины ПАКЛ. Глубина и сте-
|
|
Калликреин, |
моль/(сл) |
|
ПАКЛ, |
о. % |
|||
|
связанный с ингибиторами* |
прекалликреин |
|||||||
|
1 1 |
2 |
3 |
1 |
2 |
3 |
1 |
2 |
3 |
|
20 000 |
25 787 |
5787 |
31 934 |
8047 |
9233 |
8 |
15 |
10 |
|
21 000± |
27 83 4± |
27 83 4± |
10 000± |
7 0 0 0± |
8 0 00± |
11 |
14 |
14 |
|
±600 |
±1400 |
±1550 |
±360 |
±360 |
±420 |
|
|
|
|
23 000± |
31 934± |
|
8000± |
5900± |
- |
10 |
15 |
- |
|
±1200 |
±1600 |
|
±430 |
±340 |
|
|
|
|
|
3133± |
9 6 0 0± |
17 000± |
4867± |
6400± |
6000+ |
43 |
30 |
20 |
|
±170 |
±440 |
±880 |
±260 |
±340 |
±320 |
|
|
|
|
4800± |
10 300± |
14 000+ |
6400± |
83 00± |
10 000± |
53 |
30 |
24 |
|
±240 |
±620 |
±740 |
±340 |
±440 |
±560 |
|
|
|
|
5080± |
13 000^ |
17 000± |
6400± |
6100± |
67 0 0± |
40 |
25 |
18 |
|
±380 |
±720 |
±910 |
±280 |
±330 |
±350 |
|
|
|
|
4500± |
5000± |
8700± |
6500± |
6300± |
6300± |
46 |
37 |
27 |
|
±260 , |
±280 |
±460 |
±390 |
±380 |
±340 |
|
|
|
|
4600± |
7800± |
12 2 0 0± |
5400± |
8200± |
8800+ |
41 |
26 |
22 |
|
±250 |
±410 |
±660 |
±280 |
±440 |
±460 |
|
|
|
|
4380± |
7200± |
12 300± |
5400± |
7850± |
6800± |
41 |
26 |
22 |
|
±260 |
±380 |
±720 |
±280 |
±420 |
±390 |
|
|
|
|
6000± |
— |
_ |
18 000± |
_ |
_ |
15- |
_ |
_ |
|
±360 |
|
|
±900 |
|
|
18 |
|
|
1 - до лечения; 2 - через 5 сеансов лазеротерапии; 3 - через 10 сеансов
пень изменений всех параметров кининогенеза были различными и зависели от нозологической формы ГСЗ. Наиболее глубокая степень угнетения кининогенеза отмечалась при ОГО, а наиболее выраженное качественное изменение калликреина — при перитоните.
В процессе лечения традиционной терапией и лазером у всех больных ГСЗ вне зависимости от характера изменений кининогенеза (усилен, ослаблен) происходило его усиление, выражающееся в повышении активности общего калликреина. Степень активации кининогенеза зависела от исходного характера изменений этого процесса. У больных как основной, так и группы сравнения с исходно усиленным кининогенезом в процессе 2—4-недельного лечения активность общего калли- креина увеличивалась на 16—31 % вследствие повышения содержания на 30—33 % калликреина, связанного с ингибиторами. Величины ПАКЛ во все периоды обследования и лечения больных оставались нормальными.
При ГСЗ, сопровождающихся ослаблением кининогенеза, в процессе лечения также наступали активизация кининогенеза вплоть до его нормализации при лечении лазером и тенденция к нормализации при традиционной терапии. Повышение активности общего калликреина плазмы крови через 5 сеансов лазеротерапии соответствовало 100; 66; 66 %, а через 10 сеансов — 188; 114; 106 % при остеомиелите, перитоните и деструктивной пневмонии соответственно (р lt; 0,05—0,01). Нормализация ослабленного кининогенеза происходила за счет повышения уровня калликреина, связанного с ингибиторами (в основном тканевого происхождения). Наибольший прирост этой формы калликреина отмечался при остеомиелите — на 190 и 415 % после 5-го и 10-го сеанса лазеротерапии. Накопление данной фракции кининобразующего фермента продолжалось и через 1—1,5 мес после лазеротерапии (больше исходного на 567 %). Увеличение уровня калликреина, связанного с ингибиторами, в те же сроки лечения при перитоните и деструктивной пневмонии было менее выраженным и соответствовало 115 и 192% при перитоните и 150 и 235% при деструктивной пневмонии (р lt; 0,05—0,01). Содержание прекалликреина под влиянием лазерного излучения повышалось незначительно и было более выраженным при перитоните (больше исходного на 56 %). Тонким лабораторным показателем нормализации кининогенеза и эффективности лазеротерапии являлся ПАКЛ. Его величины в процессе лечения динамично снижались до нормы.
У больных группы сравнения в те же сроки лечения кини- ногенез оставался ослабленным. Повышение уровня калликреина, связанного с ингибиторами, в сроки, соответствующие
- му и 10-му сеансу лазеротерапии, было менее интенсивным и соответствовало 64 и 181 % при деструктивной пневмонии,
- и 93 % при остеомиелите, 70 и 165% при перитоните. Нормализации кининогенеза у больных группы сравнения не наступало. Сохраняющееся ослабление кининогенеза подтверждали остающиеся повышенными величины ПАКЛ.
Нормализации кининогенеза у больных основной группы, леченных при помощи лазера, соответствовало выраженное снижение эндогенного токсикоза. Заметно уменьшался уровень коротковолновой и длинноволновой фракций МСМ. Особенно благотворным было действие лазера на исходные показатели МСМ при деструктивной пневмонии и перитоните. Исходно завышенный на 52 % уровень длинноволновой фракции снижался наполовину после 5-го сеанса и практически нормализовался после 10-го сеанса данного лечения.
Показателем снижения интоксикации при лечении остеомиелита лазером являлось уменьшение до контрольных цифр уровня коротковолновой фракции. У пациентов группы сравнения сохранялся исходно повышенный на 25 % уровень коротковолновой фракции и на 62 % уровень длинноволновой фракции у больных перитонитом, а также на 30 % увеличенное содержание длинноволновой фракции у больных с деструктивной пневмонией (рlt;0,05—0,01). Сохранение эндогенного токсикоза подтверждалось устойчивым снижением среднемолекулярного коэффициента распределения МСМ.
Лазеротерапия уже через 1 нед способствовала значительному снижению содержания МСМ и полной нормализации их уровня через 2 нед после лазерной терапии. У больных группы сравнения сохранялся завышенный уровень МСМ. Отчетливая корреляция между статусом больного и содержанием в крови МСМ позволила предложить определение этих пептидов с целью прогнозирования течения гнойного процесса и возникновения рецидивов в различные сроки после оперативных вмешательств.
Ослабленному кининогенезу соответствовала эндогенная интоксикация, обусловленная повышением содержания обеих фракций МСМ — на 21—55 % коротковолновой и на 14—62 % — длинноволновой. Наиболее резкое повышение уровня МСМ отмечено у больных перитонитом и деструктивной пневмонией. При этих формах ГСЗ повышалась концентрация как длинноволновой, так и уровень коротковолновой фракции. Остеомиелит характеризовался преимущественным увеличением коротковолновой фракции МСМ (табл. 7.4).
Полученные нами данные о характере изменений кининогенеза и ' уровня МСМ при ГСЗ согласуются с данными литературы. В отношении состояния калликреин-кининовой системы крови и ее ключевого фермента — калликреина — отмечается двухэтапность изменений ее активности [Капитаненко А.М., Дочкин И.И., 1988]. В ранние сроки происходит активация системы, в более поздние — истощение ее [Суровикина М.С. и др., 1995]. Угнетение калликреин-кининовой системы объясняют гиперпротеолизом вследствие гидролитического действия на прекалликреин, калликреин и фактор Хагемана (XII фактор свертывания, являющийся активатором прекалли- креина) более сильных клеточных протеиназ (эластазы, трип- тазы, химазы, катепсина G), поступающих в кровоток при альтерации клеток. Это приводит к различным осложнениям вследствие срыва адаптивных реакций калликреин-кининовой системы на повреждение. Большой процент больных ГСЗ, у которых мы обнаружили значительное ослабление системного кининогенеза, можно связать с поздним (через 2—4 нед от начала возникновения патологического процесса) поступлени-
Уровень молекул средней массы до и после лечения гнойно-септических (оп. ед. М±т)
|
Лечение |
Гнойно септическое заболевание |
|
Д 254 нм* |
|
|
|
1 |
2 |
3 |
|
|
Лазеротера |
Остеомиелит |
0,291±0,03 |
0,258±0,025 |
0,250±0,022 |
|
пия (п=28) |
(п=7) Перитонит |
0,330±0,025 |
0,220±0,015 |
|
|
|
(п=13) Деструктив |
0,371+0,03 |
0,270±0,025 |
|
|
Общепри |
ная пневмония (п=8) Перитонит |
0,30±0,025 |
0,30+0,02 |
|
|
нятое (п=16) |
(п=11) Деструктив |
0,30±0,03 |
0,268+0,02 |
0,261+0,02 |
|
Практичес- |
ная пневмония (п=5) |
|
0,24±0,02 |
|
ки здоровые
(п=25)
Примечание. 1 — до лечения; 2 — через 5 сеансов лазеротерапии; тистически достоверны: р lt; 0,05—0,01.
ем больных в клинику и действием на кининобразующий фермент упомянутых клеточных протеиназ.
Наши многолетние исследования характера изменений кал- ликреин-кининовой системы крови и их клинической значимости при разнообразных воспалительных процессах у детей свидетельствуют о срыве адаптационных функций этой системы и о более неблагоприятном патогенетическом значении фазы ослабленного кининогенеза, так как развиваются более резкие изменения биохимического гомеостаза. В данной монографии это заключение получило прямое подтверждение: выявлено сочетание ослабленного кининогенеза и выраженного повышения в кровотоке содержания обеих фракций МСМ. Состояние умеренно усиленного кининогенеза (повышение активности общего калликреина порядка 30—50 %) является благоприятным фактором, предотвращающим изменения гомеостаза. Результаты наших исследований доказывают, что изменение кининогенеза составляет важное звено развития ГСЗ у детей. Патогенетическое значение имеет фаза ослабленного кининогенеза, поскольку кинины частично или полностью выключаются из числа пептидных регуляторов гомеостаза. Ослабление кининогенеза ведет к нарушению адаптационно-защитной функции калликрен-кининовой системы крови и спо-
|
|
Д 280 нм* |
|
К (Д 254/Д 280) |
||
|
1 |
2 |
|
1 |
2 |
3 |
|
0,240+0,02 |
0,234+0,02 |
0,225+0,02 |
1,43 |
1,103 |
1,111 |
|
0,32+0,03 |
0,240+0,018 |
- |
1,031 |
0,917 |
- |