Детальность пациентов после ТМАР
Как уже отмечалось, во время операции и в раннем послеоперационном периоде не было зафиксировано летальных случаев среди пациентов, перенесших ТМЛР. В отдаленном послеоперационном периоде наблюдались все пациенты из числа перенесших лазерное воздействие. Сроки наблюдения составляли от 3 мес. до 3 лет. За этот период умерло 5 (12,2%) пациентов. При этом от кардиальных причин погибли 3 пациента, от внесердечных причин - 2 больных. Рассмотрим данные случаи более подробно.
В группе больных, умерших от кардиальных причин, фактором смерти был инфаркт миокарда. Из них один больной умер через 1 год после оперативного вмешательства, двое - через 2 года. Все больные перенесли сочетанную операцию АКШ и ТМЛР В группе больных, погибших от внекардиальных причин, в одном случае фактором смерти было острое нарушение мозгового кровообращения через год после оперативного вмешательства. В другом случае отмечено прогрессирование нарушения кровообращения нижних конечностей на фоне декомпенсированного сахарного диабета, что привело к гангрене нижних конечностей, а затем и к смерти больного через 6 месяцев после изолированной лазерной реваскуляризации миокарда.
Следовательно, большая часть погибших пациентов (4 из 5) перенесла сочетанную операцию АКШ и ТМЛР, что соответствует удельному весу данных сочетанных вмешательств в общей структуре операций с использованием лазера.
Структура смертности после ТМЛР представлена на рисунке 4.9.
Полученные данные не позволили отметить значительных отклонений от общемировой статистики касательно выживаемос-
ГЛАВА 4. Трансмиокардиальная лазерная реавскуляризация...
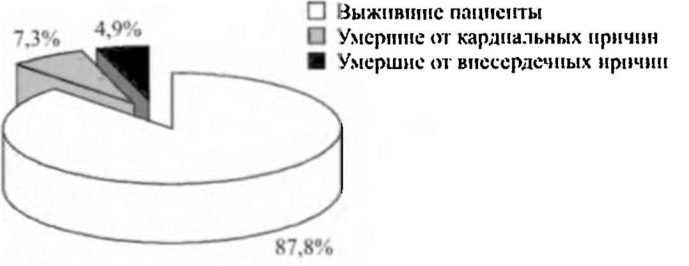
Рис. 4.9. Структура смертности после ТМАР
ти больных после ТМЛР и (или) АКШ, что позволяет говорить о ТМЛР при помощи полупроводникового лазера как о методе, который не ухудшает прогноз смертности в отдаленном послеоперационном периоде как относительно методов прямой реваскуляризации, так и относительно других лазерных систем [91,157, 182, 226, 230].
В качестве наиболее полноценного примера целесообразно привести ТМЛР, применявшуюся для лечения больного ИБС как единственный метод оперативного лечения и соответственно как главный фактор дальнейших клинических изменений.
Пример 4. Больной С., 52 года (ИБ № 5280), поступил в КХО ГУ НИИ кардиологии ТНЦ СО РАМН 18.11.2003 г. Основной диагноз: ИБС. Стенокардия напряжения III ФК. Постинфарктный кардиосклероз (05.98 г.; 08.98 г.; 2000 г.). Атеросклероз аорты, коронарных артерий. Постинфарктная аневризма Л Ж. Состояние после маммарокоронарного шунтирования передней нисходящей артерии, аортокоронарного шунтирования ветви тупого края, правой коронарной артерии от 11.1998 г. Не функционирующий шунт к ветви тупого края, окклюзия ветви тупого края, субтотальный стеноз огибающей артерии, стеноз 75% второй диагональной артерии в устье. HI. NYHA III ст.
Фоновое: гипертоническая болезнь II ст., риск 4.
Сопутствующие: язвенная болезнь ДПК вне обострения; состояние после лапаротомии по поводу желудочного кровотечения в 1998 г.
Пациент прошел алгоритм обследования и подготовки к
ТМЛР. При проведении велоэргометрии на толерантность к физической нагрузке отмечен показатель 50 Вт; причиной прекращения послужило мышечное истощение, головокружение, патологическое отклонение ST (депр. ST V5_6 до 130 мВ по мони- торированию).
При выполнении сцинтиграфии миокарда с таллием-199 выявлены стабильный дефект перфузии в области верхушки и переднеперегородочной области ЛЖ (25%), преходящая гипоперфузия базальных отделов переднеперегородочной стенки ЛЖ
(7%).
По данным коронарошунтографии: тип кровоснабжения миокарда - правый. Функционирующие шунты к ПНА (МКШ) и ПКА (АКШ). Нет шунта к ВТК, окклюзия ВТК, субтотальный стеноз ОА, стеноз 75% 2 ДА в устье. Дополнительно выполнялась спиральная компьютерная томография, ангиография сердца: состояние после аортомаммарокоронарного шунтирования. МКШ и АКШ на ПКА проходимы. АКШ на ОА облитерирован (рис. 4.10).
По результатам проведенного обследования выполнена опе-
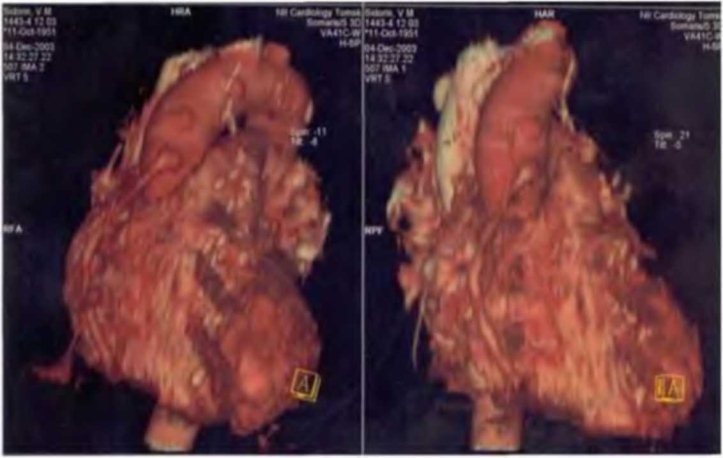
Рис. 4.10. Спиральная компьютерная томография, ангиография
сердца больного С,
рация: трансмиокардиальная лазерная реваскуляризация миокарда на область заднебоковой стенки левого желудочка (100 лазерных каналов) без ИК из левосторонней торакотомии. Послеоперационный период протекал без осложнений. Заживление послеоперационной раны первичным натяжением. Клинически функциональный класс стенокардии после операции I ФК. При проведении велоэргометрии на толерантность к физической нагрузке отмечен показатель 55 Вт; причиной прекращения послужили мышечное истощение, одышка. При выполнении сцинтиг- рафии миокарда с таллием-199 отмечена стабильность дефектов перфузии миокарда.
При обследовании через год после операции клинически функциональный класс стенокардии сохранялся I ФК. При проведении велоэргометрии на толерантность к физической нагрузке отмечен показатель 65 Вт; причиной прекращения послужило учащенное сердцебиение. При выполнении сцинтиграфии миокарда с таллием-199 выявлены стабильный дефект перфузии в области верхушки и переднеперегородочной области ЛЖ (17%), преходящая гипоперфузия средних и базальных отделов переднеперегородочной стенки ЛЖ (20%).
Через 3 года после ТМЛР функциональный класс стенокардии сохранялся на уровне I ФК. При проведении велоэргометрии на толерантность к физической нагрузке отмечен показатель 60 Вт; причиной прекращения послужило мышечное истощение. При выполнении сцинтиграфии миокарда с таллием-199 выявлены стабильный дефект перфузии в области верхушки и переднеперегородочной области ЛЖ (15%), преходящая гипоперфузия средних и базальных отделов переднеперегородочной стенки ЛЖ (20%).
При выполнении ультразвукового исследования сердца, что характерно, отмечалось увеличение сократимости облученных зон миокарда левого желудочка до 12 мес. после операции, в то время как через 3 года динамики по сравнению с предыдущим исследованием не отмечено.
Данный клинический пример демонстрирует, что при операции изолированной ТМЛР, когда отсутствовали другие существенные факторы воздействия на клиническую ситуацию, отмечалась положительная динамика в послеоперационном периоде.
На основании полученных данных можно сделать заключение, что алгоритм по отбору больных ИБС с нешунтабельными коронарными артериями адекватен. Учитывая данные по осложнениям и смертности в послеоперационном периоде, процедуру ТМЛР можно признать относительно безопасной.
Динамика, наблюдавшаяся в различные сроки обследования пациентов после операции, демонстрирует постепенное улучшение показателей со стабилизацией через 12мес. после ТМЛР. А сопоставление полученных нами во время экспериментальной части работы данных с клинической частью позволяет с большой вероятностью говорить о сходных процессах, протекающих в облученных участках миокарда, а именно процессах формирования неососудов по периферии лазерных каналов. Очевидно, что именно данный механизм лежит в основе изменений, отмеченных в процессе обследования больных.