Результаты спектрометрии стенки аорты в норме и при патологии
Целью работы явился анализ полученных в ходе выполнения исследования спектров поглощения падающего света нормальной аорты и пораженной атеросклерозом стенки аорты человека. При этом особое внимание уделялось выявлению отличий оптической плотности на пиках поглощения интактной аорты человека и атеросклеротической бляшки, что послужит диагностическим критерием при облучении указанных структур внутри сосуда.
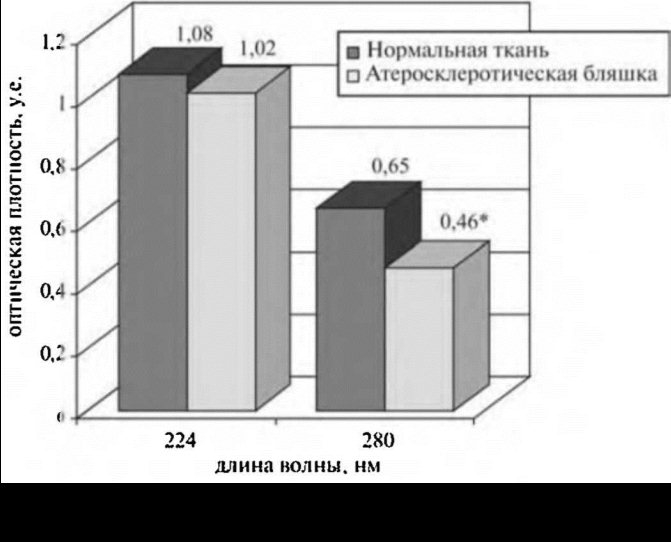
При сопоставлении спектров поглощения неизмененной аорты человека и атеросклеротической бляшки наблюдаются два характерных максимума оптической плотности при длинах волн 224 и 280 нм. Первый максимум более высокий и соответствует оптической плотности 1,08±0,043 для нормальной ткани и 1,02±0,032 для атеросклеротической бляшки (без дифференцирования по типам бляшек). Сравнивая средние показатели с использованием непараметрического критерия Вилкоксона, достоверного отличия не обнаружено, следовательно, дальнейшее исследование поглощения света тканью стенки аорты на данной длине волны (224 нм) проводить нецелесообразно.
При подходе ко второму максимуму кривая I (рис. 2.3), соответствующая спектру поглощения в ультрафиолетовой области нормальной стенки аорты, полого опускается и формирует второй пик, который и представляет наибольший интерес и соответствует длине волны 280 нм. При этом оптическая плотность нормальной ткани составляет 0,65±0,02. Вторая кривая, соответствующая спектру поглощения ткани, пораженной атеросклерозом, опускается более круто и формирует максимум при той же длине волны и оптической плотности 0,46+0,02 (табл. 2.2).
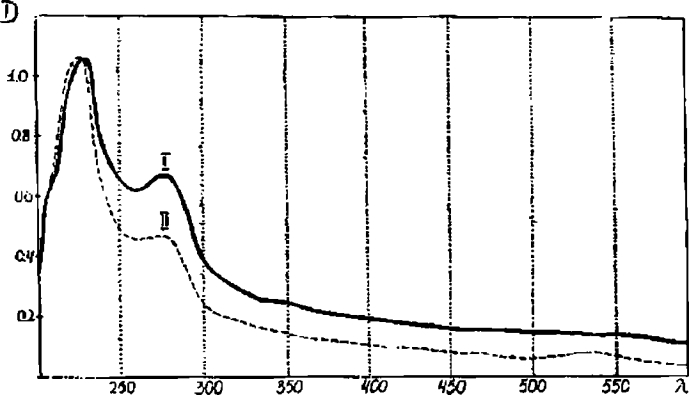
Рис. 2,3. Спектры поглощения в ультрафиолетовой области: I — нормальная стенка аорты; II — атеросклеротическая
бляшка
Таблица 2.2
Показатели оптической плотности D ткани стенки аорты в ультрафиолетовой области спектра
|
Тип ткани |
Длина волны |
|
|
|
|
224 нм |
|
280 нм |
|
Нормальная стенка аорты |
1,08±0,043 |
|
0,65±0,02 |
|
Атеросклеротическая бляшка |
1,02±0,032 |
|
0,46+0,02* |
Примечание: Х±х; * - рlt;0,05.
Характер поглощения на графиках примерно одинаков на подъемах и спусках. В первом случае кривая спектра поглощения снижалась до величины оптической плотности, равной 0,12+0,004, а во втором - до 0,03±0,035. Уже первые данные позволили предположить, что разница между этими величинами будет достаточно существенной. Данное предположение подтвердилось после математической обработки с использованием непараметрического критерия Вилкоксона с высокой степенью достоверности (рlt;0,001).
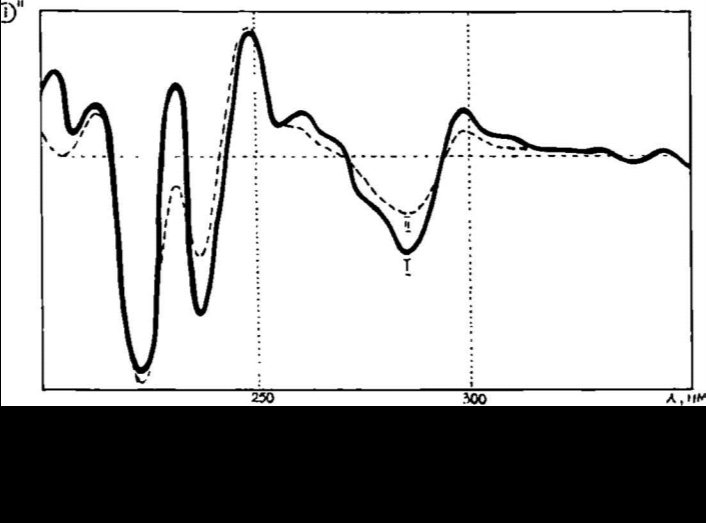
График второй производной оптической плотности, соответствующий скорости поглощения света веществом и описывающий характер поглощения, более детально демонстрировал мелкие нюансы спектра, которые на графике оптической плотности мало заметны, а также позволил более точно определить длину волны, которой соответствовали полученные максимумы поглощения (рис. 2.4).
То. на спектрах поглощения в ультрафиолетовой области (280 нм) нормальной аорты и пораженной атеросклерозом стенки аорты наблюдалось статистически достоверное снижение оптической плотности ткани бляшки на 30% по сравнению с интактной тканью стенки аорты (рис. 2.5).
Настоящая часть исследования посвящена анализу полученных в ходе исследования спектров отражения интактной аорты и аорты, находящейся в различных фазах атеросклеротического процесса. Последние позволили установить диагностические параметры отличий нормальной и пораженной атеросклерозом стенки аорты.
Отражение поверхности нормальной сосудистой стенки и атеросклеротических бляшек было измерено с помощью спектрофотометрической установки в диапазоне длин волн 280 нм - 1 мкм.
Полученный в результате измерения график зависимости интенсивности отражения от длины волны падающего излучения (спектр отражения) для удобства анализа был разбит на 2 области: отражение в ультрафиолетовом диапазоне спектра (300— 450 нм) и отражение в видимом диапазоне спектра (450-800 нм).
На спектрах отражения в ультрафиолетовом диапазоне обнаружено две характерные области:
- первая область спектра лежит в диапазоне 300-335 нм, где все образцы отражали менее 10% падающего излучения;
- во второй области спектра, которая лежит в диапазоне 400- 435 нм, нормальная стенка аорты имеет коэффициент отражения в среднем 38-40%, в то время как коэффициент отражения атреосклеротической бляшки (независимо от ее типа) варьирует от 10 до 40%.
Очевидно, что статистически значимой разницы в отражении атеросклеротической бляшки и нормальной ткани в данной области спектра не существует.
Многообещающей областью спектра для использования лазерной энергии с хирургическими целями является видимый диапазон длин волн 520-770 нм (рис. 2.6). Здесь различия в поведении спектров отражения атеросклеротических бляшек и нормальной ткани очень сильные и тонкие.
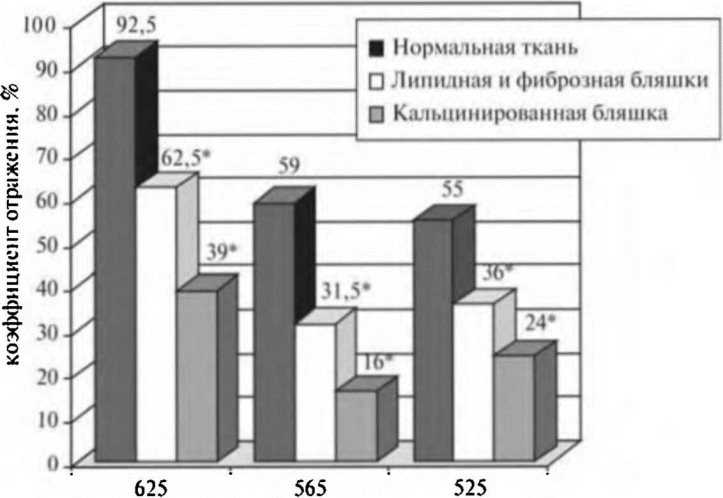
На спектрах отражения в видимом диапазоне существуют следующие характерные пики: первый пик соответствует длине волны 625 нм. Здесь нормальная ткань стенки аорты отражает в среднем 92,5+2,5% падающего света; образцы с липидными и фиброзными бляшками - 62,5+2,5%, а коэффициент отражения образцов с кальцинированными бляшками составляет 39,0±1,0%; следующий пик отражения соответствует 565 нм. Здесь нормальная ткань стенки аорты отражает в среднем 59,0±1,0% падающего излучения; липидные и фиброзные бляшки, составляющие одну группу, - 31,5+1,5%, а образцы с кальцинированными бляшками - 16,0+1,0% падающего света; пос-
2.1. Спектральные характеристики стенки аорты в норме и при атеросклерозе
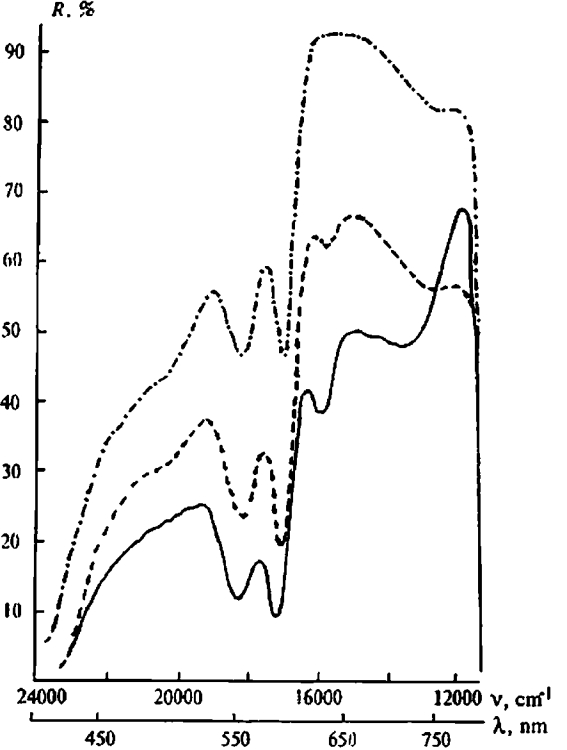
Рис. 2.6. Различные спектры отражения в диапазоне 430 — 760 им. Примечание: нормальная ткань — штрих пунктир мая линия; липидная и фиброзная бляшки - пунктирная линия; кальцинированная бляшка — сплошная линия.
ледний пик располагается в области 525 нм. По прежнему выраженным является коэффициент отражения нормальной ткани - 55,0±0,5%; образцы с липидными и фиброзными бляшками, составившими также одну группу отражают, в среднем 36,0+1,0% падающего света, кальцинированные бляшки показывают отражение незначительной интенсивности - 24,0±1,0% падающего
Таблица 2.3
Показатели коэффициента отражения R (%) ткани стенки аорты в видимой области спектра
|
Тип ткани |
Длина волны, нм |
||
|
|
625 |
565 |
525 |
|
Нормальная ткань |
92,5±2,5 |
59,0±1,0 |
55,0±0,5 |
|
Липидная и фиброзная бляшки |
62,5±2,5* |
31,5±1,5* |
36,0±1,0* |
|
Кальцинированная бляшка |
39,0±1,0* |
16,0±1,0* |
24,0±1,0* |
Примечание: Х±х; * - рlt;0,05.
света. Все различия между средними показателями отражения групп статистически достоверны при рlt;0,05 (табл. 2.3).
Очевидно, что во всех исследуемых спектральных точках ви
лл мна волны, нм
Рис. 2.7. Коэффициент отражения ткани стенки аорты в видимой области спектра. * — рlt;0,05
димого диапазона интенсивность отражения образцов нормальной стенки аорты на 30-70% больше, чем аналогичный показатель для образцов с визуально определявшимися атеросклеротическими поражениями (рис. 2.7).
Для полноты спектральной картины интактной и пораженной атеросклерозом стенки аорты необходимы запись и изучение спектров их флюоресценции, т.е. способности ткани и молекулярных структур стенки аорты излучать в ответ на возбуждение ее светом определенной длины волны [39, 56]. При проведении анализа спектров флюоресценции были выделены следующие группы образцов ткани: нормальная, непораженная атеросклерозом ткань стенки аорты; фиброзные и липидные бляшки, составляющие одну группу; кальцинированные бляшки. Типичные спектры флюоресценции нормальной ткани, липидных и фиброзных бляшек, а также кальцинированных бляшек в диапазоне 380- 650 нм представлены на рисунке 2.8.
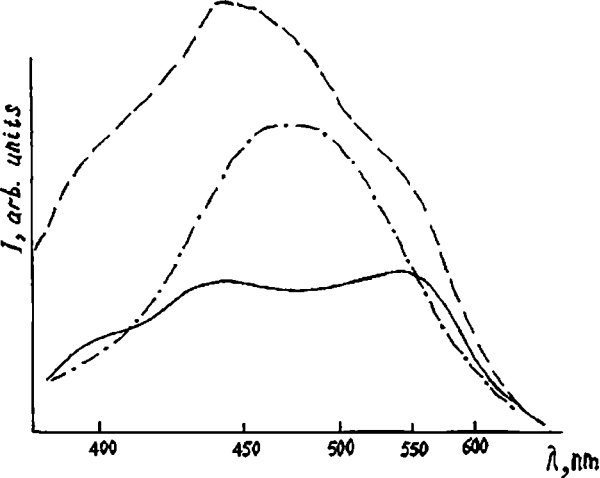
Рис. 2.8. Различные спектры флюоресценции в диапазоне 380 — 650 нм. Примечание: нормальная ткань — штрихпунктир- ная линия; липидная и фиброзная бляшки — пунктирная линия; кальцинированная бляшка — сплошная линия
За характеристику отличия выбрано отношение интенсивностей флюоресценции нормальной и пораженной атеросклерозом ткани стенки аорты для оптимальных длин волн: 440 и 470 нм (J440/J470), а также 500 и 570 нм (J500/J570), измеренное при одинаковой длине волны возбуждения. Для нормальной ткани J440/J470 составляет в среднем 0,843+0,042, a J500/J570 -0,29+0,051, вто время как для фиброзной и липидной бляшек зти показатели составили соответственно 1,19±0,035 и 0,56±0,012. Кальцинированная бляшка характеризовалась следующими показателями: J440/J470 - 0,39±0,035, J500/J570 - 0,42±0,021 (табл. 2.4). Все выявленные различия статистически достоверны при рlt;0,05 (рис. 2.9).
То. не принимая во внимание результаты, полученные при исследовании спектров флюоресценции кальцинированных бляшек, следует отметить, что если параметр J440/J470 lt; 1, то зто указывает на нормальную ткань стенки аорты. Однако если J440/J470 gt; 1, то речь может идти о наличии повреждения ткани липидной или фиброзной бляшкой. В случаях же, когда J440/ J470 = 1, нужно думать о переходе между нормальной тканью и развивающимся атеросклеротическим повреждением.
Атеросклероз, как было показано, представляет собой сложный динамический процесс, состоящий из нескольких стадий, в результате которых стенка аорты претерпевает глубочайшие изменения. В долипидную стадию в стенку проникают глобулины,
Таблица 2.4
Показатели интенсивности флюоресценции J
ткани стенки аорты
|
Тип ткани |
Длины волн, нм |
|
|
|
440/470 |
500/570 |
|
Нормальная ткань |
0,843+0,042 |
0,290±0,051 |
|
Липидная и фиброзная бляшки |
1,190±0,035* |
0,560±0,012* |
|
Кальцинированная бляшка |
0,390+0,035* |
0,420±0,02Г |
Примечание: Х±х; * - рlt;0,05.
2.1. Спектральные характеристики стенки аорты в норме и при атеросклерозе
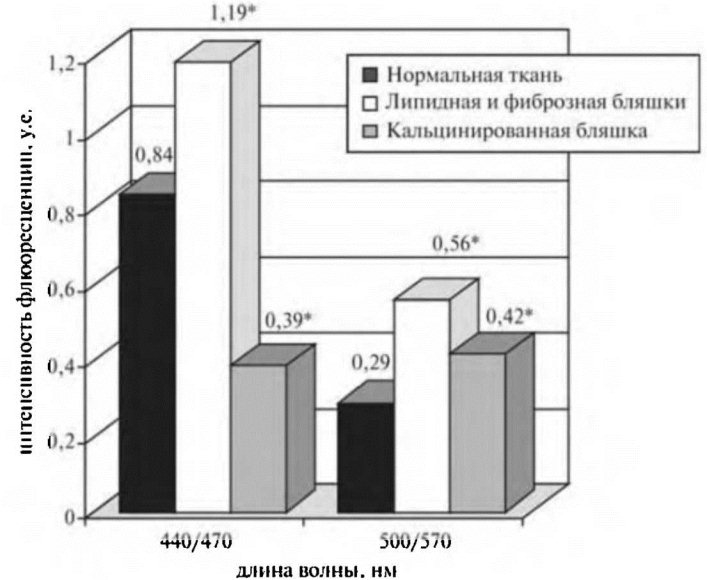
Рис. 2.9. Интенсивность флюоресценции ткани стенки аорты.
* — рlt;0,05
альбумины, фибриноген, липиды, холестерин и эфиры холестерина, содержащие жирные кислоты [6, 41].
В стадию липоидоза в интиме содержится большое количество липидов, распадающихся мукополисахаридов, на которые стенка сосудов реагирует разрастанием соединительной ткани. В стадию липосклероза образуется плотная липосклеротическая бляшка. В дальнейшем происходит усиление склероза, распад белковых и липидных масс, т.е. образуется детрит. При микроскопическом исследовании основным компонентом фиброзной бляшки являются гладкомышечные клетки, которые в большом количестве накапливаются в интиме с различной степенью отложения липидов как внутри клеток, так и во внеклеточном пространстве. Между гладкомышечными клетками вплетаются коллаген, эластические волокна и гликозаминогликаны, количество
которых также может варьировать, поэтому роль гладкомышечных клеток в утолщении интимы определяется не только их размножением и миграцией, но и синтезируемыми ими продуктами. Скапливающиеся в интиме гладкомышечные клетки, макрофаги, тучные клетки и межклеточное вещество образуют куполообразную фиброзную капсулу, покрывающую глубоко расположенные остатки погибших клеток (детрит) и внеклеточные отложения липидов [5, 22, 25, 41].
В связи с этим можно предположить, что детрит и кристаллический холестерин, инфильтрируя сосудистую стенку, снижают оптическую плотность ткани и поглощают свет меньше, чем в норме. Данное предположение основано на том, что холестерин и его фракции, деформируя молекулярную структуру стенки аорты, снижают ее способность к поглощению квантов света, поскольку известно, что чем менее упорядочена молекулярная структура ткани, тем слабее она поглощает свет [56]. Именно этим, по нашему мнению, обусловлены те характерные изменения, которые наблюдались на спектрах поглощения падающего излучения, записанных с нормальной ткани стенки аорты и пораженной атеросклерозом (липидные и фиброзные бляшки).
В экспериментальную группу при регистрации спектров отражения и флюоресценции вошли, наряду с липидной и фиброзной бляшками, кальцинированные бляшки. Атерокальциноз - завершающая стадия морфогенеза атеросклероза, хотя отложение извести начинается уже в стадии атероматоза и даже липос- клероза. Известь откладывается в атероматозные массы, фиброзную ткань и в межуточное вещество между эластическими волокнами. При значительных отложениях извести в покрышке бляшки образуются плотные и ломкие пластинки. Обызвествлению бляшек способствует зластолиз. В связи с деструкцией эластических мембран происходит накопление аспарагиновой и глутаминовой кислот. Ионы кальция связываются со свободными карбоксильными группами этих кислот и осаждаются в виде фосфата кальция [5, 22, 41].
То. основные стадии морфогенеза атеросклероза нашли свою интерпретацию в спектральных характеристиках, полученных в результате экспериментов. Например, совершенно очевидно, что степень отражения света от поверхности нор- мальнои стенки аорты и пораженной атеросклерозом различна. Причем, чем выше плотность исследуемой ткани, тем меньше света она отражает, что подтверждается и литературными данными [56]. Данный вывод нашел подтверждение также в нашем исследовании при регистрации спектра отражения. Нормальная ткань стенки аорты имела максимальную интенсивность отражения, в то время как наиболее плотная среда (кальцинированная бляшка) основную долю падающего света поглощала.
Наши результаты, полученные с помощью записи спектров флюоресценции [87], позволили нам утверждать об отличии степени флюоресценции нормальной и пораженной атеросклерозом ткани стенки аорты. Действительно, чем выше содержание в ткани липидов, холестерина и его эфиров, тем сильнее она люми- несцирует, поскольку указанные вещества, по данным литературы, обладают этой способностью в выраженной степени [53, 56, 89]. Принимая во внимание вышеуказанное обстоятельство, можно предположить, что наибольшим показателем флюоресценции будут обладать липидная и фиброзная бляшки, в меньшей степени - нормальная ткань, и совсем слабо будет люминесциро- вать кальцинированная бляшка, что и подтвердилось при записи спектров флюоресценции в эксперименте.
Т.о. полученные данные комплексного спектроскопического исследования указывают на перспективу использования для лазерной ангиопластики спектрального диапазона 520-770 нм (красная область спектра), где определяются наибольшие различия в поведении спектров отражения нормальной и пораженной атеросклерозом ткани стенки аорты. Возможно, в этой области происходит наиболее эффективное разрушение ткани атеросклеротической бляшки при минимальном повреждении окружающей нормальной ткани. Здесь наиболее перспективны лазеры на основе рубина и александрита.
Кроме того, спектральные характеристики аорты человека позволяют различать морфологические типы атеросклеротического поражения аорты между собой, а также отличать нормальную стенку аорты от пораженной атеросклерозом. Это позволяет проводить внутрисосудистую спектральную диагностику типа атеросклеротического поражения сосуда с последующим выбором оптимальных параметров лазера для осуществления эффек
тивной реканализации путем точной доставки лазерной энергии к месту поражения