Энтеральное введение
Энтеральный путь введения лекарственных веществ является наиболее распространенным. Он используется как для местной терапии органов пищеварительного тракта, так и для системного введения препаратов. Все рассматриваемые ниже закономерности относятся к последнему случаю.
С одной стороны, энтеральное введение обычно не требует участия медицинского персонала и наиболее комфортно для пациента. Как правило, при энтеральном пути введения вероятность возникновения побочных эффектов лекарственной терапии наименьшая. С другой стороны, при энтеральном назначении препаратов их фармакокинетика (а следовательно, и терапевтический эффект) подвержена наибольшим изменениям. Это связано как с особенностями функционирования желудочно-кишечного тракта (скорость эвакуации химуса и процессов всасывания из него, интенсивность местного кровотока, сопутствующие заболевания и т. д.), так и с возможностью разрушения большого количества лекарственных веществ. В желудочно-кишечном тракте ЛВ могут разрушаться или инактивироваться под влиянием:
Основные достоинства и недостатки энтерального введения лекарственных веществ суммированы в табл. 1.10.
Преимущества и недостатки энтерального пути введения лекарственных веществ
Сублингвальное и суббукальное введение
Сублингвальное (под язык) и суббукальное (защечное) введение лекарственных веществ основано на том факте, что слизистая оболочка ротовой полости имеет обильное кровоснабжение, особенно в области языка и его корня. Такое введение лекарственных препаратов обычно обеспечивает их быстрое поступление в системный кровоток (минуя печень) с высокой
степенью биодоступности и, соответственно, быстрое развитие терапевтических эффектов.
ПРИМЕР. При сублингвальном введении нитратов их максимальная концентрация в крови достигается в течение 1—2 мин40. При сублингвальном применении пропранолола его биодоступность в 3 раза выше, чем при пероральном41. Сублингвально вводят нифедипин, клонидин для купирования гипертонического криза, глицин — для нормализации мозгового кровотока. Большинство гомеопатических препаратов применяется сублингвально или суббукально.
Основные препараты для сублингвального и суббукального применения указаны в табл. 1.11. Как следует из таблицы, эти препараты относятся к разным фармакологическим группам и имеют различные спектры терапевтического действия.
При сублингвальном или суббукальном введении препаратов важно равномерно и полностью рассасывать соответствующую лекарственную форму, иначе уменьшается поступление лекарственного препарата в кровь и снижается эффективность терапии.
К сожалению, не все препараты для энтерального введения всасываются в ротовой полости. Обычно при сублингвальном введении в системный кровоток поступают неорганические соли, моносахара, аминокислоты и другие низкомолекулярные органические соединения.
Сублингвальный и суббукальный пути введения имеют ограничения при наличии любых воспалительных заболеваний ротовой полости. Кроме того, при длительном применении некоторые препараты могут сами индуцировать раздражение слизистой оболочки ротовой полости.
Ректальное введение
Прямая кишка имеет богатое кровоснабжение и развитую капиллярную сеть. Причем через нижние ректальные вены кровь от прямой кишки попадает в нижнюю полую вену, минуя портальную вену печени (v. portae). При ректальном введении лекарственных веществ отсутствует эффект первого прохождения через печень (см. гл. 3), приводящий к модификации и инактивации большого количества лекарственных препаратов. Часто ректально вводят ЛВ, инактивирующиеся печенью*. Кроме того, ректальное введение позволяет избежать механического раздражения лекарственной формой слизистых оболочек желудка. Ректальное введение также можно использовать при затруднении или невозможности перорального приема, например, при сужении пищевода или же у детей.
Благодаря богатому кровоснабжению слизистой оболочки прямой кишки, при ректальном введении лекарственные вещества быстро поступают в системный кровоток. Отсутствие процесса инактивации поступивших веществ в печени обеспечивает их высокую концентрацию, что приводит к быстрому развитию терапевтического эффекта.
ПРИМЕР. Так, при ректальном введении парацетамола его биодоступность выше и максимальная концентрация препарата в крови достигается быстрее, а анальгетический эффект сохраняется дольше, чем при пероральном применении42. Ректальное введение парацетамола приводит к более длительному сохранению его эффекта у детей, чем перо- ральное43. При ректальном введении морфина животным фармакокинетические параметры оказались сравнимы с таковыми при внутримышечном применении препарата44.
Лекарственные препараты для ректального введения достаточно распространены (табл. 1.12). Видно, что ректально применяются ЛВ, относящиеся к различным фармакологическим группам. Ректальное введение нестероидных противовоспалительных средств и ряда других лекарственных веществ позволяет избежать раздражающего действия на слизистые оболочки желудка.
К недостаткам ректального введения лекарственных средств можно отнести: неудобство применения, индивидуальную вариабельность фармакокинетических параметров (а значит, терапевтических эффектов), возможность раздражения слизистой оболочки прямой кишки.
-Ф-
Пероральное введение
Пероральное введение лекарственных веществ — пожалуй, наиболее распространенный путь поступления препаратов в организм, наиболее комфортный для пациента. Перорально применяются препараты, имеющие местное и системное действие. Последние мы рассмотрим подробнее.
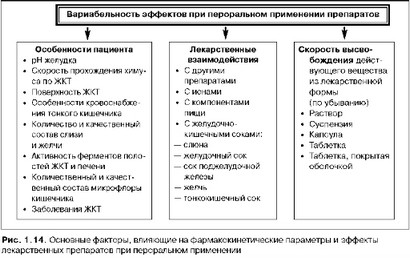
При пероральном применении ЛВ подвергаются целому ряду последовательных превращений, что обуславливает значительную вариабельность их фармакокинетических параметров и, следовательно, терапевтических эффектов. Вариабельность фармакокинетических параметров связана со скоростью высвобождения лекарственного вещества из лекарственной формы, влиянием рН желудочных соков (см. ниже), взаимодействием с компонентами пищи (см. гл. 5), особенностями кровоснабжения кишечника, биотрансформацией ЛВ в печени и другими факторами (рис. 1.14, табл. 1.13).
Многие лекарственные препараты обладают прямым или опосредованным раздражающим действием на слизистые оболочки желудочно-кишечного тракта. Так, нестероидные противовоспалительные средства первого поколения угнетают простаг- ландин-Н-синтазу (циклооксигеназу), что уменьшает биосинтез простагландинов в желудке. В тяжелых случаях при применении нестероидных противовоспалительных средств наблюдается изъязвление слизистых оболочек желудка.
-О-
Преимущества и недостатки перорального введения лекарственных препаратов приведены в табл. 1.14.
Таблица 1.14. Преимущества и недостатки перорального применения лекарственных препаратов
Рассмотрим некоторые факторы, влияющие на биодоступность лекарственных препаратов при пероральном введении, подробнее.
Желудочный сок содержит пепсин, приводящий к деградации белков, пептидов и некоторых других препаратов, например, пенициллинов. В его состав входит также соляная кислота, которая снижает рН в просвете желудка.
Натощак продукция соляной кислоты незначительна, рН желудка имеет слабокислое значение. Прием пищи приводит к стимуляции продукции соляной кислоты, причем если человек питается регулярно, то усиленная продукция соляной кислоты наблюдается за некоторое время (10—20 мин) до приема пищи. Компоненты пищи (особенно молоко, мясо, яйца) постепенно нейтрализуют соляную кислоту, однако при постепенной эвакуации химуса из просвета желудка в двенадцати- перстую кишку кислотность желудочного сока возрастает, достигая максимального значения примерно через 2 ч после приема пищи. Только через 3—4 ч после приема пищи рН желудка достигает натощакового значения (рис. 1.15)45. Поэтому пища различным образом влияет на биодоступность лекарственных препаратов (табл. 1.15).
пищи
Рис. 1.15. Схема изменения рН желудочного сока в зависимости от приема пищи
-Ф-
Таблица 1.16. Константы ионизации некоторых препаратов 46
Для слабых кислот рК меньше 7, поэтому при уменьшении рН число диссоциированных молекул уменьшается (рис. 1.16а), что приводит к повышению липофильности лекарственного вещества и улучшению его всасывания. Аналогичным образом изменяется биодоступность щелочных соединений при повышении рН (рис. 1.16б).
Исходя из приведенных выше рассуждений, казалось бы, что для повышения биодоступности лекарственные вещества, являющиеся слабыми кислотами, нужно вводить в начале еды или через 2 ч после еды, а лекарственные вещества, являющиеся слабыми основаниями, — натощак или сразу же после еды.
Однако некоторые препараты, например, макролидные антибиотики, сульфаниламиды, каптоприл, препараты железа и т.д. могут химически взаимодействовать с компонентами пищи еще в просвете желудка47.
Кроме того, после приема пищи могут наблюдаться и иные взаимодействия лекарств и компонентов диеты (см. гл. 5). Другие препараты (например, миотропные спазмолитики) хоть и не взаимодействуют с химусом, но могут отрицательно сказаться на процессах пищеварения (рис. 1.16).
Рис. 1.16. Изменение числа ионизированных молекул для слабых кислот (а) и оснований (б) рК: 1 — 2, 2 — 5, 3 — 9, 4 — 12
Поэтому, если это не оговорено иначе, лекарственные препараты принимают натощак. Такой прием позволяет свести к минимуму взаимодействие лекарственных препаратов и компонентов пищи. Натощаковым приемом считают применение лекарственных препаратов не менее чем за 30 мин до еды (при регулярном питании) или через 4 ч после приема пищи.
Стимуляторы желудочной секреции назначают за 10— 15 мин до еды.
Во время еды принимают препараты, устойчивые к действию кислот, а также пищеварительные ферменты.
После еды принимают лекарственные вещества, раздражающие слизистую оболочку желудка.
Следует отметить, что на биодоступность лекарственных препаратов может оказать влияние жидкость, использованная для их запивания (табл. 1.17).
Рис. 1.17. Влияние рН на всасывание лекарственных препаратов
Таблица 1.17. Рекомендации по использованию жидкостей для запивания лекарственных препаратов49
Рекомендуется запивать
ПРИМЕР. Вода не оказывает влияния на продукцию соляной кислоты, молоко нейтрализует ее и обладает слабым обволакивающим действием, т.е. защищает слизистые оболочки желудка от раздражающего действия препарата. Соки и кофе стимулируют повышенную продукцию ионов водорода48 и могут сами раздражать слизистые оболочки желудка.
Поэтому целесообразно запивать слабые кислоты молоком, а слабые основания — соками, если слизистые оболочки желудка при этом не раздражаются.
Следует иметь в виду, что некоторые лекарственные препараты, например, тетрациклины, препараты железа и т.д., могут химически взаимодействовать с молоком, поэтому их вместе не принимают. Кроме того, некоторые препараты, например, антациды, сами могут воздействовать на кислотность желудочного сока50, тем самым влияя на биодоступность других лекарственных веществ (см. также гл. 5)5'.
В тонкой кишке наблюдается сложная совокупность различных физико-химических процессов (рис. 1.18 )52, 53, 54
концентрации без затрат энергии преимущественно поступают вода и неорганические ионы.
Внутриклеточный транспорт55.
Внутриклеточный Сопряженный
Межклеточный
Экзоцитоз
Эндоцитоз
Пассивный
Активный
Рис. 1.18. Схема транспорта лекарственных веществ в тонкой кишке
Важно отметить, что в отличие от пассивного активный транспорт является насыщаемым, т.е. при увеличении концентрации ЛВ в просвете кишечника его всасывание может быть увеличено лишь до определенных величин, а дальнейшее повышение поступления ЛВ в просвет кишечника не приводит к увеличению процессов всасывания (рис. 1.19).
После всасывания ЛВ в кишечнике в эпителиальных клетках может наблюдаться метаболизм.
яа
св
от
гс
ее
шщ
ве
§ о
8 ° он ве
с
р
а
к
е
л
Количество поступившего лекарственного вещества
Рис. 1.19. Зависимость количества всосавшегося лекарственного вещества от поступившего
-О-
Основными параметрами, определяющими количество всосавшегося вещества в тонкой кишке, являются его растворимость в воде и проницаемость через стенку тонкого кишечника (рис. 1.20). Разработаны математические модели, предсказывающие количество всосавшегося ЛВ57. Общий вид зависимости между эффективной проницаемостью и долей всосавшегося вещества представлен на рис. 1.21 (при этом растворимость вещества предполагалась неограниченной). Из приведенных данных можно сделать вывод, что при величине эффективной проницаемости меньше 2 всасывание ЛВ в тонкой кишке будет неполным, а при величине этого показателя более 2 можно ожидать полного всасывания58.
Молекулярный вес, г/моль
Логарифм коэффициента распределения в системе октанол/ввода
Рис. 1.20. Проницаемость эпителиального барьера путем диффузии как функция молекулярного веса и липофильности лекарственных веществ 56
с
е
ще
е
Эффективная
Рис. 1.21. Связь между абсорбцией лекарственного вещества в тонкой кишке и его эффективной проницаемостью59
Особый интерес представляют вещества с низкой растворимостью, так как для них максимальная величина всасывания равна произведению растворимости на проницаемость60. Несмотря на то что процесс поступления любого ЛВ можно описать схемой:
твердая лекарственное
растворение w
лекарственная > вещество
в организм форма в растворе
для медленно растворимых веществ процесс растворения является лимитирующим (рис. 1.22).
-Q-
Для плохорастворимых препаратов скорость растворения лимитирует поступление лекарственного вещества в организм, увеличение дозы ЛС может привести к уменьшению его биодоступности. На рис. 1.23 приведены зависимости концентрации в крови плохорастворимого вещества (гризеофульви- на) для двух доз — 250 и 500 мг. При пероральном применении 250 мг препарата его растворяется больше, чем при приеме 500 мг. Поэтому меньшей дозе препарата соответствует бoльшая системная биодоступность.
Предварительное растворение или разжевывание ускоряет процесс растворения, что обычно способствует более быстрому всасыванию ЛВ. Однако при этом повышается вероятность взаимодействия ЛВ с компонентами пищи, увеличивается площадь взаимодействия ЛВ с желудочно-кишечными соками. Поэтому одни препараты перед употреблением рекомендуется разжевывать или растворять, а другие, в частности, капсулы и таблетки с энтерорастворимой оболочкой, которые защищают активное вещество от воздействия соляной кислоты в желудке, разжевывать нельзя.
-Q-
Рис. 1.23. Зависимость концентрации гризеофульвина
С одной стороны, энтеральное введение обычно не требует участия медицинского персонала и наиболее комфортно для пациента. Как правило, при энтеральном пути введения вероятность возникновения побочных эффектов лекарственной терапии наименьшая. С другой стороны, при энтеральном назначении препаратов их фармакокинетика (а следовательно, и терапевтический эффект) подвержена наибольшим изменениям. Это связано как с особенностями функционирования желудочно-кишечного тракта (скорость эвакуации химуса и процессов всасывания из него, интенсивность местного кровотока, сопутствующие заболевания и т. д.), так и с возможностью разрушения большого количества лекарственных веществ. В желудочно-кишечном тракте ЛВ могут разрушаться или инактивироваться под влиянием:
- рН;
- пристеночных ферментов и энзимов желудочно-кишечных соков;
- ферментов печени (см. гл. 3);
- желчных кислот и пигментов;
- слизи;
- нормальной микрофлоры и продуктов ее жизнедеятельности;
- компонентов химуса.
Основные достоинства и недостатки энтерального введения лекарственных веществ суммированы в табл. 1.10.
Преимущества и недостатки энтерального пути введения лекарственных веществ
Сублингвальное и суббукальное введение
Сублингвальное (под язык) и суббукальное (защечное) введение лекарственных веществ основано на том факте, что слизистая оболочка ротовой полости имеет обильное кровоснабжение, особенно в области языка и его корня. Такое введение лекарственных препаратов обычно обеспечивает их быстрое поступление в системный кровоток (минуя печень) с высокой
- 36 —
степенью биодоступности и, соответственно, быстрое развитие терапевтических эффектов.
ПРИМЕР. При сублингвальном введении нитратов их максимальная концентрация в крови достигается в течение 1—2 мин40. При сублингвальном применении пропранолола его биодоступность в 3 раза выше, чем при пероральном41. Сублингвально вводят нифедипин, клонидин для купирования гипертонического криза, глицин — для нормализации мозгового кровотока. Большинство гомеопатических препаратов применяется сублингвально или суббукально.
Основные препараты для сублингвального и суббукального применения указаны в табл. 1.11. Как следует из таблицы, эти препараты относятся к разным фармакологическим группам и имеют различные спектры терапевтического действия.
При сублингвальном или суббукальном введении препаратов важно равномерно и полностью рассасывать соответствующую лекарственную форму, иначе уменьшается поступление лекарственного препарата в кровь и снижается эффективность терапии.
|
Таблица 1.11. |
Основные препараты с системным действием для сублингвального и суббукального применения |
|
|
Препарат |
|
Основные показания к применению |
|
Сублингвальные препараты |
||
|
Биолайн Артрис |
Ревматоидный артрит |
|
|
Биклотимол |
Инфекционно-воспалительные заболевания слизистых оболочек рта |
|
|
Биотредин |
Алкогольный синдром, психостимуляция |
|
|
Глицин |
Нарушения кровообращения головного мозга, стрессы |
|
|
Клофелин |
Гипертонический криз |
|
|
Ликопид |
Комплексная терапия тяжелых воспалительных заболеваний |
|
|
Милилайф |
Астения |
|
|
Молсидомин |
Приступ стенокардии |
|
|
Нитроглицерин |
Приступ стенокардии |
|
|
Нифедипин |
Гипертонический криз |
|
|
Полиоксидоний |
Иммунодефицит |
|
|
Суббукальные препараты |
||
|
Нитроглицерин |
Приступ стенокардии |
|
|
Просидол |
Болевой синдром |
|
|
Ибуклин |
Болевой синдром |
|
|
|
||
Сублингвальный и суббукальный пути введения имеют ограничения при наличии любых воспалительных заболеваний ротовой полости. Кроме того, при длительном применении некоторые препараты могут сами индуцировать раздражение слизистой оболочки ротовой полости.
- 37 —
- Итак —
- При сублингвальном и суббукальном применении ЛВ не подвергаются воздействию желудочного сока и пресистем- ного метаболизма (см. гл. 3), быстро поступают в системный кровоток, минуя печень.
- Сублингвальный и суббукальный пути введения используются для ограниченного количества ЛВ. Небольшая всасывающая поверхность слизистой оболочки ротовой полости позволяет назначать только высокоактивные ЛВ, эффективные в небольших концентрациях. Кроме того, этот путь введения непригоден для введения раздражающих веществ и веществ, обладающих неприятным вкусом.
Ректальное введение
Прямая кишка имеет богатое кровоснабжение и развитую капиллярную сеть. Причем через нижние ректальные вены кровь от прямой кишки попадает в нижнюю полую вену, минуя портальную вену печени (v. portae). При ректальном введении лекарственных веществ отсутствует эффект первого прохождения через печень (см. гл. 3), приводящий к модификации и инактивации большого количества лекарственных препаратов. Часто ректально вводят ЛВ, инактивирующиеся печенью*. Кроме того, ректальное введение позволяет избежать механического раздражения лекарственной формой слизистых оболочек желудка. Ректальное введение также можно использовать при затруднении или невозможности перорального приема, например, при сужении пищевода или же у детей.
Благодаря богатому кровоснабжению слизистой оболочки прямой кишки, при ректальном введении лекарственные вещества быстро поступают в системный кровоток. Отсутствие процесса инактивации поступивших веществ в печени обеспечивает их высокую концентрацию, что приводит к быстрому развитию терапевтического эффекта.
ПРИМЕР. Так, при ректальном введении парацетамола его биодоступность выше и максимальная концентрация препарата в крови достигается быстрее, а анальгетический эффект сохраняется дольше, чем при пероральном применении42. Ректальное введение парацетамола приводит к более длительному сохранению его эффекта у детей, чем перо- ральное43. При ректальном введении морфина животным фармакокинетические параметры оказались сравнимы с таковыми при внутримышечном применении препарата44.
Лекарственные препараты для ректального введения достаточно распространены (табл. 1.12). Видно, что ректально применяются ЛВ, относящиеся к различным фармакологическим группам. Ректальное введение нестероидных противовоспалительных средств и ряда других лекарственных веществ позволяет избежать раздражающего действия на слизистые оболочки желудка.
К недостаткам ректального введения лекарственных средств можно отнести: неудобство применения, индивидуальную вариабельность фармакокинетических параметров (а значит, терапевтических эффектов), возможность раздражения слизистой оболочки прямой кишки.
- Также ректально применяют препараты, имеющие местное действие, но их рассмотрение выходит за рамки настоящей книги.
- 38 —
-Ф-
|
Таблица 1.12. Примеры лекарственных препаратов для ректального введения, имеющие системное действие |
|
|
Препарат |
Основные показания к применению |
|
Амброксол |
Бронхит, пневмония |
|
Аминитрозол |
Антибактериальная терапия |
|
Аминофиллин |
Хронический обструктивный бронхит |
|
Ацикловир |
Лечение и профилактика вирусных инфекций |
|
Диклофенак |
Ревматоидный артрит |
|
Индометацин |
Воспалительные заболевания суставов |
|
Напроксен |
Воспалительные заболевания суставов |
|
Парацетамол |
Лихорадка |
|
Постеризан |
Иммуномодуляция |
|
Терпон |
Затруднение отхождения мокроты |
|
Трамадол |
Выраженный болевой синдром |
|
Тыквеол |
Жировая дистрофия печени, цирроз |
|
Цитабарин |
Лейкоз, лимфома |
|
Эритромицин |
Антибактериальная терапия |
|
|
|
- Итак -
- Ректальное введение обеспечивает быстрое поступление лекарственных веществ в системный кровоток и развитие терапевтического эффекта.
- При ректальном введении наблюдается большая индивидуальная вариабельность фармакокинетических параметров.
Пероральное введение
Пероральное введение лекарственных веществ — пожалуй, наиболее распространенный путь поступления препаратов в организм, наиболее комфортный для пациента. Перорально применяются препараты, имеющие местное и системное действие. Последние мы рассмотрим подробнее.
При пероральном применении ЛВ подвергаются целому ряду последовательных превращений, что обуславливает значительную вариабельность их фармакокинетических параметров и, следовательно, терапевтических эффектов. Вариабельность фармакокинетических параметров связана со скоростью высвобождения лекарственного вещества из лекарственной формы, влиянием рН желудочных соков (см. ниже), взаимодействием с компонентами пищи (см. гл. 5), особенностями кровоснабжения кишечника, биотрансформацией ЛВ в печени и другими факторами (рис. 1.14, табл. 1.13).
Многие лекарственные препараты обладают прямым или опосредованным раздражающим действием на слизистые оболочки желудочно-кишечного тракта. Так, нестероидные противовоспалительные средства первого поколения угнетают простаг- ландин-Н-синтазу (циклооксигеназу), что уменьшает биосинтез простагландинов в желудке. В тяжелых случаях при применении нестероидных противовоспалительных средств наблюдается изъязвление слизистых оболочек желудка.
- 39 —

|
Таблица 1.13. Процессы в ЖКТ, нарушающие всасывание ЛВ |
||
|
Лекарственное вещество |
Процессы в ЖКТ, нарушающие всасываемость ЛВ |
Влияние на всасывание ЛВ |
|
Тетрациклин |
Образование комплексов |
Образование нерастворимых комплексов с ионами Ca2+, Al3+, Fe3+. Потеря активности |
|
Изопротеренол |
Конъюгация с сульфогруппой |
Потеря активности |
|
Салициламид |
Конъюгация с глюкуроновой кислотой |
Потеря активности |
|
Леводопа |
Декарбоксилирование |
Потеря активности |
|
Бензилпенициллин, эритромицин, дигоксин |
Кислотный гидролиз |
Потеря активности |
|
Ацетилсалициловая кислота |
Кислотный гидролиз |
Образование активного метаболита — салициловой кислоты |
|
Пивампициллин |
Ферментативный гидролиз |
Пролекарство, образование ампициллина |
|
Инсулин |
Ферментативный гидролиз |
Потеря активности |
|
Циклоспорин |
Окисление |
Потеря активности |
|
Сульфасалазин |
Влияние микрофлоры |
Пролекарство, образуется 5-аминосалициловая кислота |
|
Дигоксин |
Адсорбция |
Связывание (адсорбция) с холестирамином, образовавшийся комплекс не всасывается |
|
— 40 — |
||
Преимущества и недостатки перорального введения лекарственных препаратов приведены в табл. 1.14.
Таблица 1.14. Преимущества и недостатки перорального применения лекарственных препаратов
|
Преимущества |
Недостатки |
|
Удобство применения |
Медленное развитие терапевтического эффекта |
|
Возможность самостоятельного применения препаратов пациентами |
Индивидуальная вариабельность терапевтических эффектов |
|
Возможность раздражения слизистой оболочки желудочно-кишечного тракта |
Рассмотрим некоторые факторы, влияющие на биодоступность лекарственных препаратов при пероральном введении, подробнее.
Желудочный сок содержит пепсин, приводящий к деградации белков, пептидов и некоторых других препаратов, например, пенициллинов. В его состав входит также соляная кислота, которая снижает рН в просвете желудка.
Натощак продукция соляной кислоты незначительна, рН желудка имеет слабокислое значение. Прием пищи приводит к стимуляции продукции соляной кислоты, причем если человек питается регулярно, то усиленная продукция соляной кислоты наблюдается за некоторое время (10—20 мин) до приема пищи. Компоненты пищи (особенно молоко, мясо, яйца) постепенно нейтрализуют соляную кислоту, однако при постепенной эвакуации химуса из просвета желудка в двенадцати- перстую кишку кислотность желудочного сока возрастает, достигая максимального значения примерно через 2 ч после приема пищи. Только через 3—4 ч после приема пищи рН желудка достигает натощакового значения (рис. 1.15)45. Поэтому пища различным образом влияет на биодоступность лекарственных препаратов (табл. 1.15).
пищи
Рис. 1.15. Схема изменения рН желудочного сока в зависимости от приема пищи
- 41 —
-Ф-
|
Таблица 1.15. Влияние приема пищи на всасывание и биодоступность лекарственных средств |
|||
|
Лекарственные средства, одновременный прием которых с пищей приводит к: |
|||
|
снижению биодоступности |
|
повышению биодоступности |
замедлению всасывания |
|
Амоксициллин |
|
Алафосфин |
Амоксициллин |
|
Ампициллин |
|
Гетациллин |
Ацетилсалициловая кислота |
|
Ацетилсалициловая кислота |
|
Гидралазин |
Ацетоаминофен |
|
Диметилхлортетрациклин |
|
Г идрохлортиазид |
Дигоксин |
|
Доксициклин |
|
Гризеофульвин |
Метронидазол |
|
Изониазид |
|
Дикумарол |
Нитрофурантоин |
|
Каптоприл |
|
Метопролол |
Препараты калия |
|
Леводопа |
|
Пропоксифен |
Сульфален |
|
Нафциллин |
|
Пропранолол |
Сульфаметопиридазин |
|
Окситетрациклин |
|
Фенитоин |
Сульфадимезин |
|
Пивампициллин |
|
|
Хинидин |
|
Рифампицин |
|
|
Цефаклор |
|
Сульфадиметоксин |
|
|
Цефалексин |
|
Сульфален |
|
|
Цефрадин |
|
Тетрациклин |
|
|
Эритромицин |
|
Фенацетин |
|
|
|
|
Феноксиметилпенициллин |
|
|
|
|
Фуросемид |
|
|
|
|
Цефалексин |
|
|
|
|
Эритромицин |
|
|
|
|
|
|
||
|
|
Влияние рН желудочного сока на фармакокинетические параметры большого количества препаратов основано на том факте, что многие лекарственные вещества являются или слабыми основаниями, или слабыми кислотами (табл. 1.16), т.е. имеет место обратимая диссоциация молекулы, описываемая схемой: |
||
|
|
|
HA ^ H++ A— , (1.5) |
|
|
|
где HA — недиссоциированная молекула ЛВ, H+— основание, A+ — кислота. Можно показать, что доля диссоциированных молекул для схемы (1.5) описывается уравнением Хендерсона—Хассельбаха: |
||
|
для кислот |
pH = pK | g диссоциированные молекулы (1 g. недиссоциированные молекулы |
||
|
.. ,, , недиссоциированные молекулы для основании pH = pK + lg ^ , (16’) диссоциированные молекулы где pK — логарифм равновесной константы диссоциации (если pH = pK, то диссоциировано 50% молекул лекарственного вещества). |
|||
Таблица 1.16. Константы ионизации некоторых препаратов 46
|
Слабые кислоты |
рК |
Слабые основания |
рК |
Слабые основания |
рК |
|
Ампициллин |
2,5 |
Аминазин |
9,3 |
Пиндолол |
8,8 |
|
Аспирин |
3,5 |
Бунивакаин |
8,1 |
Прокаин |
9 |
|
Гидралазин |
7,1 |
||||
|
Варфарин |
5 |
Гуанетидин |
11,4 |
Прокаинамид Промазин |
9,2 9,4 |
|
Дезипрамин |
10,2 |
||||
|
Ибупрофен |
4,4 |
Дигидрокодеин |
8,8 |
Прометазин |
9,1 |
|
Кромолин натрия |
2 |
Дидрокодеин |
9 |
Псевдоэфедрин |
9,8 |
|
Леводопа |
2,3 |
Дифенгидрамин |
9 |
Скополамин |
8,1 |
|
Метилдопа |
2,2 |
Дифеноксилат |
7,1 |
Стрихнин |
8 |
|
Метотрексат |
4,8 |
Изопротеренол |
8,6 |
Тербуталин |
10,1 |
|
Пеницилламин |
1,8 |
Имипрамин |
9,5 |
Тиоридазин |
9,5 |
|
|
|
Канамицин |
7,2 |
Фенилефрин |
9,8 |
|
|
|
Клонидин |
8,3 |
Физостигмин |
7,9 |
|
Салициловая кислота |
3 |
Кодеин |
8,2 |
Флюфеназин |
8 |
|
Сульфадиазин |
6,5 |
Кокаин |
8,5 |
Хинидин |
8,5 |
|
|
|
Лидокаин |
7,9 |
|
|
|
Толбутамид |
5,3 |
Метадон |
8,4 |
Хлорохин |
10,8 |
|
|
|
Метамфетамин |
10 |
Хлорфенирамин |
9,2 |
|
Фуросемид |
3,9 |
Метараминол |
8,6 |
Циклизин |
8,2 |
|
Хлоротиазид |
6,8 |
Метилдопа |
10,6 |
|
|
|
Хлоропропамид |
5 |
|
|
|
|
|
Этакриновая кислота |
3,5 |
Метопролол |
9,8 |
|
|
|
|
|
Морфин |
7,9 |
|
|
Исходя из приведенных выше рассуждений, казалось бы, что для повышения биодоступности лекарственные вещества, являющиеся слабыми кислотами, нужно вводить в начале еды или через 2 ч после еды, а лекарственные вещества, являющиеся слабыми основаниями, — натощак или сразу же после еды.
Однако некоторые препараты, например, макролидные антибиотики, сульфаниламиды, каптоприл, препараты железа и т.д. могут химически взаимодействовать с компонентами пищи еще в просвете желудка47.
Кроме того, после приема пищи могут наблюдаться и иные взаимодействия лекарств и компонентов диеты (см. гл. 5). Другие препараты (например, миотропные спазмолитики) хоть и не взаимодействуют с химусом, но могут отрицательно сказаться на процессах пищеварения (рис. 1.16).
- 43 —
Рис. 1.16. Изменение числа ионизированных молекул для слабых кислот (а) и оснований (б) рК: 1 — 2, 2 — 5, 3 — 9, 4 — 12
Поэтому, если это не оговорено иначе, лекарственные препараты принимают натощак. Такой прием позволяет свести к минимуму взаимодействие лекарственных препаратов и компонентов пищи. Натощаковым приемом считают применение лекарственных препаратов не менее чем за 30 мин до еды (при регулярном питании) или через 4 ч после приема пищи.
Стимуляторы желудочной секреции назначают за 10— 15 мин до еды.
Во время еды принимают препараты, устойчивые к действию кислот, а также пищеварительные ферменты.
После еды принимают лекарственные вещества, раздражающие слизистую оболочку желудка.
Следует отметить, что на биодоступность лекарственных препаратов может оказать влияние жидкость, использованная для их запивания (табл. 1.17).
Рис. 1.17. Влияние рН на всасывание лекарственных препаратов
- 44 —
Таблица 1.17. Рекомендации по использованию жидкостей для запивания лекарственных препаратов49
Рекомендуется запивать
|
водой |
молоком |
кофе |
чаем |
соком |
|
Алендронат |
Аммифурин |
Индинавир |
Амброксол |
Геделикс |
|
Бетагистин |
Аскофен |
|
Бронхикум |
Димефосфон |
|
Верапамил |
Ацетилсалицилат |
|
Ге дел икс |
Колестирамин |
|
Гидроксикарбамид |
лизина |
|
Нагифен |
Нагифен |
|
Глибенкламид |
Ацитретин |
|
Остеопан |
Целлюлоза |
|
Глимеперид |
Индинавир |
|
|
|
|
Глюкозамин |
Кальция хлорид |
|
|
|
|
Витаминные препараты |
Лития карбонат |
|
|
|
|
Дипиридамол |
Остеопан |
|
|
|
|
Железа препараты |
|
|
|
|
|
Калия йодид |
|
|
|
|
|
Макролидные антибиотики |
|
|
|
|
|
Миансерин |
|
|
|
|
|
НПВС |
|
|
|
|
|
Офлоксацин |
|
|
|
|
|
Пирензепин |
|
|
|
|
|
Римантадин |
|
|
|
|
|
Сибутрамин |
|
|
|
|
|
Тиоктовая кислота |
|
|
|
|
|
Фелодипин |
|
|
|
|
|
Фенилпропраноламид |
|
|
|
|
ПРИМЕР. Вода не оказывает влияния на продукцию соляной кислоты, молоко нейтрализует ее и обладает слабым обволакивающим действием, т.е. защищает слизистые оболочки желудка от раздражающего действия препарата. Соки и кофе стимулируют повышенную продукцию ионов водорода48 и могут сами раздражать слизистые оболочки желудка.
Поэтому целесообразно запивать слабые кислоты молоком, а слабые основания — соками, если слизистые оболочки желудка при этом не раздражаются.
Следует иметь в виду, что некоторые лекарственные препараты, например, тетрациклины, препараты железа и т.д., могут химически взаимодействовать с молоком, поэтому их вместе не принимают. Кроме того, некоторые препараты, например, антациды, сами могут воздействовать на кислотность желудочного сока50, тем самым влияя на биодоступность других лекарственных веществ (см. также гл. 5)5'.
В тонкой кишке наблюдается сложная совокупность различных физико-химических процессов (рис. 1.18 )52, 53, 54
- Распределение ЛВ между химусом и просветом кишечника. Прием жирной пищи увеличивает поступление липофиль- ных веществ в химус.
- Взаимодействие ЛВ с тонкокишечным соком, соком поджелудочной железы и желчью. Эти желудочно-кишечные соки имеют щелочное значение рН, т.е. могут влиять на биодоступность лекарственных препаратов (см. рис. 1.14) или химически взаимодействовать с ними.
- Межклеточный транспорт, протекающий через поры между эндотелиальными клетками. Таким образом, по градиенту
- 45 —
концентрации без затрат энергии преимущественно поступают вода и неорганические ионы.
Внутриклеточный транспорт55.
Внутриклеточный Сопряженный
Межклеточный
Экзоцитоз
Эндоцитоз
Пассивный
Активный
Рис. 1.18. Схема транспорта лекарственных веществ в тонкой кишке
Важно отметить, что в отличие от пассивного активный транспорт является насыщаемым, т.е. при увеличении концентрации ЛВ в просвете кишечника его всасывание может быть увеличено лишь до определенных величин, а дальнейшее повышение поступления ЛВ в просвет кишечника не приводит к увеличению процессов всасывания (рис. 1.19).
После всасывания ЛВ в кишечнике в эпителиальных клетках может наблюдаться метаболизм.
яа
св
от
гс
ее
шщ
ве
§ о
8 ° он ве
с
р
а
к
е
л
Количество поступившего лекарственного вещества
Рис. 1.19. Зависимость количества всосавшегося лекарственного вещества от поступившего
- 46 —
-О-
Основными параметрами, определяющими количество всосавшегося вещества в тонкой кишке, являются его растворимость в воде и проницаемость через стенку тонкого кишечника (рис. 1.20). Разработаны математические модели, предсказывающие количество всосавшегося ЛВ57. Общий вид зависимости между эффективной проницаемостью и долей всосавшегося вещества представлен на рис. 1.21 (при этом растворимость вещества предполагалась неограниченной). Из приведенных данных можно сделать вывод, что при величине эффективной проницаемости меньше 2 всасывание ЛВ в тонкой кишке будет неполным, а при величине этого показателя более 2 можно ожидать полного всасывания58.
Молекулярный вес, г/моль
Логарифм коэффициента распределения в системе октанол/ввода
Рис. 1.20. Проницаемость эпителиального барьера путем диффузии как функция молекулярного веса и липофильности лекарственных веществ 56
с
е
ще
е
Эффективная
Рис. 1.21. Связь между абсорбцией лекарственного вещества в тонкой кишке и его эффективной проницаемостью59
- 47 —
Особый интерес представляют вещества с низкой растворимостью, так как для них максимальная величина всасывания равна произведению растворимости на проницаемость60. Несмотря на то что процесс поступления любого ЛВ можно описать схемой:
твердая лекарственное
растворение w
лекарственная > вещество
в организм форма в растворе
для медленно растворимых веществ процесс растворения является лимитирующим (рис. 1.22).
-Q-
Для плохорастворимых препаратов скорость растворения лимитирует поступление лекарственного вещества в организм, увеличение дозы ЛС может привести к уменьшению его биодоступности. На рис. 1.23 приведены зависимости концентрации в крови плохорастворимого вещества (гризеофульви- на) для двух доз — 250 и 500 мг. При пероральном применении 250 мг препарата его растворяется больше, чем при приеме 500 мг. Поэтому меньшей дозе препарата соответствует бoльшая системная биодоступность.
Предварительное растворение или разжевывание ускоряет процесс растворения, что обычно способствует более быстрому всасыванию ЛВ. Однако при этом повышается вероятность взаимодействия ЛВ с компонентами пищи, увеличивается площадь взаимодействия ЛВ с желудочно-кишечными соками. Поэтому одни препараты перед употреблением рекомендуется разжевывать или растворять, а другие, в частности, капсулы и таблетки с энтерорастворимой оболочкой, которые защищают активное вещество от воздействия соляной кислоты в желудке, разжевывать нельзя.
- 48 —
-Q-
Рис. 1.23. Зависимость концентрации гризеофульвина
Источник: Ю. Б. Белоусов, К. Г. Гуревич, «Клиническая фармакокинетика. Практика дозирования лекарств» 2005