Использование общей гипоксической пробы для определения оптимального количества заготавливаемой перед операцией аутокрови
Изучение особенностей влияния общей гипоксической пробы, используемой нами для вышеобозначенных целей, показало, что гипоксический стимул оказывал мощное действие на систему транспорта кислорода. Выявлено, что у пациентов с ИБС на основании проведения гипоксической пробы была обнаружена различная толерантность к гипоксии - высокая, средняя, низкая и непереносимость гипоксии. Критериями для отнесения пациентов в ту или иную группу явились значения показателей кислородного баланса: насыщение гемоглобина венозной крови кислородом должно быть не менее 60% (SvO2gt;60%), индекс экстракции кислорода - не более 30% (О2ЕК30%) и отсутствие роста концентрации лактата на фоне 40 мин дыхания гипоксической газовой смесью. Эти критерии были определены нами на основе многочисленных собственных наблюдений и в соответствии с литературными данными. Так, в исследованиях А.З. Колчинской с соавт. (2003), Э.О. Асанова (2006) отмечено повреждающее действие гипоксии при падении напряжения кислорода в артериальной крови до 45-50 мм рт. ст., что в 2 раза ниже нормы и соответствует показателю Sp02 около 80% [6, 32]. Авторы обозначили это значение пороговым. Учитывая серьезную патологию атеросклеротического характера у наших пациентов, влекущую за собой фоновое гипоксическое состояние, мы приняли
пороговый уровень Sv02 не менее 60%, соответствующий нижней границе физиологической нормы. В условиях умеренной гипоксии компенсаторные механизмы позволяют в довольно высоких пределах поддерживать напряжение кислорода на уровнях, соответствующих каждому из этапов его транспорта. При постепенном снижении напряжения кислорода во внешней среде клетки организма до определенного предела потребляют кислород с постоянной скоростью. Поэтому величина индекса экстракции кислорода, характеризующая биофизические условия осуществления тканевого дыхания, является одной из важнейших характеристик кислородного баланса [5, 75].
Концентрация лактата традиционно отражает выраженность кислородной задолженности тканей, поскольку при гипоксии интенсивность анаэробных процессов возрастает, в результате чего происходит избыточная продукция конечного метаболита анаэробного гликолиза в клетках [75]. Вследствие этого значения индекса экстракции кислорода и показатель уровня лактата на фоне 40 мин дыхания гипоксической газовой смесью являются стабильными и надежными критериями для определения толерантности к гипоксии и, соответственно, объема предоперационной заготовки крови.
Помимо показателей кислородного баланса, воздействие гипоксического стимула было основано на изучении гемодинамических параметров системы транспорта кислорода и показателей тканевого дыхания.
У 56 пациентов значения показателей кислородного баланса, указанные выше, наблюдались при дыхании газовой смесью с 10% содержанием кислорода (рис. 4.3). Начальный уровень венозной сатурации составил 70,3±12,42% и к 40-й мин проведения пробы значительных изменений не претерпевал (табл. 4.2).
Содержание лактата при проведении гипоксической пробы незначительно повысилось по сравнению с исходным уровнем, не выходя при этом за рамки физиологической нормы. Вероятно, отсутствие реакции со стороны кислородных показателей во время проведения гипоксической пробы с 10% содержанием кислорода следует расценивать как признак сохранности компенсаторных резервов организма, позволяющий выявить группу пациентов с высокой толерантностью к гипоксии. Функционирова-
Таблица 4.2
Показатели кислородного баланса у пациентов с ИБС при проведении общей гипоксической пробы с 10% содержанием кислорода в газовой смеси (п = 56), X ±Sx
|
|
исход |
10-я мин проведения гипоксической пробы |
20-я мин проведения гипоксической пробы |
30-я мин проведения гипоксической пробы |
40-я мин проведения гипоксической пробы |
|
Sv02(%) |
70,3± 12,42 |
62,2±5,15 |
63,6±4,30 |
65,2±5,71 |
65,4±4,84 |
|
02EI (%) |
26,б±4,32 |
27,6±4,67 |
24,5+5,21 |
22,7±4,07 |
20,7+4,48 |
|
Лактат (ммоль/л) |
0,9±0,10 |
1,2±0,41 |
1,7±0,58 |
1,5±0,28 |
1,3±0,33 |
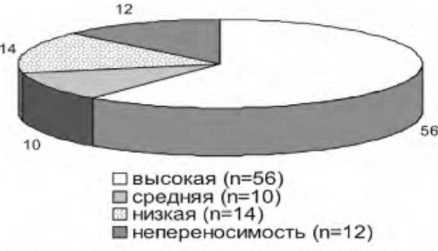
Рис. 4.3. Толерантность пациентов к гипоксии
по результатам общей гипоксической пробы (п = 92),
В % от общего количества пациентов
ние компенсаторных механизмов было направлено на сохранение стабильности кислородных показателей. Исходя из сбалансированности кислородного статуса, мы сочли возможным у этих пациентов перед операцией заготавливать аутокровь в количестве 10% объема циркулирующей крови.
Видимо, дефицит кислорода во вдыхаемой газовой смеси способствовал возбуждению хеморецепторов аортально-каро-
тидной зоны сосудистого русла и сонных артерий, а также центров, регулирующих дыхание и кровообращение. Это приводило к компенсаторному усилению легочной вентиляции и кровотока, а также перераспределению кровотока - увеличению в мозге, сердечной мышце, легких и ограничению в мышцах, коже и др., открытию незадействованных капилляров, рефлекторному выбросу эритроцитов в кровяное русло из их депо. Увеличивалась кислородная емкость крови, что с усилением кровотока обеспечивало поддержание скорости доставки кислорода на уровне, близком к имеющемуся при нормальном содержании кислорода во вдыхаемом воздухе. Следовательно, ткани в этом случае не страдали от недостатка кислорода. Вследствие поддержания
у
адекватной скорости доставки кислорода логично предположить, что существующие пути метаболической регуляции у этой категории пациентов удовлетворяли постоянную потребность тканей, в том числе и сердца, в АТФ и креатинфосфате, а также в выполнении других метаболических функций. Известно, что кардиомиоциты, в силу обладания ими максимальной энергоемкости, способны использовать энергию различных субстратов - свободных жирных кислот, глюкозы, лактата, кетоновых тел, аминокислот и т.д. Но доминирующим путем образования энергии в кардиомиоцитах является метаболизм свободных жирных кислот, обеспечивающий синтез 60-80% всего АТФ. Глюкозозависимый путь синтеза энергии обеспечивает образование 20-40% АТФ, в том числе анаэробный гликолиз - не более 2%. Поскольку для синтеза молекул АТФ, необходимого для нормальной жизнедеятельности клетки, должно образовываться соответствующее количество ацетил СоА, то подавление активности любого из двух вышеописанных путей его образования сопровождается компенсаторной активацией (по принципу реципрокного взаимодействия) другого пути [166, 169]. Вероятно, у пациентов с высокой толерантностью к гипоксии сформировался сбалансированный тип энергетического метаболизма, позволяющий противостоять гипоксическому воздействию благодаря включению механизмов компенсации к гипоксии.
Клинический пример 1. Больной 3., 59 л. И.б. №887, рост 183 см, вес 90 кг.
Основной диагноз: ишемическая болезнь сердца, III ФК.
Сопутствующие заболевания: гипертоническая болезнь 1 ст.
За 3 дня до операции пациенту выполнили общую гипоксическую пробу Перед выполнением общей гипоксической пробы кислородные показатели составили: SJD2-68%, 02Е1=26%. Через 40 мин дыхания гипоксической газовой смесью с 10% содержанием кислорода исследуемые показатели стали следующими: Sv02=65%, 02Е1=24%. Концентрация лактата исходная - 1,0 ммоль/л, в конце гипоксической пробы -1,2 ммоль/л. За 1 сут до операции выполнен забор аутокрови 10% объема циркулирующей крови (650 мл), пациент перенес процедуру хорошо. Выполнена операция - аорто-коронарное шунтирование в условиях ИК. Показатели красной крови (гемоглобин/гематокрит): начало операции - 154/49, в период проведения И К - 106/35. в конце операции, после проведения ультрафильтрации - 119/37. Длительность ИК составила 2 ч 03 мин. Заготовленная аутокровь переливалась после операции. Продолжительность ИВЛ - 8 ч. По дренажу в 1 -е сут после операции было зафиксировано 440 мл отделяемого. Консервированная кровь и ее препараты в послеоперационном периоде не переливались. Лабораторные показатели в 1-е сут после операции: гемоглобин -113 г/л, гематок- рит - 35%, альбумин - 34 г/л. Через 3 сут пациент переведен в общую палату.
Анализ параметров функционирования кардиореспираторной системы показал, что у 12 пациентов с высокой толерантностью не происходило изменения этих параметров под воздействием гипоксического стимула, то есть кардиореспираторная система реагировала на недостаток кислорода незначительно. Сбалансированность исследуемых показателей в этом случае явилась следствием особенностей метаболического ответа у части пациентов, что лежит в основе индивидуальной чувствительности к дефициту кислорода во внешней среде. У этой подгруппы пациентов на передний план выступает энергетический гомеостаз клеток и является, по сути, определяющим как в поддержании жизнедеятельности организма, так и в его адаптационном развитии.
У 10 пациентов на фоне дыхания гипоксической газовой смесью с 10% содержанием кислорода имело место снижение венозной сатурации ниже 60% и повышение индекса экстракции
кислорода выше 30%. Допустимые значения показателей кислородного баланса наблюдались в ходе пробы с 12% содержанием кислорода, что позволило выделить группу пациентов со средней толерантностью к гипоксии. У них забирали аутокровь - не более 7% объема циркулирующей крови.
Клинический пример 2. Больной К., 53 г. И. б. №976. Рост 176 см, вес 72 кг.
Основной диагноз: ишемическая болезнь сердца, III ФК.
Сопутствующие заболевания: гипертоническая болезнь 1 ст. Хронический бронхит.
За 3 дня до операции пациенту выполнили общую гипоксическую пробу, кислородные показатели составили: Sv02=72%, 02Е1=25%. Через 10 мин дыхания гипоксической газовой смесью с 10% содержанием кислорода зарегистрировано снижение Sv02 до 56%, повышение 0^1 до 34%, появились жалобы на чувство нехватки воздуха. Через 40 мин дыхания гипоксической газовой смесью с 12% содержанием кислорода 8^0^61%, 02Е1-29%. Концентрация лактата исходная -1,8 ммоль/л, в конце гипоксической пробы -2,0 ммоль/л. За 1 сут до операции выполнен забор аутокрови - 7% объема циркулирующей крови (385 мл), больной перенес процедуру хорошо. Выполнена операция - аортокоронарное шунтирование в условиях ИК. Показатели красной крови (гемоглобин/гематокрит): начало операции - 134/41, в период проведения ИК - 76/24, в конце операции после проведения ультрафильтрации - 99/31. Во время операции перелито 100 мл альбумина. Длительность ИК составила 1 ч 23 мин. Заготовленная аутокровь переливалась после операции. Продолжительность ИВЛ -11ч. По дренажу в 1-е сут после операции накопилось 320 мл отделяемого. Консервированная кровь и ее препараты в послеоперационном периоде не переливались. Лабораторные показатели в 1-е сут после операции: гемоглобин - 93 г/л, гематокрит - 28%, альбумин - 34 г/л. Через 5 сут пациент переведен в общую палату.
V _ . ^ _ _ V
этой группе пациентов, также как и в группе с высокой толерантностью, выделилась часть пациентов (2 пациента из 10) со стабильными параметрами дыхания и кровообращения (рис. 4.4).
У пациентов с низкой толерантностью к гипоксии (указанные выше кислородные показатели отмечались при дыхании гипок-
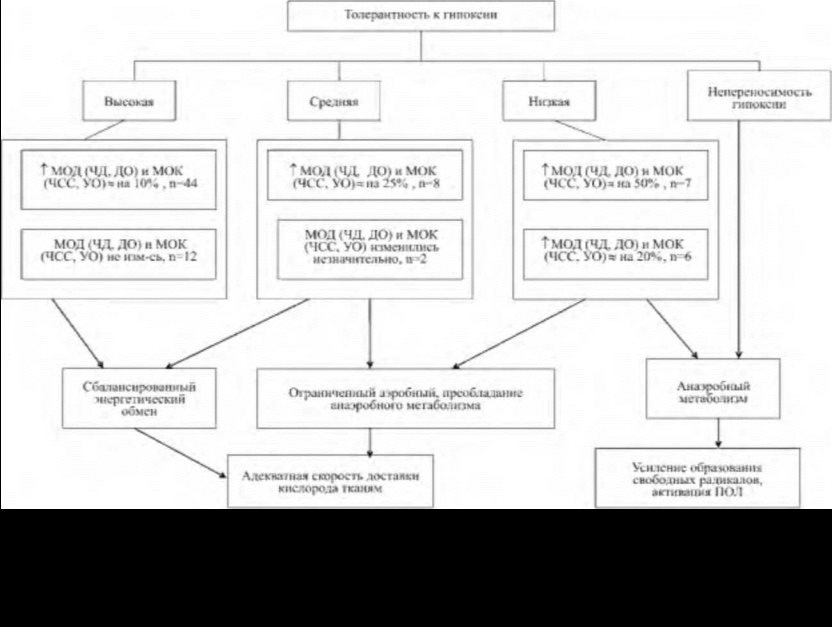
сической смесью с 14% содержанием кислорода) забирали аутокровь в объеме не более 5% ОЦК.
У таких пациентов явно снижалась эффективность предоперационной заготовки крови, поскольку объем заготавливаемой крови был настолько мал, что легко перекрывался в ходе пред- перфузионного забора во время ИК, когда уже не требовалось напряжения кардиореспираторной системы. Однако как и в случае с двумя предыдущими группами, выявились 6 пациентов, у которых не наблюдалось реакции кардиореспираторной системы (рис. 4.4).
В условиях дефицита кислорода во внешней среде у пациентов со средней и низкой толерантностью к гипоксии включение компенсаторно-приспособительных реакций не соответствовало потребности организма в энергии, и возникала необходимость повышения процента кислорода во вдыхаемой смеси. Решающим моментом для возникновения гипоксических состояний явилась недостаточная доставка кислорода из внешней среды к клетке, где он участвует в реакциях аэробного образования энергии, являясь субстратом терминального фермента митохондриальной дыхательной цепи - цитохромоксидазы. Поэтому дефицит кислорода в определенных условиях может приводить к ограничению либо полному подавлению аэробного образования энергии. Поскольку у пациентов со средней и низкой толерантностью к гипоксии процент кислорода в гипоксической смеси в конечном итоге был достаточным для нормального окислительного метаболизма, видимо, у этих категорий пациентов сбалансированность энергетического баланса достигалась преобладанием анаэробных условий образования энергии.
Выявление различной толерантности у пациентов в ответ на проведение гипоксической пробы определило дальнейший ход исследования. Нам представлялось интересным выяснить особенности энергетического метаболизма у пациентов с разной толерантностью к гипоксии. К сожалению, в рамках настоящего исследования нам не удалось детально изучить этот вопрос и обследовать разные категории толерантности к гипоксическому воздействию на предмет особенностей окислительно-восстановительных процессов, происходящих вдыхательной цепи митохондрий кардиомиоцитов. Кроме того, результаты, полученные у
пациентов с низком толерантностью к гипоксии, оказались весьма малочисленны.
Клинический пример 3. Больной Ш., 43 г. И. б. №976. Рост 166 см, вес 64 кг.
Основной диагноз: ишемическая болезнь сердца, III ФК.
Сопутствующие заболевания: гипертоническая болезнь II ст. Хронический пиелонефрит.
За 3 дня до операции пациенту выполнили общую гипоксическую пробу. В ходе пробы была констатирована низкая толерантность больного к гипоксии: непереносимость пробы с дыханием гипоксической газовой смесью с 10 и 12% содержанием кислорода. После 40 мин дыхания гипоксической газовой смесью с 14% содержанием кислорода кислородные показатели составили Sv02-62%, 02Е1=29%. Концентрация лактата исходная была равна 1,5 ммоль/л, в конце гипоксической пробы - 1,7 ммоль/л. За 1 сутдо операции выполнен забор аутокрови 5% объема циркулирующей крови (250 мл), больной перенес процедуру хорошо. Выполнена операция - аорто-коронарное шунтирование в условиях И К. Показатели красной крови (гемогло- бин/гематокрит): начало операции - 136/40, в период проведения ИК - 70/22, в конце операции после проведения ультрафильтрации - 89/30. Во время операции перелито 200 мл альбумина. Длительность И К составила 1 ч 47 мин. Заготовленная аутокровь переливалась после операции. Продолжительность ИВЛ -19 ч. По дренажу в 1 -е сут после операции зафиксировано 270 мл отделяемого. Консервированная кровь и ее препараты в послеоперационном периоде не переливались. Лабораторные показатели в 1-е сут после операции: гемоглобин -101 г/л, гематокрит - 32%, альбумин - 36 г/л. Через 7 сут пациент переведен в общую палату.
Таким образом, в результате исследования при использовании общей гипоксическом пробы у пациентов с разной толерантностью (92 чел.) выделилась группа пациентов (20 чел.), компенсаторно-приспособительные реакции которых были основаны на активации процессов клеточного метаболизма. Такая клеточная реакция, возможно, основана на существовании у этих пациентов метаболического резерва, включающего в себя наличие свободных субстратов для энергетических и метаболических реакции, скоординированность метаболических реакции и взаимосвязей между клеточными компартментами. Индивидуальная чувствительность к дефициту кислорода, предопределенная генетически, явилась основой для выделения подобных подгрупп.
В процессе исследования была выявлена группа пациентов, которым не представилось возможным использовать гипоксическую пробу в целях выявления функциональных резервов организма, поскольку через 2-5 мин от начала дыхания гипоксической смесью с 14% содержанием кислорода наступал выраженный дисбаланс исследуемых показателей кислородного статуса. Непереносимость гипоксической пробы расценивалась как снижение компенсаторных резервов организма и, следовательно, невозможность использования у этих пациентов предоперационной заготовки аутокрови.
Таким образом, использование общей гипоксической пробы позволяло предупреждать нежелательные гемодинамические реакции (падение артериального давления, тахикардия), которые могут развиваться у больных в ответ на заготовку аутокрови за счет более точной оценки адаптационного резерва систем обеспечения кислородного баланса у кардиохирургических больных и, соответственно, более рационального определения количе-
w w г-gt;
ства заготавливаемой перед операцией аутокрови. В случае заготовки одинакового количества аутокрови у всех больных без учета индивидуальных особенностей организма (в том числе сердечно-сосудистой патологии) эти осложнения могут иметь для больного тяжелые последствия, вплоть до инфаркта миокарда [93].
Источник: Шипулин В.М., Подоксенов Ю.К., Свирко Ю.С., «Кровесбережение в кардиохирургии.» 2010
А так же в разделе «Использование общей гипоксической пробы для определения оптимального количества заготавливаемой перед операцией аутокрови »
- ПРЕДИСЛОВИЕ
- ГЛАВА 1 СОВРЕМЕННЫЕПРЕДСТАВЛЕНИЯ О ПЕРИОПЕРАЦИОННОЙ ГЕМОТРАНСФУЗИОННОЙ ТЕРАПИИ
- Физиологические принципы трансфузии эритроцитов
- Переливание переносчиков газов крови
- Переливание других препаратов крови
- ГЛАВА 2 МЕХАНИЗМЫ РАЗВИТИЯ ТРАНСФУЗИОННЫХ РЕАКЦИЙ ПРИ ТРАДИЦИОННОЙ ТАКТИКЕ ПЕРЕЛИВАНИЯ КРОВИ
- Острые трансфузионные реакции иутунной природы
- Острые трансфузиояные реакции неиммунной природы
- Отсроченные трансфузионные реакции иммунной природы
- Отсроченные трансфузионные реакции неиммунной природы
- Инфекционные осложнения переливания крови
- ГЛАВА 3 АКТУАЛЬНОСТЬ СПОЛЬЗОВАНИЯ МЕТОДОВ БЕСКРОВНОЙ ХИРУРГИИ. ТОЛЕРАНТНОСТЬ К ГИПОКСИИ И КРОВОПОТЕРЕ
- Фармакологические альтернативы трансфузиям
- Трансфузионные альтернативные кровезаменители
- Аутологичное донорство
- Предоперационная заготовка аутокрови
- Интраоперационная гемодилюция
- Интраоперационный сбор крови
- Послеоперационный сбор крови
- Толерантность к гипоксии
- ГЛАВА 4 РАЗРАБОТКА НОВОЙ КОНЦЕПЦИИ РОВЕСБЕРЕЖЕНИЯ НА ОСНОВЕ ИЗУЧЕНИЯ ИНДИВИДУАЛЬНЫХ ОСОБЕННОСТЕЙ АДАПТАЦИОННОГО РЕЗЕРВА ОРГАНИЗМА К ГИПОКСИИ И КРОВОПОТЕРЕ
- Заготовка аутокрови у кардиохирургических пациентов
- Определение степени толерантности пациентов к гипоксии для выбора рациональной гемотрансфузионнои тактики
- Применение общей гипоксической пробы с целью предоперационного прогнозирования тактики гемотрансфузионной терапии в интра- и послеоперационном периодах у кардиохирургических пациентов с ИБС
- Повышение резистентности пациентов к анемии благодаря использованию адаптационной гипокситерапии в комплексе с нутритивной терапией
- Использование ультрафильтрации в целях сбережения собственной крови пациента
- ГЛАВА 5 РЕИНФУЗИЯ КРОВИ. НАШ ОПЫТ ПРИМЕНЕНИЯ ТЕХНОЛОГИИ CELL SAVER
- Опыт использования технологии Cell Saver (Dideco Compact) в отделе сердечно-сосудистой хирургии НИИ кардиологии
- Состояние периферического звена эритрона у кардиохирургических пациентов при использовании заготовки аутокрови