Особенности поверхностного рельефа красных кровяных клеток при заготовке аутокрови у пациентов с ИБС
Реализация кислородтранспортной функции эритроцитов требует поддержания их формы в виде двояковогнутого диска, а также способности к деформации, позволяющей клетке двигаться по капиллярам. Однако по структуре поверхности эритроциты даже здорового человека представляют собой довольно гетерогенную популяцию. С точки зрения микроциркуляции, кислородтранспортной функции, способности к деформации видоизмененные эритроциты менее полноценны, чем двояковогнутые дис- коциты. Нарушение морфологических свойств красных клеток крови приводит к повышению вязкости крови, формированию микроциркуляторного блока, депонированию и шунтированию крови, развитию тканевой гипоксии - важнейшего патогенетического фактора, определяющего симптоматологию заболевания [49]. В связи с этим при рассмотрении патогенетических механизмов влияния заготовки аутокрови у пациентов с ИБС наше внимание закономерно было обращено на морфологические свойства эритроцитов [11].
Исследование особенностей поверхностного рельефа красных кровяных клеток было проведено совместно с сотрудниками кафедры патофизиологии ГОУ ВПО СибГМУ Росздрава под руководством академика РАМН В.В. Новицкого.
В предыдущих исследованиях сотрудников этой кафедры было показано, что у пациентов с ИБО эритроцитарная популяция подвергается морфологической трансформации (табл. 10). Механизмы дезорганизации поверхностной архитектоники при ИБС сопряжены с дефицитом энергопродукции и активацией процессов свободно-радикального окисления [49]. Морфологическим проявлением изменений структурно-метаболических характеристик эритроцитов при ИБС является увеличение числа видоизмененных форм. Обнаружено, что возрастание числа трансформированных эритроцитов у больных ИБС по сравнению со здоровыми донорами происходило за счет увеличения численности субпопуляции как переходных форм клеток, так и необратимо измененных предгемолитических форм эритроцитов (табл. 6.3, рис. 6.2а). Наблюдалась тенденция к увеличению числа денегативных форм. При этом было снижено содержание полноценных двояковогнутых дискоцитов (81,0±3,15% против 87,4±1,36%, рlt;0,05). Изменения морфологических свойств эритроцитов у больных ИБС могут явиться причиной нарушения реологических свойств крови, формирования гиперкоагуляционного статуса [49].
После проведения кардиохирургической операции у пациентов с ИБС был выявлен факт дезорганизации поверхностного
1 w w
рельефа красных кровяных клеток, приводящей к некоторой перестройке количественного распределения отдельных морфологических форм эритроцитов с тенденцией к увеличению числа трансформированных клеток, находящихся на различных стадиях дегенерации (табл. 6.3). В целом на послеоперационных этапах исследования число двояковогнутых дискоцитов, переходных и предгемолитических форм не изменилось. Обращало на себя внимание увеличение количества дегенеративных форм эритроцитов на всех этапах послеоперационного обследования. Так, в 1 -е сут после операции число дегенеративных форм увеличилось
|
Таблица 6.3 ^ о Особенности морфологического статуса эритроцитов й у кардиохирургических пациентов с ИБС (по данным от сканирующей электронной микроскопии), X*=Sx ^ m |
|||||
|
Группы исследования |
Морфологические формы эритроцитов, % s |
||||
| Двояко
вогнутые дискоциты |
Переходные
формы |
Предгемо
литические формы |
111
Дегенера- из тивные 5 ¦р формы |
||
|
Здоровые доноры |
87,4±1,36 | 9,7±0,97 | 2,4±0,27 | 0,3±0,07 § | |
|
Пациенты с ИБС |
81,0±3,15# | 13,6±1,98# | 3,4*0,45# | 0,5±0,09 5
' -п |
|
|
Группа сравнения |
1 -е сут после операции | 82,2±2,19 | 13,1 + 1,05* | 3,8*0,33# | 0,9±0,10** 5 |
| 7-е сут после операции | 85,2±3,77 | 13,6*1,22# | 3,6*0,37# | 1,0±0,1Г* s | |
| 14-е сут после операции | 83,4±2,21 | 14,5*1,06* | 3,9±0,40* | 0,9*0,09** | |
|
Группа с заготовкой аутокрови |
1 -е сут после операции | 86,3+3,26 | 10,2*0,88А | 2,2±0,22*^ | 0,6*0,05*А |
| 7-е сут после операции | 83,6±3,74 | 11,8*1,63 | 3,4+0,38* " | 0,7+0,08* | |
| 14-е сут после операции | 81,9±3,79 | 13,3±1,09* | 4,3±0,33* | 0,7*0,06** | |
to
to
Примечание: * - рlt;0,05 по сравнению с исходными данными в аналогичной группе; 9 - рlt;0,05 по сравнению с этапом "перед операцией"; Л - рlt;0,05 по сравнению с аналогичным этапом в группе сравнения.



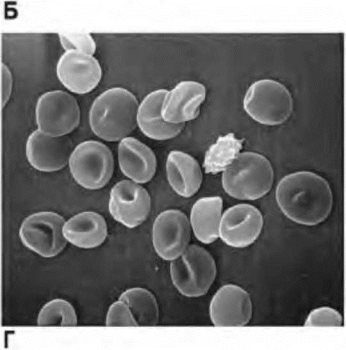
Рис. 6.2. Эритроциты периферической крови у пациента с ИБС
до оперативного вмешательства (А) и после операции аорто-
коронарного шунтирования при использовании заготовки
аутокрови (1-е сут. (Б), 7-е сут. (В), 14-е сут. (Г)). Сканирующая
электронная микроскопия (Л — х1500; Б - хЗООО; В, Г — х2000|
в 1,8 раза по сравнению с исходными значениями, на 7-е сут после операции число таковых возросло в 2 раза и на 14-е сут количество дегенеративных форм оставалось повышенным в 1,7 раза по сравнению с исходным уровнем. Такие изменения, с нашей точки зрения, являются вполне закономерными, поскольку проведение кардиохирургического вмешательства с использованием ИК сопряжено с опасностью механического и физико-химического повреждения эритроцитов. Кроме того, в условиях проведения ИК соприкосновение крови с синтетическими материа-
Таблица 6.4
Распределен и о морфологических форм эритроцитов (в %)
у кардиохирургических пациентов с ИБС при использовании
g о о
заготовки аутокрови (по данным сканирующей электронной

микроскопии), X±Sx
Продолжение таблицы 6.4
|
Куполообразные эритроциты |
1,45±0,18 |
1,72±0,11 |
1,60±0,19 |
0,70±0,13* |
1,22±0,22 |
1,75±0,23 |
|
Сферические эритроциты |
1,66±0,24 |
1,90±0,15 |
1,78±0,18 |
1,07±0,23* |
1,33±0,25 |
1,91 ±0,21 |
|
Эритроциты в виде спущенного мяча |
0,55±0,09 |
0,79±0,09 |
0,74±0,07 |
0Г36±0,07 |
0,77±0,08 |
0,75±0,05 |
|
Дегенеративные формы |
0,56±0,05 |
0,61 ±0,06 |
0,62±0,05 |
0,66±0,05 |
0,76±0,08 |
0,79±0,06* |
Примечание: * - рlt;0,05 по сравнению с исходными данными.
о
Сл
лами экстракорпорального контура приводит к активации каскада реакций, вызывающих системный воспалительный ответ, что также может индуцировать повреждение циркулирующих эритроцитов [11, 50].
Анализ процентного распределения эритроцитов периферической крови на этапах исследования у пациентов с ИБС, которым выполнена заготовка аутокрови, выявил снижение числа предгемолитических форм эритроцитов (куполообразных и сферических клеток) в 1-е сут после операции (табл, 6.4, рис. 6.26, в). При сравнении с морфологическими формами эритроцитов здоровых доноров в 1 -е сут после операции увеличилось только число дегенеративных эритроцитов. Через неделю после операции зафиксировано увеличение количества трансформированных клеток: предгемолитических форм в 1,4 раза и дегенеративных - в 1,9 раз по сравнению с таковыми у здоровых доноров. Через две недели после операции увеличилось количество переходных форм - в 1,4 раза до 13,3±1,09% (рlt;0,05), предгемолитических форм - в 1,7 раза до 4,3±0,33% (рlt;0,05), дегенеративных форм эритроцитов - в 2 раза и стало равным 0,7±0,06% (рlt;0,05) по сравнению с аналогичными формами эритроцитов у здоровых доноров (табл. 6.3-6.4, рис. 6.2г). При сравнении с исходными значениями у пациентов с ИБС через две недели после операции в 1,4 раза выросло число дегенеративных форм эритроцитов (табл. 6.3).
На электронных микрофотографиях видны двояковогнутые дискоциты, эритроциты с одним и множественными выростами, с гребнем, клетки в виде тутовой ягоды, куполообразные и сфе- роцитарные эритроциты, дегенеративно-измененные клетки.
При сравнении морфологического статуса эритроцитов у пациентов с использованием и без использования заготовки аутокрови обнаружены различия в 1-е сут после операции (табл. 6.3, 6.4). У пациентов с использованием заготовки аутокрови на этом этапе исследования выявлено меньшее процентное содержание переходных (10,2±0,88% против 13,1±1,05%, рlt;0,05), предгемолитических (2,2±0,22% против 3,8±0,33%, рlt;0,05) и дегенеративных форм эритроцитов (0,6±0,05% против 0,9±0,10%, рlt;0,05). При этом регистрировалось незначительное увеличение количества дискоцитов (86,3±3,26%). Не исключено, что это повышение может являться следствием поступления в кровоток функционально полноценных эритроцитов, заготовленных накануне. В условиях послеоперационной гипоксии такие эритроциты активнее реализуют кислородтранспортную функцию, чем эритроциты у пациентов с использованием аллокрови. Это предположение основывается на факте отсутствия изменений в значениях индекса экстракции кислорода на следующие сутки после операции у пациентов, которым выполнена заготовка аутокрови (табл. 6.2).
Проведенные исследования свидетельствуют об изменении поверхностного рельефа эритроцитов у пациентов с ИБС, прооперированных с использованием заготовки аутокрови, на следующие сутки после операции, что заключается в снижении числа трансформированных эритроцитов как жизнеспособных обратимых переходных форм, так и функционально неполноценных предгемолитических и дегенеративных форм эритроцитов за счет незначительного увеличения численности субпопуляции двояковогнутых дискоцитов.
Как видно, патогенез вовлечения системы красной крови в патологический процесс при ишемическои болезни сердца в условиях кардиохирургической операции и ИК достаточно сложен. Существует большое количество разнонаправленных патогенетических факторов, обладающих стимулирующим либо ингибирующим действием на костномозговой компартмент. Известна роль эритропоэтина как универсального регулятора эритропоэ- за в развертывании адаптивных реакций кроветворной ткани при воздействии экстремальных факторов. В литературе обсуждается роль таких особенностей кардиохирургическои операции в условиях ИК, как активация системной воспалительной реакции, развитие ишемическо-реперфузионных изменений, активация системы комплемента и гемокоагуляции, способствующих угнетению эритропоэза. Аналогичное влияние на эритроидный росток кроветворения оказывают и препараты донорской крови, содействующие клеточной активации и, следовательно, усугублению воспалительной реакции. Обширная раневая поверхность, хирургическая кровопотеря, механическое разрушение эритроцитов и выход из них биологически активных веществ во время ИК также задействованы в механизмах стимуляции эритропоэ- за. Показанная нами роль заготовки аутокрови у кардиохирургических пациентов с ИБС в механизмах усиления эритропоэза помогает объяснить более благоприятное течение послеоперационного периода у этих пациентов.
Источник: Шипулин В.М., Подоксенов Ю.К., Свирко Ю.С., «Кровесбережение в кардиохирургии.» 2010