Понятие об инфекции и иммунитете
Инфекция. Инфекция (от лат. слова infectio - загрязнение, заражение) - это проникновение патогенного возбудителя (вирусы, бактерии, простейшие и др.) в другой более высокоорганизованный растительный или животный организм с последующим антагонистическим их взаимоотношением.
Инфекционный процесс - ограниченное во времени сложное взаимодействие биологических систем микроорганизма (возбудитель) и макроорганизма, протекающее в определенных условиях внешней среды; проявляющееся на субмолекулярном, субклеточном, клеточнотканевом, органном и организменном уровнях и закономерно заканчивающееся либо гибелью макроорганизма, либо освобождением его от возбудителя.
Инфекционная болезнь - конкретная форма проявления инфекционного процесса, отражающая степень его развития и имеющая характерные нозологические признаки.
Инфекционные болезни - это обширная группа болезней, вызываемых патогенными возбудителями, которые могут передаваться от зараженного человека или животного здоровому и способны к массовому распространению. В общей структуре заболеваний человека на инфекционные болезни приходится от 20 до 40%. В 1955 г. насчитывалось 1062 известные науке инфекционные болезни. В настоящее время список их увеличился до 1200 (В.И. Покровский с соавторами, 1993 г.). За последние 20 лет медицина открыла ещё 30 «новых инфекционных болезней”. Все они вызываются живыми возбудителями. В их числе и те, которые ранее считались неинфекционными. Это язвенная болезнь желудка и двенадцатиперстной кишки, вызываемая Helicobacter pylori, цирроз печени, вызываемый вирусом гепатита С, рак шейки матки, вызываемый папилломовирусом; коронаросклероз, вызываемый хламидиями и ряд других. С возбудителями паразитарных заболеваний также связывают ряд болезней, ранее считавшихся неинфекционными. Полагают, что саркома Бэркитта - самый распространенный рак детей в Аф-
рике - является результатом малигнизации лимфоцитов за счет сочетанного воздействия вируса Эпштейна-Барра и Plasmodium falciparum (возбудитель тропической малярии). На Филиппинах каждая седьмая смерть возникает от сердечно-сосудистых заболеваний, в результате миокардита, вызванного яйцами гетерофиид - гельминтов - трематод. Возбудитель описторхоза - Opistorchis viverini отнесен к первой группе канцерогенов человека.
Возбудитель определяет не только возникновение инфекционного процесса, но и его специфичность. Так, возбудитель чумы вызывает чуму, холеры - холеру и т.д. Однако специфичность не является абсолютной. Например, одно инфекционное заболевание могут вызвать разные возбудители (сепсис) и. напротив, один возбудитель (стрептококк) может вызвать разные болезни (скарлатина, рожа, ангина).
Человек на протяжении своей жизни контактирует с огромным числом микроорганизмов, но инфекционные болезни вызывает лишь ничтожно малая их часть (1/30000). Способность вызвать инфекционный процесс в значительной степени определяется патогенностью.
Патогенность (болезнетворность) - видовой признак микроорганизма. закрепленный генетически и характеризующий способность вызвать заболевание. По этому признаку микроорганизмы делятся на патогенные, условно-патогенные и непатогенные (сапрофиты). Главными факторами, определяющими патогенность, являются вирулентность, токсикогенность и инвазивность.
Вирулентность - степень, мера патогенности, индивидуально присущая конкретному штамму патогенного возбудителя. Характеризуется тяжестью течения заболевания.
Токсикогенность - способность к выработке и выделению различных токсинов (экзо- и эндотоксинов).
Инвазивность (агрессивность) - способность к проникновению в ткани и органы макроорганизма и распространение в них,
На возможность возникновения и характер течения инфекционного процесса влияет и состояние макроорганизма. Определяющей в макроорганизме является восприимчивость, характеризующая развитие патологических реакций (болезни) в ответ на внедрение, размножение и жизнедеятельность возбудителя. Степень восприимчивости определяется резистентностью и иммунитетом.
Резистентность - естественная неспецифическая устойчивость организма к вредным воздействиям, в том числе и к воздействию патогенных микроорганизмов, Резистентность микроорганизма определяется генотипическими и фенотипическими факторами.
Иммунитет - способ защиты организма от живых тел и веществ, несущих на себе признаки генетической чужеродности (информации).
Иммунология. Иммунология - одна из наиболее бурно развивающихся наук. Возникнув первоначально как учение об иммунитете к инфекциям, в настоящее время иммунология изучает генетические, молекулярные и клеточные механизмы иммунного ответа, а также его роль при различных патологических состояниях организма. Она разрабатывает способы и методы профилактики, диагностики и лечения инфекционных болезней (иммунопрофилактика, вакцинация); злокачественных опухолей (иммуноонкология), изучает условия, способствующие пересадке чужеродных органов и тканей (трансплантационная иммунология): извращенные реакции на антигены (аллергология, иммунопатология); влияние на иммунную систему факторов окружающей среды (экологическая иммунология). Включает также иммунопатологию матери и плода, иммуногематологию и другие разделы.
С помощью новейшего направления иммунологии - иммунобиотехнологии решаются задачи создания и производства многочисленных диагностических, профилактических и лечебных иммунных препаратов.
Иммунная система организма представлена лимфоидной тканью. Её основными функциональными клетками являются лимфоциты, происходящие от кроветворной стволовой клетки и подразделяющиеся на Т- и В-лимфоциты и их субпопуляции.
Предшественники Т-лимфоцитов мигрируют в тимус, где под влиянием тимозина, тимопоэтина и других медиаторов созревают и дифференцируются, образуя разновидности Т-лимфоцитов: Т-хелперы, Т-суп- рессоры, Т-киллеры и Т-эффекторы. Предшественники В-лимфоцитов мигрируют в костный мозг, где превращаются в В-лимфоциты, которые являются предшественниками плазматических клеток, продуцирующих антитела. Макрофаги, гранулоциты также относятся к клеткам иммунной системы и происходят от кроветворных стволовых клеток.
Защитные механизмы макроорганизма достаточно сложны. В ответ на постоянный контакт с микробами, проникающими в организм из внешней среды, осуществляется защита от инфекций с помощью множества различных специфических и неспецифических механизмов. функционирующих порознь или в едином комплексе.
Неспецифические механизмы защиты от возбудителей инфекций в норме функционируют у всех индивидуумов. Они начинают «работать» сразу же после рождения ребенка, начало их функционирования не требует предварительного контакта с микроорганизмами или их антигенами. К числу этих факторов относятся физические барьеры (например, неповрежденные кожные покровы или слизистые оболочки), химические барьеры (например, соляная кислота желудочного сока, ферменты пищеварительной системы, находящиеся на поверхности кожи жирные кислоты, обладающие бактериостатическим эффектом), фагоцитирующие клетки и система комплемента. В последнюю входит несколько ферментов и более 20 различных сывороточных белков.
Специфический иммунитет. В противоположность неспецифическим защитным механизмам, система специфической иммунной защиты не может «работать в полную сипу» сразу же после рождения ребенка. Для ее развития и начала функционирования должно пройти определенное время после контакта с возбудителем инфекции или его антигенами. Специфический иммунитет может развиваться естественным путем после перенесения инфекции или искусственным способом - в результате иммунизации.
Специфический иммунитет включает два компонента - гуморальный (опосредованный антителами) и клеточные реакции, обеспечиваемые функционированием антител. Их называют гуморальными реакциями иммунитета. Они напрямую связаны с В-лимфоцитами и с их потомками - плазматическими клетками, которые обеспечивают продукцию специфических иммуноглобулинов (антител). Когда В-клетки встречаются с антигеном, начинается процесс их пролиферации. Это приводит к резкому увеличению числа лимфоцитов, способных осуществлять выработку антител к данному антигену. Клеточный иммунитет контролируется Т-лимфоцитами и осуществляется лимфоцитами и макрофагами. Этот вид иммунитета связан с функционированием различных типов Т-лим- фоцитов и выделяемых ими растворимых веществ - лимфокинов, которые действуют как сигналы между клетками различных типов, участвующих в обеспечении иммунного ответа.
Эти два компонента иммунного ответа очень тесно взаимосвязаны. Т-клетки взаимодействуют с В-клетками в процессе выработки антител к большинству антигенов. Гуморальные (антительные) и клеточные иммунные реакции индуцируются при всех инфекционных болезнях, однако интенсивность и качество каждого из этих двух компонентов варьирует при различных инфекциях.
Возникновение гуморального и клеточного иммунитета сопровождается формированием так называемой иммунологической памяти, которая проявляется в том, что при повторном контакте со специфическим антигеном вызывает ускоренный иммунный ответ. Именно иммунологическая память лежит в основе иммунитета, который раньше определяли как невосприимчивость к инфекционным заболеваниям. В настоящее время понятие “иммунитет» имеет более широкий смысл и включает в себя ответ иммунной системы на все виды антигенов. Усиленный ответ организма на повторный контакт с антигеном зависит от наличия особой субпопуляции лимфоцитов, которые носят название «клеток памяти». Это долгоживущие лимфоциты, сохраняющие после первичного контакта с антигеном информацию о нем в течение месяцев, лет, десятилетий.
Таким образом, функции иммунитета осуществляют несколько видов клеток, основными из которых являются макрофаги, Т-лимфоциты и В-лимфоциты. Деятельность этих клеток направлена на распознавание и уничтожение генетически чужеродных макроорганизму веществ, т.е. поддержание гомеостаза, и осуществляется в содружестве друг с другом, в их кооперативном взаимодействии.
Врожденный, или видовой, иммунитет представляет собой невосприимчивость одного вида животных или человека к микроорганизмам, вызывающим заболевания у других видов. Примером естественного видового иммунитета является невосприимчивость человека к чуме собак, рогатого скота и другим заболеваниям животных, которые, в свою очередь, невосприимчивы к гонорее, менингиту, кори и другим заболеваниям человека. Врожденный материнский иммунитет обусловлен антителами, передаваемыми от матери ребенку во время внутриутробного развития, а затем в процессе кормления материнским молоком.
Приобретенный иммунитет специфичен и не передается по наследству. Он формируется естественно или создается искусственно.
Естественный приобретенный иммунитет появляется после перенесенного инфекционного заболевания. По своей напряженности и длительности естественный иммунитет бывает разным. После перенесенных натуральной оспы, кори, краснухи, эпидемического паротита, скарлатины формируется пожизненный иммунитет. При некоторых инфекциях иммунитет достаточно напряженный и длительный, но не дает гарантии защиты от повторных заболеваний. И, наконец, такими инфекциями, как дизентерия, сальмонеллез, грипп, ОРЗ человек болеет часто.
Искусственно приобретенный иммунитет делится на активный и пассивный. Активный вырабатывается организмом в результате воздействия антигена на иммунную систему. Пассивный иммунитет формируется при введении иммунных сывороток, а также при пересадки иммунных клеток.
Различают также иммунитет стерильный, сохраняющийся в отсутствии микроорганизма, и не стерильный, который существует в организме в течение того времени, пока в нем находится возбудитель соответствующего заболевания, например, туберкулеза, сифилиса и некоторых других. Отдельно выделяют местный иммунитет, который формируется при участии иммуноглобулина А.
Иммунодефицитные состояния. Иммунодефициты - это снижение функциональной активности основных компонентов иммунной системы, приводящее к тому, что организм оказывается не в состоянии адекватно реагировать на чужеродные антигены. В этом случае он более подвержен инфекционным и опухолевым заболеваниям. Различают первичные и вторичные иммунодефициты.
К первичным иммунодефицитам относятся врожденные нарушения иммунной системы, связанные с генетическими дефектами одного или нескольких ее компонентов, а именно - комплемента, фагоцитоза, гуморального и клеточного иммунитета. Первичные иммунодефициты могут быть обусловлены:
> внутриутробной инфекцией (вирус краснухи, цитомегаловирус);
> расстройствами аутоиммунного характера;
> аномалией Х-хромосомы.
Вторичные иммунодефициты - это нарушения иммунной системы, которые развиваются в позднем постнатальном периоде или у взрослых и не являются результатом генетического дефекта. Среди вторичных иммунодефицитов различают 3 формы: приобретенную, индуцированную и спонтанную.
Наиболее ярким примером приобретенного иммунодефицита служит СПИД (синдром приобретенного иммунодефицита), который развивается в результате избирательного поражения одной из субпопуляций Т-лимфоцитов - Т-хелперов соответствующим вирусом.
Индуцированные вторичные иммунодефициты - это такие состояния, при которых имеется конкретная причина, вызвавшая их появление: рентгеновское облучение, кортикостероиды, цитостатики, травмы и хирургические операции, а также нарушения иммунитета, которые развиваются вторично по отношению к основному заболеванию (диабет. заболевания почек, печени, злокачественные процессы и др.). При устранении причины, вызвавшей вторичный иммунодефицит, в большинстве случаев происходит полное восстановление иммунитета.
В отличие от индуцированной, спонтанная форма вторичного иммунодефицита характеризуется отсутствием явной причины, вызвавшей нарушение иммунологической реактивности. Клинически эта форма проявляется в виде хронических, рецидивирующих инфекционно-воспалительных процессов бронхолегочного аппарата и околоносовых придаточных пазух, урогенитального и желудочно-кишечного тракта, глаз, кожи и мягких тканей, вызванных оппортунистическими микроорганизмами.
Антигены и антитела. Иммунитет к различным инфекционным болезням развивается как ответ на воздействие антигенов. Термином «антигены» обозначают молекулы, которые распознаются иммунной системой и индуцируют иммунный ответ.
Антигены - все те вещества, которые несут признаки генетической чужеродности и при введении в организм вызывают развитие специфических иммунологических реакций. Антигенами являются микробные клетки и их токсины, сывороточные и яичные альбумины, эритроциты и др. Антигенность присуща не только белкам, но и сложным полисахаридам, липосахаридам, полипептидам, некоторым искусственным высокополимерным соединениям, т.е. всем веществам, которые несут на себе специфический отпечаток чужеродности.
Простые элементы и соединения: медь, железо, сера, хлорид натрия, глюкоза, аминокислоты - не могут быть антигенами, но, соединенные с аминокислотами в полипептидную цепь достаточной величины и сложности, приобретают антигенность. Необходимо подчеркнуть значение молекулярной массы для проявления антигенности, которая должна быть не менее десятка тысяч. Антигены характеризуются следующими признаками: чужеродность, антигенность, иммуногенность, специфичность.
Чужеродность - неотделимое от антигена понятие. Применительно к данному организму без чужеродности нет антигена. Например, для организма кролика его альбумины, эритроциты и другие ткани не являются антигенами, тогда как для морских свинок это антигены.
Антигенность - мера антигенного качества. Например, большая или меньшая способность вызывать образование антител. Если в организм кролика ввести бычий сывороточный альбумин и иммуноглобулин, то вырабатываются антитела к иммуноглобулину, т.к. его антиген- ность значительно выше.
Иммуногенность - способность вызывать иммунный ответ. Это понятие в основном относится к микробным антигенам, обеспечивающим создание иммунитета к инфекциям. Например, дизентерийные возбудители обладают высокой аитигенностью, но выраженного иммунитета против дизентерии получить не удается. А брюшнотифозный микроб является и высокоантигенным и высокоиммуногенным.
Специфичность - те антигенные особенности, благодаря которым одни антигены отличаются от других. Антигены делятся на полноценные и неполноценные или гаптены. Полноценные антигены при введении в организм формируют в нем иммунный ответ и способны взаимодействовать с антителами и клетками.
Гаптены не способны индуцировать иммунный ответ, но могут взаимодействовать с готовыми антителами. Гаптены могут стать полноценными антигенами после соединения с белками, полисахаридами или искусственными высокомолекулярными электролитами.
Специфичность антигена определяется химическими группировками, которые называются антигенными детерминантами. Иммунологическая специфичность белковых антигенов определяется:
а) аминокислотным составом и последовательностью аминокислот в первичной полипептидной цепи;
б) концевыми аминокислотами цепи;
в) вторичной и третичной структурой белковой молекулы;
г) поверхностнорасположенными химическими группировками.
Специфичность полисахаридов и других органических макромолекул подчиняется тем же принципиальным закономерностям. Различают несколько типов антигенной специфичности:
Видовая специфичность - это такая специфичность, благодаря которой один вид организмов отличается от другого. С помощью антител против сывороточных белков человека судебные медики легко различаЮТ пятно крови, принадлежащее человеку, от пятна крови любого животного.
Групповая специфичность - это специфичность, которая обусловливает различия среди особей одного вида организмов.
Впервые внутривидовые антигенные различия описаны К. Ланд- штейнер в 1901 г, тем самым были открыты группы крови человека. Антигены, благодаря которым различные особи одного вида различаются между собой, получили название изоантигенов. Так, для человеческих эритроцитов, кроме изоантигенов АВО, известно более 70 других.
Типоспецифичность - понятие, аналогичное предыдущему, но имеет отношение к микробным видам. Например, пневмококки по своим полисахаридным антигенам делятся на типы I, II, III, IV и т.д., более 80. Ботулинический токсин делится на типы А, В, С, Д, Е.
Гетероспецифичность - это общие антигены, встречающиеся у разных видов. Примером является антиген Форсмана, присутствующий в эритроцитах овец, лошадей, собак, кошек, мышей, кур, но отсутствующий у человека, обезьян, кроликов, крыс уток. За счет гетероантигенов могут возникать перекрестные иммунологические реакции, приводящие к ошибочным диагностическим заключениям.
Антитела - белки, относящиеся к тому или иному классу иммуноглобулинов, синтезируются плазматическими клетками после парентерального поступления антигена. Антитела обладают способностью специфически взаимодействовать с данным антигеном, благодаря чему являются основным фактором специфического иммунитета.
Известно пять классов иммуноглобулинов: ^ М, ^ в, ^ А, ^ Е, Jg Б. Суммарное количество иммуноглобулинов в сыворотке составляет около 2,5%, не более 1/3 всех белков. Антитела циркулируют в крови и других жидкостях организма. Не следует думать, что антитела против того или иного антигена принадлежат к какому-то одному из пяти классов иммуноглобулинов. Наоборот, антитела данной специфичности почти всегда представлены разными классами. При этом наиболее общее правило следующее: первыми после иммунизации появляются антитела класса ГС М, затем ^ О и ^ А.
Иммуноглобулины:
]£ класса О - составляют основную массу сывороточных иммуноглобулинов (70-80%). В 1 л содержится 6-16 г. Это единственные антитела, которые проходят через плаценту. У новорожденного ребенка в крови имеется только этот класс иммуноглобулинов. Антитела высокоспецифичны, активны, вступают во все реакции.
]£ класса М - составляют 5-10% от массы антител. Эти антитела первичного иммунного ответа с тяжелым молекулярным весом, не проходят через плаценту. Они также активны и вступают во все реакции.
]£ класса А - составляют 10-15% от массы сывороточных антител. Эти антитела попадают из сыворотки в клетки слизистых оболочек, присоединяют там секреторный компонент и выходят за пределы слизистых оболочек в просвет кишечника, дыхательных путей и др. Они создают местный иммунитет, являясь «первой линией обороны» организма.
]£ класса Е - называются реагины, они обладают цитофильностью, фиксируются тучными клетками, базофилами. Количество их невелико - 0,2%. С этими антителами связаны аллергические реакции немедленного типа.
]£ класса Б - составляют также около 0,2%. Функция их не вполне ясна. Однако известно, что при аутоиммунных заболеваниях количество ^ Б возрастает.
Материнские ]£ О (но не ]£ М или ]£ А) проникают через плаценту, начиная с 16-й недели беременности. Это отражает процесс пассивного переноса иммунитета, который нарастает по мере увеличения сроков беременности и пропорционален концентрации ]£ О в сыворотке крови беременной женщины. Этот процесс является также отражением активного транспорта, в результате которого нормализуется концентрация ]£ О у новорожденного. Создается впечатление, что низкие концентрации материнских ]£ О стимулируют, а высокие - угнетают этот транспорт. Когда беременность достигает полного срока, концентрация ]£ в в пуповинной крови становится одинаковой или даже превышает содержание иммуноглобулинов в крови матери, У недоношенных детей концентрация ]£ в ниже, чем у детей, родившихся в срок, ^ в-антитела, приобретенные пассивно, обеспечивают защиту новорожденных и маленьких детей от вирусных и бактериальных инфекций.
Перенос ^ в-антител от матери к плоду через плаценту передает новорожденному ребенку хотя бы частично «иммунологический опыт» его матери. На территориях, где в популяции имеет место интенсивная циркуляция возбудителей инфекционных болезней, и где большинство взрослых приобретают естественный иммунитет, этот опыт существенно отличается от такового у жителей стран, где циркуляция патогенных микроорганизмов ограничена и где взрослые люди имеют низкие уровни иммунитета. В развивающихся странах отмечается пассивный перенос антител к возбудителям дифтерии, кори, полиомиелита и краснухи. Кроме того, противостолбнячные антитела, индуцированные в организме матери соответствующей прививкой столбнячным анатоксином, легко проникают через плаценту, обеспечивая защиту новорожденного от столбняка. В развитых странах, где у женщин детородного возраста титры антител к возбудителям полиомиелита и дифтерии могут быть низкими, передача этих антител новорожденным детям происходит в небольшом количестве. Если защитные материнские антитела не являются ]£ в, а относятся к другому классу иммуноглобулинов (обычно это имеет место при инфекциях, обусловленных грамотрицательными патогенными бактериями - например, кишечными палочками или сальмонеллами), плод не получает антител от матери и, следовательно, новорожденный ребенок не имеет пассивной защиты от этих инфекций.
Образование сывороточных иммуноглобулинов. Синтез иммуноглобулинов начинается в организме ребенка еще до его рождения. Было показано, что ^ М можно обнаружить уже при сроке беременности 10 недель, ^ в - 12 недель; а ^ А - при сроке 30 недель. Большая часть антител, синтезируемых организмом самого плода, относятся к иммуноглобулинами класса М. Тем не менее, плод развивается в условиях стерильности, поэтому до момента рождения иммуноглобулины в организме здорового плода продуцируются в очень ограниченном количестве.
В течение первого года жизни под влиянием антительного раздражения микроорганизмов внешней среды (т. е. при развитии естественных инфекций у новорожденных детей) или в результате введения ребенку антигенов, содержащихся в вакцинах, титры иммуноглобулинов очень быстро нарастают.
К окончанию первого года жизни концентрации ]£ в, ]£ М и ]£ А в крови ребенка составляют соответственно 60%, 100% и 30% от уровня этих иммуноглобулинов у взрослых людей.
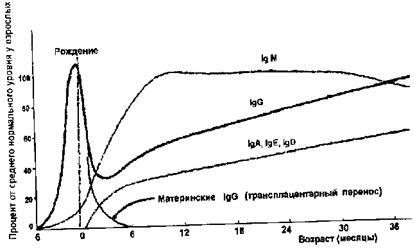
Рис. 1. Нормальная продукция сывороточных иммуноглобулинов. |
Пассивно перенесенные антитела, особенно если их уровень достаточно высок, могут транзиторно угнетать иммунный ответ организма ребенка на воздействие специфических антигенов. Этот феномен следует принимать во внимание при разработке календаря прививок. Например, иммунизацию против кори не следует осуществлять до достижения ребенком 9 месяцев, когда титры полученных через плаценту материнских противокоревых антител не снизятся в достаточной степени. Высокие титры пассивно приобретенных антител к возбудителям дифтерии, столбняка и коклюша могут угнетать иммунный ответ на все компоненты АКДС-вакцины в течение первых недель жизни ребенка. По этой причине первую дозу АКДС-вакцины не следует вводить ребенку ранее 6-недельного возраста. Этот ингибирующий эффект имеет транзиторный характер и ослабевает по мере введения последующих доз АКДС-вакцины.
У детей, родившихся недоношенными или с пониженной массой тела, ответные реакции на иммунизацию выражены в такой же степени, как и у родившихся в срок детей того же возраста.
Иммунный ответ. Классспецифические реакции иммунитета. Как естественная инфекция, так и иммунизация индуцируют выработку антител классов ]£ в, ]£ М и ]£ А. В процессе острой инфекции уже в первые дни после появления первых симптомов заболевания начинают вырабатываться Ig M-антитела, концентрация которых достигает максимума на 7-10-й дни. В течение последующих нескольких месяцев титры Ig M-антител постепенно снижаются и после выздоровления больного антитела этого класса исчезают. Таким образом, наличие в сыворотке крови Ig M-антител свидетельствует о имеющейся в настоящее время или недавно перенесенной инфекции, хотя есть и исключения из этого правила.
При естественной инфекции или после иммунизации почти одновременно с появлением в сыворотке крови Ig M-антител (или на 1-2 дня позже) начинают вырабатываться Ig G-антитела. Концентрация Ig G-антител в дальнейшем быстро нарастает. В течение многих последующих лет Ig G-антитела сохраняются в низких титрах, которые могут быть выявлены с помощью соответствующих, достаточно чувствительных методов.
После реинфекции или ревакцинации развивается, так называемая, «бустер-реакция».
Способ иммунизации или пути естественного проникновения возбудителей инфекции в организм человека определяют, какой иммунный ответ со стороны Ig A-антител будет доминирующим - системный или местный (на слизистых оболочках). Системный ответ с образованием Ig A-антител развивается при парентеральном введении вакцин или при естественных инфекциях, возбудители которых проникают во внутренние органы и размножаются в них, а также при системной циркуляции патогенных микроорганизмов. Отмечаются значительные колебания сроков начала, интенсивности и продолжительности выявления Ig A-антител, причем прогнозировать их динамику гораздо труднее, чем динамику Ig M- и Ig G-антител.
При первичном попадании антигена в организм человека для развития иммунного ответа обычно требуется около 10 дней. Этот период обозначают терминами «время lag» или «лаг-фаза». Лимфоидные клетки встречаются с антигеном, размножаются с образованием клона клеток со сходной активностью, дифференцируются и начинают синтезировать антитела. Титры антител быстро нарастают, достигают «плато», и затем постепенно снижаются.
Процесс образования антител при первой (первичной) встрече с антигеном отличается от такового после второго (повторного) контакта. При первичном ответе лаг-фаза имеет большую продолжительность, максимальный уровень антител ниже, а падение титров антител происходит быстрее, чем при вторичном иммунном ответе. При повторной встрече с тем же антигеном реакции иммунитета будут развиваться быстрее, лаг-фаза окажется короче, максимальный уровень антител - выше, а период персистенции антител - дольше.
Существенным компонентом первичного иммунного ответа являются иммуноглобулины класса М, тогда как при вторичном иммунном ответе иммуноглобулины представлены в основном ]£ в. Различия между первичным и вторичным иммунным ответом выражены в наибольшей степени в тех случаях, когда антиген стимулирует как В-лимфо- циты, так и Т-лимфоциты, т.е. когда речь идет о Т-зависимых антигенах.
Повторные дозы антигена приводят к более быстрому и более интенсивному иммунному ответу. Способность активно реагировать на бустерную дозу вакцины после нескольких ее введений также увеличивается. Например, после третьего введения столбнячного анатоксина выраженный иммунный ответ на новое введение этого антигена сохраняется около 20 лет.
Источник: С.Т. Карагулова, В.С. Тойгомбаева, «ОБЩАЯ ЭПИДЕМИОЛОГИЯ Учебное пособие» 2009
А так же в разделе «Понятие об инфекции и иммунитете »
- Медицинские иммуно-биологические препараты (МБП)
- Специфическая профилактика инфекционных болезней
- Организация прививочного дела
- Схема загрузки бытового холодильника
- Поствакцинальные осложнения. Клиника, диагностика, лечение, профилактика
- Профилактика поствакцинальных осложнений. Особенности вакцинации детей при некоторых заболеваниях и состояниях
- Эпидемиологический надзор за поствакцинальными осложнениями
- Расширенная программа иммунизации
- Тесты по разделу
- ЛИТЕРАТУРА