2.1. Экологическая эпидемиология
Экологизация медицины - один из важнейших аспектов формирования ее теории. Эта тенденция привносит в нее принцип использования знаний о различных сторонах взаимоотношений человека, природы и общества для развития практики здравоохранения и соответствует общей направленности медицинской науки к познанию закономерностей адаптации человека как целостного существа к факторам его жизни. Экологическая идея объединяет дисциплины, рассматривающие мир как относительно замкнутую систему с ограниченными ресурсами, элементы которой находятся во взаимной связи (глобальная экосистема).
Термин «экология», введенный немецким биологом Э. Геккелем в 1866 г., в настоящее время приобрел междисциплинарный характер. В эпидемиологии это понятие существует довольно давно и ранее под ним понималось выявление резервуара возбудителя тех или иных инфекций, т.е. термин употреблялся только в смысле «экология возбудителя». В частности, в одном из определений эпидемического процесса, последний рассматривается как экология возбудителя в человеческом обществе [18].
Более того, саму эпидемиологию наряду с паразитологией некоторые исследователи относят к разделу экологии [86].
В настоящее время насчитывается более 60 определений термина «экология» [87]. Применительно к эпидемиологии наиболее приемлемым, на наш взгляд, является определение В.И. Жданова с соавт. [18] «Экология изучает условия существования живых организмов, взаимосвязи между ними и средой обитания». По существу, из данного определения вытекают три основных задачи в рассмотрении экологического направления в эпидемиологии. Первая задача - изучение экологии возбудителей различных инфекций. Ее решение нашло отражение в множестве публикаций как в нашей стране, так и за рубежом [88-90], поэтому на ней мы останавливаться не будем.
Вторая задача связана с изучением влияния окружающей среды на эпидемический процесс различных инфекций. В последние годы эпидемиологические исследования, направленные на рассмотрение этой задачи, которая «корнями» уходит в учение В.И. Вернадского о биосфере и ноосфере [91], приобрели довольно массовый характер [92-95]. Как показывают результаты этих исследований, техногенное загрязнение внешней среды - фактор, сказывающийся на системе «паразит - хозяин», что отражается на уровне заболеваемости, течении инфекций и структуре инфекционной патологии среди населения, проживающего в экологически неблагополучных регионах. В частности, с позиций разрабатываемого нами направления - морской эпидемиологии [10] - техногенное загрязнение окружающей среды весьма существенно влияет на состояние водных биоценозов. В этой связи важно понять: водная среда - это «кладбище» микроорганизмов или «плацдарм» для формирования эпидемических вариантов. Как показывают исследования, с одной стороны, загрязнение водоемов (органическое и неорганическое) изменяет биологические свойства бактерий, причем нередко в сторону усиления персистентных и патогенных характеристик, с другой - создает экстремальные условия для существования многих бактерий, что приводит к резкому сокращению видового разнообразия и повышению численности тех видов, которые характеризуются более высокой экологической пластичностью [96]. Так, одними из аспектов существования популяции
49
Salmonella typhimurium в воде являются избирательное выживание вирулентных (устойчивых к фагоцитозу) бактерий, а также их адгезия к поверхности гидробионтов. Оба пути показывают способность патогенных бактерий поддерживать и увеличивать численность своей популяции в водных биоценозах, что представляет эпидемическую опасность. Абиотические и биотические факторы приводят не к «отмиранию» патогенных бактерий, а к переходу части популяции в гетероморфное состояние с различными стадиями L-трансформации [97].
Изменения, вносимые человеком в окружающую среду, порождают экологические эффекты, последствия которых подчас трудно предсказуемы, так как они носят опосредованный характер. С ними связаны и современные особенности эпидемического процесса. Под влиянием новых неблагоприятных факторов, к которым организм человека эволюционно не подготовлен, снижается уровень его защищенности, нарушаются механизмы клеточного и гуморального иммунитета, возникают различные иммунодефицитные состояния [98]. Все большее значение в патологии начинает приобретать комбинированное воздействие микроорганизмов, их токсинов с ксенобиотиками различного происхождения, обладающими токсинпотенцирующим и иммуносупрессивным действием и/ или нарушающими резистентность кожи и слизистых к колонизации несвойственными для хозяина микроорганизмами. Техногенное изменение окружающей среды способствует селекции микробных агентов с повышенным патогенным потенциалом и снижению колонизационной резистентности [95].
В частности, наши, пионерские в этом плане, исследования показали [99-109], что у детей школьного возраста, проживающих в экологически неблагополучных условиях (г. Ангарск) имеет место значимо более высокий уровень состояний блока сбалансированной патологии (неспецифическая резистентность, адаптивность и иммунный статус.) по сравнению с детьми из экологически благополучных территорий (г. Иркутск), среди которых преобладает блок нормального функционирования (р < 0,001). Более того, согласно общепринятым в педиатрии уровням оценки резистентности, у школьников Иркутска ее «хороший» уровень регистрируется значимо чаще, а «сниженный» и «низкий» уровни 50
резистентности с высокой степенью достоверности преобладают у школьников Ангарска.
Неблагоприятные тенденции наблюдаются и в отношении иммунного статуса здоровых детей, проживающих в условиях техногенного загрязнения окружающей среды. Так, в Ангарске и в экологически неблагополучных районах г. Иркутска отмечается выраженное угнетение Т-клеточного звена иммунитета, а у детей Ангарска, - значимое увеличение уровня иммуноглобулинов А, М и G и снижение способности нейтрофилов к активации.
Выявленные нами негативные тенденции в деятельности регуляторных систем у здорового детского населения, длительно проживающего в экологически неблагоприятных условиях, свидетельствуют о существенном ухудшении здоровья указанной субпопуляции. Тем не менее было бы неправомерно сводить все многообразие причинно-следственных связей в изучаемой нами системе «техногенное загрязнение окружающей среды - инфекционная патология» только к нарушениям деятельности регуляторных систем здорового организма. Опосредованное действие экологического фактора риска на проявления инфекционного процесса связано не только (даже не столько) с этиологическими, а прежде всего, с эпидемиологическими причинами, поэтому в данном случае цепь причинно-следственных связей достаточно сложна. В указанную цепь, без сомнения, могут (и должны) вписываться различные сопутствующие соматические заболевания, развивающиеся под воздействием промышленного загрязнения окружающей среды. Такие заболевания для оцениваемой нами группы инфекционной патологии относят к преморбидному фону или сопутствующей патологии. Будучи, в этом случае факторами риска второго порядка, они также вносят свой вклад в условия заражения и (или) развития инфекционных заболеваний. Таким образом, цепь причинно-следственных связей между этиологическим агентом (в нашем случае биологической природы) и конечной зависимой переменной под названием «инфекционная болезнь» достаточно сложна. В цепи промежуточных переменных они включают в себя различные социальные и природные условия и разнообразные факторы риска (первичные, вторичные, а возможно, и более высоких порядков). При наличии таких сложных связей достаточно проблематично
51
однозначно охарактеризовать ключевые условия, способствующие заражению или развитию заболевания.
С учетом приведенных выше рассуждений рассмотрим воздействие техногенного загрязнения атмосферного воздуха на частоту выявления у детей с инфекционными заболеваниями сопутствующей соматической патологии. Например, нами показано, что при вирусном гепатите В доля детей, имеющих сопутствующие заболевания, закономерно снижается от интенсивно загрязненного района (г. Ангарск) до относительно благополучного («условно чистые» районы г. Иркутска). В Ангарске этот показатель у детей с вирусным гепатитом В достигал 60,2±0,05 % случаев, а в Иркутске - лишь 34,3±0,03 % (р < 0,05). В районах Иркутска с низким уровнем загрязнения соответствующий показатель составил 26,5±0,04 %, а с высоким - 41,1±0,05 % (р < 0,05).
Аналогичное распределение получено и для других взятых в разработку инфекционных заболеваний. Например, для дизентерии Флекснера в «условно чистом» районе г. Иркутска доля детей с сопутствующей патологией составляла 31,0±0,05 %, а в «грязном» - 70,0±0,05 % (р < 0,001).
Таким образом, изменения, выявленные нами у детей на экологически неблагополучных территориях как на стадии предболезни (нарушения деятельности регуляторных систем), так и на стадии болезни (сопутствующая соматическая патология) позволяют с достаточной надежностью прогнозировать адекватное снижение в этих условиях иммунологической и эпидемиологической эффективности вакцинопрофилактики, а также более неблагоприятное течение инфекционного и (или) эпидемического процессов.
Изыскания в указанном направлении проведены нами прежде всего в Ангарске и Иркутске, а также в Шелехове и в Чите, которые также относятся к городам с высоким уровнем загрязнения атмосферного воздуха. Здесь следует отметить, что специфической особенностью г. Шелехова является наличие в атмосферном воздухе комплекса ксенобиотиков, связанных с производством алюминия. Загрязняющие вещества Читы представлены в основном выбросами автотранспорта и предприятий теплоэнергетики и их состав соответственно близок к таковому в Иркутске.
Исследования коллективного иммунитета проводились среди здорового детского населения в возрасте 9-16 лет, привитого согласно национальному календарю прививок Российской Федерации отечественными вакцинами. В них не включались дети с хроническими заболеваниями, из закрытых детских коллективов, дети-мигранты.
Результаты показали, что у привитых детей школьного возраста в экологически неблагополучных условиях уровень специфических антител ко всем изученным управляемым инфекциям оказался значимо ниже, чем в группе сравнения (рис. 2.4). При этом во всех случаях группами риска были дети 15-17 лет.
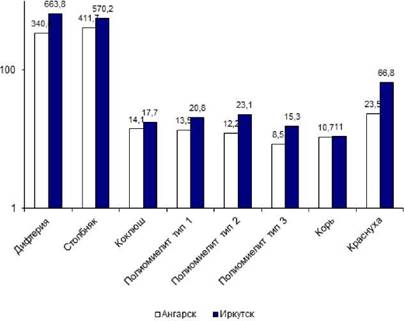
Рис. 2.4. Средние геометрические величины титров поствакцинальных антител у детей Ангарска и Иркутска (ось Y имеет логарифмический масштаб) |
Что касается степени воздействия техногенного загрязнения на поствакцинальную иммунную защиту, то в меньшей степени она проявляется в отношении столбнячного анатоксина, а в наибольшей - в отношении коклюшной вакцины и третьего типа вируса полиомиелита в живой полиомиелитной вакцине. Полученные данные вполне закономерны, так как столбнячный анатоксин сам по себе представляет собой хороший адъювант, что подтверждается высокой эффективностью вакцинопрофилактики этой инфекции. В отношении коклюша имеет место неблагополучная эпидемиологическая ситуация с достаточно высокой заболеваемостью школьников, что обусловлено быстрой истощаемостью поствакцинального иммунитета со временем. Низкий иммунный ответ на третий тип вируса полиомиелита живой полиовакцины с выраженным снижением в экологически неблагополучных регионах возможно обусловлен конкурентными взаимоотношениями в кишечнике отдельных типов вакцинных штаммов, а также кишечных энтеровирусов.
Таким образом, выявлен ряд вакцин, при которых иммунный ответ наиболее подвержен влиянию такого фактора риска, как техногенное загрязнение окружающей среды. Указанное негативное изменение иммунного ответа проявляется как в виде уязвимости специфического ответа, так и меньшей его продолжительности.
В отношении изменения интенсивности посвакцинально- го иммунного ответа с течением времени нами установлено, что в городах с высоким уровнем техногенного загрязнения окружающей среды снижение противокоревого поствакцинального иммунитета идет более быстрыми темпами по сравнению с экологически благополучными территориями (рис. 2.5). Так, через 5-6 лет после ревакцинации титры антител ниже минимального защитного наблюдаются в Ангарске, Шелехове и экологически благополучных районах Иркутска соответственно в 50,0±12,5; 52,6±11,5 и 27,3±13,4 % случаев (разница незначима). У детей, ревакцинация которых против кори была проведена 9-10 лет назад, данный показатель составил соответственно 71,9±6,0; 50,0±10,2 и 30,8±12,0 % случаев (р = 0,011, критерий %2 для трех групп).
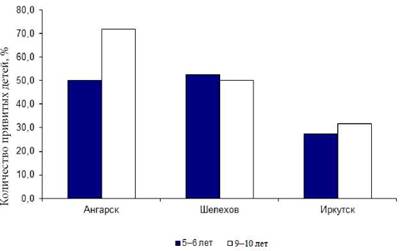
Рис. 2.5. Доля привитых против кори детей, не имеющих защитных уровней противокоревых антител через 5-6 и 9-10 лет после ревакцинации |
В целом следует отметить чрезвычайно высокий процент отрицательных и сомнительных результатов титров вакцинальных противокоревых антител у детей 10-17 лет, проживающих во всех исследуемых городах (Ангарск - 57,0 %, Шелехов - 47,7 %, Иркутск - 41,9 %), при полном отсутствии высоких уровней титров (1:160). Согласно полученных нами данных, среди подростков 15-17 лет 73,2 % в Ангарске, 48,1 % в Шелехове и 47,5 % - в Иркутске (р < 0,001, критерий %2 для трех групп) имеют уровни антител ниже минимального защитного (отрицательные или сомнительные). Таким образом, в городах Иркутской области сложилась неблагополучная ситуация по кори, особенно выраженная на территориях с высоким уровнем техногенного загрязнения окружающей среды.
Аналогичные материалы получены при сравнении уровней специфических антител в районах одного города, характеризующихся различным уровнем техногенного загрязнения атмосферного воздуха и близким составом поллютантов. Например, ис
следование поствакцинального иммунитета в Чите выявило, что уровни специфических поствакцинальных антител к вирусному гепатиту А у детей, проживающих в экологически неблагополучных районах города, были достоверно ниже, чем на контрольной территории этого же населенного пункта (рис. 2.6). К такому же выводу привели исследования коллективного иммунитета у привитых детей к дифтерии и столбняку в экологически благополучных и неблагополучных районах Иркутска.
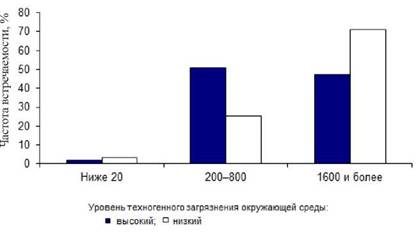
Рис. 2.6. Частота встречаемости различных титров поствакцинальных суммарных антител к вирусу гепатита А у детей 7-10 лет, проживающих в различных районах г. Читы |
Несмотря на то, что отсутствие защитных уровней поствакцинальных антител в сыворотке крови еще не говорит о незащищенности ребенка от данной инфекции, было бы неправомочным полагать, что, оказывая угнетающее влияние на неспецифические иммунные реакции (что общеизвестно и неоднократно доказано, в том числе и нашими данными), техногенное загрязнение окружающей среды не влияет, на систему специфической защиты от инфекционных болезней, естественную или искусственную, т.е. вакцинальную. Представленные результаты исследований убедительно подтверждают факт такого влияния и в наиболее обо- 56
бщенном виде могут быть сведены к следующему. Техногенное загрязнение окружающей среды является фактором риска, значимо снижающим иммунологическую эффективность вакцинопрофилактики. Влияние экологического неблагополучия в большей степени проявляется в отношении вакцинации против коклюша, дифтерии, кори, трех типов вируса полиомиелита и в наименьшей степени - против столбняка.
Кроме того, полученные нами материалы свидетельствуют, что и течение инфекционных заболеваний у детей в сравниваемых городах для всех взятых в разработку групп и (или) нозологических форм патологии, было более длительным в условиях экологического неблагополучия. При этом разница, как правило, носила значимый характер с высоким уровнем достоверности (табл. 2.3).
Таблица 2.3
Длительность течения инфекционных заболеваний у детей в г. Ангарске и Иркутске, сутки
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Как видно из представленной таблицы, аналогичная закономерность имела место и при сравнении длительности течения заболевания у инфекционных больных из разных районов одного города (Иркутск), характеризующихся высоким и низким уровнями загрязнения атмосферного воздуха.
Другим важнейшим интегральным показателем любого заболевания является тяжесть его течения, которая, как и в случае с длительностью болезни, носила более неблагоприятный характер в условиях проживания населения под действием экологического прессинга.
В качестве примера рассмотрим распределение степени тяжести гепатита А у детей, проживающих в сравниваемых городах. На приведенном ниже рисунке видны демонстративные различия в сопоставляемых показателях (рис. 2.7). В Ангарске преобладали среднетяжелые формы заболевания (74,0±4,7 %) и были нередки тяжелые случаи (2,7±1,9 %). В Иркутске при отсутствии тяжелых форм отмечалось значительно меньшее число заболеваний со среднетяжелым течением (55,2±5,3, р < 0,01). Аналогичная закономерность имеет место и при других формах инфекционной патологии детского населения, проживающего в неблагоприятных условиях атмосферного загрязнения (Ангарск и условно «грязные» районы Иркутска).
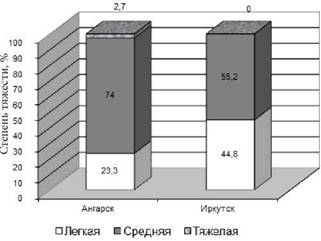
Рис. 2.7. Распределение детей с гепатитом А по степени тяжести 58 |
Следует отметить, что инфекционный процесс характеризуется более длительным течением и его утяжелением и у взрослого населения, которое работает и (или) проживает в условиях экологического неблагополучия. Этот аспект исследований показан нами на примере острых гепатитов А, В и С у рабочих предприятий нефтехимической и нефтеперерабатывающей промышленности Ангарска и у жителей этого города, не связанных по роду своей профессиональной деятельности с вредными условиями труда (прочее население города). Кроме того, в условиях экологического неблагополучия утяжеление инфекционного процесса выявлено у хирургических больных при такой полиэтиологичной группе заболеваний, как инфекции, связанные с оказанием медицинской помощи [110], а также при туберкулезе [111].
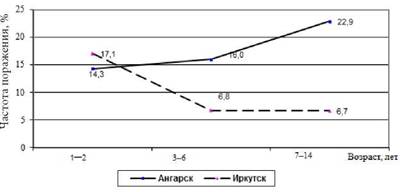
Рис. 2.8. Частота поражения ЛОР-органов при острых инфекциях дыхательных путей в разных возрастных группах у детей в Ангарске и Иркутске |
Следующим этапом оценки клинических проявлений инфекционных заболеваний на сравниваемых территориях стал анализ осложнений у населения, проживающего в условиях техногенного прессинга. Не останавливаясь подробно на этом аспекте проблемы, отметим лишь наличие значительно большего их числа при инфекционных заболеваниях в зонах с высоким уровнем промышленного загрязнения атмосферного воздуха. Весьма демонстративным примером являются полученные данные по частоте пора-
59
жения ЛОР-органов при острых инфекциях дыхательных путей у детей. Нами показано, что в Иркутске наблюдается типичное распределение данного вида осложнений, т. е. имеет место снижение этого показателя с возрастом. В Ангарске отмечается противоположная тенденция что нехарактерно, учитывая анатомо-физиологические особенности детского организма (рис. 2.8).
Весьма интересные материалы получены нами и при сравнении частоты встречаемости атипичных (в нашем случае безжелтушных) форм и хронизации инфекционного процесса при остром гепатите В (ГВ) у детей (рис. 2.9).
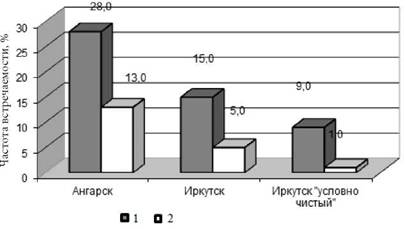
Рис. 2.9. Частота встречаемости атипичных (1) и хронических (2) форм гепатита В у детей |
Установлено, что количество безжелтушных форм ГВ значительно возрастает в загрязненных районах. Например, в Ангарске этот показатель составил 28,2±0,05 %, а в Иркутске - 15,2±0,25 % (р < 0,05). Аналогичные данные, касающиеся более высокой распространенности безжелтушных форм заболевания в Ангарске, получены и при гепатите А (ГА). В этой связи следует выделить два важнейших обстоятельства. Во-первых, увеличение безжелтушных форм имеет негативное эпидемиологическое значение в связи с тем, что способствует распространению инфекционного 60 агента в популяции. Это связано с тем, что данная категория больных не выявляется активно и соответственно среди этой группы не проводятся противоэпидемические мероприятия. Кроме того, известно, что атипичное течение (в том числе безжелтушные формы) всех видов вирусных гепатитов является результатом недостаточного иммунного ответа макроорганизма по отношению к соответствующим инфекционным агентам, что, в свою очередь, обусловливает персистенцию вирусов в течение многих лет, способствуя хронизации инфекционного процесса.
Проведенные нами исследования свидетельствуют в пользу того, что формирование хронического течения при гепатите В у больных, проживающих на территориях с высоким уровнем техногенного загрязнения, встречается значительно чаще (р < 0,05), чем у больных, проживающих в экологически более благоприятных условиях. Указанная особенность выявлена при сравнении хронизации инфекционного процесса ГВ как между Ангарском и Иркутском (12,8 и 8,0 % соответственно), так и между различными по уровню экологического напряжения районами Иркутска (4,8 и 1,0 % соответственно).
Рассмотренная закономерность по распространению атипичных (безжелтушных) форм и хронизации процесса при ГВ отчетливо видна на представленном выше рис. 2.9 при сопоставлении распределений двух сравниваемых показателей.
С учетом полученных нами материалов становится очевидным, что техногенное загрязнение атмосферного воздуха является значимым фактором риска для формирования затяжного и хронического течения гепатита В у детей (группа риска), проживающих в зонах экологического неблагополучия.
Таким образом, техногенное загрязнение атмосферного воздуха, способствуя разбалансировке регуляторных систем здорового организма и развитию сопутствующих соматических заболеваний, приводит к утяжелению клинического течения инфекционного процесса, большей его длительности, а также к более частому развитию осложнений, хронизации процесса и удлинению сроков реконвалесценции.
В качестве следующего этапа в изучении особенностей инфекционной патологии в условиях экологического прессинга нами
61
проанализирована многолетняя динамика заболеваемости. В частности, дана ее сравнительная характеристика на опытной и контрольной территориях при «естественном» развитии эпидемического процесса. Такое проявление заболеваемости зависит преимущественно от инфекционно-иммунологических отношений и оцениваемого воздействия экологического (антропотехногенного) фактора риска. При управляемых средствами иммунопрофилактики инфекциях проявления заболеваемости связаны и зависят в первую очередь от проводимой иммунизации, в связи с чем указанная группа патологии не учитывалась при указанном анализе.
Многолетняя динамика заболеваемости изучена для следующих эпидемиологически значимых групп и (или) нозологических форм инфекционной патологии: острые респираторные вирусные инфекции (ОРВИ), краснуха, острые гепатиты А, В и С (ГА, ГВ, ГС), дизентерия Зонне, дизентерия Флекснера, сальмонеллезы. Сравнительный анализ заболеваемости для краснухи и вирусных гепатитов А и В представлен до начала массовой вакцинопрофилактики.
Прежде чем перейти к оценке основных полученных результатов, отметим, что при анализе динамики инфекционной заболеваемости по ее годовым показателям далеко не по всем ее видам выявлены статистически значимые различия между территориями. Во многих случаях они проявляются лишь как тенденции с более высокими уровнями в районах экологического неблагополучия. Возможно, это связано с выраженным размахом годовых показателей, что, в свою очередь, способствует так называемой «статистической» нестабильности результатов. Тем не менее проведенный сравнительный эпидемиологический анализ динамики заболеваемости в Ангарске и Иркутске позволил достаточно объективно разделить проанализированные виды инфекционной патологии на две группы, которые неравнозначно отреагировали на техногенное загрязнение атмосферного воздуха:
первая - инфекционные заболевания, имеющие выраженные отличия в своей многолетней динамике на сравниваемых территориях (ОРВИ, краснуха, ГА, дизентерия Зонне);
вторая - инфекционные заболевания, имеющие близкие (практически синхронизированные) распределения динамических рядов на сравниваемых территориях (ГВ, ГС, дизентерия Флекснера, сальмонеллезы).
Что же разделяет эти группы? С эпидемиологических позиций очевидно, что первая группа относится к инфекциям с выраженным синусоидальным ритмом (сезонность и цикличность). Во второй группе эта эпидемиологическая особенность проявляется в значительно меньшей степени.
Сравнение многолетней динамики эпидемического процесса указанных инфекций показало, что при всех формах инфекционной патологии с выраженными ритмическими проявлениями заболеваемости (первая группа) имеют место значимо более высокие показатели в городе с высоким уровнем техногенного загрязнения атмосферного воздуха.
Другая особенность рассматриваемой группы инфекционной заболеваемости в Ангарске - ее меньшая стабильность по сравнению с Иркутском, т.е. имеет место значительно большая выраженность колебаний относительно линии тренда (рис. 2.10-2.12 ).
Нерегулярные колебания заболеваемости, выраженные в значительно большей степени в районах с высоким уровнем техногенного загрязнения атмосферного воздуха, могут быть объяснены дестабилизацией рассматриваемой биологической системы под действием экологического неблагополучия.
Для обоснования выдвинутого тезиса были использованы количественные эпидемиологические показатели и визуальная логическая оценка кривых многолетней заболеваемости. Для лучшего восприятия материала динамика заболеваемости на рисунках в зависимости от наглядности представлено или совокупным, или детским населением.
На примере ГА (см. рис. 2.11) отчетливо видно, что среди детей Иркутска продолжительность многолетних циклов составляет 6 лет, а среди детей Ангарска колеблется в пределах 4-5 лет. Изменение многолетней картины заболеваемости проявилось не только в укорочении длительности циклов, но и в значительном разбросе такого показателя, как циклическая надбавка. В Иркутске при отдельных подъемах заболеваемости он находился на относи-
63
тельно стабильном уровне (21,2-29,4 %), а в Ангарске был значительно более выражен (15,1-44,9 %) и более чем в 2 раза превышал диапазон различий на территории сравнения.
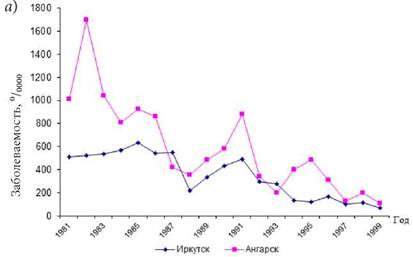 |
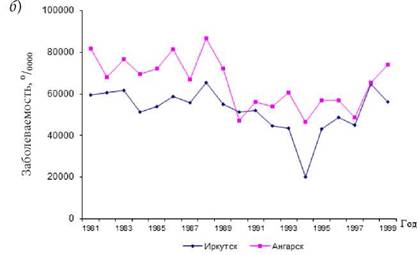
Рис. 2.10. Динамика заболеваемости детей гепатитом А (а), острыми респираторными инфекциями (б) в Ангарске и Иркутске в 1981-1999 гг. |
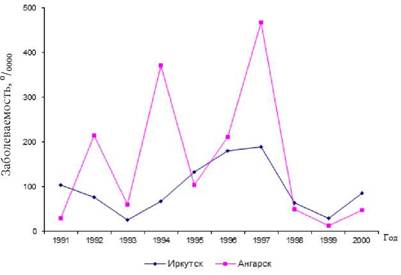
Рис. 2.11. Динамика заболеваемости населения краснушной инфекцией в Ангарске и Иркутске в 1991-2000 гг. |
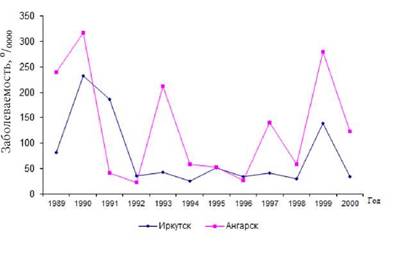
Рис. 2.12. Динамика заболеваемости населения дизентерией Зонне в Ангарске и Иркутске в 1989-2000 гг. |
Выявленные изменения в динамике инфекционной заболеваемости в Ангарске могут быть объяснены снижением неспецифической резистентности организма в виде угнетения иммунных реакций и проявлением состояния напряжения адаптации под действием комплекса ксенобиотиков [99], что, в свою очередь, способствует более ранним наступлениям периодических подъемов заболеваемости. Таким образом, в Иркутске эпидемический процесс ГА, как мы полагаем, в большей степени регулируется состоянием коллективного иммунитета. В Ангарске, за счет значительно более выраженного влияния загрязнения окружающей среды на отдельные сочлены паразитарной системы эпидемического процесса, вступают в действие дополнительные регулирующие факторы развития указанной биологической системы.
Аналогичная закономерность, связанная с искажением многолетней кривой заболеваемости в условиях экологического неблагополучия (укорочение циклов и выраженный разброс показателей) отчетливо проявляется и при всех остальных формах инфекционной патологии из группы инфекций с выраженным циклическим проявлением заболеваемости, что наглядно представлено на приведенных выше рисунках.
Одним из проявлений нестабильности эпидемического процесса в экологически неблагополучных условиях для всех форм инфекционной патологии из рассматриваемой нами первой группы инфекций является выраженный рост заболеваемости в годы ее циклических подъемов. Выявленная закономерность наиболее наглядно видна при визуальной оценке сравниваемых кривых заболеваемости краснухой (см. рис. 2.11). На представленном рисунке отчетливо видна не только выраженная интенсификация эпидемического процесса в годы подъема заболеваемости, но и значительное укорочение длительности циклов на экологически неблагополучной территории.
Как уже отмечалось выше, для второй группы инфекционной патологии (ГВ, ГС, дизентерия Флекснера, сальмонеллезы) не выявлено выраженных отличий в многолетней динамике заболеваемости между сравниваемыми территориями. Соответствующие показатели были практически синхронизиро- 66
ваны и не отличались по своим уровням, и лишь при дизентерии Флекснера при близком распределении указанных показателей имело место значимое их превышение (р < 0,05) для взрослого населения Иркутска.
Представленные результаты эпидемиологического анализа показывают, что у инфекций с выраженными ритмическими колебаниями влияние экзогенных факторов на развитие (интенсификацию) эпидемического процесса проявляется значительно более выражено по сравнению с инфекциями с их слабыми проявлениями. Влияние экзогенных факторов опосредуется прежде всего на локальном уровне развития эпидемического процесса, что имеет особое значение при факторах риска малой интенсивности.
Для обоснования этого положения рассмотрим динамику инфекционной заболеваемости в условиях плановой вакцинопрофилактики в различных по степени экологического напряжениях территориях Иркутской области. В этой связи вновь подчеркнем, что многолетняя динамика инфекционной заболеваемости, идущая без активного вмешательства вакцинации в ход эпидемического процесса, зависит преимущественно от естественно складывающихся инфекционно-иммунологических отношений и различного рода факторов риска, воздействующих на эпидемический процесс. Развитие заболеваемости при управляемых средствами иммунопрофилактики инфекциях должно быть связано и зависеть в первую очередь от качества проводимой иммунизации.
С изложенных выше позиций несомненный интерес представляет эпидемиологическая оценка фактора техногенного загрязнения при таких управляемых инфекциях, как корь и коклюш. В настоящее время эпидемиологическая ситуация в отношении обеих форм инфекционных заболеваний на территории Российской Федерации носит довольно нестабильный характер. Тем не менее в России при той и другой инфекции сохраняется цикличность, что является неблагоприятным эпидемиологическим признаком. Кроме этого отметим, что при кори в последнее время участились случаи заболевания взрослых, а при коклюше низкий уровень охвата прививками и осуществление вакцинопрофилактики только у детей до 3-летнего возраста также способствуют сдвигу забо-
леваемости на старшие возрастные группы. Приведенные данные с определенной вероятностью позволяют прогнозировать, что в ближайшие годы возможен очередной подъемом заболеваемости.
Проведение соответствующего эпидемиологического анализа (сопоставление динамических рядов, представленных показателями заболеваемости и охвата прививками) позволило нам оценить не только проявления многолетней динамики рассматриваемых показателей на сравниваемых территориях, но и эффективность вакцинопрофилактики среди детского населения в опытной группе (Ангарск) и в группе сравнения (Иркутск).
Визуальный анализ полученного материала (рис. 2.13, 2.14) свидетельствует, что в многолетней динамике заболеваемости выявляется четкая цикличность в развитии эпидемического процесса при обеих нозоформах. Длительность циклов на сравниваемых территориях была одинакова и составляла при коклюше 5 лет, а при кори (в первую половину анализируемого периода) - 4 года. При интенсивном снижении заболеваемости корью (второй период наблюдения) выраженная цикличность при этой инфекции отсутствовала, что не позволяет представить ее количественную оценку.
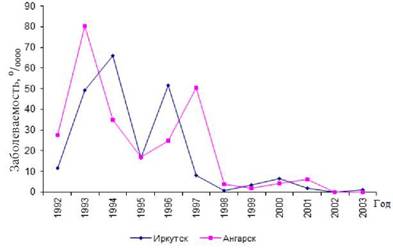
Рис. 2.13. Многолетняя динамика заболеваемости детей корью в Ангарске и Иркутске |
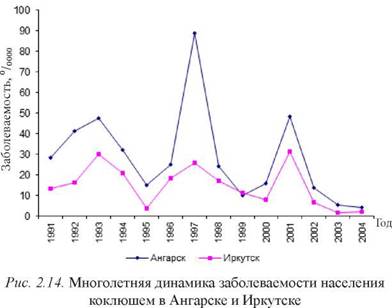 |
Подчеркнем еще раз, что проявления цикличности в Ангарске и Иркутске были упорядочены и практически не различались на сравниваемых территориях. Такая динамика заболеваемости при инфекциях с выраженным синусоидальным ритмом, существенно отличается от соответствующих показателей при инфекционных заболеваниях с выраженными многолетними ритмическими проявлениями, но протекающими без воздействия на них различного рода вакцин. Как нами было показано при ОРВИ, дизентерии Зонне, а также в допрививичный период при гепатите А и крас- нушной инфекции, имела место дестабилизация эпидемического процесса в условиях выраженного экологического неблагополучия.
Выявленные различия могут быть объяснены тем, что проявления заболеваемости при управляемых инфекциях находятся прежде всего под активным воздействием иммунопрофилактики, которая в обоих городах проводилась в соответствии с нормативными требованиями. Влияние других условий на эпидемический
процесс (в том числ
Источник: А.А. Яковлев, Е.Д. Савилов, «ПРОБЛЕМНЫЕ ВОПРОСЫ ОБЩЕЙ ЭПИДЕМИОЛОГИИ» 2015
А так же в разделе «2.1. Экологическая эпидемиология »
- ПРЕДИСЛОВИЕ
- ОТ АВТОРОВ
- ГЛАВА 1 ОБ ОПРЕДЕЛЕНИИ ЭПИДЕМИОЛОГИИ КАК НАУКИ И ПОНЯТИИ О ЕЕ ПРЕДМЕТЕ И ОБЪЕКТЕ
- Библиографический список
- ГЛАВА 2 СОВРЕМЕННЫЕ НАПРАВЛЕНИЯ В ЭПИДЕМИОЛОГИИ
- Эпидемиология хронических инфекций.
- Эпидемиология медленных инфекций.
- Эпидемиология сапронозов.
- Эпидемиология катастроф.
- Географическая (энвайроментальная) эпидемиология.
- Госпитальная эпидемиология.
- Эпидемиология неинфекционных болезней.
- 2.1. Молекулярная эпидемиология (на модели Mycobacterium tuberculosis)
- 2.1. Морская эпидемиология (история становления и основные направления развития)
- 2.4. Интеграционная эпидемиология
- Библиографический список
- ГЛАВА 3 О ПРИЧИНЕ, УСЛОВИЯХ И МЕХАНИЗМАХ ФОРМИРОВАНИЯ ЗАБОЛЕВАЕМОСТИ
- Классификация факторов риска эпидемического процесса
- Библиографический список
- ГЛАВА 4 О ВОЗМОЖНЫХ МЕХАНИЗМАХ РАЗВИТИЯ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
- Библиографический список
- ГЛАВА 5 О ВОЗМОЖНЫХ МЕХАНИЗМАХ ФОРМИРОВАНИЯ ЦИКЛИЧНОСТИ И СЕЗОННОСТИ В ЭПИДЕМИЧЕСКОМ ПРОЦЕССЕ
- Библиографический список
- ГЛАВА 6 ГЕТЕРОГЕННОСТЬ ПОПУЛЯЦИИ ВОЗБУДИТЕЛЯ И ХОЗЯИНА КАК ОСНОВА ТЕОРЕТИЧЕСКИХ ВОЗЗРЕНИЙ АКАДЕМИКА В.Д. БЕЛЯКОВА НА РАЗВИТИЕ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
- Библиографический список
- ГЛАВА 7 СИСТЕМНЫЙ ПОДХОД К ЭПИДЕМИОЛОГИЧЕСКОЙ ОЦЕНКЕ РОЛИ СОЧЕТАННЫХ ИНФЕКЦИЙ В РАЗВИТИИ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА (НА МОДЕЛИ ВИРУСНЫХ ГЕПАТИТОВ)
- Библиографический список
- ГЛАВА 8 ЭВОЛЮЦИЯ ИДЕЙ АКАДЕМИКА В.Д. БЕЛЯКОВА О САМОРЕГУЛЯЦИИ ПАРАЗИТАРНЫХ СИСТЕМ В КОНЦЕПЦИИ ИНТЕГРАЦИОННО-КОНКУРЕНТНОГО РАЗВИТИЯ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
- Библиографический список
- ГЛАВА 9 ИНТЕГРАЦИОННЫЙ ПОДХОД К ЭПИДЕМИОЛОГИЧЕСКОЙ ОЦЕНКЕ НЕКОТОРЫХ НАПРАВЛЕНИЙ ПРОФИЛАКТИКИ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ
- Библиографический список
- ГЛАВА 10 ТЕОРЕТИЧЕСКИЕ АСПЕКТЫ ЭПИДЕМИОЛОГИЧЕСКОЙ ОЦЕНКИ ПАНДЕМИИ ГРИППА А(H1N1)pdm09 2009-2010 гг.
- Библиографический список
- ГЛАВА 11 ГЛОБАЛЬНЫЙ ЭПИДЕМИОЛОГИЧЕСКИЙ НАДЗОР КАК ОТВЕТ НА ГЛОБАЛИЗАЦИЮ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
- Библиографический список
- ЗАКЛЮЧЕНИЕ
- Библиографический список