Характеристика типов аллергических реакций
Клинические особенности, дифференциальная диагностика и лечение аллергических болезней в значительной мере обусловлены механизмом их развития, характером и ксличеством аллергенного воздействия, типом специфического ответа.
По классификации Сооке (1930), аллергические реакции делятся на реакции немедленного и замедленного типа.
А.Д. Адо (1978), исходя из иммунологической патогенетической концепции аллергии, предложил реакции немедленного,
антителозависимого, типа обозначать как В-зависимые—химер- гические, связанные с выбросом соответствующих биологически активных веществ, а реакции замедленного, антителонезависимого, типа как Т-зависимые (китергические — реакции клеточного типа). Каждая из этих групп в соответствии с иммуно- компетентным механизмом развития была подразделена на подгруппы.
- В-зависимые аллергические реакции, обусловленные лимфоцитами типа В:
а) А-глобулиновые, вызываемые сскрсторным глобулином А (аллергический ринит, бронхит);
б) G-глобулиновые (феномен Артюса, сывороточная болезнь, анафилактический шок у кролика, цитотоксические реакции);
в) Е-глобулиновые (анафилаксия у человека, морской свинки, мышей, поллиноз);
г) М-глобулиновые.
- Т-зависимые аллергические реакции:
а) туберкулинового типа;
б) типа контактного дерматита;
в) реакции отторжения трансплантата.
Данная классификация имеет клинико-экспериментальное прикладное значение и углубляет наши представления при сопоставлении с известной клинико-патогенетической классификацией Gell и Coombs (1968), в которой представлены четыре основных типа реакции:
- реагиновый тип повреждения тканей (I);
- цитотоксический тип повреждения тканей (II);
- иммунокомплексный тип реакции (III);
- клеточный, замедленный тип реакции (IV).
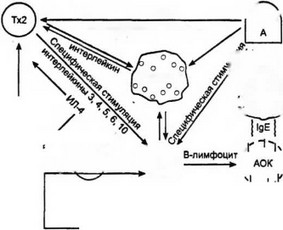
В зависимости от фазы развития А. Д. Адо (1978), В.И. Пыц- кий с соавт. (1984) каждый из названных типов подразделяют на стадии: 1) иммунологическую; 2) патохимическую и 3) патофизиологическую, что позволяет наглядно продемонстрировать этапы формирования аллергических и аутоиммунных реакций при различных патологических состояниях (рис. 1).
Реагиновый (IgE-зависимый, немедленный) тип повреждения тканей
Чаще развивается при сенсибилизации к неинфекционным аллергенам (пыльце растений, бытовым, эпидермальным, пищевым аллергенам, гаптенам).
Иммунологическая фаза реакции включает неспецифическую (взаимодействие аллергена с макрофагом) и специфическую (выработку антител к аллергену) форму реагирования че*
 ПАТОХИМИЧЕСКАЯ ПАТОФИЗИОЛОГИЧЕСКАЯ ФАЗА ФАЗА
ПАТОХИМИЧЕСКАЯ ПАТОФИЗИОЛОГИЧЕСКАЯ ФАЗА ФАЗА
Хелпер

'^птен'
т ii ii //^% /отучиая0 U клеткао
Voo о j
(™)—;gt; (О) —» Q {
|И
Хемотаксические T7V\ w факторы _ * лСу у
эоэинофилов Бронхоспазм
Гистамин Лейкотриены Брадикинин Ацетилхолин
Бронхосп'аз! Воспаление
аллергической реакции
рез систему кооперации Тх2 и В-лимфоцитов. Последние трансформируются в плазмоциты и вырабатывают специфические антитела (реагины — IgE). Опосредованная связь между неспецифическим (макрофагом) и специфическим (Тх2) звеньями иммунитета осуществляется с помощью иммуноцитокинов (ИЛ-1). Индукция синтеза IgE В-лимфоцитами опосредована через лимфокины (ИЛ-3, ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-10), секретируе- мые Тх2. В продукции IgE В-лимфоцитами важную роль играет также блокада их кластеров дифференцировки (CD40), которая реализуется с помощью лиганд CD^L — поступление второго сигнала со стороны Тх2. В запуске продукции IgE участвуют и другие иммуноцитокины, в частности ИЛ-13, который имеет некоторое сходство с ИЛ-4 (И.С. Гущин, 1998). Допускается, что активизированные тучные клетки, базофилы также могут выполнять функцию Тх2, поскольку они способны синтезировать ИЛ-4 или ИЛ-13 и могут экспрессировать CD40L. Однако наиболее вероятно, что эти клетки не участвуют в первичной индукции IgE, а лишь усиливают его выработку. Они, по-видимому, способны расширить сенсибилизирующий спектр аллергенов на фоне аллергии к одному аллергену, что часто наблюдается на практике. Следует заметить, что активизированные макрофаги, высвобождая ИЛ-12, способны тормозить синтез IgE за счет угнетения продукции ИЛ-4. Таким образом, зная систему управления синтезом IgE, можно оказывать иммунокорректирующий эффект, влиять на выброс реагинов.
Циркулируя в кровотоке, IgE оседают на тучных клетках, железистых образованиях, гладкомышечных элементах с помощью Fc-фрагмента, к которому в названных структурах имеются рецепторы. Степень сенсибилизации, уровень продукции IgE в значительной мере зависят от функции и количества Т-супрессоров — регуляторов темпа и выраженности аллергической реакции.
Патохимическая фаза реакции. Развитие аллергической реакции нельзя буквально понимать как переключение с иммунологической на патохимическую фазу, так как они тесно связаны друг с другом. В течении иммунологической фазы прослеживается участие различных каскадов иммуноцитокинов (биологически активных веществ) — выброс макрофагами ИЛ-1 и Тх2—ИЛ-4, ИЛ-5, ИЛ-6 (индукторов секреции IgE).
При развитии патохимической фазы реакции реагинового типа видное место принадлежит тучной клетке—тканевой форме базофила, которая содержит обширный набор медиаторов, сосредоточенных в гранулах. На одну клетку приходится 100— 300 гранул. Тучные клетки сосредоточены в соединительной ткани вокруг сосудов, в ворсинках кишечника, в волосяных фолликулах. В активации-дегрануляции тучных клеток участвуют ионы
Са, которые стимулируют эндомембранную проэстеразу, трансформируемую в эстеразу. Эстераза посредством фосфолипазы D способствует гидролизу мембранных фосфолипидов, обеспечивающих истончение и разрыхление мембраны, что облегчает экзоцитоз ipaHyji Данный процесс сопровождается увеличением содержания внутриклеточного Са2+ и повышением цГМФ.
Следует отметить, что подобный процесс дегрануляции тучных клеток может наблюдаться как при аллергических реакциях (индуктор аллерген +IgE), так и при холинергических, провоцируемых холодом/теплом, декстраном, рентгеноконтрастными веществами, химотрипсином, соматостатином, АТФ, т.е. ложноаллергическим механизмом (неспецифическим индуктором).
Среди биологически активных веществ, экспрессируемых из гранул тучных клеток, различают медиаторы первого порядка, которые опосредуют быстрые реакции (через 20—30 мин после воздействия аллергена), и медиаторы второго порядка, вызывающие позднюю фазу аллергической реакции (через 2—6 ч).
К медиаторам первого порядка относятся гистамин, гепарин, триптаза, ФХЭ (фактор хемотаксиса эозинофилов), ФХН (фактор хемотаксиса нейтрофилов), ФАТ (фактор активации тромбоцитов и высвобождения их медиаторов).
К медиаторам второго порядка—запуска производных ара- хидоновой кислоты относятся лейкотриены, тромбоксаны, про- стагпандины и др.
Патохимическая фаза, таким образом, ассоциируется как с иммунологической, так и с патофизиологической фазой.
Патофизиологическая фаза реакции (капилляропатия, отечный синдром, формирование клеточных инфильтратов в шоковом органе) может проявляться риноконъюнктивальным синдромом, ларинготрахеитом, атопическим дерматитом, бронхиальной астмой, анафилактическим шоком, пищевой аллергией, крапивницей, отеком Квинке.
Диагностика. См. Диагностические аллергены. В перспективе в диагностике реагинового типа реакции важное место может занять способ установления переключения дифференцировки Т-лимфоцитов при аллергическом ответе в сторону Тх2. Биологическим маркером такого переключения могло бы быть определение содержания Тх2, ИЛ-4, ИЛ-5, клетки CD30. Последняя экспрессируется на В-лимфоцитах (СО^-клетках).
Таким образом, определение кластеров дифференцировки клеток (CD) позволяет не только точно установить природу клеток (исходя из номерного знака кластера), но и своевременно определить направленность иммунологического переключения в сторону аллергической гиперреактивности (И.С. Гущин, 1998).
Источник: Н. А. Скепьян, «Аллергические болезни: дифференциальный диагноз, лечение» 2000