Рефлекторная регуляция дыхания осуществляется благодаря тому, что нейроны дыхательного центра имеют связи с многочисленными механорецепторами дыхательных путей и альвеол легких и рецепторов сосудистых рефлексогенных зон. В легких человека находятся следующие типы механорецепторов: 1) ирритантные, или быстроадаптирующиеся, рецепторы слизистой оболочки дыхательных путей; 2) рецепторы растяжения гладких мышц дыхательных путей; 3) J-рецепторы.
Рефлексы со слизистой оболочки полости носа. Раздражение ирритантных рецепторов слизистой оболочки полости носа, например табачным дымом, инертными частицами пыли, газообразными веществами, водой вызывает сужение бронхов, голосовой щели, брадикардию, снижение сердечного выброса, сужение просвета сосудов кожи и мышц. Защитный рефлекс проявляется у новорожденных при кратковременном погружении в воду. У них возникает остановка дыхания, препятствующая проникновению воды в верхние дыхательные пути.
Рефлексы с глотки. Механическое раздражение рецепторов слизистой оболочки задней части полости носа вызывает сильнейшее сокращение диафрагмы, наружных межреберных мышц, а следовательно, вдох, который открывает дыхательный путь через носовые ходы (аспирационный рефлекс). Этот рефлекс выражен у новорожденных.
Рефлексы с гортани и трахеи. Многочисленные нервные окончания расположены между эпителиальными клетками слизистой оболочки гортани и главных бронхов. Эти рецепторы раздражаются вдыхаемыми частицами, раздражающими газами, бронхиальным секретом, инородными телами. Все это вызывает кашлевой рефлекс, проявляющийся в резком выдохе на фоне сужения гортани и сокращение гладких мышц бронхов, которое сохраняется долгое время после рефлекса.
Кашлевой рефлекс является основным легочным рефлексом блуждающего нерва.
Рефлексы с рецепторов бронхиол. Многочисленные миелинизи- рованные рецепторы находятся в эпителии внутрилегочных бронхов и бронхиол. Раздражение этих рецепторов вызывает гиперпноэ, бронхоконстрикцию, сокращение гортани, гиперсекрецию слизи, но никогда не сопровождается кашлем. Рецепторы наиболее чувствительны к трем типам раздражителей: 1) табачному дыму, многочисленным инертным и раздражающим химическим веществам; 2) повреждению и механическому растяжению дыхательных путей при глубоком дыхании, а также пневмотораксе, ателектазах, действии бронхоконстрикторов; 3) легочной эмболии, легочной капиллярной гипертензии и к легочным анафилактическим феноменам.
Рефлексы с J-рецепторов. В альвеолярных перегородках в контакте с капиллярами находятся особые J-рецепторы. Эти рецепторы особенно чувствительны к интерстициальному отеку, легочной венозной гипертензии, микроэмболии, раздражающим газам и ингаляционным наркотическим веществам, фенилдигуаниду (при внутривенном введении этого вещества). Стимуляция J-рецепторов вызывает вначале апноэ, затем поверхностное тахипноэ, гипотензию и брадикардию.
Рефлекс Геринга — Брейера. Раздувание легких у наркотизированного животного рефлекторно тормозит вдох и вызывает выдох. Перерезка блуждающих нервов устраняет рефлекс. Нервные окончания, расположенные в бронхиальных мышцах, играют роль рецепторов растяжения легких. Их относят к медленно адаптирующимся рецепторам растяжения легких, которые иннервируются ми- елинизированными волокнами блуждающего нерва.
Рефлекс Геринга — Брейера контролирует глубину и частоту дыхания. У человека он имеет физиологическое значение при дыхательных объемах свыше 1 л (например, при физической нагрузке). У бодрствующего взрослого человека кратковременная двусторонняя блокада блуждающих нервов с помощью местной анестезии не влияет ни на глубину, ни на частоту дыхания.
У новорожденных рефлекс Геринга — Брейера четко проявляется только в первые 3—4 дня после рождения.
Проприоцептивный контроль дыхания. Рецепторы суставов грудной клетки посылают импульсы в кору больших полушарий и являются единственным источником информации о движениях грудной клетки и дыхательных объемах.
Межреберные мышцы, в меньшей степени диафрагма, содержат большое количество мышечных веретен. Активность этих рецепторов проявляется при пассивном растяжении мышц, изометрическом сокращении и изолированном сокращении интрафузальных мышечных волокон. Рецепторы посылают сигналы в соответствующие сегменты спинного мозга. Недостаточное укорочение инспираторных или экспираторных мышц усиливает импульсацию от мышечных веретен, которые через / -мотонейроны повышают активность «-мотонейронов и дозируют таким образом мышечное усилие.
Хеморефлексы дыхания. Рог и РСО2 ® зртериэльнои крови чс— ловека и животных поддерживается на достаточно стабильном уровне, несмотря на значительные изменения потребления О2 и выделение СОг- Гипоксия и понижение pH крови (ацидоз) вызывают усиление вентиляции (гипервентиляция), а гипероксия и повышение pH крови (алкалоз) — понижение вентиляции (гиповентиляция) или апноэ. Контроль за нормальным содержанием во внутренней среде организма О2, СОг и pH осуществляется периферическими и центральными хеморецепторами.
Адекватным раздражителем для периферических хеморецепторов является уменьшение Р02 артериальной крови, в меньшей степени увеличение Рсщ и pH, а для центральных хеморецепторов — увеличение концентрации Н4 во внеклеточной жидкости мозга.
Артериальные (периферические) хеморецепто- р ы. Периферические хеморецепторы находятся в каротидных и аортальных тельцах. Сигналы от артериальных хеморецепторов по синокаротидным и аортальным нервам первоначально поступают к нейронам ядра одиночного пучка продолговатого мозга, а затем переключаются на нейроны дыхательного центра. Ответ периферических хеморецепторов на понижение Рао2 является очень быстрым, но нелинейным. При Рао2 в пределах 80—60 мм рт. ст. (10,6—8,0 кПа) наблюдается слабое усиление вентиляции, а при Рао2 ниже 50 мм рт. ст. (6,7 кПа) возникает выраженная гипервентиляция.
Расог и pH крови только потенцируют эффект гипоксии на артериальные хеморецепторы и не являются адекватными раздражителями для этого типа хеморецепторов дыхания.
Реакция артериальных хеморецепторов и дыхания на гипоксию. Недостаток 02 в артериальной крови является основным раздражителем периферических хеморецепторов. Импульсная активность в афферентных волокнах синокаротидного нерва прекращается при Расgt;2 выше 400 мм рт. ст. (53,2 кПа). При нормоксии частота разрядов синокаротидного нерва составляет 10% от их максимальной реакции, которая наблюдается при Рао2 около 50 мм рт. ст. и ниже. Гипоксическая реакция дыхания практически отсутствует у коренных жителей высокогорья и исчезает примерно через 5 лет у жителей равнин после начала их апаптации к высокогорью (3500 м и выше).
Центральные хеморецепторы. Окончательно не установлено местоположение центральных хеморецепторов. Исследователи считают, что такие хеморецепторы находятся в ростральных отделах продолговатого мозга вблизи его вентральной поверхности, а также в различных зонах дорсального дыхательного ядра.
Наличие центральных хеморецепторов доказывается достаточно просто: после перерезки синокаротидных и аортальных нервов у подопытных животных исчезает чувствительность дыхательного центра к гипоксии, но полностью сохраняется реакция дыхания на гиперкапнию и ацидоз. Перерезка ствола мозга непосредственно выше продолговатого мозга не влияет на характер этой реакции.
Адекватным раздражителем для центральных хеморецепторов является изменение концентрации Н* во внеклеточной жидкости мозга. Функцию регулятора пороговых сдвигов pH в области центральных хеморецепторов выполняют структуры гематоэнцефалического барьера, который отделяет кровь от внеклеточной жидкости мозга. Через этот барьер осуществляется транспорт 02, С02 и Н+ между кровью и внеклеточной жидкостью мозга. Транспорт С02 и Н+ из внутренней среды мозга в плазму крови через структуры гематоэнцефалического барьера регулируется с участием фермента карбоангидразы.
Реакция дыхания на С02. Гиперкапния и ацидоз стимулируют, а гипокапния и алкалоз тормозят центральные хеморецепторы.
Для определения чувствительности центральных хеморецепторов к изменению pH внеклеточной жидкости мозга используют метод возвратного дыхания. Испытуемый дышит из замкнутой емкости, заполненной предварительно чистым 02. При дыхании в замкнутой
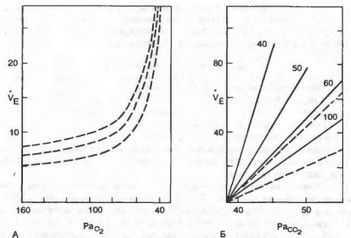
Рис. 8.12. Изменение вентиляции легких (Ve, л*мии 1) в зависимости от парциального давления Ог (А) и СО2 (Б) в альвеолярном воздухе при различном содержании Ог в альвеолярном воздухе (40, 50, 60 и 100 мм рт. ст.).
системе выдыхаемый СО2 вызывает линейное увеличение концентрации СО2 и одновременно повышает концентрацию ЬГ в крови, а также во внеклеточной жидкости мозга. Тест проводят в течение
- 5 мин под контролем содержания СО2 в выдыхаемом воздухе.
На рис. 8.12 показано изменение объема вентиляции при различном уровне напряжения СОг в артериальной крови. При Расог ниже 40 мм рт. ст. (5,3 кПа) может возникнуть апноэ в результате гипокапнии. В этот период дыхательный центр мало чувствителен к гипоксической стимуляции периферических хеморецепторов.
