Провоспалительные цитокины
Цитокины — ключевые гуморальные факторы воспаления, необходимые для реализации защитных функций врожденного иммунитета. В развитии воспаления участвуют три группы цитокинов — воспалительные, или провоспалительные цитокины, хемокины, колониестимулирующие факторы, а также функционально связанные факторы IL-12 и IFNy. Цитокинам также принадлежит важная роль в подавлении и сдерживании воспалительной реакции. К противовоспалительным цитокинам относят трансформирующий фактор роста в (TGFp), IL-10; часто роль противовоспалительного фактора играет IL-4.
Выделяют 3 основных представителя группы провоспалительных цитокинов — TNFa, IL-1 и IL-6; относительно недавно к ним были добавлены IL-17 и IL-18. Эти цитокины продуцируются в основном активированными моноцитами и макрофагами преимущественно в очаге воспаления. Провоспалительные цитокины могут вырабатываться также нейтрофилами, дендритными клетками, активированными В-, NK- и Т-лимфоцитами. В очаге проникновения патогенов цитокины первыми начинают синтезировать немногочисленные местные воспалительные макрофаги. Затем в процессе эмиграции лейкоцитов из кровотока численность клеток-продуцентов возрастает и их спектр расширяется. В частности, к синтезу провоспалительных цитокинов подключаются стимулированные продуктами микроорганизмов и факторами воспаления эпителиальные, эндотелиальные, синовиальные, глиальные клетки, фибробласты. Гены цитокинов относят к индуцибельным. Естественные индукторы их экспрессии — патогены и их продукты, действующие через TLR и другие патогенраспознающие рецепторы. Классический индуктор — бактериальный ЛПС. В то же время некоторые провоспалительные цитокины (IL-1, TNFa) сами способны индуцировать синтез провоспалительных цитокинов.
Провоспалительные цитокины синтезируются и секретируются достаточно быстро, хотя кинетика синтеза различных цитокинов этой группы неодинакова. В типичных случаях (быстрый вариант) экспрессию их мРНК отмечают через 15—30 мин после индукции, появление белкового продукта в цитоплазме — через 30—60 мин, содержание его во внеклеточной среде достигает максимума через 3—4 ч. Синтез цитокинов конкретной клеткой продолжается довольно непродолжительное время — обычно немногим больше суток. Не весь синтезируемый материал секретируется. Некоторое количество цитокинов экспрессируется на поверхности клетки или содержится в цитоплазматических гранулах. Выброс гранул могут вызывать те же активирующие сигналы, что и продукция цитокинов. Это обеспечивает быстрое (в течение 20 мин) поступление цитокинов в очаг поражения.
Провоспалительные цитокины выполняют многие функции. Основная их роль — «организация» воспалительной реакции (рис. 2.55). Один из наиболее важных и ранних эффектов провоспалительных цитокинов — усиление экспрессии молекул адгезии на эндотелиальных клетках, а также на самих лейкоцитах, что приводит к миграции в очаг воспаления лейкоцитов из кровяного русла (см. раздел 2.3.3). Кроме того, цитокины индуцируют усиление кислородного метаболизма клеток, экспрессии ими рецепторов для цитокинов и других факторов воспаления, стимуляцию выработки цитокинов, бактерицидных пептидов и т.д. Провоспалительные цитокины оказывают преимущественно местное действие. Попадание избыточно секретируемых провоспалительных цитокинов в циркуляцию способствует проявлению системных эффектов воспаления, а также стимулирует выработку цитокинов клетками, отдаленными от очага воспаления. На системном уровне провоспалительные цитокины стимулируют продукцию белков острой фазы, вызывают повышение температуры тела, действуют на
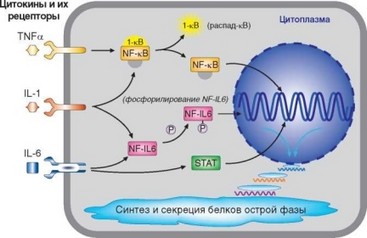
Рис. 2.55. Внутриклеточная передача сигнала, запускаемая провоспалительными цитокинами и механизмы активации провоспалительных генов
эндокринную и нервную системы, а в высоких дозах приводят к развитию патологических эффектов (плоть до шока, подобного септическому).
IL-1 — собирательное обозначение семейства белков, включающего более 11 молекул. Функция большинства из них неизвестна, однако 5 молекул — IL-1a (по современной классификации — IL-1F1), IL-1p (IL-1F2), IL-1RA (IL-1F3), IL-18 (IL-1F4) и IL-33 (IL-1F11) — активные цитокины.
IL-1a и IL-1P традиционно называют IL-1, поскольку они взаимодействуют с одним и тем же рецептором и их эффекты неразличимы. Гены этих цитокинов локализованы в длинном плече хромосомы 2 человека. Гомология между ними на нуклеотидном уровне составляет 45%, на аминокислотном — 26%. Обе молекулы имеют р-складчатую структуру: они содержат 6 пар антипараллельных р-слоев и имеют форму трилистника. Клетки синтезируют молекулу-предшественник с молекулярной массой около 30 кДа, лишенную сигнальных пептидов, что свидетельствует о необычном пути процессинга молекулы IL-1. Молекулярная масса зрелых белков — около 18 кДа.
IL-1a существует в трех формах — внутриклеточной (растворимая молекула присутствует в цитозоле и выполняет регуляторные функции), мембранной (молекула доставляется на поверхность клетки за счет механизма, аналогичного рециклингу рецепторов и заякоривается в мембране) и секре- тиуремой (молекула секретируется в первоначальном виде, но подвергается процессингу — расщеплению внеклеточными протеазами с образованием активного цитокина массой 18 кДа). Основной вариант молекулы IL-1a у человека — мембранный. В такой форме действие цитокина более выражено, но проявляется только локально.
Процессинг IL-1P происходит внутри клетки с участием специализированного фермента — IL-1-конвертазы (каспазы 1), находящегося в лизосомах.
Активация этого фермента осуществляется в составе инфламмосомы — временной надмолекулярной структуры, включающей, кроме неактивной каспазы 1, внутриклеточные рецепторы семейства NLR (см. раздел 2.2.3) — NOD1, NOD2, IPAF и др. Для активации каспазы 1 необходимо распознавание названными рецепторами PAMP, что вызвает развитие активационного сигнала. В результате происходит образование транскрипционного фактора NF-kB и индукция провоспалительных генов, а также активация инфламмосомы и содержащейся в ней каспазы 1. Активированный фермент расщепляет молекулу-предшественницу IL-1P, и образовавшийся зрелый цитокин с молекулярной массой 18 кДа секретируется клеткой.
IL-1a, IL-1P, а также рецепторный антагонист IL-1 имеют общие рецепторы, экспрессируемые спонтанно на многих типах клеток. При активации клеток на них возрастает число мембранных рецепторов для IL-1. Основной из них — IL-1RI — во внеклеточной части содержит 3 иммуноглобулиноподобных домена. Его внутриклеточная часть представляет TIR- домен, структурно сходный с аналогичными доменами TLR и запускающий те же сигнальные пути (см. раздел 2.2.1). Число этих рецепторов невелико (200—300 на клетку), но они обладают высоким сродством к IL-1 (Kd равен 10-11 М). Другой рецептор — IL-1RII — лишен сигнальной составляющей в цитоплазматической части, не передает сигнал и служит рецептором-ловушкой. В передаче сигнала от IL-1RI принимают участие те же факторы, что и для TLR (например, MyD88, IRAK и TRAF6), что приводит к аналогичным результатам — образованию транскрипционных факторов NF-kB и АР-1, вызывающих экспрессию одного и того же набора генов (см. рис. 2.12). Эти гены отвечают за синтез провоспалительных цитокинов, хемокинов, молекул адгезии, ферментов, обеспечивающих бактерицидность фагоцитов, и других генов, продукты которых участвуют в развитии воспалительной реакции. К продуктам, секрецию которых индуцируют IL-1, принадлежит и сам IL-1, т.е. в данном случае срабатывает петля положительной обратной связи.
Мишенями IL-1 потенциально могут быть любые клетки организма. В наибольшей степени его действие затрагивает эндотелиальные клетки, все виды лейкоцитов, клетки хрящевой и костной тканей, синовиальные и эпителиальные клетки, многие разновидности нервных клеток. Под влиянием IL-1 происходит индукция экспрессии больше 100 генов; с его участием реализуется больше 50 различных биологических реакций. Основные эффекты IL-1 вызывают эмиграцию лейкоцитов и активацию их фагоцитарной и бактерицидной активности. Они влияют также на свертывающую систему и сосудистый тонус, определяя особенности гемодинамики в очаге воспаления. IL-1 оказывает многоплановое действие на клетки не только врожденного, но и адаптивного иммунитета, обычно стимулируя проявления и того, и другого.
IL-1 обладает множеством системных эффектов. Он стимулирует выработку гепатоцитами белков острой фазы, при действии на центр терморегуляции гипоталамуса вызывает развитие лихорадки, участвует в развитии системных проявлений воспалительного процесса (например, в недомогании, снижении аппетита, сонливости, адинамии), что связано с действием IL-1 на ЦНС. Усиливая экспрессию рецепторов для колониестимулирующих факторов, IL-1 способствует усилению гемопоэза, с чем связано его радиозащитное действие. IL-1 стимулирует выход из костного мозга лейкоцитов, в первую очередь нейтрофилов, в том числе незрелых, что приводит к появлению при воспалении лейкоцитоза и сдвигу лейкоцитарной формулы влево (накопление незрелых форм клеток). Эффекты IL-1 влияют на вегетативные функции и даже на высшую нервную деятельность (изменение поведенческих реакций и т.д.). Мишенями IL-1 могут быть также хондроциты и осте- оциты, с чем связана способность IL-1 вызывать разрушение хряща и кости при их вовлечении в воспалительный процесс и наоборот, гиперплазия патологических тканей (паннус при ревматоидном артрите). Повреждающее действие IL-1 проявляется и при септическом шоке, повреждении суставов при ревматоидном артрите и ряде других патологических процессов.
Дублирование IL-1 эффектов бактериальных продуктов связано с потребностью в многократном воспроизведении активирующего эффекта патогенов без их диссеминации. Микроорганизмы стимулируют только клетки, находящиеся в непосредственной близости от места проникновения, прежде всего локальные макрофаги. Затем тот же эффект многократно воспроизводится молекулами IL-1p. Выполнение IL-1 указанной функции облегчается экспрессией их рецепторов почти всеми клетками организма при активации (происходит прежде всего в очаге воспаления).
Рецепторный антагонист IL-1 (IL-1RA) гомологичен IL-1a и IL-1P (гомология составляет соответственно 26% и 19%). Он взаимодействует с рецепторами IL-1, но не способен передавать в клетку сигнал. В результате IL-1RA выступает в роле специфического антагониста IL-1. IL-1RA секретируют те же клетки, что и IL-1, этот процесс не требует участия каспазы 1. Выработку IL-1RA индуцируют те же факторы, что и синтез IL-1, однако некоторое его количество спонтанно продуцируют макрофаги и гепатоциты. В результате этот фактор постоянно присутствует в сыворотке крови. Вероятно, это необходимо для предотвращения негативных последствий системного действия IL-1, вырабатываемого в значительных количествах при остром воспалении. В настоящее время проводят испытания рекомбинантного IL-1RA в качестве лекарственного препарата при лечении хронических воспалительных заболеваний (ревматоидный артрит и т.д.)
IL-18 — провоспалительный цитокин, родственный IL-ф: он также синтезируется в виде предшественника, конвертируемого с участием каспазы 1; взаимодействует с рецептором, цитоплазматическая часть которого содержит домен TIR и передает сигнал, приводящий к активации NF-kB. В результате происходит активация всех провоспалительных генов, однако она выражена слабее, чем при действии IL-1. Отдельное свойство IL-18 — индукция (особенно в сочетании с IL-12) синтеза клетками IFNy. В отсутствие IL-12 IL-18 индуцирует синтез антагониста IFNy — IL-4 и способствует развитию аллергических реакций. Действие IL-18 ограничивает растворимый антагонист, связывающий его в жидкой фазе.
IL-33 структурно очень близок IL-18. Процессинг IL-33 тоже происходит с участием каспазы 1. Однако этот цитокин отличается от других представителей семейства IL-1 выполняемыми функциями. Своеобразие действия IL-33 значительной степени обусловлено тем, что его рецептор экспрессируется избирательно на ^2-клетках. В связи с этим IL-33 способствует секреции ^2-цитокинов IL-4, IL-5, IL-13 и развитию аллергических процессов. Он не оказывает существенного провоспалительного действия.
Фактор некроза опухоли а (ФНОа или TNFa) — представитель другого семейства иммунологически значимых белков. Это провоспалительный цитокин с широким спектром активности. TNFa имеет в-складчатую структуру. Он синтезируется в виде функционально активной мембранной молекулы про-TNFa с молекулярной массой 27 кДа, представляющей трансмембранный белок II типа (т.е. его N-концевая часть направлена внутрь клетки). В результате протеолиза во внеклеточном домене формируется растворимый мономер с молекулярной массой 17 кДа. Мономеры TNFa спонтанно формируют тример с молекулярной массой 52 кДа, представляющий основную форму этого цитокина. Тример имеет колоколовидную форму, причем субъединицы соединяются своими С-концами, содержащими по 3 участка связывания с рецептором, тогда как N-концы друг с другом не связаны и не участвуют во взаимодействии с рецепторами (а следовательно, и в выполнении цитокином своих функций). При кислых значениях рН TNFa приобретает a-спиральную структуру, что обусловливает изменение некоторых его функций, в частности, усиление цитотоксичности. TNF — прототипический член большого семейства молекул суперсемейства TNF (табл. 2.31). К нему относят лимфотоксины a и в (в растворимой форме существует только первый), а также многие мембранные молекулы, участвующие в межклеточных взаимодействиях (CD154, FasL, BAFF, OX40-L, TRAIL, APRIL, LIGHT), которые будут упоминаться далее в различных контекстах. Согласно современной номенклатуре, название членов суперсемейства состоит из сокращения TNFSF и порядкового номера (для TNFa — TNFSF2, для лимфотоксина a — TNFSF1).
Таблица 2.31. Основные представители семейств фактора некроза опухоли и его рецепторов
Основные продуценты TNFa, как и IL-1, — моноциты и макрофаги. Его секретируют также нейтрофилы, эндотелиальные и эпителиальные клетки, эозинофилы, тучные клетки, В- и Т-лимфоциты при их вовлечении в воспалительный процесс. TNFa выявляют в кровотоке раньше других провоспалительных цитокинов — уже через 20—30 мин после индукции воспаления, что связано со «сбрасыванием» клетками мембранной формы молекулы, а возможно также с выбросом TNFa в составе содержимого гранул.
Есть 2 типа рецепторов TNF, общие для TNFa и лимфотоксина a — TNFRI (от tumor necrosis factor receptor I) и TNFRII с молекулярной массой соответственно 55 и 75 кДа. TNFRI присутствует практически на всех клетках организма, кроме эритроцитов, а TNFRII — преимущественно на клетках иммунной системы. TNFR образуют большое семейство, в которое входят молекулы, участвующие во взаимодействии клеток и индукции клеточной гибели — апоптоза. Сродство TNFa к TNFRI ниже, чем к TNFRII (соответственно около 5х10-10 М и 55х10-11 М. При связывании TNFa-тримера происходит необходимая для передачи сигнала тримеризация его рецепторов.
Особенности передачи сигнала от этих рецепторов во многом определяются структурой их внутриклеточной части. Цитоплазматическая часть TNFRI представлена так называемым доменом смерти, от которого поступают сигналы, приводящие к включению механизма апоптоза; TNFRII лишен домена смерти. Передача сигнала от TNFRI происходит с участием адапторных белков TRADD (TNFR-associated death domain) и FADD (Fas- associated death domain), тоже содержащих домены смерти. Помимо пути, приводящего к развитию апоптоза (через активацию каспазы 8 или синтез церамида), выделяют еще несколько сигнальных путей, включаемых с участием факторов TRAF2/5 и RIP-1. Первый из названных факторов передает сигнал по пути, приводящему к активации фактора NF-kB, т.е. по классическому пути индукции провоспалительных генов (см. рис. 2.55). Сигнальный путь, активируемый фактором RIP-1, приводит к активации MAP-каскада с конечным продуктом — транскрипционным фактором АР-1. Этот фактор включает гены, обеспечивающие активацию клетки и предотвращающие развитие апоптоза. Судьбу клетки, таким образом, определяет баланс про- и антиапоптотических механизмов, запускаемых при связывании TNFa с TNFRI.
Реализация функций TNFa связана преимущественно с действием через TNFRI — выключение соответствующего гена приводит к развитию тяжелого иммунодефицита, тогда как последствия инактивации гена TNFRII незначительны. На пике воспалительной реакции рецепторы ФНОa могут «сбрасываться» с мембраны и выходить в межклеточное пространство, где они связывают ФНОa, оказывая противовоспалительное действие. В связи с этим растворимые формы TNFR используют при лечении хронических воспалительных заболеваний. При этом оказалось, что препарат на основе растворимого TNFRII оказался клинически наиболее эффективным.
Как и IL-1, TNFa усиливает экспрессию молекул адгезии, синтез провоспалительных цитокинов и хемокинов, белков острой фазы, ферментов фагоцитарных клеток и т.д. Наряду с IL-1, TNFa участвует в формировании всех основных местных, а также некоторых системных проявлений воспаления. Он активирует эндотелиальные клетки, стимулирует ангиогенез, усиливает миграцию и активирует лейкоциты. TNFa в большей степени, чем IL-1, влияет на активацию и пролиферацию лимфоцитов. В комбинации с IFNy TNFa индуцирует активность NO-синтазы фагоцитов, что значительно усиливает их бактерицидный потенциал. TNFa стимулирует пролиферацию фибробластов, способствуя заживлению ран. При повышенной локальной выработке TNFa преобладают процессы повреждения тканей, проявляющиеся развитием геморрагического некроза. Помимо этого TNFa подавляет активность липопротеиновой липазы, что ослабляет липогенез и приводит к развитию кахексии (одно из первоначальных названий TNFa — кахексин). Повышенное высвобождение TNFa и его накопление в циркуляции, например при действии высоких доз бактериальных суперантигенов, вызывает развитие тяжелой патологии — септического шока. Таким образом, действие TNFa, направленное на выполнение защитной функции и поддержание гомеостаза, может сопровождаться тяжелыми токсическими эффектами (местными и системными), нередко служащими причиной смерти.
IL-6 — провоспалительный цитокин широкого действия. Он также служит прототипическим фактором семейства цитокинов, включающего, кроме собственно IL-6, онкостатин М (OSM), лейкемия-ингибирующий фактор (LIF), цилиарный нейротрофический фактор (CNTF), кардиотро- пин-1 (CT-1), а также IL-11 и IL-31. Молекулярная масса IL-6 — 21 кДа. IL-6 вырабатывают моноциты и макрофаги, эндотелиальные, эпителиальные, глиальные, гладкомышечные клетки, фибробласты, Т-лимфоциты типа Th2, а также многие опухолевые клетки. Выработка IL-6 миелоидными клетками индуцируется при взаимодействии их TLR с микроорганизмами и их продуктами, а также под влиянием IL-1 и TNFa. При этом в течение 2 ч содержание IL-6 в плазме крови возрастает в 1000 раз.
Рецепторы всех факторов семейства IL-6 содержат общий компонент — цепь gp130, присутствующую практически на всех клетках организма. Второй компонент рецептора индивидуален для каждого цитокина. Специфическая цепь рецептора IL-6 (gp80) отвечает за связывание этого цитокина, тогда как gp130 участвует в передаче сигнала, поскольку связана с тирозинкиназами Jak1 и Jak2. При взаимодействии IL-6 с рецептором запускается следующая последовательность событий: IL-6-мономер взаимодействует с цепью gp80, происходит димеризация комплексов (2 молекулы цитокина — 2 цепи gp80), после чего к комплексу присоединяется 2 цепи gр130, что приводит к фосфорилированию Jak-киназ. Последние фосфорилируют факторы STAT1 и STAT3, которые димеризуются, перемещаются в ядро и связывают промоторы генов-мишеней. Цепь gp80 легко «смывается» с клетки; в свободной форме она взаимодействует с цитокином, инактивируя его, т.е. выступает в качестве специфического ингибитора IL-6.
IL-6 участвует в индукции практически всего комплекса местных проявлений воспаления. Он влияет на миграцию фагоцитов, усиливая выработку СС-хемокинов, привлекающих моноциты и лимфоциты, и ослабляя продукцию СХС-хемокинов, привлекающих нейтрофилы. Провоспалительные эффекты IL-6 выражены слабее, чем у IL-1 и TNFa, в противоположность которым он не усиливает, а угнетает выработку провоспалительных цитокинов (IL-1, TNFa и IL-6) и хемокинов клетками, вовлеченными в воспалительный процесс. Таким образом, IL-6 сочетает свойства про- и противовоспалительных цитокинов и участвует не только в развитии, но и в ограничении воспалительной реакции.
IL-6 — основной фактор, индуцирующий в гепатоцитах экспрессию генов белков острой фазы. IL-6 влияет на различные этапы гемопоэза, в том числе на пролиферацию и дифференцировку стволовых клеток. Он служит ростовым фактором незрелых плазматических клеток, существенно усиливая гуморальный иммунный ответ. IL-6 влияет также на Т-лимфоциты, повышая активность цитотоксических Т-клеток.
IL-17 и связанные с ним цитокины. Группа цитокинов, включающая разновидности IL-17, привлекла всеобщее внимание в связи с открытием особой разновидности Т-хелперов — Th17, участвующей в развитии некоторых повреждающих форм воспалительных реакций, в частности, при аутоиммунных процессах (см. раздел 3.4.3.2). Роль этих цитокинов в реакциях адаптивного иммунного ответа будет рассмотрена далее. Здесь приведем только общую характеристику цитокинов и кратко рассмотрим их роль в реакциях врожденного иммунитета.
Семейство IL-17 включает 6 белков, обозначаемых буквами от А до F. Свойствами провоспалительных цитокинов из них обладают IL-17A и IL-17F. Они представляют собой гомодимеры, скрепленные дисульфидной связью; их молекулярная масса — 17,5 кДа. Эти цитокины продуцируются упомянутыми Th17, а также CD8+ Т-клетками, эозинофилами, нейтрофилами. IL-23 стимулирует развитие ТЫ7-клеток и выработку IL-17.
Рецепторы для IL-17 экспрессируются многоми клетками — эпителиальными, фибробластами, клетками иммунной системы, в частности, нейтрофилами. Основной результат взаимодействия IL-17 с рецептором состоит, как и при действии других провоспалительных цитокинов, в индукции фактора NF-kB и экспрессии многочисленных NF-KB-зависи- мых генов воспаления.
Один из важных биологических эффектов IL-17 (наряду с IL-23) — поддержание гомеостаза нейтрофилов. Эти цитокины усиливают образование нейтрофилов, стимулируя выработку G-CSF. При этом усиление или ослабление выработки IL-17 и IL-23 регулируется численностью нейтрофилов в периферических тканях: снижение числа этих клеток в результате апоптоза приводит к усилению выработки цитокинов.
Провоспалительное действие IL-17 реализуется главным образом через усиление выработки других цитокинов (IL-8, IL-6, y-CSF, ряд хемокинов) и экспрессии молекул адгезии. У мышей, трансгенных по IL-17 или по IL-23, развивается системное хроническое воспаление, имеющее интерстициальный характер, с инфильтрацией нейтрофилами, эозинофилами, макрофагами и лимфоцитами различных органов. За этими цитокинами признают ведущую роль в развитии хронических аутоиммунных заболеваний.
Семейство IL-12
IL-12 был идентифицирован по способности активировать NK-клетки, вызывать пролиферацию Т-лимфоцитов и индуцировать синтез IFNy. IL-12 занимает особое место в ряду цитокинов, вырабатываемых клетками системы врожденного иммунитета, поскольку он (как и его главные продуценты — дендритные клетки) служит связующим звеном между врожденным и адаптивным иммунитетом. С другой стороны, IL-12 входит в тандем IL-12—IFNy, которому принадлежит ключевая роль в осуществлении иммунной защиты от внутриклеточных патогенов.
IL-12 представляет димер, состоящий из субъединиц р40 и р35. Его суммарная молекулярная масса — 75 кДа. Функциональная активность IL-12 связана с его субъединицей р40. «Полномасштабный» IL-12 секретируют активированные моноциты, макрофаги, миелоидные дендритные клетки, нейтрофилы, эпителиальные клетки барьерных тканей (они продуцируют и ^-12р35 и IL-12p40 субъединицы цитокина). Большинство же клеток организма синтезирует только функционально неактивную субъединицу ^-12р35. Количество гетеродимера IL-12, секретируемого клеткой, ограничено субъединицей р35. IL-12p40 синтезируется в избытке и может димеризоваться с образованием гомодимера, выступающего в качестве антагониста IL-12, а также хемоаттрактанта. Индукторы выработки IL-12 — прежде всего патогены, распознаваемые TLR и другими паттернраспознающими рецепторами. Выработку IL-12 усиливают IL-1, IFNy, а также межклеточные взаимодействия, опосредованные CD40-CD154 и другими парами молекул семейств — TNFR.
Рецептор IL-12 сильнее всего экспрессирован на NK-клетках, активированных ТЫ-клетках и цитотоксических Т-лимфоцитах и в меньшей степени — на дендритных клетках. Экспрессия рецептора IL-12 активированными Т-клетками усиливается под влиянием IL-12, IFNy, IFNa, TNFa и при кос- тимуляции через рецептор CD28. Рецептор для IL-12 представляет димер, образованный субъединицами IL-12RP1 (100 кДа), и IL-12RP2 (130 кДа, CD212), с которым ассоциирован белок с молекулярной массой 85 кДа. В связывании IL-12 участвуют и Pj и р2 цепи, тогда как в передаче сигнала задействована преимущественно субъединица IL-12RP2. Внутриклеточный домен Pj-цепи ассоциирован с киназой JAK2, внутриклеточный домен Р2-цепи — с киназой Tyk2. Киназы фосфорилируют транскрипционные факторы STAT1, STAT3, STAT4 и STAT5.
Главная функция IL-12, обусловленная его способностью стимулировать цитотоксические лимфоциты (NK и T) и индуцировать дифферен- цировку Thl-клеток (см. раздел 3.4.3.1), — запуск клеточных механизмов защиты от внутриклеточных патогенов. IL-12 действует на NK- и NKT-клетки уже на ранних стадиях иммунных процессов, усиливая пролиферацию и цитотоксическую активность NK-клеток, а позже — цитотоксических Т-лимфоцитов и синтез всеми этими клетками IFNy. Несколько позже IL-12 индуцирует дифференцировку Thl-клеток, тоже продуцирующих IFNy. Условие индукции Thl-клеток — предварительная экспрессия активированными CD4+ Т-клетками субъединицы рецептора IL-12RP2. После этого клетки приобретают способность связывать IL-12, что приводит к активации фактора STAT4, регулирующего экспрессию генов, характерных для Thl-клеток (для экспрессии гена IFNG более важно действие транскрипицонного фактора T-bet). Одновременно IL-12 подавляет дифференцировку ^2-клеток и ослабляет выработку клетками
В-ряда антител классов IgE и IgA. Действуя на дендритные и другие АПК IL-12 индуцирует экспрессию костимулирующих молекул (CD80/86, и др.), а также продуктов МНС-II АПК. Таким образом, IL-12 играет связующую роль между врожденным и адаптивным иммунитетом и усиливает иммунные механизмы, ответственные за защиту от внутриклеточных патогенов и опухолей.
К семейству IL-12 относят IL-23, IL-27 и IL-35. Эти цитокины представляют гетеродимеры: IL-23 образован двумя субъединицами — ^-23р19 и IL-12p40 (идентична соответствующей субъединице IL-12), IL-27 — субъединицами Ebi3 и IL-27p28, IL-35 — субъединицами Ebi3 и IL-12p35. Эти цитокины продуцируются преимущественно дендритными клетками. Выработку цитокинов семейства IL-12 запускают представленные на патогенах PAMP и цитокины, в особенности GM-CSF.
Рецепция IL-23 осуществляется двумя разными структурами: субъединицу IL-12p40 распознает ргцепь рецептора для IL-12, а субъединицу ^-23р19 — особый рецептор — IL-23R. Основную роль в передаче сигнала от IL-23 играет STAT4. Рецептор для IL-27 активирует молекулы WSX-1 (гомолог р2-субъединицы IL-12R) и gp130 (полипептидная цепь, входящая в состав рецепторов для цитокинов семейства IL-6).
Подобно IL-12, IL-23 и IL-27 действуют преимущественно на CD4+ Т-клетки, способствуя их дифференцировке по Th1-пути. Особенности IL-23 — преимущественное действие на Т-клетки памяти, а также способность поддерживать развитие Т-хелперов типа Th17. IL-27 отличается от двух других цитокинов семейства способностью вызывать пролиферацию не только активированных, но и покоящихся CD4+ Т-клеток. Недавно было показано, что IL-27 и IL-35 могут выступать в качестве регуляторных (супрессорных) факторов, поскольку их субъединица Ebi3 — мишень ключевого фактора регуляторных Т-клеток FOXP3.
Колониестимулирующие факторы (CSF) (табл. 2.32) или гемопоэтины представлены тремя цитокинами — GM-CSF, G-CSF и M-CSF. К ним функционально близок IL-3 (Multi-CSF). Эти факторы называют колониестимулирующими, поскольку впервые были идентифицированы по способности поддерживать рост in vitro колоний гемопоэтических клеток соответствующего состава. IL-3 обладает наиболее широким спектром действия, поскольку поддерживает рост любых колоний гемопоэтических клеток, кроме лимфоидных. GM-CSF поддерживает рост как смешанных гранулоцитарно-моноцитарных колоний, так и отдельно колоний грану- лоцитов и моноцитов/макрофагов. G-CSF и M-CSF специализируются на поддержании роста и дифференцировки соответствующих колоний. Эти факторы не только обеспечивают выживаемость и пролиферацию кроветворных клеток указанных типов, но и способны активировать уже зрелые дифференцированные клетки (M-CSF — макрофаги, G-CSF — нейтрофилы). M-CSF участвует в дифференцировке моноцитов в макрофаги и подавляет дифференцировку моноцитов в дендритные клетки. G-CSF, помимо действия на гранулоцитарный ветвь гемопоэза, вызывает мобилизацию кроветворных стволовых клеток из костного мозга в кровоток.
Таблица 2.32. Характеристика колониестимулирующих факторов
G-CSF, GM-CSF и IL-3 структурно характеризуются как гемопоэтины, содержащие 4 а-спиральных домена. Их рецепторы содержат по 2 полипептидные цепи, их относят к семейству гемопоэтиновых рецепторов. M-CSF отличается от остальных CSF. Он представляет собой димерную молекулу и существует как в растворимой, так и в мембраносвязанной формах. Его рецептор имеет внеклеточные Ig-подобные домены и внутриклеточный домен, обладающий активностью тирозинкиназы (наименование этой киназы-протоонкогена — с-Fms — иногда переносят на весь рецептор). При связывании М-CSF с рецепторами происходит их димеризация и активация киназы.
Колониестимулирующие факторы продуцируются эндотелиальными клетками и фибробластами а также моноцитами/макрофагами. GM-CSF и IL-3, кроме того, синтезируются Т-лимфоцитами. Под влиянием бактериальных продуктов (через паттернраспознающие рецеторы) и провоспалительных цитокинов синтез и секреция колониестимулирующих факторов значительно возрастает, что приводит к усилению миелопоэза. Особенно сильно стимулируется гранулоцитопоэз, что сопровождается ускоренной эмиграцией клеток, в том числе незрелых, на периферию. Это создает картину нейтрофильного лейкоцитоза со сдвигом формулы вправо, весьма характерным для воспаления. Препараты на основе GM- и G-CSF применяют в клинической практике для стимуляции гранулоцитопоэза, ослабленного цитотоксическими воздействиями (облучение, прием химиопрепаратов при лечении опухолевых заболеваний и т.д.). G-CSF применяют для мобилизации стволовых кроветворных клеток с последующим использованием индуцированной лейкомассы для восстановления нарушенного гемопоэза.
Фактор стволовых клеток (SCF — stem cell factor, c-kit ligand) cекретируют клетки стромы костного мозга (фибробласты, эндотелиальные клетки), а также разные типы клеток в период эмбрионального развития. SCF существует в виде трансмембранной и растворимой молекул (последняя образуется в результате протеолитического отщепления внеклеточной части). SCF выявляют в плазме крови. Его молекула имеет две дисульфидные связи. Рецептор SCF — с-Кк — обладает тирозинкиназной активностью и по своей структуре близок к Flt-3 и c-Fms (рецептор M-CSF). При связывании SCF происходят димеризация рецепторов и их фосфорилирование. Передача сигнала происходит с участием PI3K и MAP-каскада.
Мутации гена SCF и его рецептора описаны давно (мутации steel); у мышей они проявляются изменением окраски шерсти и нарушением гемопоэза. Мутации, нарушающие синтез мембранной формы фактора, вызывают грубые дефекты развития эмбриона. Совместно с другими факторами SCF участвует в поддержании жизнеспособности стволовых кроветворных клеток, обеспечивает их пролиферацию, поддерживает ранние этапы гемопоэза. SCF особенно важен для эритропоэза и развития тучных клеток, а также служит ростовым фактором для тимоцитов на стадиях DN1 и DN2.
По структуре и биологической активности сходными с SCF свойствами обладает фактор Flt-3L- (Fms-like thyrosinkinase 3-ligand), в сочетании с другими факторами поддерживающий ранние этапы миелопоэза и развитие В-лифмоцитов. SCF играет роль фактора роста лейкозных миелобластов.
Хемокины, представляющие важный гуморальный фактор воспаления и врожденного иммунитета, рассмотрены выше при описании хемотаксиса лейкоцитов (см. раздел 2.3.2).
Выделяют 3 основных представителя группы провоспалительных цитокинов — TNFa, IL-1 и IL-6; относительно недавно к ним были добавлены IL-17 и IL-18. Эти цитокины продуцируются в основном активированными моноцитами и макрофагами преимущественно в очаге воспаления. Провоспалительные цитокины могут вырабатываться также нейтрофилами, дендритными клетками, активированными В-, NK- и Т-лимфоцитами. В очаге проникновения патогенов цитокины первыми начинают синтезировать немногочисленные местные воспалительные макрофаги. Затем в процессе эмиграции лейкоцитов из кровотока численность клеток-продуцентов возрастает и их спектр расширяется. В частности, к синтезу провоспалительных цитокинов подключаются стимулированные продуктами микроорганизмов и факторами воспаления эпителиальные, эндотелиальные, синовиальные, глиальные клетки, фибробласты. Гены цитокинов относят к индуцибельным. Естественные индукторы их экспрессии — патогены и их продукты, действующие через TLR и другие патогенраспознающие рецепторы. Классический индуктор — бактериальный ЛПС. В то же время некоторые провоспалительные цитокины (IL-1, TNFa) сами способны индуцировать синтез провоспалительных цитокинов.
Провоспалительные цитокины синтезируются и секретируются достаточно быстро, хотя кинетика синтеза различных цитокинов этой группы неодинакова. В типичных случаях (быстрый вариант) экспрессию их мРНК отмечают через 15—30 мин после индукции, появление белкового продукта в цитоплазме — через 30—60 мин, содержание его во внеклеточной среде достигает максимума через 3—4 ч. Синтез цитокинов конкретной клеткой продолжается довольно непродолжительное время — обычно немногим больше суток. Не весь синтезируемый материал секретируется. Некоторое количество цитокинов экспрессируется на поверхности клетки или содержится в цитоплазматических гранулах. Выброс гранул могут вызывать те же активирующие сигналы, что и продукция цитокинов. Это обеспечивает быстрое (в течение 20 мин) поступление цитокинов в очаг поражения.
Провоспалительные цитокины выполняют многие функции. Основная их роль — «организация» воспалительной реакции (рис. 2.55). Один из наиболее важных и ранних эффектов провоспалительных цитокинов — усиление экспрессии молекул адгезии на эндотелиальных клетках, а также на самих лейкоцитах, что приводит к миграции в очаг воспаления лейкоцитов из кровяного русла (см. раздел 2.3.3). Кроме того, цитокины индуцируют усиление кислородного метаболизма клеток, экспрессии ими рецепторов для цитокинов и других факторов воспаления, стимуляцию выработки цитокинов, бактерицидных пептидов и т.д. Провоспалительные цитокины оказывают преимущественно местное действие. Попадание избыточно секретируемых провоспалительных цитокинов в циркуляцию способствует проявлению системных эффектов воспаления, а также стимулирует выработку цитокинов клетками, отдаленными от очага воспаления. На системном уровне провоспалительные цитокины стимулируют продукцию белков острой фазы, вызывают повышение температуры тела, действуют на

Рис. 2.55. Внутриклеточная передача сигнала, запускаемая провоспалительными цитокинами и механизмы активации провоспалительных генов
эндокринную и нервную системы, а в высоких дозах приводят к развитию патологических эффектов (плоть до шока, подобного септическому).
IL-1 — собирательное обозначение семейства белков, включающего более 11 молекул. Функция большинства из них неизвестна, однако 5 молекул — IL-1a (по современной классификации — IL-1F1), IL-1p (IL-1F2), IL-1RA (IL-1F3), IL-18 (IL-1F4) и IL-33 (IL-1F11) — активные цитокины.
IL-1a и IL-1P традиционно называют IL-1, поскольку они взаимодействуют с одним и тем же рецептором и их эффекты неразличимы. Гены этих цитокинов локализованы в длинном плече хромосомы 2 человека. Гомология между ними на нуклеотидном уровне составляет 45%, на аминокислотном — 26%. Обе молекулы имеют р-складчатую структуру: они содержат 6 пар антипараллельных р-слоев и имеют форму трилистника. Клетки синтезируют молекулу-предшественник с молекулярной массой около 30 кДа, лишенную сигнальных пептидов, что свидетельствует о необычном пути процессинга молекулы IL-1. Молекулярная масса зрелых белков — около 18 кДа.
IL-1a существует в трех формах — внутриклеточной (растворимая молекула присутствует в цитозоле и выполняет регуляторные функции), мембранной (молекула доставляется на поверхность клетки за счет механизма, аналогичного рециклингу рецепторов и заякоривается в мембране) и секре- тиуремой (молекула секретируется в первоначальном виде, но подвергается процессингу — расщеплению внеклеточными протеазами с образованием активного цитокина массой 18 кДа). Основной вариант молекулы IL-1a у человека — мембранный. В такой форме действие цитокина более выражено, но проявляется только локально.
Процессинг IL-1P происходит внутри клетки с участием специализированного фермента — IL-1-конвертазы (каспазы 1), находящегося в лизосомах.
Активация этого фермента осуществляется в составе инфламмосомы — временной надмолекулярной структуры, включающей, кроме неактивной каспазы 1, внутриклеточные рецепторы семейства NLR (см. раздел 2.2.3) — NOD1, NOD2, IPAF и др. Для активации каспазы 1 необходимо распознавание названными рецепторами PAMP, что вызвает развитие активационного сигнала. В результате происходит образование транскрипционного фактора NF-kB и индукция провоспалительных генов, а также активация инфламмосомы и содержащейся в ней каспазы 1. Активированный фермент расщепляет молекулу-предшественницу IL-1P, и образовавшийся зрелый цитокин с молекулярной массой 18 кДа секретируется клеткой.
IL-1a, IL-1P, а также рецепторный антагонист IL-1 имеют общие рецепторы, экспрессируемые спонтанно на многих типах клеток. При активации клеток на них возрастает число мембранных рецепторов для IL-1. Основной из них — IL-1RI — во внеклеточной части содержит 3 иммуноглобулиноподобных домена. Его внутриклеточная часть представляет TIR- домен, структурно сходный с аналогичными доменами TLR и запускающий те же сигнальные пути (см. раздел 2.2.1). Число этих рецепторов невелико (200—300 на клетку), но они обладают высоким сродством к IL-1 (Kd равен 10-11 М). Другой рецептор — IL-1RII — лишен сигнальной составляющей в цитоплазматической части, не передает сигнал и служит рецептором-ловушкой. В передаче сигнала от IL-1RI принимают участие те же факторы, что и для TLR (например, MyD88, IRAK и TRAF6), что приводит к аналогичным результатам — образованию транскрипционных факторов NF-kB и АР-1, вызывающих экспрессию одного и того же набора генов (см. рис. 2.12). Эти гены отвечают за синтез провоспалительных цитокинов, хемокинов, молекул адгезии, ферментов, обеспечивающих бактерицидность фагоцитов, и других генов, продукты которых участвуют в развитии воспалительной реакции. К продуктам, секрецию которых индуцируют IL-1, принадлежит и сам IL-1, т.е. в данном случае срабатывает петля положительной обратной связи.
Мишенями IL-1 потенциально могут быть любые клетки организма. В наибольшей степени его действие затрагивает эндотелиальные клетки, все виды лейкоцитов, клетки хрящевой и костной тканей, синовиальные и эпителиальные клетки, многие разновидности нервных клеток. Под влиянием IL-1 происходит индукция экспрессии больше 100 генов; с его участием реализуется больше 50 различных биологических реакций. Основные эффекты IL-1 вызывают эмиграцию лейкоцитов и активацию их фагоцитарной и бактерицидной активности. Они влияют также на свертывающую систему и сосудистый тонус, определяя особенности гемодинамики в очаге воспаления. IL-1 оказывает многоплановое действие на клетки не только врожденного, но и адаптивного иммунитета, обычно стимулируя проявления и того, и другого.
IL-1 обладает множеством системных эффектов. Он стимулирует выработку гепатоцитами белков острой фазы, при действии на центр терморегуляции гипоталамуса вызывает развитие лихорадки, участвует в развитии системных проявлений воспалительного процесса (например, в недомогании, снижении аппетита, сонливости, адинамии), что связано с действием IL-1 на ЦНС. Усиливая экспрессию рецепторов для колониестимулирующих факторов, IL-1 способствует усилению гемопоэза, с чем связано его радиозащитное действие. IL-1 стимулирует выход из костного мозга лейкоцитов, в первую очередь нейтрофилов, в том числе незрелых, что приводит к появлению при воспалении лейкоцитоза и сдвигу лейкоцитарной формулы влево (накопление незрелых форм клеток). Эффекты IL-1 влияют на вегетативные функции и даже на высшую нервную деятельность (изменение поведенческих реакций и т.д.). Мишенями IL-1 могут быть также хондроциты и осте- оциты, с чем связана способность IL-1 вызывать разрушение хряща и кости при их вовлечении в воспалительный процесс и наоборот, гиперплазия патологических тканей (паннус при ревматоидном артрите). Повреждающее действие IL-1 проявляется и при септическом шоке, повреждении суставов при ревматоидном артрите и ряде других патологических процессов.
Дублирование IL-1 эффектов бактериальных продуктов связано с потребностью в многократном воспроизведении активирующего эффекта патогенов без их диссеминации. Микроорганизмы стимулируют только клетки, находящиеся в непосредственной близости от места проникновения, прежде всего локальные макрофаги. Затем тот же эффект многократно воспроизводится молекулами IL-1p. Выполнение IL-1 указанной функции облегчается экспрессией их рецепторов почти всеми клетками организма при активации (происходит прежде всего в очаге воспаления).
Рецепторный антагонист IL-1 (IL-1RA) гомологичен IL-1a и IL-1P (гомология составляет соответственно 26% и 19%). Он взаимодействует с рецепторами IL-1, но не способен передавать в клетку сигнал. В результате IL-1RA выступает в роле специфического антагониста IL-1. IL-1RA секретируют те же клетки, что и IL-1, этот процесс не требует участия каспазы 1. Выработку IL-1RA индуцируют те же факторы, что и синтез IL-1, однако некоторое его количество спонтанно продуцируют макрофаги и гепатоциты. В результате этот фактор постоянно присутствует в сыворотке крови. Вероятно, это необходимо для предотвращения негативных последствий системного действия IL-1, вырабатываемого в значительных количествах при остром воспалении. В настоящее время проводят испытания рекомбинантного IL-1RA в качестве лекарственного препарата при лечении хронических воспалительных заболеваний (ревматоидный артрит и т.д.)
IL-18 — провоспалительный цитокин, родственный IL-ф: он также синтезируется в виде предшественника, конвертируемого с участием каспазы 1; взаимодействует с рецептором, цитоплазматическая часть которого содержит домен TIR и передает сигнал, приводящий к активации NF-kB. В результате происходит активация всех провоспалительных генов, однако она выражена слабее, чем при действии IL-1. Отдельное свойство IL-18 — индукция (особенно в сочетании с IL-12) синтеза клетками IFNy. В отсутствие IL-12 IL-18 индуцирует синтез антагониста IFNy — IL-4 и способствует развитию аллергических реакций. Действие IL-18 ограничивает растворимый антагонист, связывающий его в жидкой фазе.
IL-33 структурно очень близок IL-18. Процессинг IL-33 тоже происходит с участием каспазы 1. Однако этот цитокин отличается от других представителей семейства IL-1 выполняемыми функциями. Своеобразие действия IL-33 значительной степени обусловлено тем, что его рецептор экспрессируется избирательно на ^2-клетках. В связи с этим IL-33 способствует секреции ^2-цитокинов IL-4, IL-5, IL-13 и развитию аллергических процессов. Он не оказывает существенного провоспалительного действия.
Фактор некроза опухоли а (ФНОа или TNFa) — представитель другого семейства иммунологически значимых белков. Это провоспалительный цитокин с широким спектром активности. TNFa имеет в-складчатую структуру. Он синтезируется в виде функционально активной мембранной молекулы про-TNFa с молекулярной массой 27 кДа, представляющей трансмембранный белок II типа (т.е. его N-концевая часть направлена внутрь клетки). В результате протеолиза во внеклеточном домене формируется растворимый мономер с молекулярной массой 17 кДа. Мономеры TNFa спонтанно формируют тример с молекулярной массой 52 кДа, представляющий основную форму этого цитокина. Тример имеет колоколовидную форму, причем субъединицы соединяются своими С-концами, содержащими по 3 участка связывания с рецептором, тогда как N-концы друг с другом не связаны и не участвуют во взаимодействии с рецепторами (а следовательно, и в выполнении цитокином своих функций). При кислых значениях рН TNFa приобретает a-спиральную структуру, что обусловливает изменение некоторых его функций, в частности, усиление цитотоксичности. TNF — прототипический член большого семейства молекул суперсемейства TNF (табл. 2.31). К нему относят лимфотоксины a и в (в растворимой форме существует только первый), а также многие мембранные молекулы, участвующие в межклеточных взаимодействиях (CD154, FasL, BAFF, OX40-L, TRAIL, APRIL, LIGHT), которые будут упоминаться далее в различных контекстах. Согласно современной номенклатуре, название членов суперсемейства состоит из сокращения TNFSF и порядкового номера (для TNFa — TNFSF2, для лимфотоксина a — TNFSF1).
Таблица 2.31. Основные представители семейств фактора некроза опухоли и его рецепторов
|
Фактор (лиганд) |
Хро мосома |
Молекулярная масса, кДа |
Рецептор |
|
TNFa (TNFSF2) |
6р |
17; тример — 52; гликозилирован- ная форма — 25,6 |
TNF-R1, TNF-R2 (TNFRSF1, TNFRSF2) |
|
Лимфотоксинa (TNFSF1) |
6р |
22,3 |
TNF-R1, TNF-R2 |
|
Лимфотоксин в (TNFSF3) |
6р |
25,4 |
LTp-R (TNFRSF3) |
|
OX-40L (TNFSF4) |
1q |
34,0 |
OX-40 (TNFRSF4; CD134) |
|
CD40L (TNFSF5; CD154) |
Xp |
39,0 |
CD40 (TNFRSF5) |
|
FasL (TNFSF6; CD178) |
1q |
31,5 |
Fas/APO-1 (CD95) (TNFRSF6) |
|
CD27L (TNFSF7, CD70) |
19p |
50,0 |
CD27 (TNFRSF7) |
|
CD30L (TNFSF8) |
9q |
40,0 |
CD30 (TNFRSF8) |
|
4-1BBL (TNFSF9) |
19p |
27,5 |
4-1BB (TNFRSF9; CD137) |
|
TRAIL (TNFSF10) |
3q |
32,0 |
ВК4б ВК5 |
|
APRIL (TNFSF13) |
17p |
27,0 |
BCMA, TACI |
|
LIGHT (TNFSF14) |
16q |
26,0 |
HVEM (TNFRSF14) |
|
GITRL (TNFSF18) |
1p |
22,7 |
GITR (TNFRSF18) |
|
BAFF (TNFSF20) |
13 |
31,2 |
BAFFR, TACI, BCMA |
Основные продуценты TNFa, как и IL-1, — моноциты и макрофаги. Его секретируют также нейтрофилы, эндотелиальные и эпителиальные клетки, эозинофилы, тучные клетки, В- и Т-лимфоциты при их вовлечении в воспалительный процесс. TNFa выявляют в кровотоке раньше других провоспалительных цитокинов — уже через 20—30 мин после индукции воспаления, что связано со «сбрасыванием» клетками мембранной формы молекулы, а возможно также с выбросом TNFa в составе содержимого гранул.
Есть 2 типа рецепторов TNF, общие для TNFa и лимфотоксина a — TNFRI (от tumor necrosis factor receptor I) и TNFRII с молекулярной массой соответственно 55 и 75 кДа. TNFRI присутствует практически на всех клетках организма, кроме эритроцитов, а TNFRII — преимущественно на клетках иммунной системы. TNFR образуют большое семейство, в которое входят молекулы, участвующие во взаимодействии клеток и индукции клеточной гибели — апоптоза. Сродство TNFa к TNFRI ниже, чем к TNFRII (соответственно около 5х10-10 М и 55х10-11 М. При связывании TNFa-тримера происходит необходимая для передачи сигнала тримеризация его рецепторов.
Особенности передачи сигнала от этих рецепторов во многом определяются структурой их внутриклеточной части. Цитоплазматическая часть TNFRI представлена так называемым доменом смерти, от которого поступают сигналы, приводящие к включению механизма апоптоза; TNFRII лишен домена смерти. Передача сигнала от TNFRI происходит с участием адапторных белков TRADD (TNFR-associated death domain) и FADD (Fas- associated death domain), тоже содержащих домены смерти. Помимо пути, приводящего к развитию апоптоза (через активацию каспазы 8 или синтез церамида), выделяют еще несколько сигнальных путей, включаемых с участием факторов TRAF2/5 и RIP-1. Первый из названных факторов передает сигнал по пути, приводящему к активации фактора NF-kB, т.е. по классическому пути индукции провоспалительных генов (см. рис. 2.55). Сигнальный путь, активируемый фактором RIP-1, приводит к активации MAP-каскада с конечным продуктом — транскрипционным фактором АР-1. Этот фактор включает гены, обеспечивающие активацию клетки и предотвращающие развитие апоптоза. Судьбу клетки, таким образом, определяет баланс про- и антиапоптотических механизмов, запускаемых при связывании TNFa с TNFRI.
Реализация функций TNFa связана преимущественно с действием через TNFRI — выключение соответствующего гена приводит к развитию тяжелого иммунодефицита, тогда как последствия инактивации гена TNFRII незначительны. На пике воспалительной реакции рецепторы ФНОa могут «сбрасываться» с мембраны и выходить в межклеточное пространство, где они связывают ФНОa, оказывая противовоспалительное действие. В связи с этим растворимые формы TNFR используют при лечении хронических воспалительных заболеваний. При этом оказалось, что препарат на основе растворимого TNFRII оказался клинически наиболее эффективным.
Как и IL-1, TNFa усиливает экспрессию молекул адгезии, синтез провоспалительных цитокинов и хемокинов, белков острой фазы, ферментов фагоцитарных клеток и т.д. Наряду с IL-1, TNFa участвует в формировании всех основных местных, а также некоторых системных проявлений воспаления. Он активирует эндотелиальные клетки, стимулирует ангиогенез, усиливает миграцию и активирует лейкоциты. TNFa в большей степени, чем IL-1, влияет на активацию и пролиферацию лимфоцитов. В комбинации с IFNy TNFa индуцирует активность NO-синтазы фагоцитов, что значительно усиливает их бактерицидный потенциал. TNFa стимулирует пролиферацию фибробластов, способствуя заживлению ран. При повышенной локальной выработке TNFa преобладают процессы повреждения тканей, проявляющиеся развитием геморрагического некроза. Помимо этого TNFa подавляет активность липопротеиновой липазы, что ослабляет липогенез и приводит к развитию кахексии (одно из первоначальных названий TNFa — кахексин). Повышенное высвобождение TNFa и его накопление в циркуляции, например при действии высоких доз бактериальных суперантигенов, вызывает развитие тяжелой патологии — септического шока. Таким образом, действие TNFa, направленное на выполнение защитной функции и поддержание гомеостаза, может сопровождаться тяжелыми токсическими эффектами (местными и системными), нередко служащими причиной смерти.
IL-6 — провоспалительный цитокин широкого действия. Он также служит прототипическим фактором семейства цитокинов, включающего, кроме собственно IL-6, онкостатин М (OSM), лейкемия-ингибирующий фактор (LIF), цилиарный нейротрофический фактор (CNTF), кардиотро- пин-1 (CT-1), а также IL-11 и IL-31. Молекулярная масса IL-6 — 21 кДа. IL-6 вырабатывают моноциты и макрофаги, эндотелиальные, эпителиальные, глиальные, гладкомышечные клетки, фибробласты, Т-лимфоциты типа Th2, а также многие опухолевые клетки. Выработка IL-6 миелоидными клетками индуцируется при взаимодействии их TLR с микроорганизмами и их продуктами, а также под влиянием IL-1 и TNFa. При этом в течение 2 ч содержание IL-6 в плазме крови возрастает в 1000 раз.
Рецепторы всех факторов семейства IL-6 содержат общий компонент — цепь gp130, присутствующую практически на всех клетках организма. Второй компонент рецептора индивидуален для каждого цитокина. Специфическая цепь рецептора IL-6 (gp80) отвечает за связывание этого цитокина, тогда как gp130 участвует в передаче сигнала, поскольку связана с тирозинкиназами Jak1 и Jak2. При взаимодействии IL-6 с рецептором запускается следующая последовательность событий: IL-6-мономер взаимодействует с цепью gp80, происходит димеризация комплексов (2 молекулы цитокина — 2 цепи gp80), после чего к комплексу присоединяется 2 цепи gр130, что приводит к фосфорилированию Jak-киназ. Последние фосфорилируют факторы STAT1 и STAT3, которые димеризуются, перемещаются в ядро и связывают промоторы генов-мишеней. Цепь gp80 легко «смывается» с клетки; в свободной форме она взаимодействует с цитокином, инактивируя его, т.е. выступает в качестве специфического ингибитора IL-6.
IL-6 участвует в индукции практически всего комплекса местных проявлений воспаления. Он влияет на миграцию фагоцитов, усиливая выработку СС-хемокинов, привлекающих моноциты и лимфоциты, и ослабляя продукцию СХС-хемокинов, привлекающих нейтрофилы. Провоспалительные эффекты IL-6 выражены слабее, чем у IL-1 и TNFa, в противоположность которым он не усиливает, а угнетает выработку провоспалительных цитокинов (IL-1, TNFa и IL-6) и хемокинов клетками, вовлеченными в воспалительный процесс. Таким образом, IL-6 сочетает свойства про- и противовоспалительных цитокинов и участвует не только в развитии, но и в ограничении воспалительной реакции.
IL-6 — основной фактор, индуцирующий в гепатоцитах экспрессию генов белков острой фазы. IL-6 влияет на различные этапы гемопоэза, в том числе на пролиферацию и дифференцировку стволовых клеток. Он служит ростовым фактором незрелых плазматических клеток, существенно усиливая гуморальный иммунный ответ. IL-6 влияет также на Т-лимфоциты, повышая активность цитотоксических Т-клеток.
IL-17 и связанные с ним цитокины. Группа цитокинов, включающая разновидности IL-17, привлекла всеобщее внимание в связи с открытием особой разновидности Т-хелперов — Th17, участвующей в развитии некоторых повреждающих форм воспалительных реакций, в частности, при аутоиммунных процессах (см. раздел 3.4.3.2). Роль этих цитокинов в реакциях адаптивного иммунного ответа будет рассмотрена далее. Здесь приведем только общую характеристику цитокинов и кратко рассмотрим их роль в реакциях врожденного иммунитета.
Семейство IL-17 включает 6 белков, обозначаемых буквами от А до F. Свойствами провоспалительных цитокинов из них обладают IL-17A и IL-17F. Они представляют собой гомодимеры, скрепленные дисульфидной связью; их молекулярная масса — 17,5 кДа. Эти цитокины продуцируются упомянутыми Th17, а также CD8+ Т-клетками, эозинофилами, нейтрофилами. IL-23 стимулирует развитие ТЫ7-клеток и выработку IL-17.
Рецепторы для IL-17 экспрессируются многоми клетками — эпителиальными, фибробластами, клетками иммунной системы, в частности, нейтрофилами. Основной результат взаимодействия IL-17 с рецептором состоит, как и при действии других провоспалительных цитокинов, в индукции фактора NF-kB и экспрессии многочисленных NF-KB-зависи- мых генов воспаления.
Один из важных биологических эффектов IL-17 (наряду с IL-23) — поддержание гомеостаза нейтрофилов. Эти цитокины усиливают образование нейтрофилов, стимулируя выработку G-CSF. При этом усиление или ослабление выработки IL-17 и IL-23 регулируется численностью нейтрофилов в периферических тканях: снижение числа этих клеток в результате апоптоза приводит к усилению выработки цитокинов.
Провоспалительное действие IL-17 реализуется главным образом через усиление выработки других цитокинов (IL-8, IL-6, y-CSF, ряд хемокинов) и экспрессии молекул адгезии. У мышей, трансгенных по IL-17 или по IL-23, развивается системное хроническое воспаление, имеющее интерстициальный характер, с инфильтрацией нейтрофилами, эозинофилами, макрофагами и лимфоцитами различных органов. За этими цитокинами признают ведущую роль в развитии хронических аутоиммунных заболеваний.
Семейство IL-12
IL-12 был идентифицирован по способности активировать NK-клетки, вызывать пролиферацию Т-лимфоцитов и индуцировать синтез IFNy. IL-12 занимает особое место в ряду цитокинов, вырабатываемых клетками системы врожденного иммунитета, поскольку он (как и его главные продуценты — дендритные клетки) служит связующим звеном между врожденным и адаптивным иммунитетом. С другой стороны, IL-12 входит в тандем IL-12—IFNy, которому принадлежит ключевая роль в осуществлении иммунной защиты от внутриклеточных патогенов.
IL-12 представляет димер, состоящий из субъединиц р40 и р35. Его суммарная молекулярная масса — 75 кДа. Функциональная активность IL-12 связана с его субъединицей р40. «Полномасштабный» IL-12 секретируют активированные моноциты, макрофаги, миелоидные дендритные клетки, нейтрофилы, эпителиальные клетки барьерных тканей (они продуцируют и ^-12р35 и IL-12p40 субъединицы цитокина). Большинство же клеток организма синтезирует только функционально неактивную субъединицу ^-12р35. Количество гетеродимера IL-12, секретируемого клеткой, ограничено субъединицей р35. IL-12p40 синтезируется в избытке и может димеризоваться с образованием гомодимера, выступающего в качестве антагониста IL-12, а также хемоаттрактанта. Индукторы выработки IL-12 — прежде всего патогены, распознаваемые TLR и другими паттернраспознающими рецепторами. Выработку IL-12 усиливают IL-1, IFNy, а также межклеточные взаимодействия, опосредованные CD40-CD154 и другими парами молекул семейств — TNFR.
Рецептор IL-12 сильнее всего экспрессирован на NK-клетках, активированных ТЫ-клетках и цитотоксических Т-лимфоцитах и в меньшей степени — на дендритных клетках. Экспрессия рецептора IL-12 активированными Т-клетками усиливается под влиянием IL-12, IFNy, IFNa, TNFa и при кос- тимуляции через рецептор CD28. Рецептор для IL-12 представляет димер, образованный субъединицами IL-12RP1 (100 кДа), и IL-12RP2 (130 кДа, CD212), с которым ассоциирован белок с молекулярной массой 85 кДа. В связывании IL-12 участвуют и Pj и р2 цепи, тогда как в передаче сигнала задействована преимущественно субъединица IL-12RP2. Внутриклеточный домен Pj-цепи ассоциирован с киназой JAK2, внутриклеточный домен Р2-цепи — с киназой Tyk2. Киназы фосфорилируют транскрипционные факторы STAT1, STAT3, STAT4 и STAT5.
Главная функция IL-12, обусловленная его способностью стимулировать цитотоксические лимфоциты (NK и T) и индуцировать дифферен- цировку Thl-клеток (см. раздел 3.4.3.1), — запуск клеточных механизмов защиты от внутриклеточных патогенов. IL-12 действует на NK- и NKT-клетки уже на ранних стадиях иммунных процессов, усиливая пролиферацию и цитотоксическую активность NK-клеток, а позже — цитотоксических Т-лимфоцитов и синтез всеми этими клетками IFNy. Несколько позже IL-12 индуцирует дифференцировку Thl-клеток, тоже продуцирующих IFNy. Условие индукции Thl-клеток — предварительная экспрессия активированными CD4+ Т-клетками субъединицы рецептора IL-12RP2. После этого клетки приобретают способность связывать IL-12, что приводит к активации фактора STAT4, регулирующего экспрессию генов, характерных для Thl-клеток (для экспрессии гена IFNG более важно действие транскрипицонного фактора T-bet). Одновременно IL-12 подавляет дифференцировку ^2-клеток и ослабляет выработку клетками
В-ряда антител классов IgE и IgA. Действуя на дендритные и другие АПК IL-12 индуцирует экспрессию костимулирующих молекул (CD80/86, и др.), а также продуктов МНС-II АПК. Таким образом, IL-12 играет связующую роль между врожденным и адаптивным иммунитетом и усиливает иммунные механизмы, ответственные за защиту от внутриклеточных патогенов и опухолей.
К семейству IL-12 относят IL-23, IL-27 и IL-35. Эти цитокины представляют гетеродимеры: IL-23 образован двумя субъединицами — ^-23р19 и IL-12p40 (идентична соответствующей субъединице IL-12), IL-27 — субъединицами Ebi3 и IL-27p28, IL-35 — субъединицами Ebi3 и IL-12p35. Эти цитокины продуцируются преимущественно дендритными клетками. Выработку цитокинов семейства IL-12 запускают представленные на патогенах PAMP и цитокины, в особенности GM-CSF.
Рецепция IL-23 осуществляется двумя разными структурами: субъединицу IL-12p40 распознает ргцепь рецептора для IL-12, а субъединицу ^-23р19 — особый рецептор — IL-23R. Основную роль в передаче сигнала от IL-23 играет STAT4. Рецептор для IL-27 активирует молекулы WSX-1 (гомолог р2-субъединицы IL-12R) и gp130 (полипептидная цепь, входящая в состав рецепторов для цитокинов семейства IL-6).
Подобно IL-12, IL-23 и IL-27 действуют преимущественно на CD4+ Т-клетки, способствуя их дифференцировке по Th1-пути. Особенности IL-23 — преимущественное действие на Т-клетки памяти, а также способность поддерживать развитие Т-хелперов типа Th17. IL-27 отличается от двух других цитокинов семейства способностью вызывать пролиферацию не только активированных, но и покоящихся CD4+ Т-клеток. Недавно было показано, что IL-27 и IL-35 могут выступать в качестве регуляторных (супрессорных) факторов, поскольку их субъединица Ebi3 — мишень ключевого фактора регуляторных Т-клеток FOXP3.
Колониестимулирующие факторы (CSF) (табл. 2.32) или гемопоэтины представлены тремя цитокинами — GM-CSF, G-CSF и M-CSF. К ним функционально близок IL-3 (Multi-CSF). Эти факторы называют колониестимулирующими, поскольку впервые были идентифицированы по способности поддерживать рост in vitro колоний гемопоэтических клеток соответствующего состава. IL-3 обладает наиболее широким спектром действия, поскольку поддерживает рост любых колоний гемопоэтических клеток, кроме лимфоидных. GM-CSF поддерживает рост как смешанных гранулоцитарно-моноцитарных колоний, так и отдельно колоний грану- лоцитов и моноцитов/макрофагов. G-CSF и M-CSF специализируются на поддержании роста и дифференцировки соответствующих колоний. Эти факторы не только обеспечивают выживаемость и пролиферацию кроветворных клеток указанных типов, но и способны активировать уже зрелые дифференцированные клетки (M-CSF — макрофаги, G-CSF — нейтрофилы). M-CSF участвует в дифференцировке моноцитов в макрофаги и подавляет дифференцировку моноцитов в дендритные клетки. G-CSF, помимо действия на гранулоцитарный ветвь гемопоэза, вызывает мобилизацию кроветворных стволовых клеток из костного мозга в кровоток.
Таблица 2.32. Характеристика колониестимулирующих факторов
|
Назва ние |
Хромо сома |
Молекулярная масса, кДа |
Клетки- продуценты |
Клетки- мишени |
Рецеп торы |
|
GM-CSF |
5q |
22 |
Макрофаги, Т-клетки, NK-клетки, стромальные клетки, эпителиальные клетки |
Макрофаги, нейтрофилы, эозинофилы, Т-клетки, дендритные клетки, гемопоэтические клетки |
GM- CSFR а/Р |
|
G-CSF |
17q |
18-22 |
Макрофаги, стромальные клетки, эпителиальные клетки |
Нейтрофилы, эозинофилы, Т-клетки, гемопоэтические клетки |
G-CSFR (1 цепь) |
|
M-CSF |
5q |
45/70 (димер) |
Макрофаги, стромальные клетки, эпителиальные клетки |
Макрофаги, гемопоэтические клетки |
c-Fms |
|
Фактор стволовых клеток |
12q |
32 |
Стромальные клетки |
Гемопоэтические клетки, В-клетки, тучные клетки |
c-Kit |
|
Flt-3- лиганд |
19q |
26,4 |
Стромальные клетки |
Гемопоэтические клетки, тучные клетки |
Flt-3 |
G-CSF, GM-CSF и IL-3 структурно характеризуются как гемопоэтины, содержащие 4 а-спиральных домена. Их рецепторы содержат по 2 полипептидные цепи, их относят к семейству гемопоэтиновых рецепторов. M-CSF отличается от остальных CSF. Он представляет собой димерную молекулу и существует как в растворимой, так и в мембраносвязанной формах. Его рецептор имеет внеклеточные Ig-подобные домены и внутриклеточный домен, обладающий активностью тирозинкиназы (наименование этой киназы-протоонкогена — с-Fms — иногда переносят на весь рецептор). При связывании М-CSF с рецепторами происходит их димеризация и активация киназы.
Колониестимулирующие факторы продуцируются эндотелиальными клетками и фибробластами а также моноцитами/макрофагами. GM-CSF и IL-3, кроме того, синтезируются Т-лимфоцитами. Под влиянием бактериальных продуктов (через паттернраспознающие рецеторы) и провоспалительных цитокинов синтез и секреция колониестимулирующих факторов значительно возрастает, что приводит к усилению миелопоэза. Особенно сильно стимулируется гранулоцитопоэз, что сопровождается ускоренной эмиграцией клеток, в том числе незрелых, на периферию. Это создает картину нейтрофильного лейкоцитоза со сдвигом формулы вправо, весьма характерным для воспаления. Препараты на основе GM- и G-CSF применяют в клинической практике для стимуляции гранулоцитопоэза, ослабленного цитотоксическими воздействиями (облучение, прием химиопрепаратов при лечении опухолевых заболеваний и т.д.). G-CSF применяют для мобилизации стволовых кроветворных клеток с последующим использованием индуцированной лейкомассы для восстановления нарушенного гемопоэза.
Фактор стволовых клеток (SCF — stem cell factor, c-kit ligand) cекретируют клетки стромы костного мозга (фибробласты, эндотелиальные клетки), а также разные типы клеток в период эмбрионального развития. SCF существует в виде трансмембранной и растворимой молекул (последняя образуется в результате протеолитического отщепления внеклеточной части). SCF выявляют в плазме крови. Его молекула имеет две дисульфидные связи. Рецептор SCF — с-Кк — обладает тирозинкиназной активностью и по своей структуре близок к Flt-3 и c-Fms (рецептор M-CSF). При связывании SCF происходят димеризация рецепторов и их фосфорилирование. Передача сигнала происходит с участием PI3K и MAP-каскада.
Мутации гена SCF и его рецептора описаны давно (мутации steel); у мышей они проявляются изменением окраски шерсти и нарушением гемопоэза. Мутации, нарушающие синтез мембранной формы фактора, вызывают грубые дефекты развития эмбриона. Совместно с другими факторами SCF участвует в поддержании жизнеспособности стволовых кроветворных клеток, обеспечивает их пролиферацию, поддерживает ранние этапы гемопоэза. SCF особенно важен для эритропоэза и развития тучных клеток, а также служит ростовым фактором для тимоцитов на стадиях DN1 и DN2.
По структуре и биологической активности сходными с SCF свойствами обладает фактор Flt-3L- (Fms-like thyrosinkinase 3-ligand), в сочетании с другими факторами поддерживающий ранние этапы миелопоэза и развитие В-лифмоцитов. SCF играет роль фактора роста лейкозных миелобластов.
Хемокины, представляющие важный гуморальный фактор воспаления и врожденного иммунитета, рассмотрены выше при описании хемотаксиса лейкоцитов (см. раздел 2.3.2).
Источник: Ярилин.А.А , «Иммунология » 2010