Иммунодиагностика
Иммунодиагностика составляет методическую основу современной иммунологии, имеет целью, в частности, характеристику функционального состояния отдельных звеньев иммунной системы и взаимодействующих с ними факторов неспецифической защиты, чтобы выявить наличие возможного дефицита какого-либо из них, определить и своевременно начать соответствующую иммунокорригирующую терапию.
Важнейшей иммунологической проблемой педиатрии считается проблема иммунологической недостаточности или ИДС. Она включает два крупных и принципиально разных раздела иммунопатологии.
- Первичные ИДС являются следствием генных мутаций и характеризуются выраженными дефектами одного или нескольких иммунных механизмов. Они легко выявляются даже при первичном иммунологическом обследовании. Заболевания достаточно редки, удельный вес их в общей патологии детского возраста невелик. Не касаясь
детальной характеристики отдельных нозологических форм, можно сказать, что они имеют общие клинические признаки: склонность к тяжелым инфекционным процессам и хроническому их течению. При изучении анамнеза ребенка выясняется повторный характер острых инфекционных заболеваний, которые могут перейти в хроническое состояние. Такие дети, безусловно, нуждаются в энергичной иммунокоррекции, проводимой в специализированных клиниках.
- Вторичные ИДС характеризуются, как правило, незначительными отклонениями от средних нормальных значений иммунологических параметров, представляют значительные трудности для диагностики и определения врачебной тактики. Природа таких парциальных ИДС различна.
Рассмотрим несколько конкретных ситуаций. Прежде всего далеко не в каждом случае снижение тех или иных иммунологических показателей должно расцениваться как ИДС. Врачи, как правило, не знают преморбидного иммунологического фона и наблюдают уже изменившийся под влиянием болезни статус. Снижение показателей в острой стадии заболевания рассматривается как наличие у данного больного ИДС той или иной степени, которая и предопределила возможность развития заболевания. Специально проведенные исследования (были сняты иммунологические параметры у детей в межэпидемический период и затем в период вспышек ОРВИ у заболевших и незаболевших детей) показали, что снижение в остром периоде ОРВИ некоторых иммунологических показателей не предшествует заболеванию, но является его следствием, результатом потребления иммунных факторов в процессе борьбы организма с инфекционным началом. Установлено также, что Т-клетки после контакта с антигеном уходят на некоторое время из циркуляции в периферические лимфоидные органы. Естественно, что в этот период, соответствующий началу заболевания, количество Т-лимфоцитов в крови снижено. Кроме того, колебания в ту или иную сторону некоторых иммунологических параметров могут быть следствием не прямого их участия в борьбе с инфекционным началом, а компенсаторной реакцией.
Нужно иметь в виду, что нередко при явных клинических признаках иммунного дефицита (например, часто болеющие дети) методами, имеющимися в распоряжении иммунологической лаборатории, функциональной неполноценности иммунной системы обнаружить не удается, так как все исследуемые параметры лежат в пределах колебаний, допустимых для здорового человека. Значит ли это, что мы должны отвергнуть диагноз ИДС? Нет, не значит. Ибо сам факт повторных чередующихся одно за другим заболеваний, безусловно, свидетельствует о том, что иммунная система организма не справляется со своей функцией. В этом случае на основании клинических данных должно быть констатировано наличие ИДС независимо от того, какие показатели различных звеньев иммунитета мы получаем при лабораторных исследованиях.
Однако мы нередко сталкиваемся с противоположной ситуацией,
когда у практически здоровых людей (например, доноров) при исследовании случайно обнаруживаются резко сниженные значения, а порой полное отсутствие того или иного фактора иммунитета. Так, нами зарегистрировано 2 случая полного отсутствия IgA (на уровне чувствительности метода Манчини) в сыворотке крови у здоровых молодых людей (25 и 32 лет). Последнее еще раз подтверждает необходимость при оценке иммунологического статуса ребенка принимать во внимание не только иммунологические параметры, но и клиническую картину состояния его здоровья.
Известно, что различные эндогенные или экзогенные влияния (недостаточность питания или потеря белка, вирусные или бактериальные инфекции, иммунодепрессантные препараты или кортикостероиды, применяемые с лечебной целью, рентгеновское облучение и ионизирующая радиация, наконец, уникальная вирусная инфекция СПИДа, избирательно повреждающая Т-хелперы) вызывают угнетение иммунного ответа, развитие ИДС, сходных по признакам с наследственными дефектами иммуногенеза.
Одной из наиболее важных и вместе с тем сложных проблем клинической иммунологии является индивидуальная оценка иммунного статуса организма в каждом конкретном случае. Сложность решения этой столь необходимой для клинициста задачи состоит в том, что очень велик индивидуальный разброс иммунологических параметров как в норме, так и при патологии. И несмотря на то что средние значения сравниваемых групп могут достоверно отличаться, большая часть абсолютных значений отдельных иммунологических параметров перекрывают друг друга, т. е. встречаются как в одной, так и в другой группе сравнения. В последние годы появился ряд работ, авторы которых пытаются преодолеть указанные трудности, используя главным образом различные математико-статистические приемы и методы.
Однако, несмотря на все преимущества предложенных подходов, возникли новые трудности при решении задач персональной идентификации, т. е. при определении параметров модели по данным наблюдения персонально для каждого исследуемого организма с учетом его индивидуальных особенностей. Эта трудность связана с тем, что математическая модель даже при всех возможных упрощениях содержит десятки параметров, значения которых важно определить в самом начале заболевания, чтобы своевременно назначить лечение и установить прогноз, но число наблюдений и лабораторных анализов в начале заболевания еще оказывается недостаточным, чтобы оценить значения всех параметров модели.
Важным шагом в осмыслении подхода к оценке иммунной системы явилась концепция «мобилей», выдвинутая Р. В. Петровым, сущность которой заключается в том, что иммунная система представляет собой совокупность компонентов, объединенных в единое целое разнообразными по силе и направлению связями. Любая нагрузка на одно из звеньев этой системы немедленно перераспределяется между другими звеньями, поэтому одно и то же интегральное состояние нормы может
достигаться совокупностью неоднозначных уровней показателей, характеризующих различные звенья иммунной системы. Одни и те же признаки патологического состояния могут быть определены сдвигами разных иммунологических показателей. Сдвиг какого-либо показателя может быть компенсирован или не компенсирован системой, и в соответствии с этим она остается в норме или развивается патологическое состояние.
Появление концепции «мобилей» стало толчком к развитию в иммунологии нового подхода к оценке иммунного статуса, который получил название функционального. Такой подход к оценке иммунного статуса предусматривал способы оценки физиологической активности ИКК. Одним из таких способов стало изучение кинетики иммунологических реакций, но наибольшее распространение получили способы тестирования ИКК после применения к ним различных воздействий, т. е. использование нагрузочных тестов. В сущности они широко вошли в клиническую практику и эффективно используются для оценки функционального состояния других органов и систем организма. Однако в клинической иммунологии этот подход не нашел широкого распространения. Нагрузочные тесты в основном применялись для исследования взаимосвязей отдельных иммунологических показателей в дискретно-динамическом анализе и для решения вопроса
о возможности использования данного фармакологического агента в качестве терапевтического средства у данного индивидуума.
Одним из первых, кто применил спонтанный и стимулированный НСТ-тест для решения вопроса о прогнозе течения заболевания был А. Д. Майанский. Затем появились работы Н. В. Васильева, Т. И. Коляды, которые для оценки функционирования иммунной системы спортсменов применяли физические нагрузки — барокамеру, велоэргометр с определением иммунологических показателей до и после применения нагрузочных тестов.
Однако использование физической нагрузки в клинической практике не всегда возможно. Поэтому в этих ситуациях более доступной и удобной является реализация нагрузочных тестов непосредственно на выделенные клетки перед их тестированием, которое может осуществляться в различных иммунологических реакциях in vitro.
Использование нагрузочных тестов в клинической иммунологии позволило впервые решить вопрос о резервах иммунологических процессов у конкретного индивидуума, т. е. ответить на вопрос, способна ли данная система увеличить свои функциональные возможности или ее резервы уже исчерпаны?
Для определения функциональных резервов фагоцитирующих клеток использовали следующие методы: 1) фагоцитарную реакцию по методу Серебрейского и Антоновой с определением показателя ФЧ (процент клеток, участвующих в захвате микроба) и ФИ (числа микробов, захваченных одной клеткой). Для определения переваривающей способности клеток реакцию учитывали через 30 мин и 2 ч. В качестве стимулятора in vitro использовали продигиозан; 2) НСТ-тест ставили
в спонтанном и стимулированном вариантах. В качестве стимулятора применяли продигиозан.
Для оценки резервов адаптации Т-системы предлагаются нагрузочные тесты (in vitro) с иммуностимуляторами (левамизол, димефосфон, тималин, Т-активин и т. д.). Помимо определения функциональных резервов Т-системы такой подход дает возможность подобрать оптимальный для конкретного больного наиболее эффективный препарат и дозу его применения.
Для характеристики способности индивидуума определенным образом реагировать при проведении серии нагрузочных тестов был введен коэффициент К, представляющий собой отношение среднего арифметического всех стимулированных реакций у данного индивидуума к его же спонтанным.
При анализе результатов исследований в группе здоровых детей было установлено существование по крайней мере 3 типов реагирования иммунокомпетентных клеток в нагрузочных тестах in vitro: увеличение числа розеткообразующих клеток, которое, как правило, сочетается с низкими исходными значениями в спонтанных реакциях (I тип реагирования, условно названный нами гиперергическим); снижение розеткообразования по отношению к спонтанной реакции (III тип — гипергический); выявлена группа детей, у которых значения спонтанных реакций не обнаруживали достоверных изменений после инкубации со стимуляторами (обозначен как II или резистентный тип).
Наличие I типа реагирования у обследованного ребенка свидетельствует о хороших резервных возможностях иммунной системы, наличие III типа — о низких резервных возможностях иммунной системы.
Следует заметить, что понятием «функциональные резервы» надо пользоваться с большими оговорками, ибо последнее само по себе предполагает, что наличие «функциональных резервов» обеспечивает эффективную защиту организма. Однако первый же анализ результатов обследования детей с бронхолегочной патологией показал, что дети с I типом реагирования, имеющие, казалось бы, значительные функциональные резервы, тем не менее тяжело больны (атопическая бронхиальная астма). Следовательно, вряд ли правомерно при обследовании здоровых детей (например, с момента рождения) прогнозировать высокую защищенность организма и легкое течение заболевания, если таковое будет наблюдаться. Скорее можно прогнозировать характер патологического процесса в случае заболевания: бурные гиперергические реакции у детей с I типом реагирования и наклонность к хроническим, вяло текущим процессам у детей с III типом реагирования.
Выявление различных типов реагирования иммунной системы как у здоровых, так и у больных детей на нагрузку, по-видимому, нужно рассматривать как генетически запрограммированные варианты нормы реакции, как одно из конкретных проявлений общефизиологической закономерности по аналогии, например, с типами конституции или нервной системы.
Аналогичный методический подход может быть распространен и
на ЕАС-РОК (комплементарное розеткообразование) для характеристики В-системы, когда в качестве нагрузки можно использовать, например, липополисахарид (ЛПС).
Другой разновидностью нагрузочных тестов можно считать разработанный Т. В. Виноградовой (1986) новый подход к оценке элиминирующей емкости лейкоцитов по отношению к ЦИК. Использование этого теста позволяет судить о перегруженности макрофагаль- но-фагоцитирующей системы ЦИК или о ее первичной функциональной слабости. Суть предлагаемого метода состоит в том, что лейкоциты, выделенные из крови больного, инкубируют с сывороткой, содержащей известные уровни ИК, и затем количественно оценивают поглощаемость последних исследуемыми клетками. Последующий «отдых» лейкоцитов в среде 199 в течение 1 ч и дополнительная нагрузка их ИК дает информацию о восстановлении фагоцитирующей способности клеток или об отсутствии такого, что позволяет решить вопрос в пользу одного из предположений.
Исследования показали, что у больных с ИК-болезнями (гломерулонефрит, аллергический альвеолит, системная красная волчанка), а также сепсисом наблюдается снижение элиминирующей способности нейтрофилов и макрофагов по сравнению с таковой у здоровых доноров. В одних случаях это было связано с перегруженностью фагоцитарной системы (сепсис), у больных же с иммунокомплексными болезнями на первое место выступала ее недостаточность, так как «дополнительный отдых» лейкоцитов не приводил к восстановлению их фагоцитирующей способности.
Еще одним подходом для определения резервов адаптации (когда невозможны нагрузочные тесты) может стать определение кинетики реакции. В частности, функциональные резервы системы комплемента (ее гемолитической активности) исследовали кинетическим методом Е. С. Леоновой (1988). Способ заключался в периодическом подсчете числа эритроцитов, остающихся нелизированными под действием комплемента сыворотки крови больных.
При обследовании детей с гнойно-септическими хирургическими заболеваниями в ряде случаев показатели конечного титрования комплемента по 100% гемолизу оказались сходными. Однако эти данные не коррелировали с клинической картиной (тяжесть заболевания, длительность его течения). В этих ситуациях проведенное дополнительное исследование кинетики активации комплемента выявило существенное различие скорости реакции (рис. 10). Так, сравнительный анализ кривых реакции двух больных свидетельствует о стремительной активации системы комплемента у больного М. и замедленной — у больного П., что соответствует данным клинического наблюдения.
Приведенные примеры иллюстрируют прогностическое значение кинетического определения активации системы комплемента, позволяющего получить принципиально новую информацию о резервных возможностях организма в условиях развития тяжелого воспалительного заболевания.
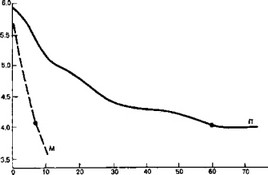
Рис. 10. Кинетика гемолитической активности комплемента.
М — у больного с гангренозно-перфоративным аппендицитом (гладкое послеоперационное течение); П — у больного сепсисом, тотальным остеомиелитом правой большеберцовой кости (тяжелое послеоперационное течение). По оси абсцисс — время (в минутах); по оси ординат — число нелизированных эритроцитов (п ¦ 105/мл).
Использование функционального подхода к оценке иммунного статуса меняет ход рассуждений. Становятся не столь важными абсолютные значения отдельных параметров и сравнение их со среднестатистическими (хотя при необходимости для этой цели могут быть использованы значения, полученные без стимулирущего воздействия). На первое место выходит анализ различий показателей, получаемых в спонтанных и нагрузочных реакциях, или данные исследования кинетики процесса. При этом повышается информативность простых широко распространенных в клинике иммунологических тестов и нет необходимости использовать строго стандартизованные методики. Автор может пользоваться любым доступным для него методом.