Проявления эпидемического процесса
Проявлениями эпидемического процесса являются его интенсивность, а также распределение заболеваний (носительства, смертности и др.) по времени, по территории и среди различных групп населения.
Заболеваемость. Интенсивность эпидемического процесса обычно характеризуется показателем заболеваемости - абсолютным или интенсивным. Необходимо, однако, иметь в виду, что между расчетным показателем заболеваемости и истинной интенсивностью эпидемического процесса всегда есть более или менее существенная разница. Это зависит от точности регистрации заболеваний, на которую влияют следующие факторы:
> действующая система регистрации и учета заболеваний, определяющая, подлежит ли каждый случай заболевания данной нозологической формой учету;
> уровень диагностики данной болезни, определяемый как научными достижениями, так и материально-технической и кадровой обеспеченностью лабораторной и клинической службы;
> обращаемость населения за медицинской помощью, зависящая не только от его культурного уровня и субъективного отношения к той или иной инфекции, но и от доступности (радиус, стоимость) медицинского обслуживания и уровня его организации;
> выраженность и тяжесть клинического проявления болезни, обусловливающая как обращаемость населения за медицинской помощью, так и возможности ее диагностики;
> эпидемиологическая ситуация, определяющая повышение активности выявления заболеваний во время эпидемических вспышек, и недостаточная настороженность медицинского персонала в условиях спорадической заболеваемости, с чем связан уровень выявления заболеваний.
Официальные данные регистрации, на основе которых анализируется заболеваемость, не могут отражать истинного уровня распространенности некоторых инфекций, поскольку эти данные включают главным образом только клинически и бактериологически подтвержденные случаи без учета субклинических и бессимптомных случаев заболевания, которые в большинстве остаются нераспознанными. Между тем, например, дизентерия Зонне характеризуется значительным удельным весом легко и субклинически протекающих заболеваний, т.е. состояний инфицированности, которые могут быть выявлены в основном лишь активно, с помощью специальных методов диагностики.
Существуют различные способы оценки соответствия регистрируемого числа заболеваний истинному. Например, если в каком-либо районе регистрируются только бактериологически подтвержденные заболевания людей сибирской язвой, то недоучет истинной заболеваемости в данном случае очевиден: заболевание сибирской язвой человека подтвердить бактериологическим методом никогда не удавалось чаще, чем в 50% случаев. Следовательно, в половине случаев диагноз должен быть подтвержден лишь на основе клинической картины или аллергологической пробы, что и следует иметь в виду при оценке регистрируемого уровня заболеваемости сибирской язвой.
Эндемическая заболеваемость или эндемия, - это постоянно регистрируемая на определенной территории заболеваемость определенной болезнью, обусловленная социальными и природными условиями (рис. 5).
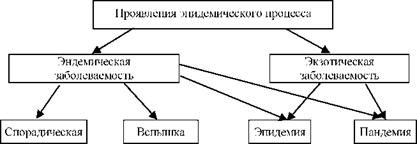
Рис. 5. Проявления эпидемического процесса. |
Экзотическая заболеваемость - заболеваемость, несвойственная данной местности. Она возникает в результате заноса или завоза возбудителя и других территорий.
Уровень заболеваемости обычно оценивают тремя степенями: спорадическая заболеваемость, эпидемия, пандемия.
Под «спорадическим» чаще всего подразумевают уровень заболеваемости, «обычный для данной местности на данном уровне ее исторического развития», «сложившийся в данной местности при данных исторических условиях», «обычно наблюдающийся в данной местности на протяжении изучаемого отрезка времени».
Понятие «эпидемия» обозначает уровень заболеваемости, значительно превышающий уровень спорадической заболеваемости данной инфекцией в данной местности. Иными словами, эпидемия - это массовое поражение значительного числа населения или отдельных его контингентов инфекционной (паразитарной) болезнью.
Эпидемическую заболеваемость также характеризуют понятия «эпидемическая вспышка», или «групповое заболевание», означающее кратковременное увеличение связанных с общим источником или фактором передачи возбудителя заболеваний в ограниченной группе населения, а также «пандемия» - эпидемия, охватившая население нескольких государств.
Следует, однако, подчеркнуть трудность изыскания какого-либо количественного критерия, с помощью которого можно было бы легко различать спорадическое и эпидемическое состояния инфекционной заболеваемости, поскольку границы между ними относительны и условны. Так, высокая заболеваемость, часто встречающаяся в какой-либо местности (например, дизентерией), рассматривается как спорадическая, тогда как такой же уровень заболеваемости более редкой болезнью (например, брюшным тифом) определяется как интенсивная эпидемия.
Оценка ситуации будет различной и применительно к разным территориям и в различные исторические периоды. Так, один и тот же уровень заболеваемости в стране, где данная инфекция является эндемической (например, холера в Индии), будет признан спорадическим, тогда как в стране, где эта инфекция обычно не встречается, он будет расценен как эпидемия.
Аналогично этому, если в прошлом какая-либо инфекционная болезнь в данной стране была широко распространена, то отмечавшийся тогда уровень заболеваемости мог считаться спорадическим, однако после ликвидации или резкого снижения заболеваемости вновь возникшие по каким-либо причинам заболевания будут расценены как эпидемия (например, дифтерия России в 60-х и в 80-90-х гг.).
Подход к понятиям «спорадическая» и «эпидемическая» заболеваемость с точки зрения анализа качественных различий между ними позволяет обнаружить в них отражение не только разной степени интенсивности эпидемического процесса, но и разных форм его проявления. Исходя из этих положений, спорадическая заболеваемость - это такой характер заболеваемости, когда регистрируемые заболевания единичны, разрозненны, т.е. когда преимущественно отсутствует эпидемиологическая связь их между собой с общим источником или общими факторами передачи возбудителя инфекции (это правильно и этимологически, поскольку греческое слово 8ротай1со8 означает единичный, случайный, появляющийся от случая к случаю).
В отличие от спорадической эпидемической можно назвать такую заболеваемость, когда регистрируемые случаи заболеваний преимущественно объединены общим источником или общими факторами передачи возбудителя инфекции, либо между ними имеется эпидемиологическая преемственность.
Такие определения призваны, прежде всего, указать, что понятия «спорадическая» и «эпидемическая» заболеваемость отражают не столько разную степень интенсивности течения эпидемического процесса, сколько качественно различные формы его проявления.
Переход спорадической заболеваемости в эпидемическую может быть связан с появлением факторов, благоприятствующих реализации механизма передачи возбудителя инфекции. Так, заболеваемость кишечными инфекциями, поддерживаемая вне сезонного подъема на уровне спорадической за счет случайных бытовых заражений (грязные руки, предметы обихода, посуда, белье), может перерастать в эпидемическую с началом сезонного подъема, т.е. в период активизации массовых факторов передачи (водного, пищевого).
В довакцинальный период в населенных пунктах, в которых отсутствовали постоянные детские дошкольные учреждения, во время летних школьных каникул заболеваемость корью могла носить прерывистый, спорадический характер, поддерживаясь за счет случайного общения восприимчивых к кори детей с источниками возбудителя инфекции. С началом занятий в школе, после заноса возбудителя инфекции в коллектив школьников, заболеваемость начинала стремительно перерастать в эпидемию, охватывая все новые контингенты восприимчивых к кори детей - сначала школьного, а затем и дошкольного возраста.
Спорадический характер заболеваемости может быть обусловлен высокой степенью невосприимчивости к инфекции постоянно проживающего в эндемичной местности населения. Перерастание спорадической заболеваемости в эпидемическую в подобных случаях может быть связано с притоком в данную местность свежих, восприимчивых к данной инфекции контингентов людей, как это, например, наблюдается при ряде трансмиссивных инфекций.
Очаговость. Показатель очаговости служит одним из эпидемиологических признаков, характеризующих интенсивность эпидемического процесса. Преобладание очагов с одним случаем заболевания или носи- тельства является признаком ограниченной активности пути передачи возбудителя инфекции. Множественность одновременно возникающих очагов или заболеваний, появляющихся в очаге в пределах срока инкубационного периода, при различных инфекциях детерминируется разными причинами. При кишечных инфекциях она определяется реализацией общего пути передачи возбудителя (вода, пищевой продукт), при инфекциях дыхательных путей - условиями заражения (детское учреждение, многосемейная квартира, кинотеатр), при кровяных инфекциях - численностью, активностью и доступностью для человека зараженных переносчиков.
Следует, однако, подчеркнуть, что в современных условиях преимущественно возникают единичные (с одним заболеванием) бытовые эпидемические очаги кишечных инфекций (сальмонеллезов, шигеллезов), эпидемиологические связи между которыми не выявляются. Неумение установить эти связи при так называемой спорадической заболеваемости приводит, как правило, и к неспособности раскрыть эпидемиологическую природу (пути и факторы передачи) групповой (вспышечной) заболеваемости, имеющей единые эпидемиологические корни со спорадической. Объективному выявлению этих связей в максимальной степени должны способствовать методы внутривидового подразделения возбудителей («эпидемиологические метки») на серовары, подсеровары, биохимические варианты.
Распределение инфекционных заболеваний во времени. Выделяют многолетние и внутригодовые колебания уровня заболеваемости (рис. 6).
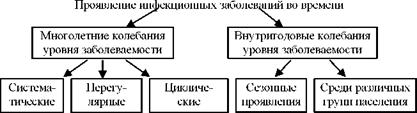
Рис. 6. Проявление инфекционных заболеваний во времени. |
Многолетние колебания уровня. Многолетние колебания уровня инфекционной заболеваемости могут быть трех типов:
1) систематические (трендовые) изменения под влиянием постоянно действующих на протяжении длительного времени факторов, главным образом социальных;
2) нерегулярные (апериодические, импульсные) колебания, детерминированные случайным (в отношении эпидемического процесса) распределением различных по своей природе факторов;
3) циклические колебания, представляющие совокупность взаимосвязанных с одной причиной изменений эпидемического процесса, повторяющихся с устойчивой вероятностью среднего периода колебаний.
Систематические изменения в динамике эпидемического процесса наиболее отчетливо проявляются под влиянием целенаправленного воздействия на него, например, в виде массовой иммунопрофилактики. Характерным примером в этом отношении являются корь и полиомиелит, заболеваемость которыми обнаружила тенденцию к стойкому снижению под влиянием плановой вакцинопрофилактики.
Причиной нерегулярных колебаний заболеваемости (вариации), как правило, являются те или иные социальные явления в жизни общества, например, подъемы заболеваемости сыпным тифом, непосредственно связанные с социально детерминированным повышением вшивости. Среди таких социальных факторов были войны, голод, полицейские репрессии (тюремные эпидемии, переходящие на местное население), пе- реселенчество, отхожие промыслы, религиозные праздники на фоне антисанитарного состояния мест скопления людей (воинские части, тюрьмы, постоялые дворы). Нерегулярные колебания в заболеваемости кишечными инфекциями могут быть связаны со вспышками, обусловленными авариями в системе водоснабжения, нарушениями технологии приготовления пищевых продуктов.
Циклические, т.е. чередующиеся и повторяющиеся в определенном порядке периоды подъема и спада заболеваемости, происходят под влиянием периодически действующих факторов.
Наглядным примером циклических колебаний эпидемического процесса может служить грипп, крупные эпидемии которого, вызванные появлением новых антигенных вариантов вируса, закономерно сменяются спадом заболеваемости в результате увеличения иммунной прослойки среди населения.
Выявлена четко выраженная периодичность в заболеваемости тифопаратифозными инфекциями. Известно, что в России клинический диагноз брюшного тифа стали выделять только в 70-х годах XIX столетия. Этиология брюшного тифа и паратифов А и В установлена на 10-20 лет позже - в 80-90-х гг. С 1889 г. «Вестник общественной гигиены» начал систематически печатать таблицы заболеваемости и смертности от инфекционных болезней по Российской империи. Однако, только в конце 1902 г. была введена регистрация заболевших в губернских городах и части уездных. Таким образом, статистические материалы конца XIX - первых лет ХХ в. менее репрезентативны, чем данные последующих лет. Тем не менее, анализ эмпирических кривых числа заболевших и уровней заболеваемости, а также сглаженных кривых за 1890-1976 гг. позволяет выявить четко прослеживающуюся регулярность подъемов заболеваемости брюшным тифом и паратифами. Оказалось, что продолжительность цикла для разных кривых колебалась от 11,5 до 12 лет. Продолжительность расчетного многолетнего цикла, установленная на основании средней продолжительности периодов эмпирических и сглаженных рядов, составила 12 лет. Длительность подъема от минимального до максимального уровня в расчетном цикле составила 4 года, а последующего снижения заболеваемости и уменьшения числа, заболевших до начала следующего подъема - 8 лет. В 70-80-е годы ХХ в. наблюдалось существенное изменение периода снижения заболеваемости - 17 лет вместо 8 расчетных, что связано с рядом качественных изменений, произошедших в эти годы в организации борьбы с заболеваемостью брюшным тифом и паратифами.
Общепризнанно, что причиной цикличности при инфекциях дыхательных путей является накопление в результате демографических процессов и исчерпание в результате заболеваний иммунной прослойки среди населения.
Известна и цикличность эпизоотического процесса в природных очагах, связанная с периодическими подъемами численности грызунов и кровососущих переносчиков, что, в свою очередь (в условиях отсутствия иммунопрофилактики), может определять цикличность заболеваемости людей туляремией, лептоспирозом, клещевым энцефалитом.
При трансмиссивных антропонозах (например, малярии) наблюдающуюся волнообразность динамики заболеваемости объясняют неодинаковым количеством осадков. Это приводит к изменению площади выплода комаров и температуры, что влияет на длительность созревания плазмодиев в их организме.
Убедительных объяснений цикличности эпидемического процесса при кишечных антропонозах пока нет.
Оценивая характер динамики заболеваемости, необходимо иметь в виду, что выявляемая тенденция может оказаться не истинной, а в значительной мере «статистической» (например, связанной с изменениями уровня диагностики). Кроме того, на характер выявляемой динамики заболеваемости может влиять и этиологическая дифференциация болезней, т.е. изменение представлений об этиологии той или иной инфекции и связанная с этим иная система учета и регистрации. Например, вычле- нились в самостоятельную нозологическую форму сальмонеллезы, ранее именовавшиеся «острыми гастроэнтеритами», «пищевыми отравлениями». Необходимость этиологического разграничения вирусных гепати-
тов по нозологическим формам (А, В, С, Дельта, Е и др.) обязывает отныне проводить их учет и анализ раздельно. Раздельного анализа требуют и разные этиологические формы дизентерии (Флекснера, Зонне, Ньюкасл, Григорьева-Шиги).
Сезонность. Другим проявлением динамики эпидемического процесса во времени служит сезонность. Сезонность - это объективно присущее эпидемическому процессу при большинстве заразных болезней свойство, выражением которого является подъем заболеваемости, закономерно повторяющийся в определенные месяцы года, обусловленный воздействием природных и социальных факторов, имеющих ритмическую сезонную периодичность.
Отражением сезонности является также период сезонного спада, в начале которого заболеваемость обычно продолжает оставаться на значительном уровне, достигая впоследствии минимума, таким образом, следствием сезонности является формирование высокого уровня заболеваемости в определенные периоды года, складывающегося из заболеваний, относящихся как к периоду подъема, так и к периоду спада. В свою очередь, уровень заболеваемости в эти периоды определяет в основном высоту годового уровня заболеваемости.
Как правило, каждая инфекционная болезнь в естественных условиях характеризуется специфичным и закономерным распределением заболеваний по месяцам, устанавливаемым по средним данным за несколько лет. Типичность внутригодового распределения заболеваний свидетельствует о наличии определенных, постоянно действующих сезонных факторов, детерминирующих определенный тип динамики заболеваемости, и задача эпидемиологии - вскрыть эти факторы в отношении каждой нозологической формы для изыскания способов их нивелировки.
В свою очередь, отклонения от типичной сезонности, рост заболеваемости в необычное время свидетельствуют о появлении или активизации действия необычных факторов, которые также необходимо выявить. Так, перемещение максимума заболеваемости кишечными инфекциями на зимне-весенние месяцы может привести эпидемиолога к гипотезе об активизации водного пути передачи возбудителей, которую, естественно, необходимо обосновать соответствующими доказательствами.
Характер сезонности может пролить свет на механизм, путь или факторы передачи возбудителя. Так, весенне-летний характер сезонности клещевого энцефалита дал возможность сделать предположение о роли клещей в передаче возбудителя этой инфекции, поскольку ее сезонность совпадала с периодом активности клещей. Кстати, само название болезни («весенне-летний энцефалит») подчеркивает характерную сезонность проявления заболеваемости этой инфекцией, переносчики возбудителя которой - иксодовые клещи - после зимнего анабиоза в поисках пищи нападают на животных и человека, передавая возбудителя в процессе кровососания.
Как известно, заболеваемости бактериальными кишечными инфекциями свойственна преимущественно летняя сезонность. Дело в том, что в жаркое время года создаются благоприятные условия для реализации пищевого пути передачи, поскольку в этот период возбудители кишечных инфекций способны активно размножаться в пищевых продуктах при нарушении правил их обработки и хранения. В жаркое время имеются условия, способствующие реализации водного пути передачи возбудителей кишечных инфекций за счет большего употребления воды для питья, купания в открытых водоемах. В связи с этим можно напомнить, что долгое время, когда полиомиелит считался инфекцией с аспирационным механизмом передачи возбудителя, его летне-осенняя сезонность считалась парадоксальной. С признанием возможности реализации и фекально-орального механизма передачи возбудителя этой инфекции свойственная ей сезонность нашла очевидное объяснение.
Дифференцированный анализ сезонности среди разных групп населения может пролить свет на различия условий их заражения. Так, сопоставление динамики внутригодовой заболеваемости тех или иных групп населения с особенностями их производственной деятельности или быта нередко помогает формулированию гипотезы о ведущих путях или факторах передачи возбудителя среди отдельных групп населения. Например, при бруцеллезе лица, занятые в животноводстве, преимущественно заражаются в период окота мелкого рогатого скота, тогда как свежие заболевания бруцеллезом среди рабочих мясоперерабатывающих предприятий возникают главным образом в осенние месяцы, во время массового убоя скота. Весенне-летний подъем заболеваемости туляремией обычно связан с промыслом водяных грызунов, который приурочен к периоду половодья (май - начало июня), тогда как сельскохозяйственные обмолотные и бытовые (домовые) вспышки обычно встречаются в конце осени и зимой.
Таким образом, анализ внутригодового распределения заболеваний может служить основанием для построения гипотезы о преобладающих в изучаемой ситуации условиях заражения людей. В связи с этим при анализе внутригодового распределения заболеваний, помимо показателя в целом по административной территории, следует изучить динамику заболеваний в различных возрастных, профессиональных или иных группах (контингентах) населения (например, среди детей, посещающих ясельные группы или группы детского сада, школьников и тех, кто не посещает детские учреждения).
Распределение инфекционных заболеваний по территории.
Территориальная неравномерность проявлений эпидемического процесса является одним из наиболее характерных эпидемиологических признаков многих заразных болезней. Характеристика пространственного распределения заболеваний используется для выявления различий в интенсивности и других особенностей эпидемического процесса на разных территориях с последующим определением причин, детерминирующих эти различия.
Часть территории земного шара, в пределах которой происходит постоянное воспроизведение заболеваний определенной болезнью, называется ареалом болезни, или ее нозоареалом (греч. nosos - болезнь + лат. area - площадь, пространство). Каждая инфекционная (паразитарная) болезнь характеризуется собственным специфическим нозоареалом.
От нозоареала отличают ареал возбудителя, т.е. область его циркуляции на земном шаре. При антропонозах ареал болезни обычно совпадает с ареалом ее возбудителя (за исключением тех случаев, когда возбудитель может сохраниться и при отсутствии на данной территории человека, например в живых переносчиках, как это наблюдается при малярии и некоторых других трансмиссивных антропонозных инфекциях, а также в объектах внешней среды, например при холере). При зоонозах и сапронозах нозоареал, как правило, меньше ареала возбудителя, который при отсутствии человека сохраняется в природе в организме животных, живых переносчиков и объектах окружающей среды (например, клещевые энцефалиты, актиномикозы).
В зависимости от особенностей распространения по территории земного шара различают болезни повсеместные (космополитические, убиквитарные), характеризующиеся глобальным нозоареалом, и эндемические (эндемичные), масштабы территориального распространения которых ограничены (табл. 5).
Повсеместными могут быть как антропонозные, так и зоонозные и сапронозные инфекции. Повсеместные антропонозы встречаются на всех континентах и во всех странах (например, корь, грипп, вирусные гепатиты и др.). Повсеместные зоонозы связаны обычно с наиболее распространенными видами позвоночных животных - резервуаров возбудителей этих инфекций, в частности с наиболее распространенными видами домашних животных. К их числу относится, например, бруцеллез, случаи заболевания которым среди животных и людей регистрируются на всех континентах.
Варианты ареалов инфекционных болезней
|
|||||||||||||||||||
Вместе с тем имеется значительное число так называемых эндемичных болезней, географическое распространение которых ограничено определенными территориями земного шара. В связи с этим различают понятия «статистическая эндемичность» и «природная эндемичность».
Статистическая эндемичность характерна для повсеместных болезней, область распространения которых не определяется природными условиями, но которые, тем не менее, постоянно встречаются в одних и не встречаются в других местностях. Подобная эндемичность той или иной болезни часто обусловливается такими социально-экономическими факторами, как санитарно-гигиенические условия жизни населения (что характерно для кишечных инфекций), масштабы иммунопрофилактики (которая может определять распространенность многих инфекций дыхательных путей).
Примером статистической эндемичности может служить современное распространение сыпного тифа, границы эндемического очага которого совпадают с местом вероятного исторического происхождения этой
инфекции: он занимает группу стран Северной Африки, от Египта и Эфиопии на востоке до Марокко и примыкающих к нему с юга ряда небольших стран на западе. Специфическими социально-бытовыми условиями жизни населения объясняют также наличие так называемого менингитного пояса в Центральной Африке, включающего Нигерию, Чад, Буркина Фасо, Судан. Нередко статистическая эндемичность связана с отсутствием достаточной медицинской помощи населению данного района.
Болезни, фиксированные на определенной территории своими биологическими связями (вследствие ограниченности области распространения источника или переносчика возбудителей либо определенных условий, необходимых для развития возбудителя вне организма источника, т.е. в организме переносчика или вне его), т.е. характеризующиеся истинной эндемичностью, называются природно-эндемическими, или природно-очаговыми.
Нозоареал природно-очаговой болезни может быть зональным или региональным. Зональными называют ареалы болезней, приуроченные к определенному географическому поясу, региональными - приуроченные к определенным районам земного шара. Иллюстрацией к этому положению может служить желтая лихорадка, географическое распространение которой характеризуется отчетливо выраженной зональной природной энде- мичностью в Африке и Америке в пределах между 42° с.ш. и 40° ю.ш.
В Африке ареал желтой лихорадки ограничен отдельными территориями в центральной, западной, южной и отчасти восточной частях континента, в зоне дождливых тропических лесов в бассейне рек Нигер и Сенегал. Здесь преимущественно распространена зоонозная форма желтой лихорадки так называемого джунглевого (сельского) типа, природным резервуаром возбудителя которой являются обезьяны, а переносчиками - многие виды комаров рода ЛёйеБ.
Желтая лихорадка также эндемична в Центральной Америке и северной части Южной Америки (Куба, Гваделупа, Боливия, Бразилия, Перу, Колумбия и др.). Полагают, что инфекция укоренилась здесь в ХУП-ХУШ вв., в период расцвета работорговли, когда на кораблях сюда были завезены зараженные возбудителем желтой лихорадки люди, а также комары - переносчики возбудителя. В Америке, главным образом во влажных районах орошаемого рисосеяния, эндемична антропонозная форма желтой лихорадки так называемого городского (урбанического) типа, резервуаром возбудителя которой являются люди, а переносчиками - комары только одного вида - ЛёйеБ aegypti, - укоренившиеся на этом континенте потомки влаго- и теплолюбивых обитателей африканских тропических лесов.
Примером региональных нозоареалов могут служить области распространения различных шистосомозов. В целом ареал шистосомозов занимает значительное пространство тропиков и субтропиков между 38° с.ш. и 35° ю.ш., эта инвазия эндемична в 73 странах с населением около 1,5 млрд человек. Из них, по оценкам ВОЗ, более 500 млн. человек подвержены риску заражения и около 200 млн. поражены этими гельминто- зами. Около 75% больных проживают в Африке, 20% - в Азии и 5% - в Америке.
Вместе с тем шистосомозы, вызываемые возбудителями разных видов, преимущественно приурочены к различным территориям. Так, мочеполовой шистосомоз, вызываемый S.haematobia, преимущественно локализуется в Африке (43 страны) и частично - в Азии (9 стран), причем на этом континенте ареал данного шистосомоза почти полностью перекрывается ареалом кишечного шистосомоза (37 стран). Кишечный шистосомоз также встречается в Америке (9 стран) и Азии (3 страны).
Ареал же японского шистосомоза, вызываемого S.japonica, ограничен только 5 странами Азии, а интеркалантного шистосомоза, вызываемого S.intercalatum, - лишь 5 странами Африки.
По форме выделяют сплошные нозоареалы (например, ареал ВИЧ- инфекции), разорванные (как ареал желтой лихорадки в Африке и в Южной Америке), ленточные (например, ареал описторхоза) и др.
Границы нозоареалов подвижны и меняются во времени, расширяясь (прогрессирующий нозоареал) или сужаясь (регрессирующий нозоа- реал). Примером прогрессирующего является нозоареал шистосомозов, регрессирующего - малярии. Нозоареал, площадь которого характеризуется быстрой сменой направления таких тенденций, называют пульсирующим (например, ареал японского энцефалита). Нозоареал, сохранившийся в первоначальном виде, называют исходным, а существенно сократившийся под влиянием хозяйственной деятельности человека - остаточным.
В современном периоде наблюдается изменение границ ареалов многих инфекционных болезней под влиянием меняющихся социальноэкономических условий жизни населения. Например, в дореволюционном периоде высокий уровень заболеваемости животных сибирской язвой в лесной и тундровой зонах России поддерживался главным образом за счет трансмиссивного распространения возбудителя инфекции, тогда как заболеваемость в южных открытых ландшафтах возникала в основном за счет алиментарных заражений животных от почвенных очагов инфекции. Массовая вакцинация скота в сочетании с неблагоприятными для существования возбудителя почвенными условиями, по-видимому, повлекла за собой угасание многих сибиреязвенных очагов на севере. В то же время наличие благоприятных для существования возбудителя почвенных условий на юге страны обусловливает сохранение почвенных очагов инфекции и поддержание заболеваемости. Аналогично этому можно проследить изменение структуры и границ нозоареалов туляремии, лептоспироза, бруцеллеза и других зоонозных инфекций.
Неравномерность территориального распределения заболеваний в пределах одного населенного пункта обычно является следствием различий в санитарном благоустройстве разных его микроучастков. Так, заболевания дизентерией или гепатитом А в пределах одного и того же населенного пункта нередко преобладают в микроучастках, отличающихся неудовлетворительным уровнем санитарно-бытового благоустройства. Существует тесная зависимость между уровнем заболеваемости этими инфекциями и такими бытовыми показателями, как типы жилища (индивидуальные или коммунальные квартиры, общежития), плотность их заселения, санитарное содержание (например, хранение и стирка грязного белья), нагрузка на санитарные узлы, санитарная грамотность населения.
Выявление преимущественной концентрации заболевших в том или ином микрорайоне населенного пункта обычно способствует установлению связи возникших заболеваний с действием определенных путей и факторов передачи возбудителя инфекции. Например, при водной вспышке кишечной инфекции, связанной с водопроводной водой, территориальное распределение заболеваний зависит от условий инфицирования воды и характера водопользования: при аварийном прорыве канализационных вод в водопроводную сеть заболевания обнаруживаются по ходу разводящей сети водопровода ниже места аварии, причем на территории с другим источником водоснабжения они отсутствуют или носят спорадический характер; при систематическом инфицировании канализационными водами открытых водоемов выше места водозабора (если отсутствует хлорирование воды, например, в техническом водопроводе) заболевания отмечаются по ходу водопровода в тех местах, где вода из него использовалась для хозяйственно-питьевых целей; при подсосе (подтекании) инфицированных стоков с поверхности почвы в водопроводную сеть заболевания обычно наблюдаются в районе пользования какой-либо водоразборной колонкой.
Фактором передачи возбудителя может быть колодезная вода. При однократном инфицировании воды в одном из колодцев (например, из приемников нечистот) случаи заболевания концентрируются вокруг данного колодца; при массивном заражении воды в результате смыва нечистот с поверхности почвы во время ливней, снеготаяния, паводка заболевания обнаруживаются вокруг различных колодцев. Причем в других местах данного населенного пункта, где есть водопровод и канализация, роста заболеваемости в это время не обнаруживают.
Наконец, если вспышка связана с использованием для хозяйственнопитьевых целей инфицированной воды из открытых водоемов, заболевания обычно концентрируются на прибрежной территории, если же речь идет о вспышке купальный сезон, такой закономерности не наблюдается.
Иной характер территориального распределения заболеваний кишечными инфекциями наблюдается при пищевом пути передачи возбудителя, причем особенности его также определяются условиями инфицирования пищевых продуктов и характером их реализации. Так, в случае инфицирования пищевых продуктов в процессе их получения, хранения или переработки (молочно-товарная ферма, птицефабрика, мясокомбинат, овощная база и др.) возможно одномоментное возникновение заболеваний на различных территориях, куда поступил инфицированный продукт, тогда как в случае инфицирования пищевого продукта на этапах его реализации (столовая, пищеблок детского учреждения или промышленного предприятия, магазин и др.) характерна территориальная разбросанность заболеваний, однако, при наличии эпидемиологической связи их с местами реализации инфицированного продукта.
При передаче возбудителей кишечных инфекций через бытовые факторы характерно наличие микроучастков с повышенной заболеваемостью на территориях с неблагоустроенными жилищными условиями.
Таким образом, характер территориального распределения заболеваний кишечными инфекциями может косвенно указывать как на преобладающий фактор передачи, так и на место и условия его инфицирования.
В соответствии с социально-экологической концепцией в территориальном аспекте эпидемиологическую соцэкосистему можно дифференцировать на локальную, региональную и глобальную. Локальные соцэкосистемы входят в состав региональных, а множество последних, в свою очередь, - в состав глобальной соцэкосистемы. При этом каждая из упомянутых эпидемиологических соцэкосистем состоит из экосистемного и соцэкосистемного уровней.
Локальная эпидемиологическая соцэкосистема - это социально - экономические условия жизни пораженного инфекцией коллектива (детский, семейный, предприятия, воинской части и др.). Данное понятие аналогично традиционному понятию «эпидемический оч
Источник: С.Т. Карагулова, В.С. Тойгомбаева, «ОБЩАЯ ЭПИДЕМИОЛОГИЯ Учебное пособие» 2009