Формулировка диагноза
- Бронхиальная астма, аллергическая форма, легкое эпизодическое течение, фаза ремиссии, ДН0. Аллергический ринит. Сенсибилизация к бытовым аллергенам.
- Бронхиальная астма, аллергическая форма, легкое персис- тирующее течение, обострение, ДНо—i. Поллиноз, риноконъюн- ктивальный синдром. Сенсибилизация к пыльце полыни.
- Бронхиальная астма, неаллергическая форма, среднее пер- систирующее течение средней тяжести, фаза обострения. Хронический бронхит, обострение. ДН1_П.
- Бронхиальная астма, смешанная форма, среднетяжелое течение, фаза обострения. Эмфизема легких, ДН|. Сенсибилизация к эпидермальным аллергенам (кошки, собаки).
Лечение
- Главное стратегическое направление в лечении аллергической и профессиональной бронхиальной астмы — определить индуктор сенсибилизации (аллерген) и максимально избавить пациента от дальнейшего контакта с ним—см. Реагиновый тип повреждения и Аллергены. Так, при «аспириновой» астме противопоказаны нестероидные противовоспалительные препараты (содержащие салицилаты или близкие к ним соединения), а также необходима гипоаллергенная диета, исключающая возможные примеси салициловой кислоты в пищевом продукте и пищевые красители (тартразин).
- Необходимо максимально ограждать больных бронхиальной астмой от контакта с курильщиками, так как пассивное курение способствует усилению симптомов астмы. К иоострению астмы предрасполагают повышение концентрации в воздушной среде частиц S02, N02, пыли.
- Обращается внимание на тщательное лечение ринита, синусита, патологии желудочно-кишечного тракта, устранение желудочно-пищеводного рефлюкса и др.
- При реагиновом типе повреждения у больных с БА решается вопрос о возможном применении специфической иммунотерапии, которая осуществляется аллергологом.
- Противовоспалительная терапия при бронхиальной астме занимает ключевое место.
При легком и среднем персистирующем течении показаны нестероидные противовоспалительные средства—хромогликат натрия, или тайлед, либо ингибиторы лейкотриеновых рецепторов, при среднем и тяжелом персистирующем течении — ингаляционные глюкокортикоиды. Противовоспалительным действием при мягком течении БА обладают кетотифен, метилксанти- ны, природные факторы — например спелеотерапия.
- Симптоматическая терапия, направленная на устранение приступов, крайне актуальна и включает симпатомиметики быстрого и пролонгированного действия.
Лекарственная терапия БА проводится во всех случаях, когда есть клинические признаки БА или регистрируется супрессия показателей внешнего дыхания, в частности ФОВ, lt; 80 %, ПОС^, lt; 80 % или индекс вариабельности ПОС^ gt;15%.
В соответствии с отчетом экспертов разных стран EPR-2 (1997) создано руководство по диагностике и лечению астмы, которое позволяет врачам лучше управлять этим заболеванием. В нем уточнен характер течения бронхиальной астмы — вместо легкой, умеренно тяжелой и тяжелой предлагается различать легкую интермиттирующую, легкую персистирующую, персисти- рующую умеренной тяжести и персистирующую тяжелую БА.
5 Н. А. Скепьян
Подчеркнуто, что у пациентов с любой тяжестью течения астмы могут наступать обострения легкой, средней и тяжелой степени.
В системе управления астмой ставятся задачи поддержания лёгочной функции, близкой к нормальной, нормального уровня активности, профилактики обострений и снижения до минимума числа госпитализаций, проведения фармакотерапии с минимальными нежелательными эффектами.
Это достигается в процессе обучения пациентов по специальной программе методам самоконтроля за состоянием обструкции, правильному использованию пикфлоуметра, спейсера, не- булайзера, элементарному дозированию и правильному приему в аэрозолях лекарственных препаратов. Решение поставленных задач осуществляется частично на основе мониторирования данных пикфлоуметрии — ПОС.^, ранним утром при легком течении БА и утром, в обед и вечером при персистирующем умеренной тяжести и тяжелом течении, с занесением данных в протокол-график (рис. 8). Мониторирование ПОС,ыд позволяет прогнозировать обострение заболевания, так как накануне его супрессия показателей развивается до появления субъективных признаков обструкции.
Полученные данные опытной ПОСВЬ1Д сопоставляются с должными ПОСвьи из табл. 13, и вычисляется процент отклонения от должного.
ПОСад опытный
ПОС^ (% от должного) 100 %.
ПОСад должный
Наряду с этим вычисляется индекс суточной вариабельности (ИСВ).
ПОС.ЫД макс - ПОСищ мин
ИСВ(%)= ¦ 100.
ПОС^и макс
При мониторировании ПОСвыд ухудшение своего состояния пациент может прогнозировать на основании вариабельных отклонений показателей пикфлоуметрии в течение суток и при нарастающей их супрессии, т.е. без расчета показателей в процентах.
Чтобы пациент мог правильно оценить состояние по регистрируемой кривой пикфлоуметрии, разработана система зон, которая для облегчения ориентировки адаптирована к цветам светофора—зеленая, желтая, красная.
Зеленая зона констатирует относительное благополучие в состоянии больного—она со. ггветствует ПОСи*» gt; 80 %, суточной вариабельности lt; 15 %. В данной ситуации симптомы астмы могут отсу гствоватъ или быть минимальными.
Желтая зона: ПОС^ в пределах 50—80 %, суточная вариабельность —20—30 %. Если эта ситуация возникает постепенно или быстро, то она обязывает увеличить объем лекарственной помощи, и обученный пациент может сам принять это решение.
Красная зона—сигнал тревоги: при падении ПОС^ lt; 50 % и увеличении суточной вариабельности gt; 30 % пациент обязан обратиться к врачу, с тем чтобы совместно с ним определить адекватную терапию БА. Переход показателей ПОСвчд с красной зоны в желтую и снижение объема проводимой терапии осуществляются под наблюдением врача.
На основании опыта мониторирования ПОСвид в сопоставлении с течением БА была сформулирована концепция ступенчатого подхода к лечению при базовом постоянном лечении противовоспалительными препаратами и препаратами для быстрого купирования БА.
При ухудшении состояния пациента количество лекарственных средств и частота их приема увеличиваются, при улучшении —уменьшаются. При такой тактике удается контролировать астму и использовать наименьшее количество медикаментов.
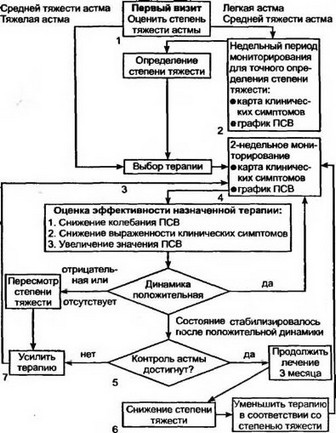
Наряду с этим приводим блок-схему (см. с. 133) метода оптимизации противоастматической терапии (А.Г. Чучалин с соавг.,
- , которая отражает необходимую последовательность действий врача при первом визите к нему пациента и при осуществлении ступенчатого лечения больных БА.
Легкая интермиттирующая астма
Противовоспалительная терапия не проводится.
Для оказания экстренной помощи рекомендуются бронхоци- лататоры короткого действия — ингаляционные р2-агонисты.
Вентолин (сальбутамол)—дозированный аэрозоль (1 вдох = 100 мкг) или вентодиск (сальбутамол) в дозе 200—400 мкг используются для контроля симптомов, но не более 1 раза в неделю. Прием сальбутамола возможен и с профилактической целью перед предполагаемым контактом с аллергеном.
Следует отметить, что вентодиск в отличие от вентолина содержит сальбутамол в виде дозированного сухого мелкодисперсного порошка, который вдыхается с помощью специального устройства—дискхалера. При обострении астмы с высокой гиперреактивностью слизистой оболочки бронхиального дерева на триггерной неспецифической основе возможна кашлевая реакция на форму препарата — микрокристаллы. Поэтому предлагаются новые технологические формы — салътос с содержанием в одной таблетке 0,00723 мг гемисукцината сальбутамола, который на осмотической основе постепенно выделяется из таблеток после их приема (А.С. Соколов, 1998).
Наряду с применением сальбутамола возможно назначение других селективных р2-агонистов: фенотерола (беротека)—200 мкг на 1 вдох или тербуталина (бриканила) — 250 мкг на 1 вдох.
Однако сальбутамол в отличие от фенотерола обладает минимальной активностью на р,-рецепторы и является одним из лучших селективных препаратов. Обеспечивает снижение высвобождения гистамина, медленнореагирующей субстанции и других медиаторов тучной клетки с помощью экспрессии на ее поверхности p-адренорецепторов—в результате снижается про
ницаемость капилляров, продукция Слизи, улучшается мукоцилиарный клиренс.
Легкая персистирующая астма
Наряду с р2-адреномиметиками быстрого действия, необходимость приема которых не превышает 2—3 раз в неделю, требуются противовоспалительные препараты (тайлед или блокаторы лейкотриеновых рецепторов, ингаляционные глюкокоргикоиды).
В качестве альтернативы ингаляционным глюкокортикоидам назначают аэрозоли кромолин-натрия (интала) от 2 мг 3 раза в день до 4—8 мг 4 раза в день. Действие препарата оценивается через 3—4 нед. Если при этом показатели пикфлоуметрии (ПОС^щ от должного) восстановились и индекс вариабельности стал менее 15 %, то Р-адреномиметики при отсутствии необходимости не принимаются, продолжается лечение инталом до 2—3 мес в профилактической дозе (2 мг 3 раза в день). При продолжающемся благополучии интал принимают эпизодически — перед ожидаемой физической нагрузкой, при триггерном воздействии факторов окружающей среды.
Если же приступы удушья периодически появляются или данные пикфлоуметрии нестабильны, то в качестве альтернативы назначают недокромил-натрий (тайлед) — натриевую соль пи- ранохинолиндикарбоновой кислоты, который хорошо сочетается с другими препаратами, подавляет как раннюю, так и позднюю фазу аллергии, оказывает преимущественно местный противовоспалительный эффект. Тайлед подавляет активность тучных клеток, эозинофилов, макрофагов, тромбоцитов, эпителиальных клеток, блокирует активность хлоридных каналов, обеспечивающих гиперполяризацию мембран, необходимую для притока в клетки кальция. В результате блокирования активности хлоридных каналов и снижения притока кальция в клетку предотвращается секреция провоспалительных медиаторов (ИЛ-1, ИЛ-8, ФНОа, гранулоцитарно-монощпарного колониестимулирующе го фактора — ГМ-КСФ), ингибируется миграция эозинофилов из кровеносных сосудов в ткани, их адгезия и хемотаксис, предотвращается повреждение эпителия бронхов. Это резко снижает пароксизмальную гиперреактивность бронхиального дерева, способствует сокращению приема р2-адреномиметиков. Курс лечения — по 2 вдоха (4 мг) 4 раза (16 мг) до стабилизации состояния — появления устойчивых показателей пикфлоуметрии, через 3—4 нед 2 вдоха 2 раза в сутки. Наши наблюдения в течение
- 8 мес лечения позволяют утверждать, что тайлед обеспечивает управление течением легкой персистирующей астмы и у отдельных пациентов персистирующей астмы средней тяжести (у подростков и пациентов до 35 лет).
К другой группе мощных противовоспалительных средств при
лечении больных БА можно отнести ингибиторы лейкотриено- вых рецепторов аколат (зафирлукаст) или сингуляр (монгелукаст).
Аколат — таблетированный препарат, средняя уточная доза—20 (40) мг, принимают 2 раза в сутки, подавляет как ранние, так и поздние реакции аллергии (Т. А. Червинская, Т.Г. Вылегжанина, 1988; Л.А. Горячкина с соавт., 1998).
По данным А.Г. Чучалина, ГЛ. Осиповой (1998), аколат (антагонист JITD4) через месяц от начала лечения в дозе 40 мг в сутки у больных БА средней тяжести облегчал симптомы астмы, обеспечивал снижение потребности в р2-агонистах в 2 раза и практически при 14-месячном применении не вызывал каких-либо побочных реакций.
Сингуляр (таблетки по 10 мг в сутки) показал высокую эффективность при БА с персистирующим легким течением, при астме, провоцируемой физической нагрузкой (в этом случае глюкокортикоиды противопоказаны), при высокой чувствительности к аспирину. Лечение сингуляром при аспириновой астме обеспечивает не только стойкий противовоспалительный эффект, но и регрессирование полипов в полости носа.
Персистирующая астма средней тяжести
Бронходилататоры короткого действия (сальбутамол — 200 мкг) назначают для экстренной помощи (при появлении удушья) не более 3—4 раз в день.
При отсутствии удушья и супрессии данных пикфлоуметрии рекомендуется таблетированный пролонгированного действия р2-агонист волмакс (сальбутамол)—8 мг 2 раза в день или ингаляционный пролонгированный fa-aroimcT серевент (сальметерол) — 50 мкг 2 раза в сутки (или в виде сухой пудры с дискхале- ром — 100—200 мкг в день). Пролонгированные Рг-адреноми- метики крайне актуальны для предупреждения ночных приступов удушья. Они обладают наиболее высокой селективностью к р2-адренорецепторам, способны подцерживать длительную пер- систирующую стимуляцию р2-адренорецепторов, не вызывают их резистенции, ингибируют антиген-индуцируемое высвобождение простагпандинов, лейкотриенов, гистамина, способствуя снижению в лаваже эозинофильного катионного белка.
Для достижения устойчивых результатов лечения необходимы более мощные противовоспалительные препараты—ингаляционные глюкокортикоиды.
В настоящее время есть много различных топических стероидов, которые позволяют при длительном приеме избегать риска возникновения системного эффекта. Для этого наряду с выбором препаратов необходимо соблюдать определенные правила приема аэрозолей — использовать спейсер, способный сепарировать крупные частицы, каждый раз после приема аэрозолей
полоскать рот, максимально по возможности задерживать вдох после впрыскивания ппококортикоида.
Противовоспалительный эффект ингаляционных глюкокортикоидов обусловлен низкой растворимостью в воде, высоким сродством к Ясирам, высокой липофильностью молекул, что позволяет создавать микродепо на слизистой оболочке бронхиального дерева. Это обеспечивает длительный контакт с клеточными структурами, проникновение в клетку через богатую липидами мембрану, связывание с рецептором в цитолизе клетки, ингиби- цию ряда продуктов воспаления — фактора агрегации тромбоцитов, лейкотриенов, простагландинов.
Таким образом, высокая липофильность ингаляционных глюкокортикоидов обеспечивает им выраженную противовоспалительную активность, низкую биодоступность — минимальный системный эффект вследствие ограниченной способности к всасыванию и попаданию в общий кровоток.
Общая биодоступность составляет у флунизогида (ингакор- та) 21 %, триамцинолона ацетонида — 22,5 %, беклометазона дипропионата (альдецина)—20 %, будезонида (пульмикорта)—
- %, флутиказона пропионата (фликсотида) — менее 1 %. Местная противовоспалительная активность глюкокортикоидов (в условных единицах) у флутиказона дипропионата составляет 945, беклометазона дипропионата — 450, бетаметазона валерата — 370, флунизолида—более 100, триамцинолона ацетонида —110.
Например, при лечении аэрозолями флунизолида в связи с высокой его биодоступностью (всасыванием) и более низкой противовоспалительной активностью, чем у флутиказона, для достижения терапевтического эффекта требуется применение более высоких доз препарата, а это значит, системные эффекты будут выше (А.Г. Чучалин с соавт., 1998). В то же время использование аэрозолей флутиказона пропионата (фликсотида) при длительном лечении больных БА дает много преимуществ, так как в случаях обострения астмы доза его может быть увеличена до 2000 мкг в сутки и при купировании приступов не нужно будет назначать на короткий период пероральные глюкокортикоиды. Следует отметить, что максимальная терапевтическая доза будезонида не превышает 1200 мкг, ингакорта — 1500 мкг.
Фликсотид можно применять как в виде дозированного аэрозольного ингалятора, так и в виде сухой пудры с дискхалером. Это позволяет обойтись без фреонов, используемых для генерации аэрозолей, не безразличных при длительном лечении аэрозолями для пациентов и для окружающей среды.
Заслуживает внимания применение в аэрозолях при долговременной терапии больных БА негалогенизированного глюко- кортикоида будезонида (пульмикорта) — ацетилового проич
водного окспреднизолона с сильным локальным противовоспалительным действием и низкой биодоступностью. 11ри этом значительная часть препарата при всасывании со слизистой оболочки органов дыхания, поступая в кровоток, метаболизируется в печени, превращаясь в неактивные метаболиты, не способные вызывать супрессию надпочечников.
Будезонид мите выпускается в виде дозированных аэрозолей (50 мкг), позволяет в ряде случаев при легком персистирующем течении астмы стабилизировать ситуацию — контролировать заболевание при дозе200мкг в сутки (2 вдоха 2 раза в сутки по 50 мкг).
Будезонид форте чаще используется при персистирующей астме средней тяжести и тяжелом течении в виде дозированного аэрозоля (200 мкг).
Аэрозоли будезонида при длительной управляемой местной терапии больных БА (около года) в сочетании с теопэком (пролонгированной формой теофиллина) позволили добиться стойкого противовоспалительного эффекта (по данным морфомет- рии), восстановления целостности цилиарных эпителиальных клеток над обнаженной базальной мембраной бронхиального дерева (А.Г. Чучалин, 1998). Кстати, вместо теопэка можно использовать неотеопэк с более длительным высвобождением кристаллов теофиллина, вмонтированного по особой технологии в виде мелкодисперсного порошка КЛН-1, через мембрану таблетки (А.С. Соколов, 1998).
У нас накоплен определенный материал, свидетельствующий, что наряду с рано начатой лекарственной терапией заслуживает внимания сочетанное применение противовоспалительной лекарственной и «экологической» (управляемой) терапии.
«Экологическая» терапия в противовес триггерному провокационному воздействию, поддерживающему воспалительный процесс, позволяет на время исключать не только специфическое (аллергенное), но и неспецифическое (триггерное) влияние на пациентов.
«Экологическая» терапия представляет собой лечение в специфической спелеосреде — экосистеме, способной привести к ремиссии заболевания, снижению гиперреактивности бронхиального дерева, сокращению объема лекарственной терапии. Эффективность подобной терапии также тем выше, чем раньше начато лечение, перспективность ее крайне высока при мягком течении бронхиальной астмы у подростков.
Бронхиальная астма—заболевание воспалительной природы, на фоне которого весьма ярко прослеживаются хаотические отклонения со стороны функциональных показателей внешнего дыхания, вариабельность их—хаотический эффект. Столь выраженная неопределенность, неравновесность этих показателей
обусловлена провоцирующими специфическими и неспецифическими факторами. Поэтому спелеотерапия представляет своеобразную экологическую систему, обеспечивающую стабилизацию хаотических эффектов у пациентов, по данным пикфлоу- метрии, и других клинических проявлений.
Спелеокомплекс на базе Республиканской больницы спелеолечения — это абактериальная среда с наличием постоянного микроклимата (температура окружающего воздуха, атмосферное давление, экранирование электромагнитного поля) в сочетании с активным образом жизни, аэроиинотерапией, оксигеноте- рапией, ингаляцией в виде микропримесей хлористого натрия (в боксах с залеганием минерала галлита), хлористого калия и магния (в боксах с залеганием минерала сильвинита).
Мы проанализировали клинико-функциональные, биохимические, иммунологические данные у 146 больных с атопической бронхиальной астмой до и после спелеолечения (наблюдение то 1 года).
Полученные результаты были оценены как отличные у 78 больных (53,7 %) с ремиссией заболевания более 5 мес, хорошие у 48 (33,1 %) с ремиссий от 2,5 до 5 мес. При этом принимались во внимание стабилизация хаотических ОФВ! (до лечения более 30 %), после лечения в пределах 10 % в течение суток, сокращение приема лекарственных препаратов — р2-агонистов в 2—3 раза, аэрозолей тайледа—в 2 раза, ингаляционных глюкокортикоидов — в 2 раза, снижение бронхиальной гиперреактивности на ингаляционную пробу с 0,1 % раствором ацетилхолина или метахолина (рис. 9).
Удовлетворительные результаты лечения отмечались у 12 пациентов (8,3 %) с неполной ремиссией до 1—2,5 мес и незначительные —у 7 человек (4,8 %) при отсутствии ремиссии. У этих пациентов оставалась высокой бронхиальная реактивность на неспецифические раздражители вследствие сопутствующего бронхита, с наличием необратимой обструкции.
В период ремиссии у больных с отличными и хорошими результатами лечения существенно повышалось качество жизни, наблюдалась высокая толерантность к физической нагрузке со стабилизацией ОФВ|, биохимических показателей крови (газовый состав, диеновые конъюгаты, малоновый ангидрид и др.).
Исследование иммунологического гомеостаза больных накануне спелеолечения свидетельствовало о преобладании гипер- пролиферативных отклонений со стороны специфических показателей иммунитет, .повышение IgE, активности комплемента). После спелеотерапии отмечалось снижение этих показателей, включая и клеточные формы иммунитета.
Таким образом, результаты лечения больных с атопической
%
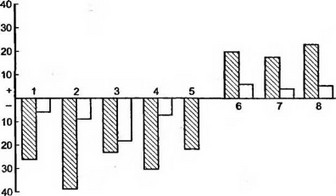
Рис. 9. Клинико-гематологические и биохимические показатели после ингаляционной фармакологической пробы с 0,1 % раствором ацетилхо- лина до (заштриховано) и после (не заштриховано) лечения в спелеокомплексе: / —мощность выдоха; 2—лейкоциты периферической крови; 3,4—эозинофилы; J — тромбоциты; 6—гистамин; 7—ацетилхо- лин; 8 — кашлевая реакция; I, 2, 3,6,7 — через 90 мин после пробы;
4, 5 — через 24 ч после пробы
БА позволяют сделать заключение, что спелеотерапия на базе Республиканской больницы спелеолечения представляет собой экосистему с комплексом лечебных факторов, оказывающих благоприятное действие на адаптационно-приспособительные реакции, бронхиальную реактивность, и способствует стабилизации хаотических отклонений у больных со стороны функциональных и биохимических показателей.
Персистирующее тяжелое течение БА. При переходе на
- ю ступень вследствие ухудшения состояния пациента может повышаться доза ингаляционных кортикостероидов (см. табл. 23), однако если этого недостаточно, то для выведения пациента из тяжелого состояния глюкокортикоиды коротким курсом (2—3 дня) могут назначаться перорально—например, медрол в таблетках.
Приводим обобщенные данные лечения больных БА (табл.
Табл. 23. Ступенчатая терапия больных БА
Степень тяжести астмы
Основные препараты и способы реабилитации
Препараты для оказания экстренной помощн
Ступень 1 Легкое эпизодическое течение
Ступень 2 Легкое пер- систирующее течение
Ступень 3 Персисти- рующее течение средней тяжести
Спелеотерапня (лечение в условиях экосистемы в течение 24 дней)
Ежедневный прием Нестероидные противовоспалительные средства:
- кромолин-натрий в виде дозированного аэрозоля
- I мг — 2 вдоха через
- 8 ч или
- недокромил-иатрий в виде дозированного аэрозоля — 2 мг — 2 вдоха 2—4 раза
При необходимости можно добавить пролонгированные бронходилататоры:
- серевент (сальметерол)
-— 50 мкг 1—2 раза
в сутки или
- волмакс — 8 мг 2 раза в сутки.
Спелеотерапня (лечение в условиях экосистемы в течение 24 дней) через
- месяцев 2 раза в год Ежедневный прием Ингаляционные кортикостероиды:
- фликсотид (флутиказона пропионат) в виде дозированного аэрозольного ингалятора или сухой пудры
Бронходилататоры короткого действия
Ингаляционный (^-агонист:
- вентолин (сальбутамол) 100 мкг или
- интал плюс (1 мг кромо- лин-натрия +100 мкг сальбутамола) для контроля симптомов, но не чаще 1—2 раз в неделю или перед предполагаемым контактом с аллергеном
Бронходилататоры короткого действия
Ингаляционный р2-аго- нист:
- вентолин (сальбутамол)
- 100—200 мкг или
- дитек (0,05 мг фенотеро- ла + 1 мг хромогликата натрия) или
- интал плюс (1 мг кромо- лин-натрия +100 мкг сальбутамола)
Бронходилататоры короткого действия
Ингаляционный р2-агонист:
- вентолин (сальбутамол)
- 100—200 мкг или
Продолжение табл. 23
|
Степень тя |
Основные препараты и |
Препараты для оказания |
|
жести астмы |
способы реабилитации |
экстренной помощи |
|
с дискхапером—400— |
• вентодиск (сальбутамол) |
|
|
1000 мкг/сут или |
— 200—400 мкг для кон |
|
|
• будезонид (пульмикорт) |
троля симптомов не чаще |
|
|
в виде аэрозольного ин |
3—4 раз в день или |
|
|
галятора — 400—1000 |
• фенотерол (беротек) в |
|
|
мкг или |
виде дозированного аэро |
|
|
• апьдецин (беклометазо |
золя — 100 мкг не чаще |
|
|
на дипропионат) — 800 |
3—4 раз в сутки или при |
|
|
мкг/сут или |
легком затруднении ды |
|
|
• флунизолид (ингакорт) |
хания |
|
|
— 800 мкг/сут |
• дитек (0,05 мг фенотеро- |
|
|
Пролонгированные брон- |
ла+ 1 мг хромогаиката |
|
|
ходнлататоры |
натрия) не более 3—4 раз |
|
|
Ингаляционный пролонги |
в сутки |
|
|
рованный р2*агонист: |
• интал плюс (1 мг кромо- |
|
|
* серевент(сапьметерол)в |
лин-натрия +100 мкг саль |
|
|
виде дозированного аэро |
бутамола) |
|
|
зольного ингалятора или |
|
|
|
сухой пудры, ингапируе- |
|
|
|
мой с помощью дискхалера, |
|
|
|
— 100—200 мкг/сут или |
|
|
|
* таблетированный пролон |
|
|
|
гированный р2-агонист |
|
|
|
волмакс (сальбутамол) — |
|
|
|
8 мг 2 раза в день или |
|
|
|
• теопэк — 100—200— |
|
|
|
300 мг 2 раза в сутки |
|
|
|
или неотеопэк. |
|
|
|
Спелеотерапия (лечение |
|
|
в условиях экосистемы в течение 24 дней) через 6 месяцев 2 раза в год.
Нестерондные противовоспалительные средства:
- кромолин-натрий (интал) в виде дозированного аэрозоля — 100 мг 2—4 раза в сутки.
При аллергической форме БА с мягким течением в качестве альтернативы ингаляционным кортикостероидам:
Продолжение табл. 23
|
Степень тя |
Основные препараты н |
Препараты для оказания |
|
жести астмы |
способы реабилитации |
экстренной помощи |
|
• тайлед (недокромил-нат- |
|
|
|
рий) — 2 мг (дозированный |
|
|
|
аэрозоль) от 4—8 до 16 мг |
|
|
|
в сутки (тайлед минт при |
|
|
|
длительном приеме не вы |
|
|
|
зывает поперхивания) |
|
|
|
Ступень 4 |
Ежедневный прием |
|
|
Персисти- |
Ингаляционные кортико |
Бронходилататоры ко |
|
рующее тя |
стероиды: |
роткого действия |
|
желое тече |
• фликсотид (флутиказона |
Ингаляционный р2-аго- |
|
ние |
пропионат) в виде аэрозоль- |
нист: |
|
ного ингалятора или сухой |
• вентолин (сальбутамол) |
|
|
пудры с дискхалером — |
—100 мкг или |
|
|
800—2000 мкг/сут или |
• вентодиск (сальбутамол) |
|
|
• будезонид (пульмикорт) |
— 200—400 мкг |
|
|
в виде аэрозольного ингаля |
|
|
|
тора — 800—1300 мкг/сут |
|
|
|
или |
|
|
|
• альдецин (беклометазона |
|
|
|
дипропионат) —1000 мкг/сут |
||
|
или |
|
|
|
• флунизолид (ингакорг) |
|
|
|
— 1000 мкг |
|
|
|
Пролонгированные брон- |
|
|
|
ходилататоры (особенно |
|
|
|
для купирования ночных |
|
|
|
симптомов) |
|
|
|
Ингаляционный пролонги |
|
|
|
рованный Рг-эгонист: |
|
|
|
• серевент (сальметерол) в |
|
|
|
виде аэрозольного ингалято |
||
|
ра или сухой пудры, ингали |
|
|
|
руемой с помощью дискха- |
|
|
|
лера,—100—200 мкг/сут или |
||
|
• таблетированный пролон |
|
|
|
гированный Рг'ЗГОНИСТ |
|
|
|
волмакс (сальбутамол)— |
|
|
|
8 мг 2 раза в день или |
|
|
|
• теопэк — 100—200— |
|
|
|
300 мг 2 раза в сутки или |
|
|
|
неотеопэк. |
|
|
|
При наличии бронхита |
|
|
|
• атровент — 20 мг (до |
|
|
|
зированный аэрозоль) |
|
|
Источник: Н. А. Скепьян, «Аллергические болезни: дифференциальный диагноз, лечение» 2000