Лекция 3 ЭЛИМИНАЦИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Элиминация (лат. elimino, eliminatum — выносить за порог, удалять) — это удаление лекарственных средств из организма в результате биотрансформации и экскреции.
Лекарственные средства элиминируются только из центральной камеры. Лекарства, находящиеся в периферической камере, предварительно транспортируются в центральную камеру, а затем подвергаются элиминации.
Элиминация лекарственных средств из плазмы крови происходит согласно экспоненциальной кинетике первого порядка — выводится постоянная часть от концентрации за единицу времени. При работе систем элиминации в условиях насыщения возникает кинетика нулевого порядка — выводится постоянное количество препарата за единицу времени.
Элиминацию лекарственных средств характеризует ряд фармакокинетических параметров:
Различают печеночный (метаболический, желчный) и почечный клиренсы. Например, у циметидина — противогистаминного средства, применяемого для терапии язвенной болезни, почечный клиренс равен 600 мл/мин, метаболический — 200 мл/мин, желчный — 10 мл/мин. Клиренс зависит от состояния ферментных систем печени и интенсивности печеночного кровотока. Для элиминации препарата с быстрым метаболизмом в печени — местного анестетика лидокаина — основное значение имеет печеночный кровоток, для элиминации антипсихотических средств группы фенотиазина — активность ферментных систем детоксикации.
При повторном применении лекарственных средств в биофазе циторецепторов создается равновесное состояние, когда количество поступающего препарата равно количеству элиминируемого. При равновесном состоянии концентрация колеблется в небольших пределах, а фармакологические эффекты проявляются в полной мере. Чем короче период полуэлиминации, тем скорее достигается равновесная концентрация и тем больше разница между максимальной и минимальной концентрациями. Обычно равновесное состояние наступает через 3 — 5 периодов полуэлиминации.
БИОТРАНСФОРМАЦИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Биотрансформация представляет собой метаболические превращения лекарственных средств. В большинстве реакций образуются метаболиты, более полярные, чем исходные лекарственные средства. Полярные метаболиты хуже растворяются в липидах, но обладают высокой растворимостью в воде, меньше подвергаются энтерогепатической циркуляции (выведение с желчью в кишечник и повторное всасывание в кровь) и реабсорбции в почечных канальцах. Без биотрансформации одна терапевтическая доза снотворного средства этаминала могла бы находиться в организме 100 лет.
Эндобиотики подвергаются превращениям под влиянием специфических ферментов, осуществляющих метаболизм их эндогенных аналогов. Ксенобиотики используют для метаболизма ферменты с малой субстратной специфичностью, например, окисляются при участии цитохрома Р- 450. Его предшественник появился у бактерий 1,5 млрд лет тому назад. После расхождения путей эволюции растений и животных 1,2 млрд лет тому назад у животных возникли изоферменты цитохрома Р-450 3 и 4 для обезвреживания токсических веществ растений. Выход жизни из моря на сушу 400 млн лет тому назад сопровождался появлением большого числа новых видов растений, часть которых образовывала неизвестные ранее токсические продукты. У животных для безопасного питания этими растениями сформировались изоферменты 1 и 2.
Биотрансформация ксенобиотиков происходит в печени (90 — 95 %), слизистой оболочке тонкого кишечника, почках, легких, коже, крови. Наиболее изучены процессы биотрансформации на мембранах гладкого эндоплазматического ретикулума (ЭПР) печени. Опыты показали, что при гомогенизации и ультрацентрифугировании клеток канальцы ЭПР разрываются и превращаются в
функционально активные фрагменты — микросомы. Реакции биотрансформации протекают также в ядре, цитозоле, митохондриях, на плазматической мембране.
Процессы биотрансформации разделяют на две фазы. В реакциях первой фазы — метаболической трансформации — молекулы лекарственных средств подвергаются окислению, восстановлению или гидролизу. Большинство лекарственных средств преобразуется в неактивные метаболиты, но также могут появляться активные и токсические производные (табл. 6). В редких случаях изменяется характер фармакологической активности (антидепрессант ипрониазид превращается в противотуберкулезное средство изониазид). Во второй фазе — реакциях конъюгации — лекарственные средства присоединяют ковалентной связью полярные фрагменты с образованием неактивных продуктов. Для реакций конъюгации необходима энергия.
Таблица 6. Активные метаболиты лекарственных средств
Реакции метаболической трансформации
Окисление
В ЭПР функционируют НАДФ»Н- и НАД»Н-зависимые дыхательные цепи. В НАДФ»Н-зависимой системе терминальным переносчиком электронов является цитохром Р-450 — мембраносвязанный липофильный фермент группы многоцелевых монооксигеназ2, гемопротеин, состоящий из белка и системы порфирина с трехвалентным железом. буква Р в названии происходит от слова пигмент, число 450 означает, что восстановленный, связанный с окисью углерода цитохром максимально поглощает свет с длиной волны 450 нм.
Цитохром Р-450 глубоко погружен в липидный бислой мембраны ЭПР и функционирует совместно с НАДФ»Н-зависимой цитохром Р-450-редуктазой (коферменты — флавинадениндинуклеотид и флавинаденин-мононуклеотид). Соотношение количества молекул цитохрома Р-450 и редуктазы составляет 10:1. Активный центр этих ферментов ориентирован на цитоплазматическую поверхность ЭПР. Цикл окисления лекарственных средств при участии цитохрома Р-450 состоит из следующих реакций (рис. 1):
Монооксигеназы включают кислород в окисляемые субстраты
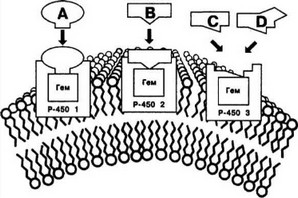
Рис. 2. Изоферменты цитохрома Р-450
НАД»Н-зависимая электрон-транспортная цепь включает цитохром b5, НАД»Н-цитохром b5- редуктазу и стероид-КоА-десатуразу. Гемсодержащий фермент цитохром b5 представляет собой двухдоменный белок. Глобулярный цитозольный домен связывается с редуктазой, короткая спирализованная гидрофобная цепь погружена в мембрану ЭПР. Электроны от НАД»Н переносятся редуктазой на окисленное железо цитохрома bs. Стероил-Ко^-десатураза катализирует образование двойных связей в жирных кислотах.
Суперсемейство цитохромов Р-450 поражает своими почти неограниченными метаболическими возможностями. Оно включает более 1000 клонированных вариантов, способных катализировать около 60 типов энзиматических реакций с тысячами потенциальных субстратов. В клетках человека обнаружено 17 семейств цитохрома Р-450, разделенных на 39 подсемейств. Изоферменты обозначаются следующим образом: первая цифра обозначает семейство, затем латинская буква указывает на подсемейство, последняя цифра соответствует конкретному изоферменту. В молекулах изоферментов одного семейства идентичны более 40 % аминокислот, в молекулах одного подсемейства — более 55 %.
Метод фенотипирования позволяет установить субстратную специфичность изоферментов цитохрома Р-450 по соотношению концентраций неизмененного вещества и его метаболитов в крови. Методом генотипирования с помощью полимеразной цепной реакции (ПЦР) изоферменты идентифицируют по их генам, так как каждый изофермент кодируется одним из 53 генов, локализованных в разных локусах хромосом. Большинство реакций катализируют изоферменты цитохрома Р-450 семейств 1, 2 и 3 (рис. 2, табл. 7).
Реакция окисления ксенобиотиков при участии цитохрома Р-450 расщепляется с образованием свободных радикалов кислорода и токсических промежуточных продуктов (эпоксиды, N-, S-окиси, альдегиды). свободные радикалы и активные интермедиаты, инициируя перекисное окисление мембранных липидов, вызывают некроз клеток, появление неоантигенов, тератогенный, эмбриотоксический эффекты, мутации, канцерогенез и ускорение старения. По этой причине не существует абсолютно безвредных ксенобиотиков.
Таблица 7. Содержание изоферментов цитохрома Р-450 в печени человека, их вклад в окисление лекарственных средств, локализация в хромосомах, индукторы и ингибиторы
Токсические продукты биотрансформации обезвреживаются конъюгацией с восстановленным глутатионом и ковалентным связыванием с альбуминами. Повреждение молекулы альбумина не опасно для организма, так как этот белок синтезируется в печени со скоростью 10 — 16г в сут. и присутствует в высоких концентрациях в ЭПР.
Ксенобиотики в процессе окисления могут разрушать цитохром Р-450. Такие вещества получили название «суицидные субстраты». Свойствами «суицидных субстратов» обладают четыреххлористый углерод, фторотан, парацетамол, преобразуемые цитохромом Р-450 в свободные радикалы. Их
эффект можно рассматривать не только как токсический, но и как защитный — элиминируются молекулы цитохрома Р-450, генерирующие реакционноспособные метаболиты.
Восстановление
Реакции восстановления характерны для альдегидов, кетонов и карбоновых кислот. В ряде случаев восстановление и окисление катализируются одним и тем же ферментом и являются обратимыми (восстановление — окисление продукта метаболизма спирта этилового — уксусного альдегида). Восстанавливаются окисленные метаболиты лекарственных средств — кетоны и карбоновые кислоты (фенамин превращается в фенилизопропанол через стадию фенилацетона).
Ароматические соединения, содержащие нитрогруппу, подвергаются в анаэробных условиях нитроредукции. Промежуточные продукты этой реакции — нитрозо- и гидроксиламиносоединения. В печени функционируют микросомальная и цитоплазматическая нитроредуктазы, в кишечнике — бактериальная нитроредуктаза.
Лекарственные средства с азогруппой восстанавливаются в первичные амины в микросомах печени и кишечной микрофлорой, например, салазопиридазин, применяемый для терапии неспецифического язвенного колита, расщепляется по азосвязи с освобождением сульфапиридазина и кислоты 5- аминосалициловой.
Гидролиз
Гидролиз необходим для биотрансформации лекарственных средств, имеющих строение сложных эфиров и замещенных амидов. Происходит в цитозоле и ЭПР эпителия кишечника и гепатоцитов, а также в крови при участии эстераз и амидаз. При гидролизе молекулы лекарственных средств распадаются на фрагменты, один из которых — кислотный или спиртовый — может проявлять фармакологическую активность.
В медицине используют пролекарства, активируемые гидролазами организма, например, левомицетина стеарат, не обладающий горьким вкусом левомицетина, в кишечнике освобождает активный антибиотик.
Растворимый препарат для инъекций левомицетина сукцинат образует левомицетин под влиянием гидролаз тканей.
Таблица 8. Изоферменты УДФ-глюкуронилтрансферазы, их субстраты, локализация генов изоферментов
Конъюгация
Наибольшее значение имеет глюкуронирование — присоединение активированной уридиндифосфатом (УДФ) глюкуроновой кислоты к алифатическим, ароматическим спиртам, карбоновым кислотам, веществам с аминогруппой и сульфгидрильной группой. Глюкуронирование катализирует УДФ-глюкуронилтрансфераза. Этот фермент функционирует в ЭПР и цитозоле клеток печени, почек, кишечника, кожи. Семейство глюкуронилтрансфераз включает более 20
изоферментов.
О-, N- и S-глюкурониды хорошо растворяются в воде и подвергаются экскреции с мочой и желчью. Глюкурониды, экскретируемые с желчью, в кишечнике под влиянием фермента бактерий Р- глюкуронидазы превращаются в исходные липофильные вещества и повторно всасываются в кровь, что дает начало энтерогепатической циркуляции (сердечные гликозиды наперстянки, левомицетин).
Таблица 9. Реакции трансформации ксенобиотиков
Сульфатирование представляет собой перенос неорганического сульфата от 3'-фосфоаденозил-5'-
фосфосульфата на гидроксил алифатических спиртов и фенолов при участии фермента цитозоля — сульфотрансферазы.
Некоторые лекарственные средства в малых дозах образуют сульфоконъюгаты, в больших дозах
При ацетилированш уксусная кислота ацетилкоэнзима А присоединяется к аминам, гидразинам, сульфаниламидам. Реакция катализируется ацетилтрансферазой цитозоля клеток. Ацетилированные метаболиты плохо растворяются в воде и элиминируются медленно.
Метилирование — перенос метила от S-аденозилметионина на лекарственное средство под влиянием метилтрансферазы. Это единственная реакция, которая не сопровождается образованием полярных метаболитов.
В последнее время установлено, что в реакциях конъюгации могут появляться токсические метаболиты — N-сульфоэфиры, N-ацетоксиариламины. Они алкилируют ДНК и вызывают мутагенез и канцерогенез.
Примеры реакций биотрансформации ксенобиотиков приведены в табл. 9.
Индивидуальные особенности биотрансформации
Особенностью человека является относительно раннее появление в онтогенезе ферментных систем, обеспечивающих метаболизм лекарственных средств. Система ферментов печени начинает функционировать в гестационном периоде (6 — 8-я нед. развития). Биотрансформацию осуществляет также плацента.
К моменту рождения в печени могут окисляться многие химические соединения. Однако активность ферментов биотрансформации у новорожденных составляет только 20 — 80% активности у взрослых. Так, скорость гидроксилирования анилина и деметилирования морфина достигает 30 — 40% скорости, регистрируемой у взрослых. Конъюгация с глюкуроновой и серной кислотами полностью развивается только к концу первого года жизни ребенка.
У новорожденных отмечаются качественные отличия в характере биотрансформации. Функционирует атипичный изофермент цитохрома Р-450 ЗА7, преобладают реакции метилирования (теофиллин превращается в кофеин).
В пожилом возрасте метаболическая трансформация лекарственных средств (анаприлин, транквилизаторы, антидепрессанты) замедляется вследствие снижения на 18 — 25 % массы паренхимы печени, перестройки ее структуры, накопления в гепатоцитах липофусцина, ухудшения печеночного кровотока, уменьшения активности цитохрома Р-450. Реакции глюкуронивания обычно не нарушаются. Возможно качественное изменение реакций биотрансформации у пожилых людей. Известно, что у лиц молодого возраста преобладает ацетилирование изониазида, а у пожилых людей
У женщин выше, чем у мужчин, активность цитохрома Р-450 ЗА4 печени, поэтому значительно быстрее происходит элиминация субстратов этого изофермента — эритромицина, верапамила и мидазолама. Эстрогены ингибируют активность цитохромов Р-450 1А2 и 2D6, что замедляет инактивацию нейролептика клозапина и антидепрессанта нортриптилина. В печени женщин медленнее протекает конъюгация салициловой кислоты с глицином.
При беременности биотрансформация ряда лекарственных средств (дифенин, гидрокортизон) замедляется, так как гормоны прогестерон и прегнандиол ингибируют цитохром Р-450 и глюкуронилтрансферазу (следует учитывать пониженное содержание альбуминов в крови беременных, увеличение у них объема распределения лекарств, усиление почечной экскреции).
При голодании окисление лекарственных средств тормозится, так как возникает дефицит цитохрома Р-450 и микросомальных белков, изменяется структура ЭПР печени. Напротив, реакции глюкуронирования при безбелковой диете усиливаются. Недостаток в пищевом рационе липотропных веществ — метионина, холина, цианокобаламина сопровождается угнетением биотрансформации из-за ожирения печени. Ненасыщенные жирные кислоты, витамины А, В1, С и E стимулируют биотрансформацию. Углеводы повышают глюкуронирование, серосодержащие аминокислоты — сульфатирование.
В составе табачного дыма индукторами метаболизма являются кадмий и полициклические углеводороды (повышают активность цитохрома Р-450 1А1 легких и 1А2 печени), ингибиторами — окись углерода, акролеин и синильная кислота.
Существенное нарушение биотрансформации возникает при патологии печени. У больных гепатитом и циррозом уменьшается активность цитохрома Р-450 и систем конъюгации, ухудшается белковосинтетическая функция печени, формируются портокавальные анастомозы (между воротной и нижней полой венами).
Возможны индивидуальные колебания скорости биотрансформации, обусловленные генетическими различиями активности ферментов. Наибольшим полиморфизмом обладают изоферменты цитохрома
P-450 1A2,2C19,2D6. Мутация изофермента цитохрома Р-450 2D6 тормозит детоксикацию
психотропных и противоаритмических средств. Хорошо известны ситуации, когда проявляются различия активности ацетилтрансферазы. При лечении туберкулеза изониазидом (гидразид изоникотиновой кислоты) у части больных не появляются побочный эффекты, другие пациенты жалуются на головную боль, головокружение, тошноту, рвоту, боль за грудиной, раздражительность, бессонницу, тахикардию, полиневрит. Побочное действие изониазида связано с тем, что его доза оказалась завышенной вследствие недостаточного ацетилирования в печени.
Различают медленных, средних и быстрых инактиваторов изониазида. Скорость ацетилирования мало сказывается на результатах лечения туберкулеза, но отражается на выраженности побочных эффектов. Медленным инактиваторам изониазид назначают в уменьшенной дозе, в комбинации с витамином В .
Регистрируется корреляция между медленным ацетилированием и заболеванием раком мочевого пузыря, между быстрым ацетилированием и развитием рака прямой кишки. Это объясняется тем, что ароматические амины подвергаются конъюгации с образованием N-глюкуронидов. Конъюгаты транспортируются в прямую кишку, где гидролизуются p-глюкуронидазой до N-гидроксисоединений. Последние в эпителии прямой кишки вступают в реакцию О-ацетилирования с образованием N- ацетоксиариламинов, способных повреждать ДНК через стадию нитрениевых ионов.
Различия в скорости ацетилирования установлены для противоаритмического средства новокаинамида, вазодилататора апрессина. Соотношение людей с различной активностью ацетилтранферазы неодинаково в этнических группах населения. Медленными инактиваторами изониазида являются 5 % эскимосов, 45% американцев, 50%жителей Западной Европы и Индии, 5 — 10% японцев.
Лекарственные средства элиминируются только из центральной камеры. Лекарства, находящиеся в периферической камере, предварительно транспортируются в центральную камеру, а затем подвергаются элиминации.
Элиминация лекарственных средств из плазмы крови происходит согласно экспоненциальной кинетике первого порядка — выводится постоянная часть от концентрации за единицу времени. При работе систем элиминации в условиях насыщения возникает кинетика нулевого порядка — выводится постоянное количество препарата за единицу времени.
Элиминацию лекарственных средств характеризует ряд фармакокинетических параметров:
- константа скорости элиминации — часть от концентрации в крови, удаляемая за единицу времени (вычисляется в %);
- период полуэлиминации — время, за которое концентрация в крови снижается наполовину (Т1/2);
- клиренс (англ. clearance — очищение) — объем жидких сред организма, освобождающихся от лекарственных средств в результате биотрансформации, выведения с желчью и мочой (вычисляется в мл/мин/кг).
Различают печеночный (метаболический, желчный) и почечный клиренсы. Например, у циметидина — противогистаминного средства, применяемого для терапии язвенной болезни, почечный клиренс равен 600 мл/мин, метаболический — 200 мл/мин, желчный — 10 мл/мин. Клиренс зависит от состояния ферментных систем печени и интенсивности печеночного кровотока. Для элиминации препарата с быстрым метаболизмом в печени — местного анестетика лидокаина — основное значение имеет печеночный кровоток, для элиминации антипсихотических средств группы фенотиазина — активность ферментных систем детоксикации.
При повторном применении лекарственных средств в биофазе циторецепторов создается равновесное состояние, когда количество поступающего препарата равно количеству элиминируемого. При равновесном состоянии концентрация колеблется в небольших пределах, а фармакологические эффекты проявляются в полной мере. Чем короче период полуэлиминации, тем скорее достигается равновесная концентрация и тем больше разница между максимальной и минимальной концентрациями. Обычно равновесное состояние наступает через 3 — 5 периодов полуэлиминации.
БИОТРАНСФОРМАЦИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Биотрансформация представляет собой метаболические превращения лекарственных средств. В большинстве реакций образуются метаболиты, более полярные, чем исходные лекарственные средства. Полярные метаболиты хуже растворяются в липидах, но обладают высокой растворимостью в воде, меньше подвергаются энтерогепатической циркуляции (выведение с желчью в кишечник и повторное всасывание в кровь) и реабсорбции в почечных канальцах. Без биотрансформации одна терапевтическая доза снотворного средства этаминала могла бы находиться в организме 100 лет.
Эндобиотики подвергаются превращениям под влиянием специфических ферментов, осуществляющих метаболизм их эндогенных аналогов. Ксенобиотики используют для метаболизма ферменты с малой субстратной специфичностью, например, окисляются при участии цитохрома Р- 450. Его предшественник появился у бактерий 1,5 млрд лет тому назад. После расхождения путей эволюции растений и животных 1,2 млрд лет тому назад у животных возникли изоферменты цитохрома Р-450 3 и 4 для обезвреживания токсических веществ растений. Выход жизни из моря на сушу 400 млн лет тому назад сопровождался появлением большого числа новых видов растений, часть которых образовывала неизвестные ранее токсические продукты. У животных для безопасного питания этими растениями сформировались изоферменты 1 и 2.
Биотрансформация ксенобиотиков происходит в печени (90 — 95 %), слизистой оболочке тонкого кишечника, почках, легких, коже, крови. Наиболее изучены процессы биотрансформации на мембранах гладкого эндоплазматического ретикулума (ЭПР) печени. Опыты показали, что при гомогенизации и ультрацентрифугировании клеток канальцы ЭПР разрываются и превращаются в
функционально активные фрагменты — микросомы. Реакции биотрансформации протекают также в ядре, цитозоле, митохондриях, на плазматической мембране.
Процессы биотрансформации разделяют на две фазы. В реакциях первой фазы — метаболической трансформации — молекулы лекарственных средств подвергаются окислению, восстановлению или гидролизу. Большинство лекарственных средств преобразуется в неактивные метаболиты, но также могут появляться активные и токсические производные (табл. 6). В редких случаях изменяется характер фармакологической активности (антидепрессант ипрониазид превращается в противотуберкулезное средство изониазид). Во второй фазе — реакциях конъюгации — лекарственные средства присоединяют ковалентной связью полярные фрагменты с образованием неактивных продуктов. Для реакций конъюгации необходима энергия.
Таблица 6. Активные метаболиты лекарственных средств
|
Лекарственное средство |
Активный метаболит |
|
Амитриптилин |
Нортриптилин |
|
Анаприлин (пропранолол) |
Гидроксипропранолол |
|
Бутадион (фенилбутазон) |
Оксифенилбутазон |
|
Дигитоксин |
Дигоксин |
|
Имипрамин |
Дезипрамин |
|
Кислота ацетилсалициловая |
Кислота салициловая |
|
Кодеин |
Морфин |
|
Кортизон |
Г идрокортизон |
|
Метилдопа |
Метилнорадреналин |
|
Новокаинамид |
N-ацетилновокаинамид |
|
Сибазон (диазепам) |
Нордазепам, оксазепам |
|
Теофиллин |
Кофеин |
|
Хлозепид (хлордиазепоксид) |
Деметилхлордиазепо ксид, нордазепам, оксазепам |
Реакции метаболической трансформации
Окисление
В ЭПР функционируют НАДФ»Н- и НАД»Н-зависимые дыхательные цепи. В НАДФ»Н-зависимой системе терминальным переносчиком электронов является цитохром Р-450 — мембраносвязанный липофильный фермент группы многоцелевых монооксигеназ2, гемопротеин, состоящий из белка и системы порфирина с трехвалентным железом. буква Р в названии происходит от слова пигмент, число 450 означает, что восстановленный, связанный с окисью углерода цитохром максимально поглощает свет с длиной волны 450 нм.
Цитохром Р-450 глубоко погружен в липидный бислой мембраны ЭПР и функционирует совместно с НАДФ»Н-зависимой цитохром Р-450-редуктазой (коферменты — флавинадениндинуклеотид и флавинаденин-мононуклеотид). Соотношение количества молекул цитохрома Р-450 и редуктазы составляет 10:1. Активный центр этих ферментов ориентирован на цитоплазматическую поверхность ЭПР. Цикл окисления лекарственных средств при участии цитохрома Р-450 состоит из следующих реакций (рис. 1):
- окисленный цитохром Р-450 присоединяет лекарственное средство;
- бинарный комплекс цитохром — лекарство восстанавливается цитохром Р-450-редуктазой, используя электрон НАДФ»Н;
- восстановленный комплекс цитохром Р-450 — лекарство связывается с молекулярным (триплетным) кислородом;
- происходит активация кислорода электроном НАДФ»Н (триплетный кислород становится синглетным);
- на финальном этапе один атом кислорода включается в молекулу окисляемого лекарственного средства, второй — включается в молекулу воды;
Монооксигеназы включают кислород в окисляемые субстраты

Рис. 2. Изоферменты цитохрома Р-450
-
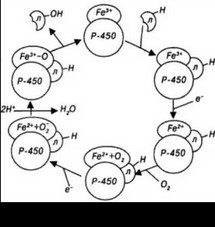 цитохром Р-450 регенерирует в исходную окисленную форму.
цитохром Р-450 регенерирует в исходную окисленную форму.
НАД»Н-зависимая электрон-транспортная цепь включает цитохром b5, НАД»Н-цитохром b5- редуктазу и стероид-КоА-десатуразу. Гемсодержащий фермент цитохром b5 представляет собой двухдоменный белок. Глобулярный цитозольный домен связывается с редуктазой, короткая спирализованная гидрофобная цепь погружена в мембрану ЭПР. Электроны от НАД»Н переносятся редуктазой на окисленное железо цитохрома bs. Стероил-Ко^-десатураза катализирует образование двойных связей в жирных кислотах.
Суперсемейство цитохромов Р-450 поражает своими почти неограниченными метаболическими возможностями. Оно включает более 1000 клонированных вариантов, способных катализировать около 60 типов энзиматических реакций с тысячами потенциальных субстратов. В клетках человека обнаружено 17 семейств цитохрома Р-450, разделенных на 39 подсемейств. Изоферменты обозначаются следующим образом: первая цифра обозначает семейство, затем латинская буква указывает на подсемейство, последняя цифра соответствует конкретному изоферменту. В молекулах изоферментов одного семейства идентичны более 40 % аминокислот, в молекулах одного подсемейства — более 55 %.
Метод фенотипирования позволяет установить субстратную специфичность изоферментов цитохрома Р-450 по соотношению концентраций неизмененного вещества и его метаболитов в крови. Методом генотипирования с помощью полимеразной цепной реакции (ПЦР) изоферменты идентифицируют по их генам, так как каждый изофермент кодируется одним из 53 генов, локализованных в разных локусах хромосом. Большинство реакций катализируют изоферменты цитохрома Р-450 семейств 1, 2 и 3 (рис. 2, табл. 7).
Реакция окисления ксенобиотиков при участии цитохрома Р-450 расщепляется с образованием свободных радикалов кислорода и токсических промежуточных продуктов (эпоксиды, N-, S-окиси, альдегиды). свободные радикалы и активные интермедиаты, инициируя перекисное окисление мембранных липидов, вызывают некроз клеток, появление неоантигенов, тератогенный, эмбриотоксический эффекты, мутации, канцерогенез и ускорение старения. По этой причине не существует абсолютно безвредных ксенобиотиков.
Таблица 7. Содержание изоферментов цитохрома Р-450 в печени человека, их вклад в окисление лекарственных средств, локализация в хромосомах, индукторы и ингибиторы
|
Изофер менты цитохро ма Р-450 |
Содерж ание в печени, % |
Вклад в окисление, % |
Локус в хромосоме (первая цифра — номер хромосомы) |
Индукторы |
Ингибиторы |
|
1А1 |
lt;1 |
2,5 |
15q22-q24 |
Полициклические ароматические углеводороды (в легких преобразуются в канцерогенные метаболиты) |
|
|
1А2 |
13 |
8,2 |
15q22-qter |
Фенобарбитал, гексамидин, дифенин, рифампицин, полициклические ароматические углеводороды, никотин |
Амитриптилин, имипрамин, такрин, мексилетин, верапамил, дилтиазем, тиклопидин, эритромицин, кларитромицин, фторхинолоны (ципрофлоксацин, норфлоксацин, эноксацин), препараты интерферона, фурацилин |
|
1В1 |
lt;1 |
Не установлен |
2q22-q22 |
|
|
|
2А6 |
4 |
2,5 |
19q13.2 |
Фенобарбитал |
Ритонавир |
|
2В6 |
lt;1 |
3,4 |
19q13.2 |
Фенобарбитал, гексамидин, дифенин |
Орфенандрин |
|
2С8 |
Не установ лено |
Не установлен |
10q24.1 |
Фенобарбитал, гексамидин |
|
|
2С9 |
18 |
15,8 |
10q24.1-24.3 |
Дифенин, рифампицин |
Бутадион, диклофенак, кетопрофен, амиодарон, флувастатин, зафирлукаст, тетурам, сульфаметоксазол, дапсон |
|
2С18 |
Не установ лено |
Не установлен |
Локус в хромосоме 10 |
|
Циметидин |
|
2С19 |
1 |
8,3 |
10q24.1-24.3 |
Фенобарбитал, гексамидин, дифенин, рифампицин |
Имипрамин, флувоксамин, флуоксетин, омепразол |
|
2D6 |
2,5 |
18,8 |
22q13.1 |
|
Тиоридазин, галоперидол, имипрамин, кломипрамин, флувоксамин, флуоксетин, пароксетин, сертралин, хинидин, пропафенон, амиодарон, циметидин |
|
2Е1 |
7 |
4,1 |
10q24.3qter |
Этиловый спирт, пиразол, пиридин |
Тетурам, ритонавир |
|
ЗА4 |
28 |
34,1 |
7q22.1 |
Фенобарбитал, гексамидин, дифенин, карбамазепин, глюкокортикоиды, рифампицин, рифабутин, сульфинпразон |
Флуоксетин, флувоксамин, пароксети н, хинидин, дилтиазем, циметидин, зафирлукаст, эритромицин, кларитромицин, флуконазол, итраконазол, клотримазол, индинавир, нелфинавир, метронидазол |
|
ЗА5 |
Не установ лено |
11 |
7q22.1 |
Фенобарбитал, гексамидин, дифенин, рифампицин |
Кетоконазол, клотримазол, миконазол, метронидазол |
Токсические продукты биотрансформации обезвреживаются конъюгацией с восстановленным глутатионом и ковалентным связыванием с альбуминами. Повреждение молекулы альбумина не опасно для организма, так как этот белок синтезируется в печени со скоростью 10 — 16г в сут. и присутствует в высоких концентрациях в ЭПР.
Ксенобиотики в процессе окисления могут разрушать цитохром Р-450. Такие вещества получили название «суицидные субстраты». Свойствами «суицидных субстратов» обладают четыреххлористый углерод, фторотан, парацетамол, преобразуемые цитохромом Р-450 в свободные радикалы. Их
эффект можно рассматривать не только как токсический, но и как защитный — элиминируются молекулы цитохрома Р-450, генерирующие реакционноспособные метаболиты.
Восстановление
Реакции восстановления характерны для альдегидов, кетонов и карбоновых кислот. В ряде случаев восстановление и окисление катализируются одним и тем же ферментом и являются обратимыми (восстановление — окисление продукта метаболизма спирта этилового — уксусного альдегида). Восстанавливаются окисленные метаболиты лекарственных средств — кетоны и карбоновые кислоты (фенамин превращается в фенилизопропанол через стадию фенилацетона).
Ароматические соединения, содержащие нитрогруппу, подвергаются в анаэробных условиях нитроредукции. Промежуточные продукты этой реакции — нитрозо- и гидроксиламиносоединения. В печени функционируют микросомальная и цитоплазматическая нитроредуктазы, в кишечнике — бактериальная нитроредуктаза.
Лекарственные средства с азогруппой восстанавливаются в первичные амины в микросомах печени и кишечной микрофлорой, например, салазопиридазин, применяемый для терапии неспецифического язвенного колита, расщепляется по азосвязи с освобождением сульфапиридазина и кислоты 5- аминосалициловой.
Гидролиз
Гидролиз необходим для биотрансформации лекарственных средств, имеющих строение сложных эфиров и замещенных амидов. Происходит в цитозоле и ЭПР эпителия кишечника и гепатоцитов, а также в крови при участии эстераз и амидаз. При гидролизе молекулы лекарственных средств распадаются на фрагменты, один из которых — кислотный или спиртовый — может проявлять фармакологическую активность.
В медицине используют пролекарства, активируемые гидролазами организма, например, левомицетина стеарат, не обладающий горьким вкусом левомицетина, в кишечнике освобождает активный антибиотик.
Растворимый препарат для инъекций левомицетина сукцинат образует левомицетин под влиянием гидролаз тканей.
Таблица 8. Изоферменты УДФ-глюкуронилтрансферазы, их субстраты, локализация генов изоферментов
|
Изоферменты |
Субстраты |
Локализация генов |
|
|
хромосома |
локус |
||
|
UGT1A1 |
Билирубин, бупренорфин |
1 |
1q21-q23 |
|
UGT1A2P |
— |
||
|
UGT1A3 |
— |
||
|
UGT1A4 |
Имипрамин, амитриптилин, доксепин, хлорпромазин, ламотриджин, ципрогептадин, кетотифен |
||
|
UGT1A5 |
— |
||
|
UGT1A6 |
Парацетамол, ибупрофен, буметанид, вальпроаты, фенол |
||
|
UGT1A8 |
Пропофол |
||
|
UGT12B4 |
Хиодезоксихолевая кислота |
4 |
4q13 |
|
UGT12B7 |
Морфин, ибупрофен, кетопрофен, фенопрофен, оксазепам |
||
|
UGT12B8 |
Андростендиол |
||
|
UGT12B9 |
— |
||
|
UGT12B10 |
— |
||
|
UGT12B11 |
— |
||
|
UGT12B15 |
— |
||
Конъюгация
Наибольшее значение имеет глюкуронирование — присоединение активированной уридиндифосфатом (УДФ) глюкуроновой кислоты к алифатическим, ароматическим спиртам, карбоновым кислотам, веществам с аминогруппой и сульфгидрильной группой. Глюкуронирование катализирует УДФ-глюкуронилтрансфераза. Этот фермент функционирует в ЭПР и цитозоле клеток печени, почек, кишечника, кожи. Семейство глюкуронилтрансфераз включает более 20
изоферментов.
О-, N- и S-глюкурониды хорошо растворяются в воде и подвергаются экскреции с мочой и желчью. Глюкурониды, экскретируемые с желчью, в кишечнике под влиянием фермента бактерий Р- глюкуронидазы превращаются в исходные липофильные вещества и повторно всасываются в кровь, что дает начало энтерогепатической циркуляции (сердечные гликозиды наперстянки, левомицетин).
Таблица 9. Реакции трансформации ксенобиотиков
|
Реакции |
Примеры лекарственных средств |
|
|
ОКИСЛЕНИЕ |
||
|
Алифатическое гидроксилирование Ароматическое гидроксилирование О-деалкилирование N-деалкилирование Окислительное дезаминирование |
RCH2CH3-gt; RCHCHj ROCH3 -gt; ROH + НС^ RNHCH3 -gt; RNH2 + HC*° RCH2NH2-gt; NH3 + HCt° |
Этаминал, ибупрофен, бутамид, циклоспорин Фенобарбитал, дифенин, бутадион, анаприлин Кодеин, индометацин Морфин, кодеин, сибазон, имипрамин, теофиллин, эритромицин Норадреналин, адреналин, гистамин, сибазон, фенамин |
|
ВОССТАНОВЛЕНИЕ |
||
|
Восстановление альдегидов, кетонов, кислот Нитроредукция Азоредукция |
r,n=nr2-gt; r,nh2 + r2nh2 |
Варфарин Нитразепам, левомицетин, нитрофураны, метронидазол Салазопиридазин |
|
ГИДРОЛИЗ |
|
|
|
Гидролиз эфиров Гидролиз амидов |
0 r,cor2 -gt; R,C00H + r2oh 0 R,CNHR2-gt; R,C00H + R2NHj |
Кислота ацетилсалициловая, новокаин, дитилин Лидокаин, новокаинамид, индометацин |
|
КОНЪЮГАЦИЯ |
||
|
Глюкуронирование |
|
Морфин, парацетамол, сибазон |
|
Суль фатирование |
З'-фосфоадено- З'-фосфо- зил-5'-фосфо- аденозил- |
Парацетамол, метилдопа, стероиды |
|
Ацетилирование |
RNhl2 +Д -gt; Сч+ KoA-SH KoAS СН3 RNH СНЭ |
Клоназепам,апрессин, сульфаниламиды, изониазид |
|
Метилирование |
S-аденозилме- S-аденозил- тионин гомоцистеин |
Норадреналин, адреналин, морфин, гистамин |
Сульфатирование представляет собой перенос неорганического сульфата от 3'-фосфоаденозил-5'-
фосфосульфата на гидроксил алифатических спиртов и фенолов при участии фермента цитозоля — сульфотрансферазы.
Некоторые лекарственные средства в малых дозах образуют сульфоконъюгаты, в больших дозах
- глюкурониды.
При ацетилированш уксусная кислота ацетилкоэнзима А присоединяется к аминам, гидразинам, сульфаниламидам. Реакция катализируется ацетилтрансферазой цитозоля клеток. Ацетилированные метаболиты плохо растворяются в воде и элиминируются медленно.
Метилирование — перенос метила от S-аденозилметионина на лекарственное средство под влиянием метилтрансферазы. Это единственная реакция, которая не сопровождается образованием полярных метаболитов.
В последнее время установлено, что в реакциях конъюгации могут появляться токсические метаболиты — N-сульфоэфиры, N-ацетоксиариламины. Они алкилируют ДНК и вызывают мутагенез и канцерогенез.
Примеры реакций биотрансформации ксенобиотиков приведены в табл. 9.
Индивидуальные особенности биотрансформации
Особенностью человека является относительно раннее появление в онтогенезе ферментных систем, обеспечивающих метаболизм лекарственных средств. Система ферментов печени начинает функционировать в гестационном периоде (6 — 8-я нед. развития). Биотрансформацию осуществляет также плацента.
К моменту рождения в печени могут окисляться многие химические соединения. Однако активность ферментов биотрансформации у новорожденных составляет только 20 — 80% активности у взрослых. Так, скорость гидроксилирования анилина и деметилирования морфина достигает 30 — 40% скорости, регистрируемой у взрослых. Конъюгация с глюкуроновой и серной кислотами полностью развивается только к концу первого года жизни ребенка.
У новорожденных отмечаются качественные отличия в характере биотрансформации. Функционирует атипичный изофермент цитохрома Р-450 ЗА7, преобладают реакции метилирования (теофиллин превращается в кофеин).
В пожилом возрасте метаболическая трансформация лекарственных средств (анаприлин, транквилизаторы, антидепрессанты) замедляется вследствие снижения на 18 — 25 % массы паренхимы печени, перестройки ее структуры, накопления в гепатоцитах липофусцина, ухудшения печеночного кровотока, уменьшения активности цитохрома Р-450. Реакции глюкуронивания обычно не нарушаются. Возможно качественное изменение реакций биотрансформации у пожилых людей. Известно, что у лиц молодого возраста преобладает ацетилирование изониазида, а у пожилых людей
- окисление.
У женщин выше, чем у мужчин, активность цитохрома Р-450 ЗА4 печени, поэтому значительно быстрее происходит элиминация субстратов этого изофермента — эритромицина, верапамила и мидазолама. Эстрогены ингибируют активность цитохромов Р-450 1А2 и 2D6, что замедляет инактивацию нейролептика клозапина и антидепрессанта нортриптилина. В печени женщин медленнее протекает конъюгация салициловой кислоты с глицином.
При беременности биотрансформация ряда лекарственных средств (дифенин, гидрокортизон) замедляется, так как гормоны прогестерон и прегнандиол ингибируют цитохром Р-450 и глюкуронилтрансферазу (следует учитывать пониженное содержание альбуминов в крови беременных, увеличение у них объема распределения лекарств, усиление почечной экскреции).
При голодании окисление лекарственных средств тормозится, так как возникает дефицит цитохрома Р-450 и микросомальных белков, изменяется структура ЭПР печени. Напротив, реакции глюкуронирования при безбелковой диете усиливаются. Недостаток в пищевом рационе липотропных веществ — метионина, холина, цианокобаламина сопровождается угнетением биотрансформации из-за ожирения печени. Ненасыщенные жирные кислоты, витамины А, В1, С и E стимулируют биотрансформацию. Углеводы повышают глюкуронирование, серосодержащие аминокислоты — сульфатирование.
В составе табачного дыма индукторами метаболизма являются кадмий и полициклические углеводороды (повышают активность цитохрома Р-450 1А1 легких и 1А2 печени), ингибиторами — окись углерода, акролеин и синильная кислота.
Существенное нарушение биотрансформации возникает при патологии печени. У больных гепатитом и циррозом уменьшается активность цитохрома Р-450 и систем конъюгации, ухудшается белковосинтетическая функция печени, формируются портокавальные анастомозы (между воротной и нижней полой венами).
Возможны индивидуальные колебания скорости биотрансформации, обусловленные генетическими различиями активности ферментов. Наибольшим полиморфизмом обладают изоферменты цитохрома
P-450 1A2,2C19,2D6. Мутация изофермента цитохрома Р-450 2D6 тормозит детоксикацию
психотропных и противоаритмических средств. Хорошо известны ситуации, когда проявляются различия активности ацетилтрансферазы. При лечении туберкулеза изониазидом (гидразид изоникотиновой кислоты) у части больных не появляются побочный эффекты, другие пациенты жалуются на головную боль, головокружение, тошноту, рвоту, боль за грудиной, раздражительность, бессонницу, тахикардию, полиневрит. Побочное действие изониазида связано с тем, что его доза оказалась завышенной вследствие недостаточного ацетилирования в печени.
Различают медленных, средних и быстрых инактиваторов изониазида. Скорость ацетилирования мало сказывается на результатах лечения туберкулеза, но отражается на выраженности побочных эффектов. Медленным инактиваторам изониазид назначают в уменьшенной дозе, в комбинации с витамином В .
Регистрируется корреляция между медленным ацетилированием и заболеванием раком мочевого пузыря, между быстрым ацетилированием и развитием рака прямой кишки. Это объясняется тем, что ароматические амины подвергаются конъюгации с образованием N-глюкуронидов. Конъюгаты транспортируются в прямую кишку, где гидролизуются p-глюкуронидазой до N-гидроксисоединений. Последние в эпителии прямой кишки вступают в реакцию О-ацетилирования с образованием N- ацетоксиариламинов, способных повреждать ДНК через стадию нитрениевых ионов.
Различия в скорости ацетилирования установлены для противоаритмического средства новокаинамида, вазодилататора апрессина. Соотношение людей с различной активностью ацетилтранферазы неодинаково в этнических группах населения. Медленными инактиваторами изониазида являются 5 % эскимосов, 45% американцев, 50%жителей Западной Европы и Индии, 5 — 10% японцев.
Источник: Венгеровский А.И., «Лекции по фармакологии» 2007