ЭФФЕКТИВНОСТЬ МЕТОДОВ ОЧИСТКИ ПИТЬЕВОЙ воды ОТ КИШЕЧНЫХ ВИРУСОВ
Присутствие биологически активных кишечных вирусов в воде централизованного водопровода представляет потенциальную эпидемическую опасность в отношении полиомиелита, других энтеровирусных инфекций и эпидемического гепатита. Находясь в питьевой воде даже в очень низких концентрациях, кишечные вирусы могут привести к появлению спорадических случаев заболеваний и даже вспышек инфекции.
Вопрос о концентрации вирусов в воде, которые могут вызывать заболевания у человека, широко обсуждался на симпозиуме, посвященном теме «Распространение вирусов водным путем» (Berg, 1967). Сделан вывод о том, что доза вируса, патогенная для культуры ткани (1 ЦПД50 или 1 БОЕ), является минимальной пероральной заражающей дозой и для человека. Исходя из этого положения, следует выдвигать требования к степени очистки хозяйственнопитьевой воды от кишечных вирусов для достижения ее эпидемической безопасности.
При существующих ныне методах очистки сточных вод и возрастающем загрязнении водоемов хозяйственно-бытовыми стоками в воде водоисточника может оказаться до 30 вирусных частиц в 1 л (Ш. Чанг,
1968) . Известно, что применяемые методы очистки и обеззараживания питьевой воды направлены в основном на удаление и инактивацию микроорганизмов, обладающих равной или меньшей устойчивостью к физическим и химическим факторам, чем группа бактерий кишечной палочки, индекс которых служит главным санитарным показателем эпидемической безопасности воды в отношении кишечных бактериальных инфекций. Неоднократные случаи выделения энтеровирусов из воды, прошедшей очистку и обеззараживание на крупных современных водопроводных станциях (А. М. Ошеровпч, Г. С. Часовни- кова, 1969; Coin е. а., 1967, и др.), указывают на недостаточную эффективность существующих методов обработки воды. Поэтому необходимо повысить эффективность очистки и обеззараживания воды, а следовательно, и улучшить ее качественные показатели.
Экспериментально доказано, что при современных технических возможностях реально достижимая максимальная степень снижения содержания вирусов в воде в процессе обработки ее на водопроводной станции составляет 99,999% от исходного их количества. В таком случае остаточная концентрация вирусов в воде, выходящей со станции, будет не более 1 БОЕ/Ю л (Чанг, 1968; Poynter с. а., 1973; Sobsey е. а., 1973, и др.). В производственных условиях эффективность методов очистки и обеззараживания питьевой воды зависит от многих трудно контролируемых привходящих факторов и чаще всего оказывается много ниже указанного выше показателя.
В настоящее время из-за отсутствия достаточно чувствительных количественных методов исследования воды на наличие вирусов нет возможности установить какие-либо нормы допустимого содержания кишечных вирусов в питьевой воде. Предполагают, что питьевую воду, содержащую менее одной вирусной частицы в 1 л, можно считать безопасной в отношении вирусных инфекций (Berg, 1967). Однако необходимо заметить, что титр вирусов, установленный в бляшкообразующих единицах, фактически не может дать истинного представления об общем количестве вирусных частиц, находящихся в питьевой воде, так как, во-первых, многие бляшки образуются не одной, а несколькими вирусными частицами, во-вторых, многие известные энтеровирусы не образуют бляшек и,
в-третьих, вирус гепатита вообще не обнаруживают, гак как он фактически еще нс известен (Berg, 1973; Denis, 1973; McLean, 1964, и др.).
В целях повышения эпидемической безопасности питьевой воды в государственные стандарты на питьевую воду, вышедшие за последние годы, были введены определенные требования, предусматривающие проведение очистки и обеззараживания воды до степени, гарантирующей максимальное удаление из нее биологически активных кишечных вирусов.
В новый ГОСТ 2874-73 «Вода питьевая», вступивший в действие у нас в стране с января 1975 г., были введены новые показатели: мутность воды не более 1,5 мг/л; при обеззараживании концентрация остаточного свободного хлора в воде не менее 0,3 мг/л при контакте не менее 30 мин, концентрация остаточного озона — 0,3 мг/л после озонирующей установки.
В третьем издании «Международного стандарта на питьевую воду» ВОЗ (1971) указано, что обеззараживание воды в отношении вирусов происходит при содержании остаточного свободного хлора в воде не менее 0,5 мг/л после срока контакта не менее 1 ч или при содержании остаточного озона не менее 0,4 мг/л после 4 мин контакта.
В докладе (AWWA Committee on Viruses, 1969) Комитета о вирусах Американской ассоциации по водоснабжению сказано, что питьевая вода не содержит вирусов после осветления до мутности не более одной единицы Джексона и последующего обеззараживания при содержании 1 мг/л остаточного хлора (в виде НОС1) после 30 мин контакта.
Выдвинутые выше требования к условиям очистки и обеззараживания питьевой воды в отношении кишечных вирусов основывались на результатах многолетнего изучения процессов механического удаления, а также физической и химической инактивации вводе разных вирусов. Исследования в этом направлении велись в лабораторных и полупроизводственных условиях, а также и на действующих водопроводных станциях. Модельными вирусами служили разные серологические типы энтеро- и аденовирусов.
Для вирусов кишечника человека пока еще не существует общепринятого санитарно-показательного микроорганизма, который мог бы надежно представлять группу кишечных вирусов в санитарно-вирусологических исследованиях. В связи с этим много работ было посвящено изучению санитарно-показательного значения для кишечных вирусов как бактерий группы кишечных палочек, так и других кишечных микроорганизмов — фагов бактерий кишечной группы, энтерококков и др. Постановка таких исследований была вызвана тем, что в настоящее время вирусологический контроль за степенью очистки и обеззараживания воды в отношении кишечных вирусов пока еще не доступен для широкой санитарной практики.
Коагуляция. При централизованном водоснабжении вода открытого водоема на водопроводной станции подвергается комплексной обработке, первые этапы которой (коагуляция, флоккуляция, отстаивание, фильтрация и т. д.) обеспечивают осветление ее за счет удаления взвешенных веществ, в том числе бактерий и вирусов. Однако воду, осветленную, но не подвергнутую заключительному обеззараживанию, нельзя считать эпидемиологически безопасной в отношении кишечных вирусных инфекций. Вместе с тем бактерицидная и вирулицидная эффективность всех известных химических и физических способов обеззараживания питьевой воды в значительной мере зависит от степени предварительной очистки ее от взвешенных частиц. Последние оказывают отрицательное влияние на исход всех обеззараживающих процессов вследствие того, что они связывают окислители, препятствуют проникновению радиации, а главным образом защищают от инактивации адсорбированные на них микроорганизмы и вирусы.
При коагуляции и флоккуляции воды, как правило, происходит механическое удаление вирусных частиц вместе с осаждением хлопьев, образовавшихся в результате взаимодействия коагулянта или флоккулянта со взвешенными в воде веществами. Кроме того, при коагуляции может протекать и неспецифическая реакция между вирусом, действующим как белок, и катионом — коагулянтом. Вследствие агрегации в хлопья вирус выпадает в осадок, из которого его можно извлечь и даже реактивировать. Эффективность процесса коагуляции воды зависит не только от дозы коагулянта, но и от таких факторов, как pH, температура и состав воды, скорость размешивания коагулянта, плотность образовавшихся хлопьев и т. д.
Процесс удаления вирусов из воды в ходе коагуляции был изучен (Чанг, 1968) в опытах, поставленных с речной водой, зараженной вирусом Коксаки, кишечной палочкой и бактериофагом. Добавление к воде 15 и 25 мг/л сульфата алюминия обеспечивало удаление из нее вируса Коксаки соответственно на 95,7 и 98,6%. Двухэтапная коагуляция 25 мг/л квасцов удаляла 99,9 % вируса и 99,9% кишечной палочки. При коагуляции воды 15 и 25 мг/л РеС13 содержание вируса Коксаки падало соответственно на 99,8 и 99,9%. Сезонные колебания температуры и изменения степени мутности воды оказывали значительное влияние на эффективность процесса коагуляции. Сильное повышение мутности воды требует соответствующего увеличения дозы коагулянта. При введении в воду достаточного количества коагулянта устранение взвешенных веществ сопровождалось параллельным удалением кишечной палочки и вирусов. Снижение дозы коагулянта более отрицательно влияло на эффективность очистки воды от вирусов и фагов, чем от бактерий. Снижение температуры воды до 5°С не ухудшало окончательного эффекта очистки воды от вируса при условии, если срок коагуляции был увеличен.
Коагуляция воды приводит к значительному снижению содержания в ней и этиологического агента (вируса) эпидемического гепатита: добровольцы, пившие воду, зараженную фекалиями больных эпидемическим гепатитом, а затем осветленную коагуляцией квасцами, заболевали гепатитом через более длительный инкубационный период, чем добровольцы, пользовавшиеся зараженной водой, не подвергавшейся коагуляции.
Мнения исследователей расходятся в отношении влияния, которое оказывают сопутствующие органические вещества в воде на степень очистки ее от вирусов в процессе коагуляции.
По данным Frankova (1964), достаточно полное удаление вируса происходило при добавлении 200— 500 мг/л коагулянта в воду, зараженную культуральной жидкостью, содержащей вирус, или взвесью мозговой ткани. Однако коагуляция теми же дозами коагулянта воды, содержащей вирус, предварительно очищенной (фильтрацией) от взвеси сопутствующих органических веществ, вызывала лишь незначительное снижение концентрации вируса в обработанной воде. Добавление к воде в процессе коагуляции поливинилового спирта (0,01%) в значительной мере повышало эффективность очистки воды от вируса. С другой стороны, путем добавления к воде возрастающих концентраций (0—200 мг/л) яичного и сывороточного белков, а также осажденных и биологически очищенных сточных вод Сhaudhuri и Еngelbrecht (1970), напротив, доказали отрицательное влияние наличия в воде сопутствующих органических веществ на эффективность очистки воды от вирусов в процессе коагуляции.
К числу средств, позволяющих ускорить и улучшить процессы коагуляции и отстаивание водьг, относятся высокомолекулярные активаторы — флоккулян- ты минерального и органического происхождения. Флоккулянты способствуют слипанию взвешенных частиц и их более быстрому осаждению. В последние годы они находят все более широкое применение в практике водоснабжения. Экспериментальное изучение (Сhaudhuri, Еngelbrecht, 1970; Тhoruр е. а., 1970) степени удаления бактериофагов из воды при добавлении коагулянта вместе с флоккулянтами еще раз доказало, что удаление вируса из воды происходит параллельно с устранением мутности. Оптимальный эффект по этим двум показателям был получен при введении коагулянта [А12(504)3- 18Н20] в дозе 40— 50 мг/л.
Изучение динамики поглощения алюминия фагом при уровнях pH воды в пределах 5—9 показало, что меньшее количество алюминия поглощалось при pH 5, когда происходило максимальное удаление фага. При этом содержание в воде ионов кальция и магния в пределах 50 мг/л нс оказывало отрицательного влияния ни на динамику поглощения алюминия фагом, ни на степень удаления фага из воды в процессе коагуляции.
В связи с возрастающим применением синтетических полиэлектролитов в водопроводной практике представлялось целесообразным изучить их влияние как непосредственно на вирусы, так и на ход удаления их из воды в процессе коагуляции и флоккуляции.
При самостоятельном использовании катионные полиэлектролиты (Primafloc С-7 и Catfloc) инактивировали изучаемые фаги за час контакта. Анионные полиэлектролиты (Primafloc А-10 и № 243) не оказывали на них никакого действия (Chaudhuri, Engel- brecht, 1970). Катионные полиэлектролиты оказались эффективными первичными коагулянтами (в отсутствие квасцов) при использовании их в концентрациях 5—12,5 мг/л. Добавление, катионных полиэлектролитов в концентрациях 0,5—1 мг/л к коагулянту усиливало реакцию коагуляции и повышало при этом степень очистки воды от фага. Анионные полиэлектролиты не оказывали влияния на действие коагулянта и поэтому не могли быть использованы как первичные коагулянты.
При использовании полиэлектролита (в малых концентрациях) в качестве флоккулянта, т. е. усилителя основного коагулянта, степень удаления вирусов из воды повышалась с 56—58 до 80—94%, если в воду добавляли 1 мг/л катионного полиэлектролита, но совершенно не изменялась при добавлении анионного и неионного полиэлектролитов. При этом процесс коагуляции и удаления вирусов был более выражен в воде, содержащей 20 мг/л ионов Са++ и Mg++> чем в воде, содержащей ионы Na+ и К+. (Thorup е. а., 1970).
Установлено, что инактивация вируса полиомиелита в воде может произойти в процессе устранения жесткости (Berg е. а., 1968; Wolf е. а., 1974; Sattar е. а., 1974, и др.).
При обработке Са(ОН)2 жесткой воды, содержащей Са(НС03)2, концентрация вируса снижалась на 43—81%, что соответствовало количеству осажденной соли СаС03. Осаждение из жесткой воды солей магния сопровождалось удалением из воды более чем 99% вирусов (Wentworth е. а., 1968).
При- коагулировании известью Са(ОН)2 в дозе 200—500 мг/л воды, зараженной аттенуированным штаммом вируса полиомиелита типа I, содержание в ней вируса после отстаивания осадка снижалось на 70—90,8%, а при последующей фильтрации через песок— еще на 82—99,8%, что в общей сложности составило 98,6—99,997%). Так как увеличение дозы извести повышало уровень pH воды, то можно допу
стить, что при pH выше 10 происходило не только механическое удаление вируса, но и инактивация его щелочной средой (Berg е. а., 1968).
Оценка разных способов осветления воды с учетом как их стоимости, так и эффективности в отношении снижения мутности и содержания вирусов показала, что методы первичной коагуляции воды сульфатом алюминия, хлоридом железа и сульфатом железа являются наиболее перспективными. При этом степень удаления из воды фага составляла 99—99,9% (Shelton, Drowry, 1973; York, Drowry, 1974).
Фильтрация. После коагуляции и отстаивания вода подвергается фильтрации. На водопроводах в качестве фильтрующего материала, как правило, применяется песок и лишь в отдельных случаях на небольших установках используется гранулированный уголь.
Сущность фильтрации заключается в пропускании воды через толщу мелкозернистого материала, на поверхности или в самом верхнем слое которого задерживаются взвешенные частицы. На медленных песчаных фильтрах по мере эксплуатации на поверхности песка образуется биологическая пленка, которая сильно повышает эффективность процесса фильтрации. Биологическая пленка сама превращается в фильтр и задерживает наиболее мелкую взвесь, которая прошла бы сквозь слой песка. На скорых фильтрах вместо биологической пленки на поверхности песка образуется пленка из мелких хлопьев коагулянта, которая также повышает степень задержки взвешенных частиц на фильтре. Эффективность процесса скорой фильтрации находится в прямой зависимости от предварительного процесса коагуляции (Robeck е. а., 1964, и др.).
Меньшая эффективность скорой фильтрации перед медленной оказалась еще более выраженной в отношении вирусов, чем бактерий. Экспериментально установлено, что после медленной фильтрации в воде оставалось 1—3% бактерий, вирусов и фагов, а после быстрой фильтрации — 90% вирусов, 65% фагов и 25—30% бактерий (Gilcreas, Kelly, 1955).
При скорой фильтрации через песчаный фильтр удалялось лишь незначительное количество внесенного в воду вируса полиомиелита. При медленной фильтрации воды, содержащей хорошо перемешанный коагулянт, 98% вируса задерживалось на слое песка тол-
щиной около 20 см. Повышение дозы квасцов и тщательное смешивание их с водой приводили к большому образованию и отстаиванию осадка, а последующая фильтрация воды через песок удаляла до 99% и более общего количества внесенного в воду вируса (Robeck е. а., 1964).
При обработке воды с большим содержанием взвешенных веществ значительное число вирусных частиц проскакивало через фильтр, несмотря на то что мутность получаемого фильтрата была в пределах нормы. Добавление к воде вместе с коагулянтом полиэлектролита в количестве 0,05 кг/л в значительной степени повышало стабильность хлопьев в воде и эффективность фильтрации даже при сильной перегрузке песчаного фильтра. Очевидно, задержка вируса происходила в основном в слое песка, пропитанного коагулянтом, так как сам песок обладал слабой адсорбционной способностью в отношении вирусов.
Если на сухом свежем песке адсорбировалась лишь небольшая часть присутствовавших в воде вирусных частиц (0,1—0,51g LDso/o.25 мл), то на увлажненном песке их задерживалось уже много больше (1—2 1g). Максимальный эффект очистки воды от вируса получали при фильтрации се через песок, взятый' непосредственно из действующих фильтрационных установок водопроводных станций. Высокие адсорбционные свойства этого песка также объясняются наличием слоя коагулянта на поверхности песчинок (Nestor, Costin, 1971).
Вирусы могут адсорбироваться на частицы глины, находящиеся во взвешенном состоянии в естественной воде водоема или искусственно введенные в воду в процессе ее обработки. Изучение динамики адсорбции фага Т2 и вируса полиомиелита типа I частицами глины (Kaolinite 4, Montmorillonite 23, Illite 35), взвешенными в пробах воды с разными концентрациями (0,001—0,1 A4) солей натрия и кальция, показало, что при одинаковом содержании глины в воде процент удаления вирусов из воды возрастал с увеличением концентрации в воде катионов Na и Са. Наиболее эффективное удаление (99%) биологически активных вирусов всеми тремя сортами глины было получено при наличии в воде катионов Na. Высокая степень очистки воды от вирусных частиц (97—98%) сопровождалась
образованием хлопьев, которые выпадали - в осадок. При этом адсорбированный вирус не инактивировался и после элюцип восстанавливал свою активность (Carlson с. а., 1968). V
Оценка глин как возможных сорбентов для очистки воды должна проводиться с учетом их сорбционных способностей и эффективных концентраций в воде. При этом желательно принимать во внимание и влияние уровня pH воды на степень сорбции различных видов вирусов на глине (Chaudhuri, Engelbrecht 1970- Brown е. а., 1974).
Вопрос о целесообразности использования различных глин в целях повышения степени очистки воды от вирусов еще не решен. Не все глины, способные адсорбировать вирусы, могут быть использованы в водопроводной практике. Вбольшинстве случаев достаточно высокий процент (
 90) удаления вирусных частиц из воды происходит лишь при условии введения сорбентов в исключительно высоких концентрациях, которые практически не приемлемы для режимов очистки воды (Т. А. Николаева и др., 1979).
90) удаления вирусных частиц из воды происходит лишь при условии введения сорбентов в исключительно высоких концентрациях, которые практически не приемлемы для режимов очистки воды (Т. А. Николаева и др., 1979).
Активированный уголь применяется в практике водоснабжения в основном для удаления из воды некоторых органических примесей, придающих воде привкус и запах. В дозах и при условиях, в которых активированный уголь применяется в широкой практике водоснабжения, он не оказывает какого-либо существенного влияния на очистку воды от вирусов. Адсорбционная способность активированного угля была исследована в отношении вирусов полиомиелита эпидемического гепатита и вируса энцефаломиелита мышей (Clarke, Chang, 1959).
В последние годы было проведено детальное изучение механизма и динамики адсорбции ряда вирусов па частицах активированного угля. При этом вирусы рассматривались как коллоидные частицы белка разного размера (20—200 мл), действующие по принципу амфотерных электролитов, заряд которых зависит от pH воды. Оказалось, что разные вирусы обладают различными изоэлектрическими точками, т. е адсорбируются на частицах угля при разных значениях pH воды: бактериофаг Т2 адсорбируется в основном при pH 4,2 и ниже, аденовирус -при pH 3,9, вирус ящура — при pH 6,0. В отношении исследованного бакте-
риофага установлено, то степень адсорбции его на активированном угле увеличивается с повышением pH от 0 до 7, а затем начинает понижаться (Cookson,
1969) .
При наличии в воде сопутствующих органических веществ адсорбционная емкость угля в отношении вирусов истощается скорее, чем в отношении остальных органических веществ, находящихся в воде. В процессе элюции вирусные частицы удаляются вместе с органическими веществами (Sproul, 1972).
Высокая адсорбционная способность некоторых ионообменных смол позволила широко использовать их в практике водоснабжения для умягчения, опреснения, обеззараживания и других видов обработки воды.
При помощи фильтрации через колонку с сильно- основным анионитом АВ-17 удалось получить обеззараживание воды, содержавшей модельный энтеровирус (вирус энцефаломиелита мышей) (Е. В. Штанни- ков, 1965). Обеззараживающее действие анионита, вероятно, является результатом комбинированного эффекта сорбции вируса на анионите и инактивации его сильнощелочным фильтратом, образующимся вследствие реакции с анионитом содержащихся в воде солей.
Изучая механизм адсорбции вирусов на порошкообразной окиси железа, Larin и Gallimore (1971) установили, что степень адсорбции вируса из жидкости зависит в основном от размера частиц окиси железа, а не от их магнетического состояния. С уменьшением размера частиц возрастает площадь их адсорбционной поверхности, а следовательно, и количество адсорои- рованного вируса.
Анализируя результаты приведенных выше экспериментальных работ, можно сделать вывод, что в процессе коагуляции, флоккуляции и фильтрации очистка воды от взвешенных веществ (мутности), бактерии и вирусов происходит параллельно. При этом динамика процесса зависит от качества обрабатываемой воды а также от вида и дозы вводимых реагентов. Положительное влияние на исход процесса коагуляции воды (степень осветления и очистки воды от вирусов) оказывают следующие условия: повышение дозы коагулянта до оптимального уровня, двухэтапное введение коагулянта, добавление к коагулянтам флокку- лянтов (минеральных, органических, ’синтетических), предварительное хлорирование воды. От полноты предварительной коагуляции зависит и степень дальнейшего осветления воды на скорых фильтрах. Таким образом, степень удаления вируса в процессе осветления воды может достигать 99,9% и более. Однако такой высокий процент очистки воды от вируса удается получить лишь в экспериментальных условиях, когда можно контролировать отрицательное влияние различных привходящих факторов.
Наряду с большим количеством разнообразных экспериментальных данных о возможности удаления вирусов из воды при помощи тех или иных коагулянтов, флоккулянтов и сорбентов имеются весьма ограниченные .сведения о наблюдениях, проведенных на действующих водоочистных установках.
На водопроводных станциях гг. Нанси и Люневиль (Франция) энтеровирусы и фаги были выделены как из воды, поступающей на водоочистные сооружения, так и из прошедшей коагуляцию, отстаивание и фильтрацию (Foliguet е. а., 1966).
Primavesti (1970) из сильно загрязненной реки Рура (ФРГ) в большинстве случаев удавалось выделять вирусы полиомиелита и Коксаки, и лишь после соответствующей коагуляции и интенсивного хлорирования энтеровирусы в данной воде ни разу не обнаружились.
Судя по результатам круглогодичных вирусологических исследований воды (на энтеровирусы и фаги), проведенных на одной из крупных водопроводных станций нашей страны, коагуляция, первичное хлорирование, отстаивание и фильтрация постепенно снижают содержание в воде вирусов, но не устраняют их полностью (Е. Л. Ловцевич, 1974).
По мнению Ш. Чанг (1968), в производственных условиях в результате осветления удается удалить из воды не более 90—95% находящихся в ней вирусов. Полноценная санитарно-вирусологическая оценка" эффективности функционирования водоочистных установок на действующей водопроводной станции в настоящее время практически не осуществима из-за недостаточно высокой чувствительности методов обнаружения вирусов в воде.
Представление о количественном удалении вирусов из воды на разных этапах ее очистки можно получить при опытной обработке ее на действующих полупроиз- водственных установках. При этом есть возможность ставить опыты с водой с заданными свойствами (мутность, цветность, pH, концентрация вирусов, фагов, бактерий группы кишечной палочки и т. д.). Принимая во внимание чувствительность имеющихся методов индикации изучаемых микроорганизмов, воду, предназначенную для обработки, можно заражать ими в концентрациях, достаточно высоких для определения степени (процента) их удаления после каждого последовательного этапа очистки и обеззараживания.
Такие исследования были проведены на опытнотехнологической установке (ОТУ) Научно-исследовательского института коммунального водоснабжения и очистки воды Академии коммунального хозяйства имени К- Д. Памфилова (Е. Л. Ловцевич и др., 1974). Были пущены линии установок, моделирующие следующие этапы обработки питьевой воды: 1) коагуляцию, отстаивание и фильтрацию на скорых вертикальных фильтрах; 2) коагуляцию и фильтрацию через контактный осветитель. Опыты ставили на воде с искусственно заданной мутностью (7,1 — 13,4 мг/л) и цветностью (20—28°), зараженной смесью микроорганизмов, выделенных из речной воды, в том числе санитарно-показательной кишечной палочкой, а также фагом TI Е. coli и вакцинным штаммом (LSc2ab) вируса полиомиелита типа I. Дозы коагулянта, максимально устраняющие мутность, колебались в пределах 4—7 мг/л. При этом во всех опытах достигалась высокая степень осветления воды: мутность снижалась до 0,1—1,5 мг/л, а цветность —до 0°. Предварительное (первичное) хлорирование производили дозами от 1 до 2,8 мг/л.
Уровень остаточного хлора в воде на выходе с контактного осветлителя и со скорого фильтра колебался в пределах 0,4—0,5 мг/л. Полученные результаты исследований представлены в табл. 9.
В процессе очистки воды наблюдались определенные закономерности: снижение мутности и цветности воды сопровождалось уменьшением содержания в воде как бактерий, так и вирусов. При этом вирус из воды удалялся в меньшей степени, чем остальные микро-
Степень удаления из воды бактерий и вирусов в процессе осветления
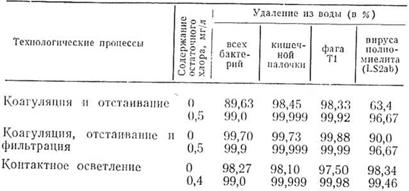 |
организмы. Степень очистки воды была выше в воде с более высокой исходной мутностью.
Удаление из воды бактерий и вирусов (после коагуляции) путем пропускания ее через контактный осветлитель не уступало по эффективности методу скорой фильтрации.
В тех случаях, когда коагуляция и отстаивание оказывались малоэффективными, воду подвергали фильтрации через скорый фильтр, что значительно повышало степень осветления воды и удаление из нее микроорганизмов и вирусных частиц.
Первичное хлорирование повышало эффект всех процессов очистки воды от всех исследованных микроорганизмов и вирусных частиц, но больше всего от вируса полиомиелита (от 63,4 до 96,67%), а в отсутствие хлора вирусных частиц удалялось намного меньше, чем всех других исследованных агентов.
Таким образом, наблюдения, сделанные в производственных и полупроизводственных условиях, также как и данные экспериментальных исследований, доказывают, что существующие процессы коагуляции и фильтрации воды обеспечивают значительное снижение содержания в ней взвешенных веществ, бактерий и вирусов, но не устраняют их полностью. Воду, осветленную этими двумя способами, но не подвергнутую последующему обеззараживанию, нельзя считать эпидемически безопасной в отношении кишечных бактериальных и вирусных инфекций. Вместе с тем, как уже
говорилось выше, эффективность всех известных мето- дов обеззараживания воды в значительной мере зависит от степени предварительной ее очистки, чем и объясняются высокие требования, предъявляемые стандартами, к допустимой мутности питьевой воды.
А так же в разделе «ЭФФЕКТИВНОСТЬ МЕТОДОВ ОЧИСТКИ ПИТЬЕВОЙ воды ОТ КИШЕЧНЫХ ВИРУСОВ »
- РОЛЬ ВОДНОГО ФАКТОРА В РАСПРОСТРАНЕНИИ КИШЕЧНЫХ ВИРУСНЫХ ИНФЕКЦИЙ
- МЕТОДЫ ИНДИКАЦИИ КИШЕЧНЫХ ВИРУСОВ В ВОДЕ РАЗЛИЧНОЙ СТЕПЕНИ ЗАГРЯЗНЕНИЯ
- РАСПРОСТРАНЕНИЕ КИШЕЧНЫХ ВИРУСОВ В ВОДЕ
- ВЫЖИВАЕМОСТЬ КИШЕЧНЫХ ВИРУСОВ В ВОДЕ РАЗЛИЧНОЙ СТЕПЕНИ ЗАГРЯЗНЕНИЯ
- ЭФФЕКТИВНОСТЬ МЕТОДОВ ОБЕЗЗАРАЖИВАНИЯ ПИТЬЕВОЙ ВОДЫ В ОТНОШЕНИИ КИШЕЧНЫХ ВИРУСОВ
- ЭФФЕКТИВНОСТЬ МЕТОДОВ ОЧИСТКИ И ОБЕЗЗАРАЖИВАНИЯ СТОЧНЫХ ВОД В ОТНОШЕНИИ КИШЕЧНЫХ ВИРУСОВ