I. ПЛАСТИЧЕСКАЯ ХИРУРГИЯ
Пластическая хирургия — область медицины, включающая восстановление формы и/или функции отдельных частей тела или органов, утраченных или повреждённых в результате заболеваний и травм или удалённых оперативным путём. Кроме того, пластические хирурги занимаются лечением врождённых аномалий и коррекцией дефектов, отражающихся на деятельности человека. Методы пластической хирургии: перемещение, трансплантация тканей и имплантация замещающих ткани материалов.
А. История. Пластическая хирургия — одна из старейших областей хирургии. В древнеиндийских эпосах есть упоминания о том, что члены некоторых каст могли воссоздавать нос из кожи лица. В тибетских монастырях найдены ещё более древние книги с описанием подобных операций. В Европе описание пластических операций при врождённой расщелине верхней губы впервые встречается в работах римского врача Корнеяиуса Цёлъса. Хирург Бранка из Катании (Сицилия) произвел в 1442 г. операцию с целью восстановления тканей носа. Во второй половине XVI века своими пластическими операциями прославился итальянец Гаспар Тальякдцци — профессор из Болоньи, описавший способы восстановления целостности носа, ушных раковин, дефектов губ. В 1597 г. Тальякдцци предложил для пластики носа использовать кожный лоскут плеча на питающей ножке. В том же году им была издана одна из первых книг по пластической хирургии. После работ Бранка и Тальякдцци ринопластика с помощью лоскута кожи, взятого с плеча, и вообще какая-либо пластика лоскутом кожи на ножке, взятом с иной части тела, получила название итальянский способ пластики. В 1818 г. фон Грэфе впервые применил термин «пластика» в своей монографии по реконструкции носа; с тех пор этот термин ассоциирован с хирургией, восстанавливающей форму или функцию органа. В 1794 г. в медицинской литературе появилось описание восстановления дефекта кожи лоскутом на ножке, выкраиваемым из прилежащей к дефекту кожи {индийская пластика). В 1814 году английский хирург Карпи с успехом произвёл две подобные операции. Индийская пластика привилась в Европе. Позднее во Франции получил распространение метод пересадки кожных лоскутов, когда на поражённую часть лица пересаживали участок кожи, не граничащий с раной, — французская мастика (метод Цёльса). Затем Шимандвский внедрил ринопластику с использованием выкроенного из лобной кости лоскута в качестве опоры для мягких тканей, что предупреждало западение сформированного носа. Результаты пластических вмешательств того времени часто были неудовлетворительными из-за присоединения раневой инфекции. С внедрением асептики количество удачных операций {в т.ч. пластических) значительно увеличилось. Стала возможной трансплантация, т.е. свободная пересадка ткани без питающей ножки. В декабре 1869 г. французский хирург Ревердён сделал сообщение о свободной пересадке отдельных лоскутов кожи. В 1875 г. Вольф впервые с успехом произвёл пересадку полнослойного лоскута кожи площадью 5x2,5 см, он подчеркнул важность пересадки кожи вместе с подлежащей тканью. В 1929 г. Блёйер и Браун предложили пересаживать т.н. расщеплённые кожные лоскуты.
Специализированные стационары пластической хирургии для оказания помощи воинам с обезображивающими ранениями впервые стали создавать во время первой мировой войны. В 1930 г. французские хирурги основали Общество пластической и эстетической хирургии, а в 1933 г. в Париже прошёл первый международный конгресс по пластической хирургии. Через год бельгийский хирург Колет начал издавать международный журнал «Новости пластической хирургии».
Б. Кожа (cutis) — орган, служащий наружным покровом тела и выполняющий функции защиты организма, обмена веществ, терморегуляции и др. В этом покрове тела присутствуют придатки кожи (железы, ногти, волосы), сформированные из эпителиального и соединительнотканного компонентов.
- При проведении пластических оперший важны цвет, эластичность, растяжимость и упругость кожи.
- Слои кожи — эпидермис, собственна кожа (дерма). Глубже расположена подкожная жировая клетчатка.
а. Эпидермис состоит из десятков слоев эпителиальных клеток — кератиноцитов. В зависимости от толщины эпидермиса (в среднем у новорождённого 0,05 мм, у женщины 0,6 мм, у мужчины 0,8 мм), различают кожу с большим ороговением (толстая кожа — подошва стопы и кожа пятки — 5-5,6 мм) и кожу с малым ороговением (тонкая кожа — веки — 0,8-0,85 мм).
Обновление эпидермиса. Эпителиальные клетки постоянна смещаются от базальной мембраны эпидермиса (граница с дермой) кнаружи, формируя на поверхности слой отпадающих кератиновых чешуек (кератинизация). Это перемещение занимает примерно 20 дней. Так происходит постоянное обновление эпидермиса за счёт расположенных на базальной мембране камбиальных клеток.
Кератиноциты — мишени ряда гормонов и факторов роста. Их основные эффекты — стимуляция пролиферации клеток и усиление кератинизации.
(0 Пролиферация кератиноцитов. Стимулируют факторы роста (эпидермальный, трансформирующий и кератиноцитов [фибробластов фактор роста FGF7]).
(Н) Кератинизация. Стимулирует 1сс,25-дигидроксихолекальциферол (активная форма витамина D, кальцитриол), подавляющий в кератиноцитах синтез ДНК.
б. Дерма — соединительнотканная часть кожи, состоит из двух слоев.
- Сосочковый слой. Рыхлая волокнистая соединительная ткань, содержит мнсго- численные кровеносные капилляры, а также чувствительные нервные окончания, расположенные преимущественно во вдающихся в эпидермис конической формы сосочках.
- Сетчатый слой. Сосочковый слой постепенна переходит в плотную неоформленную волокнистую соединительную ткань сетчатого слоя, содержащего колли- гзн I типа, обеспечивающий прочность кожи. Условная граница между этими двумя слоями собственно кожи проходит на уровне расположения концевых отделов сальных желёз.
- Кровоснабжение кожи. Артерии кожи отходят ст сплетения, расположенного в псд- ксжнсй клетчатке. В сетчатом слое присутствуют многочисленные артериовенозные анастомозы. На границе сосочкового и сетчатого слоев имеется подсосочковая сеть, от которой к поверхности кожи отходят короткие артериальные ветви, снабжающие кровью группы сосочков. Кроме того, от подсоссчковой сети отходят артерии для волос и сальных желёз. Поверхностная капиллярная сеть, играющая важную роль в терморегуляции, расположена тотчас под эпидермисом. Диаметр капилляров кожи от 0,02 мм (туловище) до 0,2 мм (ушные раковины). На лице частое воздействие ультрафиолетовыгх лучей, суровые климатические условия, пожилой возраст приводят к стойкому расширению капилляров и венул (эктазии).
- Регенерация кожи
а. Поверхностные повреждения. При поражении поверхностных слоев кожи эпидермис восстанавливается за счёт кератиноцитов волосяных фолликулов и потовых желёз, расположенных в глубоких слоях собственно кожи.
б. Глубокие повреждения. При более глубоких повреждениях кожи (например, при ожогах III степени, когда разрушается не только эпидермис, но также волосяные фолликулы и потовые железы) раны небольших размеров заживают самостоятельно за счёт миграции и размножения кератиноцитов соседних участков эпидермиса. Этот способ заживления оказывается недостаточным в случае больших ран, требующих специального лечения.
в. Большие дефекты кожи. Для восстановления больших неглубоких дефектов кожи используют расщеплённые трансплантаты — фрагменты кожного покрова, переносимые с одной части тела на другую. Наряду с этим методом, для лечения обширных кожных ран используют предварительно культивированный in vitro эпителиальный трансплантат.
Расщеплённый трансплантат состоит из эпидермиса и собственно кожи. Часть собственно кожи вместе с волосяными фолликулами и потовыми железами остаётся на месте забора трансплантата и покрывается эпидермисом за счёт мигрирующих из этих источников кератиноцитов.
- Заживление кожных ран (см. также главу 2 I). На дне раны в пределах собственно кожи образуется небольшое количество фибрина. Эпидермис краёв раны растёт вглубь, покрывая открытую поверхность соединительнотканной части кожи, с последующим восстановлением непрерывности эпителиального пласта. В заполнении дефекта собственно кожи участвуют фибробласты (преимущественно из подкожной клетчатки). Последняя также служит источником капилляров для регенерирующей соединительной ткани кожи. Размножение фибробластов и клеток сосудистой стенки поддерживают факторы роста (например, секретируемые макрофагами). Толстая кожа заживает хуже по сравнению с тонкой, тёмная кожа — хуже светлой, на ней чаще образуются гипертрофические рубцы и келоиды. Продольные разрезы, пересекающие сгибательные поверхности суставов, ведут к образованию гипертрофических контракционных рубцов.
При усиленном потоотделении характерны: склонность к возникновению экземы вокруг раны, расстройства процессов заживления, образование неполноценных рубцов. Повышенное содержание в крови кортикостероидов ведёт к замедлению процессов заживления, небольшие дозы инсулина ускоряют эти процессы.
В. Шовные материалы и техника закрытия ран
- Шовный материал — общее название материалов, применяемых для соединения краёв раны или перевязки сосудов. Выбор шовного материала зависит от вида и объёма хирургического вмешательства.
а. Диаметр нити. Для идентификации шовного материала применяют систему USP: диаметр нити (в мм) обозначают различным количеством нулей (11/0 — одиннадцать нулей, 10/0,9/0 и т.д.). Чем больше нулей, тем тоньше нить (например, нить 3/0 — условный размер 0,20-0,29, что соответствует 2 мм; нить 8/0 — условный размер
- 040-0,049 - 0,4 мм).
б. Шовный материал при большинстве проводимых операций — единственное инородное тело, остающееся в тканях. Основные требования к шовному материалу: биосовместимость, резорбтивность и атравматичность.
- Биосовместимость — отсутствие токсического, аллергенного и тератогенного эффектов шовной нити на ткани организма.
- Резорбтивность (биодеградация) — способность материала распадаться и выводиться из организма. Шовный материал должен удерживать ткани до образования рубца, а затем он становится ненужным. Темп рассасывания (биодеградации) не должен превышать скорость образования рубца (исключение — шов сосудистого протеза).
- Прочность нити и сохранение её свойств до образования рубца —
важные параметры шовного материала. Чем тоньше нить, тем меньшая масса инородного шовного материала остаётся в тканях; следовательно, уменьшается реакция тканей. Поэтому предпочтительнее использовать нити малых диаметров, но такие нити менее прочны. При этом нужно учитывать не столько прочность самой нити, сколько прочность нити в узле (для большинства нитей потеря прочности в узле составляет 20-50%).
- Атравматичность зависит от структуры и вида нити, её манипуляционных свойств (эластичности и гибкости). Понятие атравматичности включает несколько свойств, присущих шовным материалам.
- Поверхностные свойства нити. Кручёные и плетёные нити имеют шероховатую поверхность и при прохождении через ткани создают пилящий эффект. Мононити (монофиламентные) или полинити (полифиламентные) с полимерным покрытием уменьшают пилящий эффект и облегчают скольжение нити (выпускают кручёные, плетёные и комплексные нити). Однако полимерное покрытие уменьшает надёжность узла и требует наложения узлов сложной конфигурации.
- Способ соединения нити с иглой. Лучшими считают атравматические иглы, в них нить впаяна в иглу и представляет как бы её продолжение. В микрохирургии, где необходимы нити особо малых размеров, некоторые иглы делают путём напыления металла на нить.
- Манипуляционные свойства нити. К ним относят эластичность и гибкость. Манипулировать жёсткими нитями труднее, они повреждают ткани, и образование рубца всегда проходит через стадию воспаления. В то же время излишняя эластичность может привести к расхождению краёв раны. Наилучшими манипуляционными свойствами обладает шёлк (золотой стандарт).
- Классификация шовного материала. Классификация основана на способности шовного материала к рассасыванию. Различают рассасывающиеся и нерассасывающиеся нити,
а. Рассасывающиеся материалы
- Кетгут получают из тонкой кишки овец или телят. Продолжительность поглощения материала фагоцитами варьирует от 2 неддо 6 мес. Скорость резорбции кетгута и реакция тканей уменьшаются при инфильтрации кетгута солями хрома. Кетгут — один из наиболее реактогенных шовных материалов. Так, при ушивании чистой раны кетгутом достаточно ввести в неё 1000 микробных тел стафилококка, чтобы вызвать её нагноение. Кетгут теряет 50% прочности в течение 2-10 сут. Низкая прочность кетгута заставляет хирургов использовать нить с большим диаметром. Кетгут достаточно широко используют хирурги России. Мировая практика призывает отказаться от применения кетгута (и шёлка) в пользу синтетических шовных материалов.
- Коллаген и сухожильная нить подобны кетгуту. Нити на основе коллагена не нашли широкого применения из-за высокой стоимости производства и отсутствия преимуществ по сравнению с кетгутом.
- Материалы на основе полигликолидов (например, викрил фирмы Ethicon, дексон [Devis amp; Geek], дар-вин [Ergon sutramed], полисорб [USSC]). Нить из поли- гликолевой кислоты прочнее кетгута, время полного рассасывания от 2 неддо 2 мес. Эти полифиламентные нити (за исключением полисорба) не рекомендуют применять при шве апоневроза, т.к. нити недостаточно долго сохраняют прочность. Полисорб в 1,5 раза прочнее викрила, лучше викрила, дексона и дар-вин'а сохраняет прочность в тканях и обладает повышенной прочностью узла, это один из наиболее перспективных рассасывающихся шовных материалов.
- Пaлидиaксанaн (например, PDS, PDS2 фирмы Ethicon, максан (Davis amp; Geek]) — монофиламентные нити. Они эластичнее полифиламентного материала, обладают более длительными сроками потери прочности и рассасывания (например, PDS в первый месяц теряет лишь 30-50% прочности). Время пaлнaго рассасывания — 6 мес. К недостаткам этих нитей можно отнести необходимость применения узлов сложной конфигурации.
- Материалы на основе целлюлозы (например, окцелон и кацелон). Выпускаются с различными сроками рассасывания: от нескольких дней до нескольких недель.
- Полиуретан. Нити из полиуретана обладают рядом положительных свойств. Они биосовместимы, вызывают минимальную реакцию организма и рассасываются в срок до года. В России и за рубежом проводятся исследования по применению этих материалов в клинике. Все рассасывающиеся ниши нельзя применять для протезирования сосудов и клапанов сердца.
б. Нерассасывающиеся швы не удовлетворяют основному требованию — биодеградации, но они незаменимы при протезировании, а также при наложении швов на ткани,
длительные сроки находящиеся под натяжением. Эти материалы дёшевы и удобны.
Различают органические и синтетические нерассасывающиеся шовные материалы, а
также проволоку и скрепочные швы.
- Органические (например, шёлк и хлопок) наиболее реакгогенны. У шёлка выражены сорбционные свойства, поэтому он фиксирует микрофлору.
- Синтетические шовные материалы
(а) Полиамидные (капрон, нейлон и дакрон). Из всех синтетических нитей дают наиболее выраженную реакцию тканей. Полиамидные нити полностью разрушаются и выводятся из организма от 3 мес до 2 лет. Большинство фирм выпускают полиамиды в виде плетёной или мононити (при этом реактогенность нити значительно снижается, а её сорбционные свойства уменьшаются). Хороши для кожи, подкожной клетчатки, мышц, трахеи, бронхов.
(б) Полиэфирные (лавсан, нейлон, эти6энд, мерсилен, М-дек). Полиэфирные нити инертнее шёлка и полиамидов, но их прочность в области узла невелика. В настоящее время область их применения постоянно уменьшается, они уступают полиамидам по прочности, а полиолефинам по инертности, прочности и надёжности узла.
(в) Полиолефины (прэлен фирмы Ethicon, полипропилен [Sharpoint], суржипрэ [USSC], суржилен [Devis amp; Geek]) наиболее инертны, имеют высокую надёжность узла. Эти нити удобны при сшивании кожи. Выпускаются только мэнэни- ти. Благодаря своим уникальным свойствам, могут быть использованы даже в инфицированных тканях.
(г) Фторполимерные нити (например, Gore-Tex) ещё инертнее полиолефинов; благодаря их высокой тромборезистентности, их используют в сердечно-сосудистой хирургии.
- Проволока применяется в основном для шва грудины и мелких трубчатых костей (например, фаланги пальцев). В России разработана прэвэлэка для шва ЖКТ, грыжевых ворот.
- Скрепочный шов (клипсы) получает всё большее распространение. Ранее шира- ко использовавшиеся танталовые скрепки заменяют более прочными титановыми. Самые нейтральные в отношении тканевой реакции среди нерассасывающихся швов. Разработаны аппараты, накладывающие механический шов на кожную рану металлическими скрепками (Ethicon, USSC), а также для фиксации кожного трансплантата рассасывающими скэбами (пэлисэрб), для наложения внутрикажнаго шва (USSC).
- Иглы и шовный материал. Риск развития некроза и рубцов снижается при использовании атравмитических игл и подходящего шовного материала.
Атравматинеские иглы применяют во всех областях хирургии. Их основные характа- ристики: длина, диаметр, форма. По форме различают иглы колющие, режущие, колющие с режущим концом, ланцетовидные, тупоконечные. Иглы должны быть прочными, острыми, устойчиво фиксироваться в иглодержателе, идеальная нетравмирующая игла по диаметру не должна превышать диаметр нити.
- Операционная рана и наложение швов
а. Линия разреза. Разрез должен совпадать с направлением нервных вслсксн и сосудов (тем самым сохраняются иннервация и васкуляризация окружающих тканей). Правильно спланированный разрез имеет длину, достаточную для обеспечения необходимого для операции рабочего пространства. При определении направления разреза необходимо помнить следующее:
- естественное заживление раны происходит от края к краю, а не от конца к концу;
- расположение волокон в области предполагаемого разреза определяется типом ткани;
- необходимо, чтобы разрез проходил в естественных складках кожи, которые в большинстве случаев соответствуют линиям Лангера.
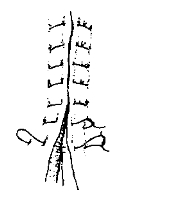
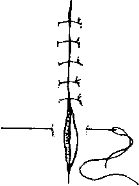
б. Швы (рис. 24-1).
- Узловые швы захватывают одинаковые по толщине участки кожи и подкожной клетчатки. Для меньшей травматизации целесообразно применять режущие иглы.
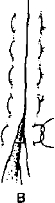

Д
Рис. 24-1 Варианты ушивания операционной раны. Швы: А узловой; Б — вертикальный
матрацный; В — горизонтальный матраnный; Г — внутрикожные; Д непрерывный сбвивней
Вкол и выкол располагаются на одной линии и строго перпендикулярно ране. Стежки должны быть достаточно редкими, чтобы сопоставлялись края раны. Каждую нить после проведения завязывают и отрезают. Узел вяжут над точками вко- ла или выкола, но не над самой раной. Такие швы при закрытии ран более надёжны, при разрыве одной нити остальные швы продолжают удерживать края раны. Могут применяться при инфицированных ранах, т.к. распространение микроорганизмов вдоль линии узловых швов менее вероятно. В косметической и эстетической хирургии узловые швы практически не применяют.
- Матрацные швы. Вертикальный матрацный шов — прерывистый шов, при наложении которого иглу выводят из ткани на ту же сторону края раны, где её вводят. При этом нить ложится перпендикулярно краям раны. Следующий стежок делают на другом крае. Сопоставление краёв раны очень хорошее. Горизонтальный матрацный шов накладывают, если нужно приподнять края раны. Односторонний матрацный шов — вкол и выкол производят с одной стороны раны через всю толщу кожи, с другой стороны игла захватывает только дерму на той же глубине. Применяют для фиксации отдельных, особо чувствительных мест. Горизонтальные матрацные (или П-образные) швы отличаются от вертикальных тем, что нить на поверхности кожи ложится параллельно линии разреза. Применяют при затруднениях в сопоставлении краёв кожной раны.
- Внутрикожные швы. Стежки накладывают, не выводя нить на поверхность кожи, параллельно ей и на одинаковой глубине. Преимущество — отсутствие шовных меток на коже, поэтому их часто применяют в пластической хирургии. Могут быть как истинно внутрикожные, так и подкожные. Все они непрерывные.
- Непрерывный обвивной шов Мультановского — закрепляющий. Каждый стежок захлёстывается петлёй, благодаря чему натяжение нити не передаётся на ранее наложенные стежки. Часто применяют для сшивания позадиушных ран у детей и ран волосистой части головы кетгутом. Отпадает необходимость удалять стежки. Достигают удовлетворительного косметического эффекта и быстрого восстановления микроциркуляции в краях раны.
- Во избежание образования грубых послеоперационных рубцов для сближения краёв раны используют также специальные клейкие полоски из синтетического материала.
- Шов жировой клетчатки. Целесообразнее сшивать лишь фасции жировой клетчатки. Желателен непрерывный съёмный шов или узловой из рассасывающихся материалов.
- Скрыиые швы предпочтительнее при пластических операциях (снижается натяжение по краям раны).
- Неверное сопоставление краёв раны приводит к образованию грубого рубца.
в. Срок снятия шва. Большинство хирургов считает, что не может существовать стандартных сроков снятия швов, т.к. в каждом конкретном случае присутствуют различные факторы, влияющие на заживление послеоперационной раны. При косметических операциях срок удаления швов не имеет особого значения, если использовать внут- рикожные швы. В клинических условиях удаление швов происходит на 3-10-й день после операции, т.е. когда прочность рубца достигает 5-10% нормальной прочности тканей. Длительное пребывание шовного материала в ране для удержания её краёв бессмысленно, т.к. через две недели рана становится достаточно прочной, чтобы существовать без швов. Удержание краёв раны в течение длительного времени (при большом натяжении в ране) без ухудшения косметического состояния рубца возможно
только внутренним (внугрикожным) швом — косметическим. Нет единого мнения о необходимости удаления внутрикожно наложенной синтетической нити. Правильная адаптация краёв раны при косметическом шве позволяет снять швы на 3-й, самое позднее на 7-й день, когда шовный материал фактически теряет значение как удерживающая сила.
г. Косметически приемлемый внешний вид — главная задача при выполнении пластических операций. При выполнении любых хирургических вмешательств необходимо добиваться заживления раны первичным натяжением. Заживление раны вторичным натяжением (например, при неправильной технике наложения шва) приводит к образованию рубца, вызывающего косметический дефект. Неправильное заживление кожных ран может повлечь за собой новые, более серьезные осложнения (операционные грыжи, гипертрофические уродующие рубцы).
д. Заживление операционной раны и последующее образование рубца зависят от времени удаления шовного материала. Следует отметить целесообразность раннего удаления швов, что снижает выраженность кожных меток и уменьшает частоту нагноений. В результате ускоряется заживление, формируется нежный послеоперационный рубец, уменьшается время восстановления тканей. Шовный материал, находящийся в ране, нарушает процесс формирования соединительной ткани. После удаления швов устраняется сдавление тканей, улучшается лимфо- и кровообращение.
е. Шовные метки — следы, возникающие в результате давления швов на кожу. Они более выражены при натяжении раны, отёке, инфицировании, при вовлечении больших тканевых поверхностей.
Г. Кожные трансплантаты — участки эпидермиса и дермы, взятые для пересадки на другую область тела. Различают аутотрансплантаты — используют собственные ткани организма, аллотрансплантаты — от генетически чужеродного индивида того же вида, изотрансплантаты — пересадка кожи от одного однояйцового близнеца к другому и ксенотран- сплантаты — от особи другого вида. В настоящее время используют терминологию, принятую на Международном симпозиуме по трансплантологии в Вене (1967).
- Типы. Кожные трансплантаты классифицируют в зависимости от их толщины.
а. Расщеплённые кожные трансплантаты содержат эпидермис и часть дермы. Подразделяются (в зависимости от толщины входящей в трансплантат дермы) на тонкие (0,25 мм), средние (0,5 мм) и толстые (0,6-0,65 мм). В детском возрасте не следует иссекать трансплантат, толщина которого превышает 0,4 мм. Донорские области — живот, ягодицы и бёдра.
- Преимущества расщеплённых кожных трансплантатов.
(а) Большие площади донорских поверхностей.
(б) Простота забора трансплантата.
(в) Возможность повторного использования донорской поверхности через 10-14 дней.
(г) Малый риск развития первичных контрактур.
(д) Возможность закрытия больших поверхностей.
(е) Возможность хранения для дальнейшего применения.
- Недостатки расщеплённых кожных трансплантатов.
(а) Более выраженный косметический дефект по сравнению с полными трансплантатами.
(б) Относительно неудовлетворительное приживление.
(в) Гиперпигментация.
(г) Высокий риск развития вторичных контрактур.
б. Полные (полнослойные) кожные трансплантаты содержат эпидермис и дерму без подкожной жировой клетчатки. Их применяют в тех случаях, когда трансплантат
должен соответствовать высоким механическим и эстетическим требованиям. Пересадка нерасщеплённого кожного лоскута может быть использована только для закрытия сравнительно небольших кожных дефектов на определённых участках тела. Чаще всего это кожные покровы лица или кистей. Донорские места — заушная и надключичная области.
- Методы забора. Трансплантаты забирают ручным способом, захватывая участки подкожной жировой клетчатки. Используют ножи с лезвиями № Ю или № 15.
- Уход за донорской поверхностью осуществляют первичным закрытием раны. Возможна подсадка расщеплённых трансплантатов.
- Уход за реципиентной поверхностью подобен уходу при расщеплённых трансплантатах.
- Преимущества полных кожных трансплантатов.
(а) Лучший косметический эффект.
(б) Низкий риск развития вторичных контрактур.
(в) Повышенная прочность приживления.
- Недостатки полных кожных трансплантатов.
(а) Ограниченные донорские площади.
(б) Повышенный риск развития первичных контрактур.
в. Смешанные трансплантаты состоят из нескольких тканей {например, фаланга, состоящая из кожи, жировой клетчатки, кости; сегмент ушной раковины, содержащий хрящ и кожу). Пластику с использованием смешанных трансплантатов чаще проводят пациентам молодого возраста или в тех случаях, когда дистальная часть трансплантата находится на расстоянии менее 1 см от источника кровоснабжения.
- Трансплантация собственной кожи (аутокожа)
а. Расщеплённые трансплантаты удобнее забирать специальными инструментами, нежели ручным способом.
- Методы забора трансплантатов
(а) Скальпелем или ножом Тирша срезают небольшие фрагменты.
(б) Электродерматом Брауна или Пёджеша снабжён быстро вращающимся ножом и винтом, регулирующим глубину забора. Забирает длинные полосы кожи.
- Уход за донорской поверхностью подразумевает устранение капиллярного кровотечения, что способствует эпителизации.
(а) Чаще всего достигают после обработки раны 3% р-ром перекиси водорода, наложением однослойной марлевой стерильной повязки и многократной обработкой р-ром перманганата калия этой повязки. Образовавшийся струп самостоятельно удаляется вместе с марлей через 2 нед.
(б) Ячеистая, неприлипающая марля абсорбирует струп. Струп отделяется от раны через 2 нед.
(в) Полупроницаемые мембраны. Ими покрывают донорскую поверхность (впитывают экссудат, тем самым ускоряя эпителизацию и уменьшая болевой синдром) или формируют над донорской поверхностью пузырь, содержащий и удерживающий экссудат, ускоряя при этом процесс эпителизации и уменьшая болевой синдром.
- Уход за реципиентной поверхностью (трансплантатам)
(а) Гемостаз необходим для обеспечения адекватного контакта тканей.
(б) Инфицирование. При опасности инфицирования для улучшения дренирования раны на трансплантате делают насечки. Промежутки между насечками эпите- лизируются достаточно быстро. Насечки также используют для увеличения
площади поверхности трансплантата. Открытый метод применяют у ожоговых пациентов с большими поверхностями трансплантатов. При этом возрастает вероятность инфицирования.
(в) Фиксация. Трансплантаты фиксируют при помощи швов или лент. Там, где возможно смещение трансплантата, выполняют наружную фиксацию с помощью повязки по типу узла над болюсом (т.е. большой повязки из марли или ваты).
- Приживление трансплантатов
а. Сосудистое ложе необходимо для питания трансплантированных тканей.
- Имбибиция (пропитывание) плазмой трансплантата обеспечивает его приживление в первые 48 ч. Оседающий фибрин удерживает трансплантат.
- Срастание (сосудистое прививание) происходит с 4 по 7 день с момента пересадки. К этому сроку трансплантаты приобретают физиологичную окраску.
б. Контакт трансплантата с подлежащими тканями необходим для приживания. Причины отсутствия контакта:
- натяжение трансплантата,
- наличие жидкости (кровь, плазма или гной) под трансплантатом,
- трение между трансплантатом и его ложем.
в. Подготовка ран к трансплантации. Чем хуже состояние тканей воспринимающего ложа, тем тоньше должен быть трансплантат. Приводим последовательный перечень тканей (от наиболее подходящих к наименее подходящим) для свободной пересадки кожи: здоровая мышечная ткань, кориум, надкостница, мелкозернистая подкожная клетчатка, апоневроз, поверхностная фасция, крупнодольчатая клетчатка. Сами раны подготавливают обычным способом (спирт и другие антисептики).
Инфицированные раны не пригодны для трансплантации. Для очищения раны применяют механическую санацию. В этих случаях целесообразнее алло- или ксенот- рансплантаты.
- Виды кожной пластики
а. Первичная пластика. Первичную пластику проводят в течение первых суток после травмы
б. Отсроченная пластика. К ней прибегают через 1-2 нед после возникновения травмы.
- Аутопластика. Аутопластику также можно выполнять:
а. за счёт местных тканей (сближение краёв раны, нанесение послабляющих разрезов);
б. за счёт лоскутов на питающей ножке, расположенных по соседству с дефектом (использование плоских, мостоввдных лоскутов [разработал НФ Склифосовский в 1885 г.;
в отличие от итальянского способа, лоскут имеет две питающие ножки], перемещение встречных треугольных лоскутов по Лимбергу или лоскутов, взятых с отдалённых участков тела, — отдалённая этапная пластика с помощью филатовского стебля);
в. за счёт микрохирургической пересадки свободных сложносоставных лоскутов.
Д. Лоскут — участок тканей (кожа с подкожной клетчаткой), отделённый оперативным путём для трансплантации и имеющий значительную площадь при небольшой толщине. Необходимо сохранить источник кровоснабжения лоскута, если лоскут не свободный. Лоскуты используют для закрыпия дефектов, требующих заполнения объёмом ткани.
- Виды лоскутов
а. Кожные лоскуты
- Произвольные лоскуты. Источник кровоснабжения — дермалъно-субдермamp;пъ- ное сплетение. Эти лоскуты обладают недостаточным кровоснабжением. Примеры:
(а) Z- образная пластика,
(б) V-Y-образные лоскуты,
(в) ротационные лоскуты (на широкой питающей ножке),
(г) транспозиционные лоскуты (мостовидный, филатповскш стебель).
- Артериализированные лоскуты снабжены кожной артерией и веной, образую- ' щими подкожное сплетение, что позволяет забирать значительные по длине лоскуты. Примеры;
(а) лоскуты, взятые со лба;
(б) паховые лоскуты,
(в) лоскуты кожи, покрывающей дельтовидную и грудную мышцы.
б. Мышечные лоскуты имеют удовлетворительное кровоснабжение. Их применяют при костных повреждениях, обычно совместно с кожными трансплантатами. Кожномышечные лоскуты — лоскуты, содержащие мышцы и кожу с подкожной клетчаткой.
- Анатомические границы лоскута определяют по источнику кровоснабжения. Сосуды (артерию и вену) надо найти, идентифицировать и сохранить.
- Применение мышечных лоскутов особенно полезно при реконструкции нижних конечностей и в зонах недостаточной васкуляризации.
в. Кожно фасциальные лоскуты содержат кажу, падкажную клетчатку, подлежащую фасцию с артерией. Мобилизацию подлежащей мышцы не производят. Донорскую поверхность закрывают кожным трансплантатом.
г. Свободные сложносоставные лоскуты — лоскуты, при заборе отделённые ат естественного источника кровоснабжения. Могут быть кожно-жировыми, кожно-фасциальными, мышечными, кожно-мышечными, сухожильными, костными, костно-мышечными. Реваскуляризацию обеспечивают микрохирургическим анастомозом с использованием операционного микроскопа с увеличением от 5 до 20.
- Применение лоскутов
а. Закрытие ран в зонах пониженной васкуляризации (раны над оголёнными костями, хрящами, нервами или сухожилиями).
б. Пластика лица (носа или губ).
в. Для увеличения поверхности и объёма тканей, покрывающих кость {например, у больных с пролежнями).
Е. Реконструкция врождённых аномалий развития.
- Врождённые аномалии развития (пороки развития) возникают идиопагически, в результате генных и хромосомных дефектов, а также при воздействии различных экзогенных факторов (токсические вещества, радиация, лекарственные препараты и т.п.) при внутриутробном развитии, чаще в эмбриогенезе. Лечение и реконструкция многих аномалий не ограничены областью пластической хирургии {например, пороки ЖКТ).
- Деформации лица и верхней челюсти — область челюстнэ-лицевэй хирургии.
а. Аномалии костей и мягких тканей
- Синдром Грёга — наследственная семейная аномалия развития; характерные симптомы включают г
Источник: Лопухин Ю.М., Савельев В.С., «Хирургия» 1997