Иммунологическая память
В процессе иммунного ответа происходит элиминация патогена. Устойчивость к нему, называемая протективным иммунитетом, поддерживается упомянутыми эффекторными факторами (антитела, цитотоксические Т-лимфоциты, другие активированные клетки адаптивного и врожденного иммунитета) (рис. 1.9). Однако срок жизни этих клеток и гуморальных факторов ограничен. После их разрушения организм сохраняет иммунитет к патогену, но он имеет другую основу. Выше отмечалось, что при иммунном ответе одновременно с эффекторными клетками образуются клетки памяти, не вовлекаемые в текущий иммунный ответ, но формирующие пул защитных клеток при повторной встрече с тем же антигеном. Клетки памяти морфологически не отличаются от наивных клеток, но несут ряд характерных мембранных молекул, определяющих пути рециркуляции, отличные от таковых для наивных лимфоцитов. Численность клеток в каждом клоне клеток памяти на 2—3 порядка выше, чем в клонах наивных лимфоцитов. В-клетки памяти уже прошли этап переключения изотипа секретируемых антител и V-гены их иммуноглобулинов содержат соматические мутации, произошедшие в зародышевых центрах. CD4+ Т-клетки памяти уже дифференцированы на субпопуляции. Все это ускоряет развитие иммунного ответа при повторной встрече с антигеном — вторичного иммунного ответа.
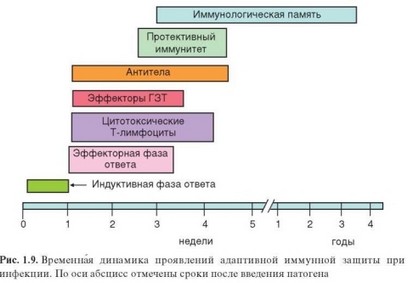
Однако природа этой повышенной эффективности клеток памяти пока не вполне ясна.
Как известно, основное и наиболее эффективное направление практической иммунологии, с развитием которого связано зарождение этой науки, — вакцинация, т.е. индукция эффективной иммунологической памяти без проявления заболевания. В последние годы сходные принципы стали использовать в лечебных целях: проводят большую работу по созданию онковакцин, аллерговакцин, а также вакцин для лечения аутоиммунных заболеваний. Во всех этих случаях поставленной цели пытаются достигнуть не столько путем формирования клеток памяти (хотя и это имеет место, по крайней мере, при создании онковакцин), сколько путем переориентации иммунного ответа, вызываемого вакцинами, в желаемом направлении. Например, при аллергии пытаются индуцировать Th1-опосредованный иммунный ответ на аллерген вместо уже сформировавшегося ^2-ответа, обусловливающего проявления аллергии. При аутоиммунных процессах пытаются индуцировать анергию к аутоантигенам; при опухолях — наоборот, усиливают иммунный ответ на опухолевые антигены и направляют его по TM-пути.
Источник: Ярилин.А.А , «Иммунология » 2010
А так же в разделе «Иммунологическая память »
- Зарождение иммунологии
- Развитие иммунологии до середины ХХ века
- «Новая иммунология» 50-80-х годов ХХ века
- Современный этап развития иммунологии — молекулярная иммунология
- ЕСТЕСТВЕННАЯ ИСТОРИЯ ИММУНИТЕТА
- КРАТКОЕ ИЗЛОЖЕНИЕ ИММУНОЛОГИИ
- Молекулы-мишени иммунитета (образы патогенности, антигены) и распознающие их рецепторы
- Иммунная система
- Первая линия иммунной защиты
- Адаптивный иммунный ответ
- Эффекторные механизмы иммунного ответа. Взаимосвязь факторов врожденного и адаптивного иммунитета
- РЕЗЮМЕ