Свежезамороженная (антигемофильная) плазма (СЗП) в суточной дозе 10— 15 мл/кг способна поддерживать концентрацию фактора VIII на уровне выше
- 6% (средняя норма — 100%) при повышении этого показателя сразу же после быстрой трансфузии — до 15—25%. Такой уровень достаточен для предупреждения и купирования небольших геморрагий. К лечению плазмой следует прибегать только при отсутствии у врача других, более концентрированных и очищенных, препаратов антигемофилических факторов свертывания. При этом нужно учитывать, что введения чрезмерно больших количеств СЗП, особенно в течение ряда дней подряд, могут стать причиной гиперволемии и подчас весьма тяжелых сердечно-сосудистых осложнений, электролитных нарушений, перегрузки организма балластными белками, а также вторичных иммунных и аллергических синдромов. При использовании не вирусинакгивиро- ванных препаратов плазмы и других компонентов крови возрастает также опасность заражения больного возбудителями гепатита, герпеса, СПИДа и ряда других заболеваний.
Криопреиипитат. осаждаемая при низкой температуре фракция плазмы, давно используется в терапии гемофилии А и ряда других заболеваний и синдромов, связанных с дефицитом ФСК VIII, XIII и фактора Виллебранда. Фактор VIII содержится в нем в 3—5 раз более концентрированном виде, чем в СЗП, тогда как фактор IX — в небольшом количестве. Криопреципитат вызывает значительно меньшую нагрузку на гемодинамику реципиента, поскольку вводится в значительно меньшем обьеме и содержит во много раз меньшее количество альбумина, чем плазма. Поэтому у больного в процессе лечения существенно не увеличивается ОЦК и онкотическое давление крови, не подвергаются вторичной дилюции ФСК, не развиваются при курсовом применении гемодинамические расстройства и дегидратация тканей.
Главными недостатками криопреципитата являются его нестандартизиро- ванность по содержанию фактора VIII и других ФСК, что затрудняет подбор нужных доз препарата и требует систематического контроля за содержанием фактора VIII в плазме больного в процессе лечения, а также необходимость его хранения и транспортировки при температуре —30—40°С. После оттаивания и согревания до температуры тела препарат должен вводиться больному внутривенно немедленно (струйно!!!) в неразбавленном виде, без чего достичь с его помощью необходимой концентрации в крови больного невозможно. Случайно оттаившие в процессе хранения и транспортировки препараты повторному замораживанию не подлежат. В силу этих особенностей криопреципитат пригоден только для болюсного, а не длительного трансфузионного введения в кровоток больного.
Достоинством криопреципитата являются простота и невысокая стоимость его получения. Неоднократно предпринимались попытки получить, с одной стороны, криопреципитат более высокой и стабильной активности, а с другой — изготовления этого препарата в сухой (лиофилизированной) форме (З.С. Барка- ган и др., 1991). Однако исследования в этом направлении пока не завершены.
Криопреципитат служит также промежуточным продуктом получения концентратов фактора VIII средней и высокой степени очистки, хотя имеются и другие способы выделения очищенного фактора VIII. В одних из этих препаратов коагуляционная часть фактора VIII (VIII:C) фигурирует в комплексе с фактором Виллебранда (AHF Kabi, Hemate-P), в связи с чем они пригодны для трансфузионной терапии как гемофилии А, так и болезни Виллебранда. В других же очищенных препаратах имеется только фактор VIII:C и они предназначены только для заместительной терапии гемофилии А.
Рекомбинантные препараты фактора VIII представлены только VIII:C компонентом, причем чаще всего не всем этим белком, а коагуляционно активными его доменами (большинство из них частично или полностью лишены В-цепи этого белка). Вместе с тем эти активные фрагменты фактора VIII сохраняют способность соединяться с содержащимся в плазме и в тромбоцитах фактором Виллебранда, в силу чего данный комплекс образуется в крови больного после введения в его кровяное русло r-YIII:C (К.Е. Hansmann et al., 1993).
Очищенные препараты фактора VIII:C, полученные из плазмы или реком- бинантно, могут применяться при гемофилии А в очень больших дозах, что делает их незаменимыми при терапии больных с тяжелыми травмами, для прикрытия больших хирургических вмешательств и для преодоления действия иммунных ингибиторов фактора VIII как у больных гемофилией, так и при самопроизвольных формах этой патологии.
При подборе доз препаратов фактора VIII руководствуются следующим.
- При гемартрозах, небольших кровотечениях, малых хирургических вмешательствах (удалении одного—двух зубов, кроме III моляра) концентрацию факторов VIII и (или) IX следует поддерживать на уровне не выше 8—10%, для чего достаточно введение 15—20 мл/кг СЗП в сутки (лучше в два приема) или 15—25 ед/кг криопреципитата в 1—2 приема.
- При тяжелых гемартрозах, больших подкожных или внутримышечных гематомах, одновременном удалении более 3 зубов, наложении аппаратов внешней фиксации (Илизарова, Волкова—Оганесяна), некоторых полостных операциях (аппендэктомия и др.) уровень фактора VIII должен поддерживаться выше 25—35%, что уже не может быть реализовано с помощью трансфузий СЗП. В этих случаях должны вводиться криопреципитат или концентраты факторов свертывания в суточной дозе 35—45 ед/кг.
- Геморрагии при больших травмах и операциях, макрогематурии, забрю- шинных гематомах, кровоизлияниях в мозг и профузных желудочно-кишечных кровотечениях требуют поддержания уровня фактора VIII в плазме выше 40—50%, а в ряде случаев — выше 60%. Для этого суточную дозу криопреципитата или концентратов фактора VIII повышают до 60—150 ед/кг. Еще более высокие дозы необходимы для преодоления ингибирующего действия на свертывание антител к фактору VIII. Во всех этих случаях предпочтение должно быть отдано очищенным концентратам фактора VIII, из которых в России разрешены для клинического применения препараты «Гемофил», «Профилат», «фактор VIII Хьюман», либо рекомбинантным препаратам этого фактора.
Частота введения антигемофильных препаратов определяется тем, насколько при каждом их введении удалось повысить концентрацию в плазме фактора VIII. Так, если концентрация была повышена до 40%, то уже через 6—8 ч она снижается в среднем до 20%, тогда как при повышении до 120%, 20%-ный уровень будет достигнут только через сутки. Иначе говоря, чем больше начальная доза препарата, тем реже могут выполняться его последующие введения. При этом следует руководствоваться показателями полужизни введенного препарата в кровотоке (см. табл. 35), а также исходным уровнем дефицитного фактора в крови больного. Высокоактивные концентраты фактора VIII, как и концентраты других ФСК, могут вводиться не только разовыми (болюсными) инъекциями, но и длительными трансфузиями, чем обеспечивается более равномерное поддержание нужной концентрации фактора в крови больного.
Следует также учитывать, что на одну и ту же дозу препарата разные больные могут отвечать неодинаковым повышением уровня фактора свертывания (даже вне зависимости от наличия и изменения титра антител к ФСК в плазме больного). Учитывая это, различие многие авторы подразделяют больных гемофилией на нормо- и гипореепондеров. Эти различия еще более возрастают
при одновременном введении больным кровезаменителей, вызывающих разбавление вводимых ФСК, что при гемофилии следует по возможности избегать. Все это диктует необходимость динамического контроля за концентрацией антигемофильных факторов в крови больных в процессе лечения.
Применяется ряд ориентировочных расчетов, необходимых для достижения нужной концентрации фактора VIII.
По данным Р.А. Рутберг и Ю.Н. Андреева (1972), Ю.Н. Андреева (1975) и других авторов, каждая единица фактора VIII, введенная на 1 кг массы тела больного, повышает концентрацию этого фактора в плазме на 1,3±0,6%. Отсюда предлагается следующий расчет необходимой дозы препарата:
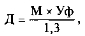
где: Д — доза криопреципитата (ед); М — масса тела больного (кг); Уф — заданный уровень фактора VIII.
Используются и другие формулы. Так, по D.Y. Mason, G.I.C. Ingram (1971) дозу препаратов антигемофилического глобулина рассчитывают по формуле:
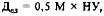
где: Д — необходимая доза (ед); М — масса тела (кг); НУ — необходимый уровень фактора в плазме больного (% или ед/100 мл).
По данным M.W. Hilgartner (1974), эта формула правильна для взрослых с массой тела более 60 кг, тогда как для больных с массой тела менее 60 кг умножать следует не на 0,5 массы, а на 0,7, а при массе тела менее 30 кг — на 1. По нашим данным, эти поправки очень важны, поскольку при использовании всегда одной и той же формулы больные с большой массой тела получают избыточную дозу препаратов фактора VIII, а с малой (дети) — недостаточную дозу, которая может не обеспечить надежного купирования и предотвращения геморрагий.
Интенсивность и продолжительность трансфузионной терапии определяются также клинической ситуацией. Так, при острых гемартрозах сроки такого лечения могут быть сокращены с 4—6 дней до 1—2 дней в случае проведения ранней пункции полости сустава, аспирации его содержимого и последующего введения в него лекарственной смеси из глюкокортикоидов пролонгированного действия, кислорода и поливинилпирролидона (А.В. Чан- цев, 1995). Существенно могут быть сокращены сроки введения концентратов фактора VIII и при ортопедической коррекции с помощью аппаратов Илизарова — после сформирования спицевых каналов, что происходит через
- 7 дней от момента наложения аппарата, угроза кровотечения из этих ходов исчезает, и постоянная трансфузионная терапия может быть прекращена и заменена лишь однократными введениями препаратов фактора VIII в дни усиления дистрации (Е.А. Рас попова, 1991).
В послеоперационном периоде препараты лучше отменять не сразу, а постепенно (через 2—4 дня), снижая их суточную дозировку.
