Физиологические и фармакологические особенности местной анестезии
Молекулы всех местных анестетиков состоят из трех основных компонентов: липофилической части, гидрофи- лического амина и средней цепи. Липофилическая часть позволяет местному анестетику проникать через жировые субстраты клетки в нервную ткань, гидрофилическая (аминная) часть обеспечивает распад молекулы и проникновение ее через интерстициальную жидкость в нерв.
Высокоэффективные анестетики имеют сбалансированные свойства. В частности, если агент имеет недостаточно выраженную гидрофилическую часть или лишен ее, то его можно применять только для аппликаций, т.е. поверхностно. Эффективность* любого анестетика зависит от многих факторов, из которых основным является КОС тканей. В норме pH тканевой жидкости составляет 7,3— 7,4; pH раствора анестетика колеблется от 3,8 до 6,5. В случае сдвига pH в кислую сторону большая часть анестетика подвергается воздействию катионов, что обеспечивает эффективность его действия. При воспалительном процессе pH ткани снижается до 6,0 или ниже, в результате чего уменьшается количество анестетика, проникающего в нерв, а катионы, находящиеся в избытке, при этом не проявляют необходимой активности. Таким образом, эффективность любого анестетика зависит от pH ткани.
Нейрофизиология. В основе местной анестезии лежат прекращение проведения импульса по чувствительным
нервным волокнам и блокада рецепторов. Анестетик, воздействуя на нервную мембрану, предотвращает ее деполяризацию, без которой невозможно проведение нервного импульса. Нервные клетки прямо или косвенно участвуют в процессах обмена и питания нервной мембраны, которая отвечает за генерирование и передачу импульса. Мембрана передает импульс от периферии к центру. Если распространение импульса прерывается, то устраняется боль. Мембрана представляет собой бимолекулярный липидный покров, расположенный между мономолекулярными слоями полипептидов. Как видно на рис. 1, она состоит из протеиновых, жировых и белковых оболочек, разделенных иенами, аксоплазмой и экстрацеллюлярной жидкостью.
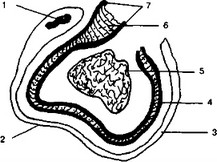
Рис. 1 Разрез нерва 1 — ядро, 2 — клетка Шванна, 3 — миелин; 4 — нервная мембрана; 5 — аксоплазма; 6 — липидный слой, 7 — протеиновая оболочка.
При метаболизме нервной мембраны осуществляется контроль концентрации различных ионов в межтканевой жидкости. Изменение ионных градиентов приводит к ее деполяризации и изменению направления распространения импульса. Ее высокая устойчивость к воздействию внешних факторов при патологических состояниях связана с нарушением прохождения через нее ионов калия, натрия, хлоридов, которые в норме обычно проникают беспрепятственно.
Нервное волокно окружено миелиновым слоем, который располагается на нерве в виде цилиндра, состоящего из леммоцитов (клетки Шванна) и защищает его от внешних воздействий. Миелин является абсорбционным барьером, и местные анестетики не всегда могут проникнуть через него. Миелиновый слой может прерываться, обнажая нервную мембрану. Эти прорывы известны под названием узлов. В этих местах растворы анестетиков легко диффундируют в нервную мембрану, вызывая блокаду нерва.
Распространение импульса. Возникающий электрический импульс представляет собой быстро изменяющийся потенциал мембраны, распространяющийся от болевой точки по типу волны деполяризации, которая называется потенциалом действия. В состоянии покоя наружная поверхность мембраны заряжена положительно, внутренняя — отрицательно. При возникновении стимула она медленно возрастает до определенного уровня, называемого порогом нервного волокна. Когда этот порог достигает критического уровня, возникает деполяризация. Если критический уровень не достигается, то импульс не возникает (иллюстрация принципа «все или ничего»). После достижения порога разность потенциалов увеличивается, а затем происходит реполяризация и потенциал мембраны возвращается к исходному уровню, наблюдающемуся в состоянии покоя. Деполяризация и реполяризация происходят по всей длине нервного волокна. Нервная мембрана, находящаяся в состоянии покоя, является барьером для ионов натрия. Во время деполяризации ион натрия двигается в мембране по натриевому каналу. Изменение потенциала приводит к выходу ионов калия («натриевый насос»). Это вызывает новый потенциал действия и уменьшение разности потенциалов по всей мембране.
Все изложенное выше можно выразить в виде резюме: согласно современным представлениям, процесс передачи возбуждения и проницаемость мембраны зависят от состояния клетки. Распространение импульса делится на три этапа: поляризацию, деполяризацию и реполяризацию. На первом этапе внутриклеточная концентрация калия превышает концентрацию натрия, что препятствует
возникновению отрицательного потенциала (потенциал покоя) на внутренней поверхности мембраны, поддерживаемого внутриклеточными анионами. Стабильно и положение ионов натрия, поскольку они не могут войти в клетку, так как вследствие поляризации мембрана в этот момент малопроницаема для натрия (рис. 2). В последующем, когда потенциал покоя понижается до соответствующей пороговой величины, увеличивается проницаемость мембраны для ионов натрия, которые под влиянием ионного и электростатического градиентов проходят внутрь клетки. В результате этого происходит деполяризация мембраны и возникает положительный потенциал действия, способствующий проведению импульса по нервной клетке (рис.З). Вслед за возбуждением наступает рефрактерный период, в котором потенциал мембраны снижается до величины потенциала покоя. В состоянии реполяризации нервная клетка подготовлена к восприятию и проведению очередного импульса (Щекунов B.C., 1976 г.).
Механизм воздействия местных анестетиков заключается в торможении распространения импульсов и изменении проницаемости мембраны для ионов натрия, вследствие чего невозможна ее деполяризация. Точно так же изменяется проницаемость мембраны для ионов калия, но в меньшей степени. Под влиянием местных анестетиков изменяется скорость распространения импуль-
|
|
|
|
|
V |
|
|
|
|
|
|
|
2 |
|
|
|
2 |
|
|
gt; |
|
|
|
|
|
Ъ,\ |
О |
|
|
° °( о *
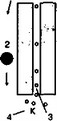
Рис 2 Нервная мембрана в состоянии покоя
- — экстрацеллюлярная
жидкость;
- — натриевый канал.
- — калиевый канал,
- — аксоплазма
Na
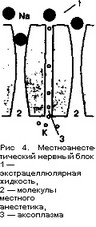
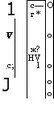
сов, и таким образом достигается пороговый потенциал. По существу феномен деполяризации связан с продвижением ионов натрия по натриевым каналам. Считается, что действие всех местных анестетиков осуществляется путем изменения проходимости натриевых каналов нервной мембраны. Лидокаин, новокаин, мепивокаин связывают рецепторы, расположенные на внешней поверхности нервной мембраны в натриевых каналах (рис. 4) (Allen G.D., 1984).

 Возникновение потенциала действия приводит к распространению возбуждения на другие участки нервного волокна, к проникновению в аксоплазму ионов натрия и выходу ионов калия («натрий-калиевый насос*). Этот процесс регулируется ионами кальция, при повышении концентрации которых во внеклеточной жидкости возрастает мембранный порог. Известно, что местноанестезирующие средства действуют как синергисты кальция.
Возникновение потенциала действия приводит к распространению возбуждения на другие участки нервного волокна, к проникновению в аксоплазму ионов натрия и выходу ионов калия («натрий-калиевый насос*). Этот процесс регулируется ионами кальция, при повышении концентрации которых во внеклеточной жидкости возрастает мембранный порог. Известно, что местноанестезирующие средства действуют как синергисты кальция.
Вследствие развития воспалительного процесса в тканях, через которые вводится местный анестетик, возникает блокада натриевого канала на внешней поверхности мембраны (рис. 5). Такой же эффект можно наблюдать при токсическом воздействии на рецепторы мембраны. Таким образом, можно выделить ряд этапов развития потенциала действия, под воздействием местных анестетиков на ткани:
- связывание рецепторов в нервной мембране;
- уменьшение проницаемости нервной мембраны для ионов натрия;
- снижение скорости деполяризации, приводящее к блокаде порогового потенциала (пороговый потенциал не возникает);
- прекращение развития потенциала действия, что приводит к блокаде импульсного сигнала в нерве.
Поскольку местный анестетик оказывает действие на мембрану нервного волокна, при инъекции происходит его диффузия через различные слои соединительной ткани.
Концентрация анестетика должна быть достаточной, чтобы он мог преодолеть узлы Раньвера. Наибольшие трудности диффузии возникают при контакте с эпиневри- ем, представляющим собой соединительную основу. Внешняя оболочка эпиневрия образует нервный «щит», надежно защищающий нерв от внешних воздействий. Примерно 5000 нервных волокон занимают площадь в
- мм. Все эти структуры действуют как барьер при движении анестетического агента к нервному волокну. Достаточная концентрация раствора анестетика позволяет ему не только проникнуть в нервное волокно, но и обеспечить его полную блокаду. С помощью современных местных анестетиков можно достичь этой цели без нарушения целости или деструкции нерва.
В настоящее время блокаду нервных волокон принято делить на три стадии:
- выключение болевой и температурной чувствительности;
- выключение тактильной;
- выключение проприоцептивной чувствительности и одновременно проводимости двигательных импульсов, т.е. наступление мышечной релаксации.
Восстановление различных видов чувствительности идет в обратном порядке: вначале появляются произвольные мышечные сокращения и проприоцептивные ощущения, затем восстанавливается протопатическая чувствительность и в последнюю очередь — эпикритическая. В том случае, если необходимо продлить блокаду с помощью повторной инъекции, новую порцию раствора анестетика подводят к нервному стволу в то время, когда начинается восстановление функции некоторых наружных волокон. Процесс идет в обратном направлении, и блокады удается достигнуть быстрее при меньшем объеме раствора анестетика и более низкой его концентрации по сравнению с начальной.
Источник: Грицук С.Ф., «Анестезия в стоматологии» 1998