Эпителиального генеза передняя доля гипофиза (синтез тропных гормонов, экспрессия гена проопиомеланокортина), перикарионы нейросекреторных нейронов гипоталамуса
(синтез рилизинг-гормонов, аргинин вазопрессина [антидиуретический гормон, АДГ], окситоцина,
нейрофизинов), гипоталамо-гипофизарный тракт (транспорт гормонов по аксонам нейросекреторных нейронов), аксо-вазальные синапсы (секреция аргинин вазопрессина и окситоцина в капилляры задней доли гипофиза, секреция рилизинг-гормонов в капилляры срединного возвышения), портальная система кровотока между срединным возвышением и передней долей гипофиза в совокупности формируют гипоталамо-гипофизарную систему (рис. 9-6).
А. Гипофиз анатомически имеет ножку и тело, гистологически подразделяется на адено- и нейрогипофиз.
- Развитие (рис. 9-7). Гипофиз образуется из двух зачатков — эктодермального и нейрогенного.
Рис. 9-6. Анатомия гипофиза [из Bloom W, Fawcelt DW, 1969]
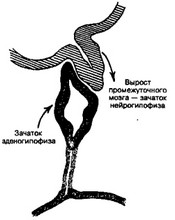
а. Карман Ратке. На 4-5-й неделе эктодермальный эпителий крыши ротовой бухты образует карман Ратке — вырост, направляющийся к мозгу. Из этого гипофизарного кармана развивается аденогипофиз (передняя, промежуточная и входящая в состав ножки гипофиза туберальная доли).
Краниофарингиома — врождённая доброкачественная дисэмбриональная опухоль, развивающаяся из эпителия гипофизарного кармана Ратке. Интракраниальная часть опухоли нередко достигает гигантских размеров. Опухоль содержит кисты и петрификаты.
б. Processus infundibularis. Навстречу карману Ратке растёт выпячивание промежуточного мозга, дающее начало нейрогипофизу (задняя доля гипофиза, нейрогипофи- зарная часть ножки гипофиза и отчасти срединное возвышение).
- Аденогипофиз (рис. 9-8) состоит из передней и промежуточной долей и туберальной части ножки гипофиза.
а. Передняя доля — эпителиальная эндокринная железа, её клетки синтезируют и секретируют различные гормоны (тропные и продукты экспрессии гена проопиомела- нокортина). Синтез и секреция тропных гормонов находятся под контролем гипотала- мических рилизинг-гормонов, поступающих в капилляры передней доли гипофиза (вторичная капиллярная сеть на рисунке 9-9).
- Гормоны. Разные эндокринные клетки передней доли синтезируют различные пептидные гормоны.
(а) Тропные гормоны. В передней доле синтезируются СТГ (соматотрофный гормон, соматотро1ф][п]ин, гормон роста), ТТГ (тиреотропный гормон, тирот- рофин), АКТГ (адренокортикотропный гормон), гонадотропины (лютеинизи- рующий гормон — ЛГ [лютропин] и фолликулостимулирующий гормон — ФСГ [фоллитропин]), пролактин.
(б) Экспрессия гена проопиомеланокортина может привести к синтезу и секреции ряда пептидов (АКТГ, 0- и у-липотропины, a-, P- и у-меланотропины, р-эндор- фин, АКТГ-подобный пептид), из которых гормональная функция установлена для АКТГ и меланотропинов; функции остальных пептидов изучены недостаточно.
Глюкокортикоиды подавляют синтез мРНК прогормона с Mr 31 кД, содержащего последовательность для АКТГ.
- Цитология. Эндокринные клетки передней доли, синтезирующие пептидные гормоны, содержат элементы гранулярной эндоплазматической сети, комплекс Гольджи, многочисленные митохондрии и секреторные гранулы различного диаметра. Клетки расположены анастомозирующими тяжами и островками между кровеносными капиллярами с фенестрированным эндотелием. В последние выводятся гормоны, из капилляров к клеткам поступают либерины и соматостатин.
- Точная идентификация аденоцитов, синтезирующих конкретные гормоны, проводится иммуноцитохимически.
- Морфологическая классификация аденоцитов основана на связывании стандартных красителей (хромофильные и хромофобные [плохо окрашивающиеся] клетки),
(а) Хромофильные клетки подразделяют по окрашиванию секреторных гранул
на базофильные и оксифильные (ацидофильные) аденоциты. Дальнейшую идентификацию проводят на полутонких срезах и в ЭМ (преимущественно по величине гранул).
- Ацидофилы синтезируют, накапливают в гранулах и секретируют соматот- рофин и пролактин.
- Соматотрофы имеют гранулы диаметром до 400 нм.
- Лактотрофы содержат мелкие (около 200 нм) гранулы. При беременности и лактации вёличина гранул может достигать 600 нм.
[IIIl Соматомаммотрофы. Продукт экспрессии имеет эффекты как СТГ, так и пролактина.
- Базофилы
- Кортикотрофы экспрессируют ген проопиомеланокортина (преимущественно АКТГ), содержат гранулы диаметром около 200 нм.
- Тиротрофы синтезируют ТТГ, содержат мелкие (около 150 нм) гранулы.
- Гонадотрофы синтезируют ФСГ и лютропин, размеры гранул варьируют от 200 до 400 нм. ФСГ и ЛГ синтезируются в разных подтипах гонадотрофов.
(б) Хромофобные клетки — гетерогенная популяция клеток.
- Камбиальный резерв.
- Дегранулировавшие клетки (оксифилы и базофилы разных типов).
- Регенерация аденоцитов, как производных эктодермального эпителия, происходит из камбиальных клеток (скорее всего, хромофобные клетки). Гипертрофия эндокринных клеток наблюдается при ряде состояний (например, при беременности синтезирующие пролактин аденоциты не только гипертрофируются, но и увеличиваются в количестве).
- Аденомы гипофиза классифицируют по преобладающему в их составе типу эндокринных клеток. Соматотрофные (соматотрофиномы) опухоли вырабатывают гормон роста, кортикотропные опухоли — АКТГ, лактотропные — пролактин.
б. Туберальная доля состоит из тяжей эпителиальных клеток, между ними расположены гипофизарные воротные вены (w. portae hypophysis на рисунке 9-9), соединяющие первичную капиллярную сеть (срединное возвышение) и вторичную капиллярную сеть (передняя доля гипбфиза). Эндокринная функция эпителиальных клеток тубе- ральной доли практически отсутствует, редко встречаются базофильные аденоциты.
в. Средняя (промежуточная) доля гипофиза у человека выражена слабо, иногда встречаются клетки с экспрессией гена проопиомеланокортина.
- Нейрогипофиз включает заднюю долю гипофиза, нейрогипофизарную часть ножки гипофиза и срединное возвышение (это образование, строго говоря, рассматривают как часть гипоталамуса). Гистологически нейрогипофиз состоит из клеток нейроглии, объединяемых термином питуициты, кровеносных сосудов, аксонов гипоталамо-гипофи- зарного тракта и их окончаний на кровеносных капиллярах (аксо-вазальные синапсы). Собственная эндокринная функция питуицитов неизвестна, они содержат многочисленные промежуточные филаменты, пигментные гранулы и липидные включения.
а. Задняя доля. Гормоны в задней доле не синтезируются, но через стенку кровеносных капилляров в кровь секретируются аргинин вазопрессин, окситоцин и нейрофи- зины, поступающие по аксонам гипоталамо-гипофизарного тракта.
б. Нейрогипофизарная часть ножки гипофиза содержит проходящие в заднюю долю аксоны гипоталамо-гипофизарного тракта.
в. Срединное возвышение. Здесь часть аксонов гипоталамо-гипофизарного тракта заканчивается аксо-вазальными синапсами на стенке кровеносных капилляров (первичная капиллярная сеть на рисунке 9-9). Через стенки этих капилляров в кровь происходит секреция рилизинг-гормонов, мишенями которых являются эндокринные клетки передней доли.
- Аксо-вазальные синапсы образованы терминальными расширениями аксонов нейросекреторных нейронов гипоталамуса, контактирующими со стенкой кровеносных капилляров срединного возвышения и задней доли гипофиза. Аксоны имеют локальные утолщения (тельца Херринга), заполненные пузырьками и гранулами с гормонами.
а. Срединное возвышение. В кровь поступают рилизинг-гормоны.
б. Задняя доля. В кровь поступают антидиуретический гормон (АДГ), окситоцин и нейрофизины.
- Портальная система кровотока состоит из первичной капиллярной сети срединного возвышения, воротных вен туберальной части аденогипофиза и вторичной капиллярной сети передней доли. Ток крови — от срединного возвышения к передней доле. Воротная система обеспечивает поступление к эндокринным клеткам передней доли синтезируемых нейросекреторными нейронами гипоталамуса рилизинг-гормонов.
Б. Нейросекреторные нейроны гипоталамуса — типичные нервные клетки. Синтезируемые в перикарионах этих нейронов рилизинг-гормоны, аргинин вазопрессин, нейрофизи- ны и окситоцин по аксонам этих нейронов в составе мембранных пузырьков транспортируются к аксо-вазальным синапсам (II А 4). Такие гормон-продуцирующие нервные клетки входят в состав многих ядер гипоталамуса, в т.ч. надзрительного (и. supraopticus) и около- желудочкового (я. paraventricularis). Частично аксоны таких нейронов заканчиваются в эпендимной выстилке III желудочка.
- Регуляция активности. Синтетическая и секреторная активность нейросекреторных нейронов находится под контролем (синаптические связи нейронов, нейромедиаторы, гормоны).
а. Вышележащие отделы мозга, замыкающие многочисленные сигналы извне и из внутренней среды организма.
б. Дофамин через его рецепторы (см. табл. 9-1).
в. Гормоны. Циклический синтез гонадолиберинов находится под контролем гормонов яичника (см. главу 15.3 В 4).
г. Суточный ритм синтеза и секреции гормонов гипоталамуса.
- Влияние на аденогипофиз (табл. 9-1).
В. Гипоталамо-гипофизарный тракт (рис. 9-8) образован аксонами нейросекреторных нейронов гипоталамуса. Синтезируемые в нейросекреторных нейронах гормоны при помощи аксонного транспорта достигают аксо-вазальных синапсов нейрогипофиза (II А 4).
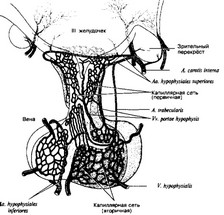
Г. Кровоснабжение гипофиза (рис. 9-9). Приносящие гипофизарные артерии в медиоба- зальном гипоталамусе (срединное возвышение) образуют первичную капиллярную сеть. Терминали аксонов нейросекреторных клеток гипоталамуса заканчиваются на этих капиллярах. Кровь из первичной капиллярной сети собирается в портальные вены, идущие по гипофизарной ножке (туберальная часть) в переднюю долю. Здесь портальные вены переходят в капилляры вторичной сети. Обогащённая гормонами передней доли кровь из вторичной капиллярной сети поступает в общую циркуляцию через выносящие вены.
Д. Гипоталамические рилизинг-гормоны. К настоящему времени выделены, изучены и получены методами генной инженерии соматостатин и несколько либеринов (соматолибе- рин, гонадолиберин, тиролиберин и кортиколиберин), ожидается появление фармакологических препаратов: активирующего гипофизарную аденилатциклазу полипептида, пролак- тиностатина, меланостатина.
Таблица 9-1. Гипоталамические нейрогормоны и их эффекты на секрецию гормонов аденогипофиза (Merck Manual of Diagnosis and Therapy, c.1056)
|
Гипоталамический нейрогормон и его структура |
Гипофизарный гормон |
Эффект |
|
|
ТРГ |
пп, 3 AK |
ТТГ, пролактин |
T |
|
Гонадолиберин |
пп, 10 AK |
Гонадотрофы, пролактин? |
T |
|
Дофамин |
биогенный амин |
Гонадотрофы, ТТГ, пролактин |
I |
|
Кортиколиберин |
пп, 41 AK |
АКТГ |
T |
|
Соматолиберин |
пп, 40-44 AK |
СТГ |
T |
|
Соматостатин |
пп, 14 AK |
СТГ, ТТГ, АКТГ |
I |
Примечания. AK — аминокислота, пп — пептидный, ТРГ — ТТГ-рилизинг гормон
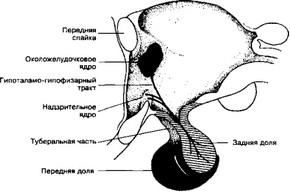
Рис. 9-8. Гипоталамо-гипофизарный тракт [из HamAW, 1974]
- Соматостатин
а. Ген соматостатина 557(182450, 3q28).
б. Структура (рис. 9-10). Циклический тетрадекапептид C76H104N18O19S2, мол. масса 1637,9.
в. Распространённость. Синтезируется многими нейронами ЦНС, 5-клетками островков Лангерханса поджелудочной железы, эндокринными клетками ЖКТ и ряда других внутренних органов.
г. Функции. Соматостатин — мощный регулятор функций эндокринной и нервной систем, ингибирует синтез и секрецию множества гормонов и секретов.
- Передняя доля гипофиза. Соматостатин подавляет синтез и секрецию гормона роста, АКТГ и тиротропина.
- Островки Лангерханса. Соматостатин подавляет секрецию инсулина и глюкагона.
Соматостатинома. При опухолях, содержащих 5-клетки, развивается выраженная гипогликемия, для снятия которой применяют аналог соматостатина — октреотид.
- Энтероэндокринная система. Соматостатин ингибирует секрецию гастрина, холецистокинина, секретина.
- Почка. Соматостатин подавляет секрецию ренина.
- Желудок. Соматостатин ингибирует желудочную секрецию. Это свойство используют при желудочных кровотечениях.
д. Рецепторы. Соматостатин реализует эффекты через связанные с G-белком мембранные высокоаффинные рецепторы. Идентифицировано 5 подтипов рецепторов соматостатина (аббревиатура — SSTR), имеющих выраженную органную специфичность распределения.
- Подтип I (SSTRl) экспрессируется в тощей кишке и желудке.
- SSTH2 характерен для почки и мозжечка.
- SSTR3 — мозг и островки Лангерханса.
- SSTR4 — развивающийся мозг, ЦНС, лёгкие
- SSTR5 — разные органы.
- Соматолиберин
а. Характеристика. Соматолиберин — пептид, содержащий 44 аминокислотных остатка, синтезируется нейросекреторными нейронами гипоталамуса, некоторыми опухолями островковых клеток поджелудочной железы (соматолибриномы).
Ala-Gly-Cys-Lys-Asn-Phe-Phe-T гр Cys-Ser-Thr-Phe-Thr-Lys
Соматостатин
5-oxoPro-His-Trp-Ser-Tyr-Gly-Leu-Arg-Pro-GlyNH2
Гонадолиберин
PyroGIu-His-ProNH2
Тиролиберин
б. Функция. Гипоталамический соматолиберин стимулирует секрецию гормона роста в передней доле гипофиза.
- Гигантизм врождённый развивается при избыточной стимуляции секретирующих СТГ аденоцитов (например, имеются сообщения о мальчиках ростом 182 см в возрасте 7 лет и 208 см в 12 лет).
- Низкорослость. Соматолиберин небезуспешно применяют в педиатрии при отставании в росте тела.
в. Рецептор соматокринина (соматолиберина) относят к семейству связанных с G-белком рецепторов типа секретина.
Мыши little (lit) имеют точечную мутацию гена для соматокрининового рецептора, их используют как модель дефектных соматотрофов гипофиза.
- Гонадолиберин (люлиберин) и пролактиностатин
а. Ген LHRH (152760, 8р21-р11.2) кодирует последовательность из 92 аминокислот для гонадолиберина и пролактиностатина.
б. Структура (рис. 9-10). Люлиберин — декапептид.
в. Мишени гонадолиберина — гонадотрофы, а пролактиностатина — лактотрофы передней доли гипофиза.
г. Функции. Гонадолиберин — ключевой нейрорегулятор репродуктивной функции, стимулирует синтез и секрецию ФСГ и ЛГ в продуцирующих гонадотрофы клетках, а пролактиностатин подавляет секрецию пролактина из лактотрофных клеток передней доли гипофиза.
- Колмена синдром (аносмия у мужчин и женщин, мужской гипогонадизм) развивается при недостаточности Гонадолиберина.
- Аналоги гонадолиберина применяют при лечении рака простаты и молочной железы.
д. Рецепторы люлиберина — трансмембранные гликопротеины, связанные с G-белком.
- Тиролиберин — трипептид (рис. 9-10), синтезируется многими нейронами ЦНС (в т.ч. нейросекреторными нейронами околожелудочкового ядра).
а. Мишени тиролиберина — тиротрофы и лактотрофы передней доли гипофиза.
- Пролактин. Тиролиберин стимулирует секрецию пролактина из лактотрофов.
- ТТГ. Тиролиберин стимулирует секрецию тиротропина из тиротрофов.
- СТГ. В патологических ситуациях тиролиберин стимулирует секрецию гормона роста из соматотрофов.
б. Рецепторы. Связывание тиролиберина с рецепторами активирует синтез инозитолтрифосфата в клетках-мишенях.
- Кортиколиберин
а. Ген CZfir(122560, 8ql3) кодирует 191-аминокислотный прогормон.
б. Структура. Кортиколиберин — пептид из 41 аминокислотного остатка.
в. Синтез. Кортиколиберин синтезируется в нейросекреторных нейронах околожелудочкового ядра гипоталамуса, плаценте, Т-лимфоцитах.
Влияние глюкокортикоидов
(а) Гипоталамус. Глюкокортикоиды подавляют синтез гипоталамического кор- тиколиберина.
(б) Плацента. Глюкокортикоиды стимулируют синтез плацентарного кортико- либерина.
г. Функции кортиколиберина многочисленны.
- Передняя доля гипофиза. Стимуляция экспрессии АКТГ и других продуктов экспрессии гена проопиомеланокортина.
- Стресс. Кортиколиберин — координатор эндокринных, нейровегетативных и поведенческих ответов в стрессовых ситуациях. Последние всегда затрагивают ось гипоталамус-гипофиз-надпочечник.
- Плацента. Плацентарные часы (см. главу 3 IX Е).
- Недостаточность кортиколиберина с вторичной адренокортикальной и тиреоид- ной недостаточностью, гипогликемией — аутосомно-рецессивное заболевание.
д. Рецепторы кортиколиберина относят к семейству связанных с G-белком рецепторов типа секретина.
е. Связывающий кортиколиберин белок содержится в крови и инактивирует этот гормон.
- Меланостатин — /,-пролил-?-лейцилглицинамид, подавляет образование меланотропинов.
- Активирующий гипофизарную аденилатциклазу полипептид (ген РАСАР, 102980, 18р11) выделен из гипоталамуса, обнаружен в ЦНС, ЖКТ, мозговой части надпочечников, яичках. Этот полипептид имеет 80% гомологии с VIP (вазоактивный интестинальный полипептид).
а. Рецепторы. Многие эндокринные клетки экспрессируют трансмембранные рецепторы активирующего гипофизарную аденилатциклазу полипептида. Несколько типов рецепторов посредством Gs активирует аденилатциклазу.
- Тип I (ген ADCYAP1, 102981, 7р14). Обнаружены в гипоталамусе, стволовой части головного мозга, гипофизе, хромаффинной ткани, поджелудочной железе, яичках.
- Тип II (ген VIPR1, 192321, Зр22) полностью соответствует обнаруженному в ЦНС рецептору типа I для VIP.
- Тип III найден в хромаффинных клетках надпочечников, связывает также VIP.
б. Эффекты. Активирующий гипофизарную аденилатциклазу полипептид стимулирует секрецию гормона роста, АКТГ, инсулина, катехоловых аминов, а также выступает в роли нейромедиатора и модулятора синаптической передачи как в ЦНС, так и на периферии.
Е. Тропные гормоны
- Гормоны роста. К этой группе относят гормон роста и хорионический соматомаммот- рофин. Пять генов этих гормонов находится в хромосоме 17 (17q22-q24).
а. Гены
- Гормон роста гипофизарный (СТГ, соматотрофин [соматотропин], соматот- рофный [соматотропный] гормон, ген hGH-N, 139250) нормально экспрессируется только в ацидофильных клетках (соматотрофы) передней доли гипофиза.
- Вариант гормона роста (ген hGH-V).
- Подобный соматотрофину гормон (ген hCS-L, 139240).
- Хорионический соматомаммотрофин (гены CS-A и CS-B), как и гены HGH- V и hCS-L, экспрессируется только в клетках синцитиотрофобласта (другими словами, гены принадлежат геному плода, на гаплоидный геном приходится 6 копий гена). Этот гормон известен также как плацентарный лактоген.
- Пролактин имеет эффекты СТГ.
б. Структура
- Нативный гормон роста — полипептидная цепь (191 аминокислотный остаток,
С990Н1529N2630299S7’ Mlt;WI' МЗССЗ 22.124).
- Рекомбинантный СТГ содержит полную последовательность нативного сома- тотропина и N-концевой метионин (C995H1637N263O301S8).
Для коррекции дефицита СТГ применяют гормон, выделенный из гипофизов трупов человека. В 1986 г. появился рекомбинантный СТГ, в настоящее время в развитых странах используют только рекомбинантный СТГ (например, генотропин). Поскольку источник рекомбинантного СТГ практически не ограничен, открываются возможности для применения СТГ при низкорослости разного генеза. Например, получены обнадёживающие результаты при лечении девочек с синдромом Тёрнера и детей с идиопати- ческой низкорослостью.
- Плацентарный лактоген содержит 190 аминокислот, мол. масса 22.125.
в. Регуляторы экспрессии
- Соматолиберин стимулирует синтез и секрецию СТГ.
- Соматостатин подавляет секрецию СТГ.
- Другие факторы. На секрецию СТГ влияют физическая нагрузка, гипогликемия, аминокислоты (например, аргинин), (i-адреноблокаторы, половые гормоны, лекарственные препараты (например, /-дофа, клонидин).
- Суточная периодичность. Пик секреции СТГ приходится на третью и четвёртую фазы сна.
г. Функции
- СТГ — анаболический гормон, стимулирующий рост всех тканей.
- Метаболические эффекты СТГ двуфазны (на примере введения экзогенного СТГ).
(а) Начальная фаза (инсулиноподобный эффект). СТГ увеличивает поглощение глюкозы мышцами и жировой тканью, а также поглощение аминокислот и синтез белка мышцами и печенью. Одновременно СТГ угнетает липолиз в жировой ткани.
(б) Отсроченная фаза (антиинсулиноподобный эффект). Через несколько часов происходят угнетение поглощения и утилизации глюкозы (содержание глюкозы в крови увеличивается) и усиление липолиза (содержание свободных жирных кислот в крови увеличивается).
- Голодание. При голодании и недостаточном питании секреция СТГ увеличивается. В сочетании с другими гормонами (кортизол, адреналин и глюкагон) СТГ адаптирует организм к этим ситуациям.
(а) Поддержание уровня глюкозы крови.
(б) Мобилизация жира как источника энергии.
- Эффекты СТГ опосредуют соматомедины.
- Наиболее очевидны эффекты СТГ на рост длинных трубчатых костей.
(а) Недостаточность СТГ
- Идиопатическая недостаточность СТГ составляет большинство случаев дефицита СТГ. Обычно развивается вследствие патологии гипоталамуса, приводящей к дефициту соматолиберина.
- Мутации гена СТГ (первичная недостаточность) приводят к развитию различных форм недостаточности гипофизарного гормона роста (гипофизарная карликовость).
- Вторичная недостаточность может развиваться как следствие иной патологии: опухоли ЦНС (краниофарингиома, глиома, пинеалома), травма, затронувшие гипоталамус или гипофиз хирургические вмешательства, облучение, инфекционная инфильтрация.
- Эмоциональная депривация в детском возрасте (скорее всего, вследствие уменьшения секреции соматолиберина).
(б) Избыток СТГ, как правило, развивается при СТГ-секретирующих аденомах. По завершении окостенения точек роста развивается акромегалия, у детей (до завершения остеогенеза) — гипофизарный гигантизм.
д. Соматомедины (инсулиноподобные факторы роста) опосредуют эффекты СТГ. По этой причине диагностика недостаточности СТГ (например, существуют формы гипофизарной карликовости при нормальном уровне СТГ) требует определения в крови не только содержания СТГ, но и соматомединов.
е. Рецептор СТГ относят- (вместе с рецептором пролактина, интерлейкинов 2, 3, 4, 6, 7 и эритропоэтина) к семейству цитокиновых рецепторов. СТГ связывается также с рецептором пролактина.
- АКТГ и меланотропины (меланокортины).
а. Полицистронный ген проопиомеланокортина POMC (176830, 2р25) содержит последовательности для АКТГ и p-липотропина. Так называемый большой АКТГ содержит а-меланотропин (аминокислотные остатки 1-13) и АКТГ-подобный пептид (18-39), а p-липотропин — у-липотропин (в свою очередь содержащий р-меланотропин) и р-эндорфин.
б. Структура
- АКТГ состоит из 39 аминокислот.
(а) а-АКТГ — первые 24 аминокислотных остатка, обеспечивающие полную биологическую активность гормона. Эта последовательность устойчива к действию протеаз.
(б) р-АКТГ — отлепляемый протеазами от АКТГ фрагмент (не входящий в состав а-АКТГ), определяет видовую специфичность гормона.
- p-Меланотропин содержит 22 аминокислотных остатка.
в. Синтез АКТГ осуществляют базофильные аденоциты (кортикотрофы) преимущественно передней и в меньшей степени промежуточной доли гипофиза, а также некоторые нейроны ЦНС. Эктопическая секреция АКТГ характерна для некоторых опухолей лёгкого, щитовидной и поджелудочной желёз.
г. Регуляторы экспрессии
- Кортиколиберин стимулирует синтез и секрецию АКТГ (вероятно, и других продуктов гена РОМО.
- Глюкокортикоиды
(а) Высокие дозы глюкокортикоидов ингибируют секрецию как АКТГ, так и кортиколиберина.
(б) Низкие концентрации глюкокортикоидов в крови стимулируют секрецию АКТГ.
- Меланостатин подавляет секрецию меланотропинов (вероятно, и АКТГ).
- Стресс (например, эмоциональный, лихорадка, острая гипогликемия, хирургические операции) стимулирует секрецию АКТГ.
- Суточный ритм. Секреция АКТГ начинает расти после засыпания и достигает пика при пробуждении.
д. Функции
- Меланокортины контролируют пигментацию кожи и слизистых оболочек (см. главу 16 Б 2 б).
- Экспрессия АКТГ и меланокортинов в значительной степени сочетаются.
- АКТГ стимулирует синтез и секрецию гормонов коры надпочечников (главным образом, глюкокортикоидов).
(а) Гиперсекреция АКТГ ведёт к гиперплазии коры надпочечников с увеличением секреции не только глюкокортикоидов, но и минералокортикоидов.
- Болезнь Иценко-Кушинга развивается вследствие повышенной секреции гипофизом АКТГ (например, при вырабатывающих АКТГ аденомах).
- Синдром Кушинга — состояние любого происхождения, характеризующееся повышенным уровнем глюкокортикоидов.
(б) Дефицит АКТГ вызывает эндокринную недостаточность надпочечников,
- Первичная недостаточность развивается при патологии коры надпочечников,
- Вторичная недостаточность — следствие патологии гипофиза (например,
мутации гена проопиомеланокортина).
Гиперпигментация кожи и слизистых оболочек характерна для первичного поражения надпочечников.
- Гиперпигментация возникает вследствие эффектов меланотропинов (этот гормон аденогипофиза, как и АКТГ, образуется из одной большой молекулы-предшественника — проопиомеланокортина, секреция же АКТГ увеличивается в ответ на снижение содержания кортизола в плазме).
- При вторичной надпочечниковой недостаточности уровень АКТГ (а значит, и меланотропинов) не увеличен; следовательно, гиперпигментация для данного состояния не характерна.
е. Рецепторы относятся к мембранным, связанным с G-белком. Идентифицировано 2 подтипа рецепторов меланокортина. Подтип 2 связывает АКТГ.
Мутации рецепторов приводят к развитию резистентности коры надпочечников к АКТГ (глюкокортикоидная недостаточность).
- Гонадотропные гормоны. К этой группе относят гипофизарные фоллитропин (ФСГ) и лютропин (ЛГ), а также хорионический гонадотропин (ХГТ) плаценты. Гонадотропные гормоны, а также тиротропин (ТТГ) — гликопротеины, состоящие из дв^х CE. а-СЕ всех 4 гормонов идентична, р-СЕ различна.
а. Фоллитропин (фолликулостимулирующий гормон, ФСГ).
- Гены. CE гликопротеина кодируют разные гены.
(а) Ген FSHA (118850, 6q21.1-q23) кодирует a-цепь. Этот же ген для ЛГ, ХГТ, ТТГ именуется LHA, CGA, TSHA соответственно.
(б) Ген FSHB (136530, 11 pi 3) кодирует специфичную для ФСГ (5-цепь.
- Протяжённая делеция, включающая ген FSHB, приводит к развитию WAGR- синдрома.
- Сдвиг рамки Кодонов 61-86 вследствие замены первого нуклеотида и делеции второго и третьего кодонов 61 GTG ([GTG, val] -»[GAG, glu]) ведёт к экспрессии дефектного ФСГ (невозможность связывания с рецептором ФСГ). У женщины с этим генным дефектом (р) отмечены первичная аменорея и отсутствие овуляции. Заместительное введение нормального ФСГ компенсировало патологию и привело к беременности.
- Структура
(а) а-СЕ 4 тропных гормонов (ФСГ, ЛГ, ХГТ, ТТГ) идентична, Mr — 14000.
(б) р-СЕ ФСГ, ЛГ, ХГТ, ТТГ, Mr около 17000.
- Регуляторы экспрессии
(а) Гонадолиберин стимулирует синтез и секрецию ФСГ и ЛГ в базофилах (гонадотрофы) передней доли гипофиза.
(б) а Ингибин — пептидный гормон, вырабатываемый зернистыми клетками фолликулов яичника и клетками Сертдли яичка, — подавляет секрецию ФСГ, взаимодействуя с мембранными рецепторами типа II активина.
(в) Активины — пептидные гормоны, вырабатываемые зернистыми клетками фолликулов яичника и в плаценте, — стимулируют секрецию ФСГ in vitro. Значение активинов для регуляции овариального цикла пока находится под вопросом.
- Функции
(а) Женщины. ФСГ, как и ЛГ, существенно важен для регуляции овариального цикла (см. главу 15.3 В 4).
(б) Мужчины. Мишени ФСГ — клетки Сертдли (регуляция сперматогенеза).
- Рецептор ФСГ — трансмембранный гликопротеин, связанный с G-белком.
б. Лютропин (лютеинизирующий гормон, ЛГ).
- Гены. CE гликопротеина ЛГ кодируют разные гены.
(а) Ген LHA (118850, 6q21.1-q23) кодирует а-цепь.
(б) Ген LHB (152780, 19q 13.32) кодирует специфичную для ЛГ р-цепь.
Мутации. Известно несколько мутаций гена LHB. Последствия для носителей мутантного гена самые различные (разные формы гилогонадизма, гермафродитизма,
евнухоидизм), что определяется не в последнюю очередь кариотипом носителя. Как правило, молекула ЛГ иммунологически активна, биологически не функциональна.
- Структура
(а) а-СЕ 4 тройных гормонов (ЛГ, ФСГ, ХГТ, ТТГ) идентична, M 14000.
(б) р-СЕ с Mr 17000.
- Гонадолиберин стимулирует синтез и секрецию ЛГ в ЛГ-гонадотрофах.
- Функции
(а) Женщины. ЛГ — стимулятор эндокринной функции яичников (подробнее см. главу 15.3 В 4).
(б) Мужчины. ЛГ (стимулирующий интерстициальные клетки гормон) в клетках Лёйдига яичек стимулирует синтез тестостерона.
- Рецептор ЛГ и ХГТ — трансмембранный гликопротеин, связанный с G-белком, — кодируется геном LHCGR (152790, 2р21). He исключено наличие в Х-хромосоме второго гена для клеток Лёйдига.
(а) Гипоплазия клеток Лёйдига — следствие нескольких известных мутаций гена.
(б) Преждевременное половое созревание мальчиков — результат мутаций кодонов 1624-1741 экзона 11.
- Преждевременный пубертат. Преждевременное изосексуальное половое созревание: девочки — менархе (первое менструальное кровотечение) до 8,5 лет, мальчики — маскулинизация до 10 лет. Причины далеко не всегда ясны, но в любом случае происходит увеличение секреции гипофизарных гонадотропинов.
- Недостаточность гонадотропинов приводит, как правило, к гипогонадотроф- ному гипогонадизму. Причины недостаточности гонадотрофов многочисленны.
(а) Гипопитуитаризм (пангипопитуитаризм).
(б) Нервно-психическая анорексия.
(в) Синдром Кдлмена.
(г) Синдром Прадер-Вшми.
в. Хорионический гонадотропин (ген CGA для а-СЕ ХГТ и ген CGB для р-СЕ ХГТ [118860, 19ql3.32]) — гликопротеин, синтезируемый клетками трофобласта с 10-12-го дня эмбриогенеза. При беременности ХГТ взаимодействует с клетками жёлтого тела (синтез и секреция прогестерона).
Саркома Капоши. ХГТ лизирует клетки этой опухоли (скорее всего, механизмом апоптоза), но не клетки нормального эндотелия.
- Тиротропин (тиреотропный гормон, ТТГ).
а. Гены
- Ген TSHA (118850, 6q21.1-q23) кодирует а-цепь.
- Ген TSHB (152780, 1р13) кодирует специфичную для ТТГ (5-цепь.
б. Структура
- а-СЕ 4 тропных гормонов (ТТГ, ЛГ, ФСГ, ХГТ) идентична, Mr 14000.
- р-СЕ с Mr 17000.
в. Синтез ТТГ происходит в базофильных клетках (тиротрофы) передней доли гипофиза.
г. Регуляторы экспрессии
- Соматостатин подавляет секрецию ТТГ.
Изолированная недостаточность ТТГ встречается крайне редко; как правило, выражена при гипопитуитаризме или пангипопитуитаризме. В частности, по этой причине при дефиците СТГ необходимо определить содержание T4 в крови.
- Тиролиберин стимулирует синтез и секрецию ТТГ.
- Гормоны щитовидной железы (T3 и T4), циркулирующие в крови, регулируют секрецию ТТГ по принципу отрицательной обратной связи.
(а) Увеличение содержания свободных T4 и T3 подавляет секрецию ТТГ.
(б) Уменьшение содержания свободных T4 и T3 стимулирует секрецию тиротропина.
д. Функции. Тиротропин стимулирует дифференцировку эпителиальных клеток щитовидной железы (кроме т.н. светлых клеток, синтезирующих тирокальцитонин) и их функциональное состояние (включая синтез тироглобулина и секрецию T3 и T4). Вторичный гипотиреоидизм развивается при дефиците ТТГ.
е. Рецептор ТТГ
- Ген TSHR (*275200, 14q31) кодирует трансмембранный гликопротеин, связанный с G-белком.
- Связывание аутоантител. Внеклеточный домен рецептора ТТГ имеет участки связывания с т.н. стимулирующими щитовидную железу Ig (в т.ч. аутоантиген системной красной волчанки [локус 22qll-ql3]).
- Экспрессия гена происходит в фолликулярных клетках щитовидной железы, а также в ретробульбарных тканях, что объясняет офтальмопатии при болезни Грейвса.
- Мутации гена многочисленны, их последствия — синдромы резистентности щитовидной железы к эффектам ТТГ. Эндокринная функция щитовидной железы при этих синдромах может быть увеличена (гипертиреоидизм), уменьшена (гипотиреоидизм) или нормальна (эутиреоидизм).
- Пролактин
а. Ген PRL (176760, 6р22.2-р21.3) кодирует полипептид, имеющий сходство аминокислотных последовательностей с СТГ и хорионическим соматомаммотрофином (плацентарный лактоген).
б. Синтез пролактина происходит в ацидофильных аденоцитах (лактотрофы) передней доли гипофиза. Количество лактотрофов составляет не менее трети всех эндокринных клеток аденогипофиза. При беременно
