Гемолитические анемии, связанные с недостаточностью активности ферментов глутатионовой системы
Глутатионовый путь защищает эритроцитарные мембраны и гемоглобин от повреждения перекисями. В эритроцитах в силу их специфической функции содержится большое количество молекул железа и кислорода. При окислении двухвалентного железа кислородом образуются свободные радикалы, которые способны инициировать цепи окисления: Fe2+ + 02 + Н' —gt; Fe3+ + Н02\ Токсический эффект в клетке оказывают свободные Ге2т-ионы, которые способны вызывать реакции инициации образования свободных радикалов, индуцировать перекисное окисление липидов и образование активного гидроксильного иона (*ОН). Кислород непосредственно участвует в образовании перекисей и радикалов (Н202, ЧЭН, R', RO', R()2’, где R-радикал длинноцепочечной жирной кислоты), которые вызывают окисление белков мембран и увеличение проницаемости липидного слоя мембран для Н+, Са2+ и других ионов и метаболитов. В результате эритроциты гемолизируются.
Восстановление гидроперекисей (ROOH) до спиртов (ROH) могут осуществлять нуклеофильные соединения, в эритроцитах это глутатион. Для защиты от активных Fe2+ и радикалов кислорода в эритроцитах постоянно в процессе пентозофосфатного пути расходуется энергия на образование НАДФН, который служит источником поддержания высокой концентрации восстановленной формы глутатиона (Г-SH), используемого для удаления перекисей и радикалов (рис. 86).
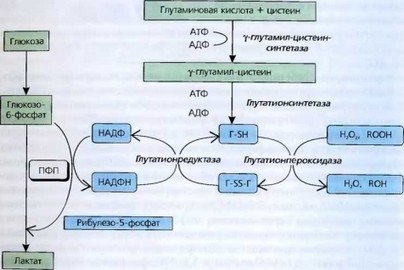
Рис. 86. Сопряжение пентозофосфатного и глутатионового путей. Г-SH - восстановленная форма глутатиона; f-SS-Г - окисленная форма глутатиона; ROOH - гидроперекись; ROH - спирт
Таким образом, для удаления токсичных гидроперекисей и радикалов в эритроците не только должен активно функционировать пентозофосфатный путь образования НАДФН, но и происходить постоянно синтез глутатиона. В синтезе глутатиона используются 2 фермента: глутатионредуктаза и глутатионсинтетаза. При дефиците этих ферментов в клинике отмечаются признаки гемолитической анемии.
Метаболизм пуринов и пиримидинов включает 3 фермента, изменение активности которых ведет к гемолитической анемии. Аденозинтрифосфа- таза участвует в обеспечении работы Na-, К-АТФ-азы или Na-mcoca на эритроцитарной мембране. Аденозиндезаминаза превращает АТФ, АДФ и АМФ в инозин после дефосфорилирования. При редкой врожденной ауто- сомно-доминантной гемолитической анемии активность фермента повышена в 35-70 раз, происходит разрушение АТФ, не хватает энергии для удаления Na из эритроцитов, что приводит к гемолизу. Пиримидин-5 ’-нукпеотидаза участвует в катаболизме рибосомальной РНК, при снижении ее активности наступает агрегация РНК, которая выявляется в виде базофильной зернистости в эритроцитах. Агрегация РНК в ретикулоцитах ведет к снижению эластичности мембраны эритроцитов и их гемолизу. Гемолитическая анемия сопровождается спленомегалией.
Дефицит пири ми дин-5’-нуклеотидазы может быть вызван тяжелым отравлением свинцом, имеет место при р-талассемии.
Ферментами фосфолипидного метаболизма эритроцитарной мембраны являются лецитин-холестерин-ацилтра! юфераза (ЛХАТ) и лизолецитин-ацил- трансфераза (ЛАТ), они поддерживают оптимальное соотношение лизолеци- тина с лецитином на внешней стороне эритроцитарной мембраны. Дефицит этих ферментов приводит к морфологическим изменениям эритроцитов (мишеневидные эритроциты) и к умеренной гемолитической анемии.
Метгемоглобинредуктаза ши НАДН-зависимая метгемоглобинредук- таза (диафораза) и цитохром-b5-редуктаза превращают метгемоглобин в гемоглобин (рис. 87). Метгемоглобин - производное гемоглобина, в котором Fe2+ переходит в Fe3+.
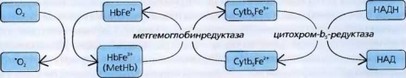
Рис. 87. Образование и удаление метгемоглобина
При обмене в эритроцитах образуется немного метгемоглобина, который восстанавливается обратимо в гемоглобин под воздействием фермента метгемоглобинредуктазы. В крови метгемоглобин не превышает 2% общего содержания гемоглобина. Врожденный дефицит фермента метгемоглобинредуктазы сопровождается увеличением в крови MetHb, что нарушает доставку кислорода к тканям и вызывает развитие цианоза. Повреждение только в эритроцитах не ведет к тяжелым гемолитическим кризам. Однако недостаточность цитохром-Ь5-редуктазы может быть генерализованным заболеванием, затрагивающим большинство тканей организма, при этом развивается прогрессирующая энцефалопатия.
Восстановление гидроперекисей (ROOH) до спиртов (ROH) могут осуществлять нуклеофильные соединения, в эритроцитах это глутатион. Для защиты от активных Fe2+ и радикалов кислорода в эритроцитах постоянно в процессе пентозофосфатного пути расходуется энергия на образование НАДФН, который служит источником поддержания высокой концентрации восстановленной формы глутатиона (Г-SH), используемого для удаления перекисей и радикалов (рис. 86).

Рис. 86. Сопряжение пентозофосфатного и глутатионового путей. Г-SH - восстановленная форма глутатиона; f-SS-Г - окисленная форма глутатиона; ROOH - гидроперекись; ROH - спирт
Таким образом, для удаления токсичных гидроперекисей и радикалов в эритроците не только должен активно функционировать пентозофосфатный путь образования НАДФН, но и происходить постоянно синтез глутатиона. В синтезе глутатиона используются 2 фермента: глутатионредуктаза и глутатионсинтетаза. При дефиците этих ферментов в клинике отмечаются признаки гемолитической анемии.
Метаболизм пуринов и пиримидинов включает 3 фермента, изменение активности которых ведет к гемолитической анемии. Аденозинтрифосфа- таза участвует в обеспечении работы Na-, К-АТФ-азы или Na-mcoca на эритроцитарной мембране. Аденозиндезаминаза превращает АТФ, АДФ и АМФ в инозин после дефосфорилирования. При редкой врожденной ауто- сомно-доминантной гемолитической анемии активность фермента повышена в 35-70 раз, происходит разрушение АТФ, не хватает энергии для удаления Na из эритроцитов, что приводит к гемолизу. Пиримидин-5 ’-нукпеотидаза участвует в катаболизме рибосомальной РНК, при снижении ее активности наступает агрегация РНК, которая выявляется в виде базофильной зернистости в эритроцитах. Агрегация РНК в ретикулоцитах ведет к снижению эластичности мембраны эритроцитов и их гемолизу. Гемолитическая анемия сопровождается спленомегалией.
Дефицит пири ми дин-5’-нуклеотидазы может быть вызван тяжелым отравлением свинцом, имеет место при р-талассемии.
Ферментами фосфолипидного метаболизма эритроцитарной мембраны являются лецитин-холестерин-ацилтра! юфераза (ЛХАТ) и лизолецитин-ацил- трансфераза (ЛАТ), они поддерживают оптимальное соотношение лизолеци- тина с лецитином на внешней стороне эритроцитарной мембраны. Дефицит этих ферментов приводит к морфологическим изменениям эритроцитов (мишеневидные эритроциты) и к умеренной гемолитической анемии.
Метгемоглобинредуктаза ши НАДН-зависимая метгемоглобинредук- таза (диафораза) и цитохром-b5-редуктаза превращают метгемоглобин в гемоглобин (рис. 87). Метгемоглобин - производное гемоглобина, в котором Fe2+ переходит в Fe3+.

Рис. 87. Образование и удаление метгемоглобина
При обмене в эритроцитах образуется немного метгемоглобина, который восстанавливается обратимо в гемоглобин под воздействием фермента метгемоглобинредуктазы. В крови метгемоглобин не превышает 2% общего содержания гемоглобина. Врожденный дефицит фермента метгемоглобинредуктазы сопровождается увеличением в крови MetHb, что нарушает доставку кислорода к тканям и вызывает развитие цианоза. Повреждение только в эритроцитах не ведет к тяжелым гемолитическим кризам. Однако недостаточность цитохром-Ь5-редуктазы может быть генерализованным заболеванием, затрагивающим большинство тканей организма, при этом развивается прогрессирующая энцефалопатия.
Источник: Долгов В.В., Луговская С.А., Морозова В.Т., Почтарь М.Е., «Лабораторная диагностика анемий» 2009
А так же в разделе « Гемолитические анемии, связанные с недостаточностью активности ферментов глутатионовой системы »
- Гемолитические анемии, связанные с нарушением структуры мембраны эритроцитов (эритроцитопатии)
- Микросфероцитарная гемолитическая анемия (микросфероцитоз, болезнь Минковского-Шоффара)
- Овалоцитарная гемолитическая анемия (овалоклеточная, наследственный овалоцитоз, эллиптоцитоз)
- Гемолитичесние анемии, обусловленные нарушением струнтуры липидов мембраны эритроцитов (анантоцитоз)
- Гемолитические анемии, обусловленные дефицитом ферментов эритроцитов (эритроцитарные энзимопатии)
- Гемолитические анемии, связанные с недостаточностью активности ферментов гликолиза
- Гемолитические анемии, связанные с недостаточностью активности ферментов пентозофосфатного шунта