Дискретный плазмаферез у детей с тяжелыми формами гнойно-септических заболеваний
Одной из задач настоящего исследования была разработка методики дискретного плазмафереза у детей с тяжелыми формами гнойно-септических заболеваний.
Оснащение для проведения дискретного плазмафереза
- Рефрижераторная центрифуга типа К-70 или ЦЛ-4000, способная давать более 2000 об/мин и вмещать контейнеры емкостью 300—500 мл.
- Полимерные контейнеры типа "Гемакон-500", "Компо- пласт-300" или другие с гемоконсервантом.
- Одноразовые системы для переливания крови.
- Для контроля за гемодинамикой во время дискретного плазмафереза необходимы аппарат для измерения артериального давления, аппарат для измерения центрального венозного давления, секундомер.
- Для осуществления дискретного плазмафереза нужны ги- периммунные плазмы (антистафилококковая, антисинегной- ная, антипротеиновая или ассоциированная), нативная донорская плазма, плазмозаменители (альбумин, протеин, гемодез, реополиглюкин и др.), свежецитратная кровь, раствор гепарина, 0,9 % раствор хлорида натрия, 10 % раствор хлорида кальция.
- На случай возникновения осложнений необходимо иметь протамина сульфат, адреналин, сердечные гликозиды, антигистаминные препараты, седативные средства, а также другие медикаменты для проведения противошоковых мероприятий.
Дискретный плазмаферез должен проводиться в операционной или процедурном кабинете бригадой: хирургом или реаниматологом и медицинской сестрой.
Показания для дискретного плазмафереза
- Инфекционно-токсический шок.
- Выраженная эндогенная интоксикация при перитоните, остром гематогенном остеомиелите, острой гнойно-деструктивной пневмонии, сепсисе и других гнойно-септических процессах.
- Генерализация и прогрессирование гнойно-септического процесса.
- Высокая концентрация токсических факторов в крови больных с гнойно-септическими заболеваниями.
- Неэффективность традиционных методов лечения гнойно-септических заболеваний.
- Устойчивость к антибактериальным препаратам патогенной микрофлоры или же непереносимость антибиотиков у больных с гнойно-септическими заболеваниями.
Дискретный плазмаферез (ДПА) у детей с тяжелыми формами ГСЗ, сопровождающимися выраженной эндогенной интоксикацией, септическим шоком, прогрессированием гнойно-инфекционного процесса применяли в комплексе интенсивной терапии в 1—3-й сутки после оперативного вмешательства либо при поступлении больных в клинику, если необходимое оперативное пособие было выполнено в больнице по месту жительства. У 2 больных ДПА применили для ликвидации тяжелой эндогенной интоксикации в предоперационном периоде.
Методика дискретного плазмафереза у детей с тяжелыми формами гнойно-септических заболеваний. Перед началом Д ПА производилась катетеризация подключичной вены по Сель- дингеру, определялись основные показатели гемодинамики: ЧСС, артериальное давление, ЦВД.
ЧСС только у 6 больных была в пределах нормальных возрастных значений. У остальных отмечалась тахикардия, причем у 60 % больных ЧСС превышала возрастную норму на 50—90 %, артериальное давление у большинства больных было в пределах возрастных значений и только у 10 больных оно было снижено до 85,7±0,8 % и у 16 — повышено до 115,4±1,5 %.
ЦВД у 41 больного было от 5 до 60 мм водн. ст., у 38 — 60— 100 мм водн. ст. и у 14 детей ЦВД превышало 100 мм водн. ст. Высокое ЦВД объясняется массивной инфузионной терапией, проводившейся у данных пациентов до поступления в клинику и до ДПА.
У 20 больных всех возрастных групп определен ОЦК радионуклидным методом с помощью альбумина, меченного 1311. Изучение ОЦК было необходимо для определения объема экс- фузии крови, плазмоэкстракции и плазмозамещения.
У обследованных детей ОЦК был в пределах возрастной нормы (10 больных) или повышенным (10 больных), что так же, как и повышенные значения ЦВД, объясняется проводившейся инфузионной терапией.
Показатели ЧСС и артериального давления в этих группах детей практически не отличаются от ЦВД детей с исходным ОЦК 125,9±1,8 %.
В связи с тем что при ДПА производится эксфузия крови у больного, для предотвращения гиповолемии во время сеанса ДПА необходимо перед ДПА иметь ОЦК не менее 100 %. При невозможности определить ОЦК и отсутствии клиники сердечной недостаточности можно ориентироваться на показатели ЧСС, артериального давления и ЦВД.
В тех случаях, когда ЦВД ниже 60 мм водн. ст., артериальное давление меньше, чем 90 % от возрастной нормы, ЧСС превышает нормальные значения на 85—90 %, показана внутривенная инфузионная подготовка, направленная на коррекцию ОЦК, повышение ЦВД и артериального давления и стабилизацию ЧСС.
Подготовка к ДПА проведена у 38 больных, ЦВД которых было пониженным (в среднем до 28,2±1,6 мм водн. ст.) при ЧСС 148,3±6,9 % и артериальном давлении 92,6±0,9 %.
Инфузионная среда для подготовки к ДПА состояла из 10 % раствора альбумина, гемодеза и крови (при гемоглобине крови ниже 80—90 г/л). Общий объем внутривенно вводимых плаз- мозаменителей и крови составил 10—15 мл/кг массы тела. Подготовку к ДПА заканчивали при повышении артериального давления до нормальных или несколько повышенных значений и повышении ЦВД выше 60—70 мм водн. ст.
После подготовки артериальное давление повысилось до 102,6±1,4 %, ЦВД — до 104,5+4,0 мм водн. ст., ЧСС уменьшилась незначительно. Обычно на подготовку к ДПА требуется не более 30—40 мин.
Непосредственно перед ДПА ЧСС у всех больных в среднем составила 148,9±4,0 %, артериальное давление — 101,7±1,6 %, ЦВД — 89,6±4,7 мм водн. ст.
Исходные показатели гемодинамики у детей различных возрастных групп отражены в табл. 2.1. ЧСС у детей до 3 лет составила в среднем 138,2+7,1 %, а у детей старше 3 лет тахикардия была более выраженной и колебалась в пределах 150— 160 % от возрастной нормы. Артериальное давление у детей до 11-летнего возраста в среднем составило 103—106 %, а у более старших детей оно было несколько пониженным — 95,3±2,2 %. ЦВД у детей различных возрастных групп существенно не отличалось.
Таким образом, дискретный плазмаферез начинали на фоне выраженной тахикардии, обусловленной тяжелой гнойно-инфекционной патологией, при нормальных значениях артериального давления и ЦВД выше 70 мм водн. ст.
Таблица 2.1
Изменение гемодинамики у детей различных возрастных групп во время ДПА
|
Возраст |
Всего боль ных |
Время исследования |
чес, % |
АД,Ж |
ЦВД, мм водн. ст. |
|
От 6 мес |
30 |
Перед 1-й экс- |
138,2+7,0 |
103,0+1,9 |
106,1+2,1 |
|
до 3 лет |
|
фузией |
|
|
|
|
|
|
После 1-й экс |
144,5+6,0 |
91,2+1,8 |
36,0+3,0 |
|
|
|
фузии |
|
|
|
|
|
|
После 1-й ин- |
136,6+6,1 |
99,0+1,9 |
94,4+2,1 |
|
|
|
фузии |
|
|
|
|
|
|
После ДПА |
124,7+5,2 |
101,4+1,5 |
95,0±1,5 |
|
От 3 до |
12 |
То же |
158,2+8,1 |
106,2±4,9 |
78,7+8,7 |
|
7 лет |
|
|
165,8+8,7 |
87,6±3,0 |
21,9+4,0 |
|
|
|
|
151,8+8,7 |
100,1+3,7 |
71,9+6,2 |
|
|
|
|
133,1+7,4 |
105,6±2,5 |
71,2+4,9 |
|
От 7 до |
24 |
» » |
150,9+6,2 |
105,1+2,6 |
93,4±5,3 |
|
11 лет |
|
|
154,8+5,3 |
94,1+2,1 |
35,5±3,5 |
|
|
|
|
147,2+5,7 |
98,3+2,2 |
82,2+3,5 |
|
|
|
|
140,8+4,4 |
102,1+2,2 |
78,3+3,4 |
|
Старше |
30 , |
» » |
150,9+4,5 |
95,3±2,2 |
74,6±5,9 |
|
И лет |
|
|
147,2+4,7 |
89,7+1,5 |
31,6+2,2 |
|
|
|
|
141,2+4,3 |
95,4+1,9 |
87,2+3,0 |
|
|
|
|
133,8+3,7 |
99,5±2,0 |
80,0±3,0 |
После коррекции ОЦК, ЦВД, артериального давления и ЧСС внутривенно вводили гепарин— 100 ЕД/кг массы тела, антигистаминные препараты в возрастной дозировке, при психомоторном возбуждении ребенка — седативные средства (седуксен или реланиум). После этого начинали эксфузию крови больного через катетер подключичной вены в полимерный контейнер типа "Гемакон-500", "Компопласт-300" с гемоконсервантом через магистраль контейнера. Объем эксфузии зависит от возраста больного и показателей гемодинамики, прежде всего от ЦВД и артериального давления.
В процессе эксфузии постоянно контролировали ЧСС, ар. териальное давление и ЦВД, не допуская снижения артериального давления до критического уровня (70/40 мм рт.ст.), увеличения ЧСС выше 10—15 % от исходных значений и снижения ЦВД ниже 20—25 мм водн. ст. Полученные данные гемодинамики показали, что при эксфузии в среднем 12—18 % от ОЦК (возрастной нормы) артериальное давление снижалось на 10,8 %, ЧСС увеличивалась на 4,3 %, а ЦВД снижалось до 32,3+1,7 мм водн. ст.
Изучение показателей гемодинамики в зависимости от ЦВД показало, что у 30 больных при ЦВД выше 100 мм водн. ст. возможна эксфузия 17—20 % ОЦК (в среднем — 18,4+1,0 %), при этом ЦВД снижалось со 124,1+7,4 до 43,3±4,1 мм водн. ст., ЧСС возрастала на 8,8 %, а артериальное давление снижалось на 15,6 %.
У 46 больных с исходным ЦВД 100 мм водн. ст. (в среднем — 74,8±3,6 мм водн. ст.) при эксфузии 12,8—0,4 % ОЦК артериальное давление снижалось на 8,8 %, ЧСС возрастала на 10— 15 %, а ЦВД снижалось до 27,6±2,0 мм водн. ст.
Характер изменений показателей гемодинамики у детей всех возрастных групп был однозначным: после эксфузии 10—20 % ОЦК (в зависимости от исходного ЦВД) отмечено снижение артериального давления примерно на 6—15 %, возрастание ЧСС на 5—8 % и снижение ЦВД до 21—36 мм водн. ст.
При расчете объемов эксфузии и инфузии при ДПА у детей следует ориентироваться на данные Russel, приведенные в табл. 2.2.
Полученные нами результаты исследований позволили определить объем одной эксфузии крови у детей в зависимости от возраста (табл. 2.3).
Таблица 2.2
Абсолютные и относительные количества крови и плазмы у детей различных возрастов (Russel)
|
Возраст |
Относительное количество, мл |
Относительная величина от массы тела, % |
||
|
кровь |
плазма |
кровь |
плазма |
|
|
4-6 мес |
487 |
273 |
8 |
4,8 |
|
7-9 мес |
574 |
338 |
8,2 |
4,8 |
|
До 12 мес |
623 |
379 |
'7,3 |
4,4 |
|
2 года |
857 |
502 |
8,1 |
4,7 |
|
3 года |
956 |
547 |
8,5 |
4,8 |
|
4 года |
1090 |
625 |
8,0 |
4,6 |
|
5 лет |
1316 |
732 |
9,0 |
5,1 |
|
6 лет |
1500 |
855 |
8,3 |
4,8 |
|
7 лет |
1535 |
913 |
8,4 |
5,0 |
|
8 лет |
1902 |
1083 |
8,8 |
5,0 |
|
9 лет |
1898 |
1092 |
8,0 |
4,6 |
|
10 лет |
2288 |
1292 |
9,1 |
5,1 |
|
11 лет |
2317 |
1297 |
8,2 |
4,6 |
|
12 лет |
2682 |
1485 |
9,1 |
5,1 |
|
13 лет |
2937 |
1304 |
1,6 |
4,2 |
|
14 лет |
3624 |
2186 |
8,5 |
5,1 |
Примерные объемы эксфузии крови, плазмоэкстракции и плазмозаме- щения при ДПА в зависимости от возраста больных
|
Возраст |
Объем одной эксфузии крови, мл |
Количество эксфузии |
Общий объем плазмоэкстракции и плазмозамещения, мл |
|
6—9 мес |
70-85 |
4-5 |
300-350 |
|
9—12 мес |
90-120 |
3-4 |
350-400 |
|
1—3 года |
120-150 |
3-4 |
400-550 |
|
3—5 лет |
150-229 |
3-4 |
550-700 |
|
5—7 лет |
125-180 |
3-4 |
700-900 |
|
7-10 лет |
200-300 |
4 |
900-1200 |
|
10-13 лет |
300 |
4-5 |
1200-1500 |
|
13-15 лет |
300-400 |
4 |
1500 |
После эксфузии контейнер с кровью больного отсоединяют от катетера и подключичной вены ив ту же вену через одноразовую систему для переливания крови производят инфузию растворов. Состав инфузионной среды зависит прежде всего от исходных показателей гемоглобина и эритроцитов. В тех случаях, когда исходный гемоглобин ниже 100 г/л, количество эритроцитов ниже 3,3-1012/л, внутривенно вводят свежецитрат- ную кровь — 8—12 мл/кг массы тела (в зависимости от степени анемии) и 10 % раствор альбумина или другие плазмозамени- тели.
В тех случаях, когда исходный гемоглобин в пределах 100— 120 г/л, инфузионная среда для первой инфузии состоит на 30—50 % объема из свежецитратной крови и на 70—50 % — из раствора альбумина или плазмозаменителей.
При исходном уровне гемоглобина выше 120 г/л, количестве эритроцитов более 4,0-1012/л состав растворов для первой инфузии состоит только из раствора альбумина и плазмозаменителей.
Для первой инфузии лучше пользоваться таким плазмоза- менителем, как 10 % раствор альбумина, так как внутривенное введение альбумина способствует выходу токсинов вместе с жидкостью из интерстициального пространства в сосудистое русло и стимулирует лимфоотток [Ломаченко И.Н., 1985]. Это приводит к накоплению токсичных продуктов в сосудистом русле, которые из него выводятся во время сеанса ДПА, тем самым усиливается детоксикационное действие ДПА.
Объем внутривенно вводимой жидкости после первой эксфузии крови зависит от объема удаленной крови, показателей гемодинамики, прежде всего ЦВД и артериального давления.
При исходном ЦВД ниже 100 мм водн. ст. объем первой инфузии равен объему эксфузии крови. При исходном ЦВД выше 100 мм водн. ст. объем инфузии уменьшается для того, чтобы после инфузии не было значительного превышения ЦВД, а артериальное давление и ЧСС возвратились к исходным значениям.
Уменьшение объема инфузии до 12—15 % ОЦК, в . среднем — 13,5±1,0 % (объем инфузии составляет 80—85 % от объема эксфузии крови), привело к тому, что ЦВД после инфузии составило 92,9±3,0 мм водн. ст., артериальное давление —104,5±2,2 %, ЧСС— 141,3±6,0%. В среднем у всех больных после первой инфузии ЧСС составила 142,9±2,8 %, артериальное давление — 97,9±0,8 %, ЦВД - 85,7±2,5 мм водн. ст.
Аналогичные изменения показателей гемодинамики после первой инфузии произошли у детей всех возрастных групп (см. табл. 2.1).
Закончив первую инфузию, сразу же начинают вторую экс- фузию крови больного в объеме 12—16 % от ОЦК в полимерный контейнер с консервантом.
Одновременно с первой инфузией контейнер с кровью больного (первый эксфузат) помещают в рефрижераторную центрифугу и центрифугируют при 2000 об/мин в течение 10 мин, после чего из контейнера плазму удаляют через магистраль контейнера, а эритроцитная масса с сохраненной лейкоцитарной пленкой остается в контейнере.
Для удаления токсинов с мембран эритроцитов применяют двукратное "отмывание" эритроцитов 0,9 % раствором хлорида натрия. Для этого в контейнер с эритроцитной массой добавляют равное количество 0,9 % раствора хлорида натрия, перемешивают и контейнер вновь центрифугируют при 2000 об/мин в течение 5 мин. После центрифугирования жидкость над эритроцитной массой удаляют через магистраль контейнера и к глобулярному объему вновь добавляет равное количество
- 9 % раствора хлорида натрия, центрифугирование повторяют при тех же условиях. После удаления жидкости из контейнера к эритроцитной массе добавляют 20—50 мл 0,9 % раствора хлорида натрия (в зависимости от эритроцитной массы) и эритроцитную массу реинфузируют больному после второй эксфузии крови.
Эксфузию крови у больного с последующим "отмыванием" эритроцитов производят до 5 раз, при этом, начиная со второй инфузии, в сосудистое русло вводят эритроцитную массу больного после "отмывания" и плазмозаменители. После 2-й—3-й — 4-й эксфузии крови вводят плазмозаменители (альбумин, протеин, гемодез, реополиглюкин или др.) и нативную донорскую плазму, а в конце ДПА (начиная с 4—5-й инфузии) вводят специфическую гипериммунную плазму (антистафилококко- вая, антисинегнойная, антипротейная или ассоциированная).
Объемы плазмоэкстракции и плазмозамещения во время ДПА должны быть равны, без учета 0,9 % раствора хлорида натрия, введенного вместе с эритроцитной массой больного.
Во время ДПА производят постоянный контроль за показателями гемодинамики. Во время последующих эксфузий крови и инфузий эритроцитной массы и плазмозаменителей происходят изменения гемодинамики, аналогичные закономерностям, выявленным при первой эксфузий крови и первой инфузий растворов. В процессе ДПА происходит постепенное снижение ЧСС и стабилизация артериального давления и ЦВД. После ДПА ЧСС, по нашим данным, составило 132,6±2,4 %, артериальное давление — 101,7+1,1 %, ЦВД — 82,7±2,2 мм водн. ст.
Эта закономерность характерна для больных всех возрастных групп. Во время ДПА обязателен строгий контроль за количеством взятой крови, объемом инфузий, плазмоэкстракции и плазмозамещения.
Инфузионная среда для плазмозамещения во время ДПА состоит в среднем из:
- свежецитратной крови — 10,4±0,9 %;
- специфических гипериммунных плазм — 48,5+1,3 %;
- нативной донорской плазмы — 9,6+1,2 %;
- низкомолекулярных плазмозаменителей— 16,2+1,1 %;
- 10 % раствора альбумина — 15,3±0,6 %.
Разработанная методика ДПА у детей с тяжелыми формами
ГСЗ не приводит к существенному изменению соотношения плазменного и глобулярного компонентов крови — гемато- критное число крови до ДПА составило 32,7+0,7 %, после ДПА- 34,2+0,8 % (р gt; 0,05).
Определение ОЦК с помощью радиоактивного йода дает возможность провести коррекцию ОЦК после ДПА (табл. 2.4).
Таблица2.4
Показатели ОЦК до и после дискретного плазмафереза
|
Исходный ОЦК, % |
М±т, % |
ОЦК после ДПА, % |
п |
P |
|
90-110 |
98+1,8 |
106,5+1,2 |
10 |
0,05 |
|
gt; ПО |
125,9+1,8 |
117,3+1,4 |
10 |
0,05 |
Во время и по окончании ДПА внутривенно вводят 10 %
. раствор хлорида кальция из расчета 10 мл на 500 мл введенной . плазмы и крови, необходимый для инактивации цитратного . гемоконсерванта, введенного вместе с плазмой и донорской '""'¦д кровью.
- Интенсивную детоксикационную инфузионную терапию *т. после ДПА проводят в полном объеме.
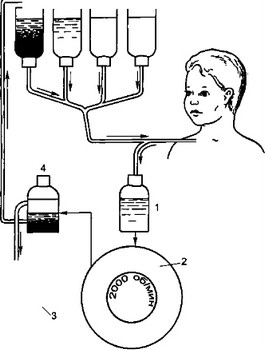

Общая схема дискретного плазмафереза представлена на рис. 2.1.
Осложнения дискретного плазмафереза. Осложнения при дискретном плазмаферезе могут возникнуть как непосредственно во время его проведения, так и в отдаленные сроки после операции.
Во время ДПА может отмечаться кратковременная гипово- лемия при эксфузии крови или при неадекватном возмещении плазмоэкстракции. По нашим данным, гипотония возникла у
- больных. После введения плазмозамещающих растворов, устранения гиповолемии произошла быстрая стабилизация пока
зателей гемодинамики и ДПА был продолжен. При стойкой гипотонии необходимо прекратить плазмаферез, провести коррекцию ОЦК, ввести преднизолон (3—5 мг/кг массы тела) и другие препараты, направленные на стабилизацию артериального давления. Стойкой гипотонии в наших наблюдениях не было. Тщательное выполнение методики, строгий контроль за объемом эксфузии крови, плазмоэкстракции и плазмозамеще- ния позволяют избежать данного осложнения.
На введение плазмы и плазмозамещающих растворов может развиться аллергическая реакция в виде озноба, повышения температуры, крапивницы, кожного зуда. Указанное осложнение возникло у двух больных во время ДПА. Введением анти- гистаминных препаратов, раствора хлорида кальция и . прекращением введения препаратов удалось купировать это осложнение. ДПА был продолжен и протекал в дальнейшем без особенностей.
Наиболее грозным осложнением при ДПА может быть анафилактический шок. В наших наблюдениях такого осложнения не было. При возникновении анафилактического шока следует проводить весь комплекс лечебных противошоковых мероприятий.
Также может наблюдаться цитратная интоксикация, вызванная введением больших доз гемоконсерванта с плазмой и кровью. Своевременная и адекватная инактивация цитратного гемоконсерванта раствором хлорида кальция (10 мл 10 % раствора хлорида кальция на 500 мл введенной плазмы и крови) позволила нам избежать этого осложнения.
Необходимо подчеркнуть, что аллергические реакции, анафилактический шок, сывороточный гепатит при ДПА встречаются не чаще, чем при проведении традиционного лечения тяжелых форм ГСЗ, так как этим больным в процессе лечения вводят большое количество плазмы, крови, плазмозамените- лей.
Противопоказания к дискретному плазмаферезу у детей
с тяжелыми формами гнойно-септических заболеваний.
Абсолютные противопоказания:
- терминальное состояние;
- аллергия на введение плазмы, белковых препаратов и плазмозаменителей.
Относительные противопоказания:
- неустойчивая гемодинамика с выраженной гипотонией: артериальное давление ниже 80—90 % от возрастной нормы, ЦВД ниже 60 мм водн. ст., тахикардия выше возрастной нормы на 85-90 %;
- дефицит ОЦК;
- снижение уровня гемоглобина ниже 80—90 г/л.
При наличии относительных противопоказаний необходима подготовка больных к ДПА: нормализация ОЦК путем гемотрансфузий, введения плазмы и плазмозаменителей; лечебные мероприятия по улучшению гемодинамики, КОС, водноэлектролитного обмена и т.д.
Основные этапы проведения плазмафереза у детей
с тяжелыми формами гнойно-септических заболеваний.
- Определение основных показателей гемодинамики и их коррекция.
- Внутривенное введение гепарина в дозе 100 ЕД/кг массы тела и антигистаминных препаратов.
- Эксфузия 12—16 % ОЦК в полимерный контейнер с консервантом.
- Внутривенная инфузия 10 % раствора альбумина и свеже- цитратной крови.
- Центрифугирование эксфузата при 2000 об/мин в течение 10 мин и отделение плазмы от глобулярного объема.
- Двукратное "отмывание" эритроцитной массы 0,9 % рас
твором хлорида натрия центрифугированием при 2000 об/мин в течение 5 мин. '
- Вторая эксфузия 12—16 % ОЦК больного с последующим центрифугированием, отделением плазмы и "отмыванием" эритроцитов.
- Реинфузия "отмытой" эритроцитной массы и инфузия плазмозаменителей.
- Эксфузия крови с "отмыванием" эритроцитов повторяется 5—8 раз.
- Плазмопотеря компенсируется адекватным количеством специфической гипериммунной плазмы, нативной донорской плазмы, плазмозаменителями.
Время плазмафереза 3—4 ч.
Механизм действия дискретного плазмафереза. Несмотря на использование плазмафереза в лечении различных заболеваний, механизм его действия изучен недостаточно. Очевидны следующие факторы лечебного действия ДПА при гнойно-септических заболеваниях.
- Механически вместе с плазмой больного из сосудистого русла удаляются токсичные вещества, продукты промежуточного обмена, деградации нуклеинового и липидного обмена, биологически активные вещества, иммунные комплексы, антитела и т.д.
- Периодически возникающая в процессе ДПА гипотония, уменьшение ОЦК, введение в сосудистое русло раствора альбумина и других веществ, обладающих высокоонкотическим действием, ведет к выходу токсинов вместе с жидкостью из тканевых депо и интерстициального пространства в сосудистое
? русло и усилению лимфооттока. Попав в сосудистое русло, \ токсичные вещества выводятся из него во время ДПА. iJ. 3. Снижение концентрации токсичных веществ ведет к уст-
ч1 ранению блокады системы макрофагов, печени, почек и других
V1 механизмов физиологической детоксикации и более активному ' включению их в процесс детоксикации, способствует более :! адекватному иммунному ответу.
- . 4. Целенаправленное замещение плазмы больного специфи
ческой гипериммунной плазмой, нативной донорской плаз-
- мой, белковыми и другими плазмозаменителями позволяет наряду с детоксикацией провести экстренную иммунокоррекцию, нормализовать гомеостаз и устранить другие нарушения.
А так же в разделе «Дискретный плазмаферез у детей с тяжелыми формами гнойно-септических заболеваний »
- Значение эндотоксикоза в патогенезе гнойно-септических заболеваний
- Консервативные методы борьбы с эндотоксикозом
- Методы экстракорпоральной детоксикации при гнойно-септических заболеваниях у детей
- Экстракорпоральная детоксикация (плазмаферез)
- . 2.4.2. Влияние дискретного плазмафереза , на некоторые показатели интоксикации и гомеостаза при тяжелых формах : гнойно-септических заболеваний у детей
- Оценка эффективности дискретного плазмафереза при гнойно-септических заболеваниях
- Глава 3 КАЛЛИКРЕИН-КИНИНОВАЯ СИСТЕМА И ЕЕ РОЛЬ ПРИ ГНОЙНО-СЕПТИЧЕСКИХ ЗАБОЛЕВАНИЯХ