Метод идентификации отдельных антителообразующих (АОК), разработанный и предложенный в 1963 г. Нобелевским лауреатом Н. Йерне и А. Нордином, дает возможность анализировать популяции лимфоидных клеток с точным учетом абсолютного числа АОК. Несмотря на то что прошло более 45 лет со дня сообщения о новом методе, он до сих пор используется при иммунологических исследованиях. Появились новые, получающие все большее распространение способы оценки АОК, но метод Н. Йерне, или, как его еще называют, метод локального гемолиза, или бляшкообразования в агаре, благодаря своей информативности и доступности остается в практике экспериментальной иммунологии, в частности при изучении действия различных факторов (физических, фармацевтических, токсических и др.) на антителообразование у экспериментальных животных. Доступен метод и для иммунологического практикума.
Основной принцип метода локального гемолиза состоит в том, что определенное число клеток лимфоидных тканей (селезенка, лимфатические узлы) мышей, иммунизированных эритроцитами барана, смешивают in vitro с эритроцитами барана и расплавленным, но не влияющим на жизнеспособность клеток агаром. Смесь помещают на чашку Петри и после инкубации при 37 °С в присутствии комплемента визуально подсчитывают число зон гемолиза («бляшек») в агаровой пластинке. В центре каждой «бляшки» находится АОК, представляющая собой плазматическую или лимфобластную клетку. Зная взятое для посева на агар число лимфоидных клеток, можно высчитать количество АОК на фиксированное число кариоцитов (например, на 1 млн или 10 млн) или на целый орган (селезенка).
Прямой способ (принцип описан выше) выявляет АОК, продуцирующие IgM антитела, лизирующие эритроциты в присутствии комплемента.
С помощью непрямого способа (рис. 3.6, см. также цв. вклейку) представляется возможность выявить АОК, продуцирующие IgG антитела (АТ). Для этих целей суспензию клеток дополнительно обрабатывают кроличьей антисывороткой, содержащей АТ против IgG мышей, на пике выработки IgM-AT. Антисыворотка, содержащая IgM-AT против IgG мышей, взаимодействует in vitro в агаре с IgG-AT против эритроцитов барана с присоединением комплемента. Этот комплекс способен лизировать эритроциты. Таким образом, при непрямом методе выявляется сумма АОК, продуцирующих IgM и IgG антитела.
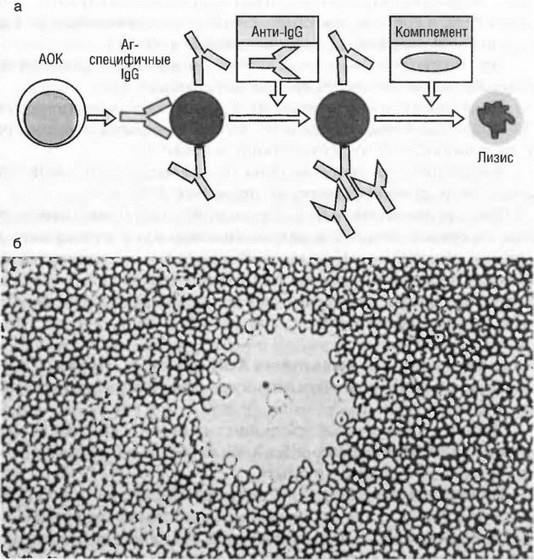
Рис. 3.6. Непрямой метод Йерне: а — схема постановки метода; б — зона гемолиза, в центре АОК
Использование эритроцитов барана, конъюгированных с растворимыми антигенами, дает возможность изучить динамику образования АОК к некорпускулярным антигенам. Метод локального гемолиза в модификации может быть применен для анализа АОК у разных видов животных, а также у человека.
Впервые метод Н. Йерне позволил выявить количественные закономерности динамики антителообразования при первичной и вторичной иммунизации животных. Перечислим указанные закономерности.
Основной принцип метода локального гемолиза состоит в том, что определенное число клеток лимфоидных тканей (селезенка, лимфатические узлы) мышей, иммунизированных эритроцитами барана, смешивают in vitro с эритроцитами барана и расплавленным, но не влияющим на жизнеспособность клеток агаром. Смесь помещают на чашку Петри и после инкубации при 37 °С в присутствии комплемента визуально подсчитывают число зон гемолиза («бляшек») в агаровой пластинке. В центре каждой «бляшки» находится АОК, представляющая собой плазматическую или лимфобластную клетку. Зная взятое для посева на агар число лимфоидных клеток, можно высчитать количество АОК на фиксированное число кариоцитов (например, на 1 млн или 10 млн) или на целый орган (селезенка).
Прямой способ (принцип описан выше) выявляет АОК, продуцирующие IgM антитела, лизирующие эритроциты в присутствии комплемента.
С помощью непрямого способа (рис. 3.6, см. также цв. вклейку) представляется возможность выявить АОК, продуцирующие IgG антитела (АТ). Для этих целей суспензию клеток дополнительно обрабатывают кроличьей антисывороткой, содержащей АТ против IgG мышей, на пике выработки IgM-AT. Антисыворотка, содержащая IgM-AT против IgG мышей, взаимодействует in vitro в агаре с IgG-AT против эритроцитов барана с присоединением комплемента. Этот комплекс способен лизировать эритроциты. Таким образом, при непрямом методе выявляется сумма АОК, продуцирующих IgM и IgG антитела.

Рис. 3.6. Непрямой метод Йерне: а — схема постановки метода; б — зона гемолиза, в центре АОК
Использование эритроцитов барана, конъюгированных с растворимыми антигенами, дает возможность изучить динамику образования АОК к некорпускулярным антигенам. Метод локального гемолиза в модификации может быть применен для анализа АОК у разных видов животных, а также у человека.
Впервые метод Н. Йерне позволил выявить количественные закономерности динамики антителообразования при первичной и вторичной иммунизации животных. Перечислим указанные закономерности.
- При первичной иммунизации мышей эритроцитами барана вначале возрастает число АОК, продуцирующих IgM-AT (пик образования АОК в среднем у мышей — 4—5 сут), а затем, через 1—2 дня, увеличивается число АОК, продуцирующих IgG-AT.
- При вторичной иммунизации иммунный ответ осуществляется преимущественно за счет АОК, вырабатывающих IgG.
- После иммунизации число АОК возрастает за несколько дней до 50—500 млн клеток. Накопление АОК в лимфоидной ткани предшествует выявлению циркулирующих в крови АТ.
- В небольшом количестве (1 на 10 млн кариоцитов) АОК пред- существуют в лимфоидных тканях (фоновые АОК).
- Нарастание числа АОК после иммунизации происходит постепенно, по кривой, близкой к экспоненциальной, т.е. в результате размножения изначально небольшого числа клеток-предшественников.
- АОК после иммунизации выявляются в основном в селезенке, лимфатических узлах, в костном мозгу и отсутствуют в других тканях (печень, легкие, почки, мозг).
