В настоящее время слюнные железы рассматривают и как региональный комплекс тимиколимфэтической системы, что подтверждается рядом факторов. В поднижнечелюстных железах найдены плазматические клетки. Предполагается, что в этих клетках вырабатываются иммуноглобулины, обнар живаемые в слюне, поэтому возможна связь слюнных желез с иммунокс мпетентной системой и возникновения аутоиммунньх заболеваний. Многократные клинические наблюдения подтверждают наличие ряда заболеваний слюнных желез, в патогенезе которых определяются признаки нарушения иммунного статуса. К таким заболеваниям относят болезнь и синдром Микулича [Miculicz J., 1888, 1892], болезнь и синдром Шегрена [Sjogren Н., 1933], синдром Хегрфордта [Неег- fordt Ch. J., 1909]. Они имеют общие признаки (системное поражение слезных и слюнных желез, длительное хроническое течение процесса с периодическим обострением), но этиология и патогенез их различны.
Болезнь (синдром) Микулича. Сочетанное увеличение слезных и всех слюнных желез называют болезнью Микулича, а если оно наблюдается при лейкозе, лимфогранулематозе, туберкулезе, сифилисе, эндокринкых нарушениях, то синдромом Микулича.
J. Miculicz в 1892 г. описал заболевание, которое ему пришлось наблюдать в 1888 г. на протяжении 14 мес у крестьянина 42 лет. Основные клинические признаки заключались в увеличении слезных и всех слюнных желез.
Заболевание началось около полугода назад с нрипухания слезных желез. Глазная щель сузилась, и стало трудно смотреть. Никаких других субъективных ощущений не было. Вскоре увеличилгсь поднижнечелюстные, что мешало при разговоре и во время еды, а в дальнейшем и околоушные железы.
При обследовании больного отклонений от нормы не обнаружено. Слезные железы резко увеличены, плотны, бугристы, безболезненны. Зрение не нарушено. Все слюнные железы, большие и малые, также значительно увеличены, имели плотноэластическую консистенцию, безболезненны, умеренно подвижны. Слюны в полости рта много, слизистая оболочка не изменена. Произведено частичное удаление слезных желез, но вскоре они вновь увеличились до прежних размеров. Лишь после полного удаления слезных и поднижнечелюстных желез крестьянин мог возвратиться к своему труду и чувствовал себя хорошо. Однако через 2 мес он заболел и на 9-й день умер от перитонита. Околоушные и малые слюнные железы, несколько увеличившиеся после операции, перед смертью стали быстро уменьшаться и припухлость почти полностью исчезла.
J. Miculicz произвел патологоанатомическое исследование поднижнечелюстных желез. Вся увеличенная железа имела нормальное строение; ее можно было разделить на дольки и доли. На разрезе ткань железы отличалась от нормальной бедностью сосудов, имела бледно-красноватожелтый цвет. Железа была мягкой консистенции, имела сальную проз рачную поверхность. Микроскопически неизмененные ацинусы были раздвинуты круглоклеточной тканью, клетки которой имели различные размеры. Между ними располагалась тонкая эндоплазматическая сеть. В более крупных клетках можно было распознать митозы. Сходная картина наблюдалась в слезных железах.
Автор отмечает, что у этого больного увеличение всех слюнных и слезных желез протекало без признаков воспаления, без выявляемого участия всего организма. Микроскопическое исследование позволило установить, что собственно паренхима желез играет пассивную роль. Увеличение размеров желез обусловлено лишь массивной мелкоклеточной инфильтрацией интерстициальной соединительной ткани, которая скорее всего соответствует лимфа- деноидной ткани. J. Miculicz считает, что заболевание слезных желез не только является самым постоянным, но и возникает раньше других патологических факторов. Общность процесса в слюнных и слезных железах автор объясняет наличием патологического разрастания лимфоидной интерстициальной ткани, которая имеется в тех и других железах. По мнению автора, в описанном наблюдении речь может идти об инфекционном или паразитарном процессе.
В последующие годы в литературе многократно было описано заболевание под названием «болезнь Микулича», при котором основным симптомом было увеличение слюнных и реже слезных желез. Известны случаи заболевания с поражением лимфатического аппарата, селезенки, печени. Заболевание получило ряд новых названий: «синдром Микулича», «симптомокомплекс Микулича», «аллергический ретикулоэпителиальный сиалоз Микулича», «лимфо- миелоидный сиалоз», «лимфоцитарная опухоль» и др. Заболевание стали определять как результат поражения всего лимфатического аппарата, в том числе слюнных и слезных желез, по типу алейкемического (реже лейкеми- ческого) лимфоматоза. Таким образом, этиология и патогенез болезни остаются неизвестными, клиника мало изучена. В настоящее время наиболее вероятной причиной заболевания считают нейротрофические и эндокринные аутоиммунные расстройства.
Клиническая картина заболевания слюнных желез характерна. Припухшие железы плотны, безболезненны, кожа, покрывающая их, в цвете не изменена. Локализация
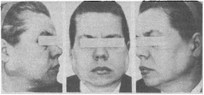
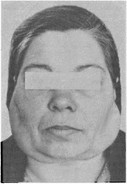
Рис. 21. Фотографии больной с болезнью Шегрена в клинически выраженной стадии. Определяется увеличение околоушных желез.
следовании околоушных желез в период ремиссии они часто были увеличены, плотны, бугристы, безболезненны (рис. 21). Обычно поражались обе парные железы. Иногда отмечалось увеличение лимфатических узлов, причем больных беспокоил только сам этот факт. Припухлость периодически уменьшалась и увеличивалась; увеличение сопровождалось ухудшением общего самочувствия. Обострение протекало тяжело, с высокой температурой тела, сильными болями, слизисто-гнойным отделяемым из протока. После стихания процесса железы оставались плотными, бугристыми. Обострение чаще наблюдалось с одной стороны. При сиалометрии из околоушных желез справа и слева в среднем получено по 0,6 ±0,2 мл слюны, из поднижнечелюстных — соответственно 0,7 мл справа и 0,3 мл слева. Число функционирующих малых слюнных желез на нижней губе равно 16 ±2. Цитологическое исследование секрета позволило отметить в препаратах клетки слюнных трубок и кубический эпителий.
При радиосиалографии средние показатели концентрационной способности слюнных желез соответствуют нарушению функции II степени (стадия декомпенсации), время МНР укорочено, процент МПР уменьшен. На сканограмме нет четкого изображения околоушных и поднижнечелюстных желез, их изображения сливаются. О площади желез можно судить только при суммарном подсчете изображения обеих желез соответствующей стороны. Контуры желез четкие, но неровные. Штриховка равномерная, иногда с участками выпадения радиоактивности. Нет четкого
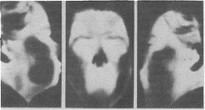
Рис. 22. Термовизиограмма той же больной, что на рис. 21, в правой и левой боковых (а, в) и прямой (б) проекциях видны участки гипертермии над околоушными и поднижнечелюстными железами (отчетливо выражен белый цвет). Особенно хорошо они определяются на боковой проекции.
отграничения околоушных и поднижнечелюстных желез от участка повышенной интенсивности изображения в центре (полость рта). В подобных случаях на сканограмме в боковой проекции иногда получается раздельное изображение околоушных и поднижнечелюстных желез, по которому можно определить их площадь.
На эхограмме хорошо определяются листки капсулы, ткань железы акустически неоднородная, с плотными включениями. На термовизиограмме у всех наших больных отмечена гипертермия над околоушными железами (рис. 22). Температура была тем выше, чем более выражено припухание железы. После лечения температура снижалась, но не до нормы.
При сиалографии в железе определяются полости различных размеров, контуры их нечеткие, изображение паренхимы не определяется. Мелкие протоки железы прерывисты, выявляются не везде. Околоушные и поднижнечелюстные протоки имеют неровные, нечеткие контуры (рис. 23, 24). Симптом повышенной проницаемости протоков выражен тем сильнее, чем активнее протекает процесс. На основании сиалограмм можно сделать вывод, что хронический сиаладенит при болезни и синдроме Шегрена протекает как паренхиматозный.
При морфологическом исследовании биоптатов малых
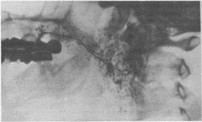
Рис. 23. Сиалограмма левой околоушной железы в боковой проекции больной с болезнью Шегрена в клинически выраженной стадии. Контуры протоков неровные и нечеткие. Контрастная масса проникла через стенки протоков и определяется в виде нечетких, неправильной формы участков за пределами протоков.
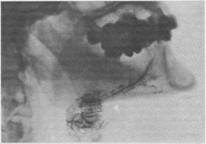
Рис. 24. Сиалограмма правой поднижнечелюстной железы той же больной, что на рис. 23. Изменения в поднижнечелюстной железе сходны с таковыми в околоушной.

слюнных желез нижней губы отмечена очагово-диффузная лимфоплазмоклеточная инфильтрация. Концевые отделы дистрофичны, часть из них по периферии содержит слизь; ацинусы вблизи инфильтрата кистозно расширены. Пролиферированный эпителий и миоэпителий нередко закрывают просвет протоков. На фоне лимфоидной инфильтрации часто определяется нарушение целостности базальной мебраны. В некоторых протоках клетки инфильтрата проникают в стенку протока с ее деструкцией. Можно предположить, что указанные морфологические нарушения являются причиной повышения проницаемости стенок протоков для контрастного вещества.
В поздней стадии хронического сиаладенита при болезни и синдроме Шегрена припухлость слюнных желез часто бывает огромной (рис. 25). Больных беспокоит частое обострение сиаладенита. Слизистая оболочка полости рта сухая. В период ремиссии железы плотны, подвижны, безболезненны, кожа над ними истончена. Иног-
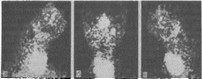
Рис. 26. Сцинтиграмма слюнных желез больного с болезнью Шегрена в поздней стадии. В области околоушных и поднижнечелюстных желез в боковых (а, в) и прямой (б) проекциях снижение накопления радионуклида, радиоактивность мало отличаются от фоновой.
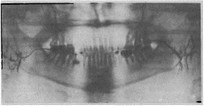
Рис. 27. Пантомосиалограмма околоушных желез больной с болезнью Шегрена в поздней стадии. Паренхима и мелкие протоки в железе не определяются. Протоки I порядка и околоушной проток имеют неровные, нечеткие контуры. Контрастная масса выходит за пределы протоков.
протоков вследствие сдавления их лимфоидной тканью на сиалограмме, кроме больших размеров железы, можно выявить нечеткость тени паренхимы. Протоки очень узкие, имеют ровные контуры. Указанные признаки со временем прогрессируют и может наступить период, когда тень паренхимы железы по периферии не будет определяться, поскольку железистые зоны не заполняются контрастным веществом. Контуры протоков железы при этом остаются ровными, но просвет их настолько узок, что на сиалограмме их ход можно проследить лишь с помощью лупы. Описанная рентгенологическая картина слюнной железы при болезни Микулича соответствует тем патологоанатомическим изменениям, которые находят при микроскопическом исследовании слюнных желез.
При генерализованном поражении лимфоидного аппарата, в том числе слезных и слюнных желез, клиническое проявление болезни и результаты специального общего обследования больного позволяют установить признаки лимфогранулематоза. При этом заболевание диагностируют как синдром Микулича. Фактически это опухолевое перерождение лимфоретикулярной системы.
Лечение болезни Микулича представляет большие трудности. Применение, как предлагают некоторые авторы, препаратов мышьяка и калия йодида не приводит к прекращению процесса. Отмечается лишь некоторое улучшение состояния больных. Хорошие результаты дает рентгенотерапия: припухлость желез резко уменьшается или полностью исчезает. Однако эффект лечения нестойкий, часто наступают рецидивы. Мы рекомендуем проведение новокаиновой блокады, применение галантамина, что улучшает трофику тканей и стимулирует секреторную функцию слюнных желез. В случаях хронического воспаления желез, осложняющего течение основного заболевания, следует провести противовоспалительное лечение (введение в протоки железы бактериофага, антибиотиков, компресс с димексидом и др.). В комплекс лечебных мероприятий следует включать также препараты, повышающие неспецифическую резистентность организма: витамины, натрия нуклеинат и др. Кроме того, при лечении больных с синдромом Микулича применяют стероидные препараты. Эти больные должны находиться под наблюдением ревматолога, стоматолога, окулиста, онколога, гематолога и терапевта.
Болезнпь (синдром) Гужеро — Шегрена. Снонимы: ксеродерматоз, синдром Предтеченского — Гужеро —
Шегрена, сухой синдром, синдром Съегрена, болезнь (синдром) Шегрена — заболевание неясной этиологии, характеризующееся сочетанием признаков недостаточности желез внешней секреции: слезных, слюнных, потовых, сальных, слизистых и др.
В 1933 г. Н. Sjogren дал описание симптомокомплекса у 19 больных с сухим кератоконъюнктивитом, а в 1940 г. — у 50 больных. Он отметил жалобы на чувство песка в глазах, светобоязнь, уменьшение секреции слез (даже когда больной плачет, глаза остаются сухими). Кроме того, больных беспокоила сухость слизистой оболочки носа, глотки, гортани. Отмечались разрушение зубов, ахилия, повышение СОЭ, лимфоцитоз. У 80% больных наблюдался полиартрит. Большинство больных составляли женщины, лишь двое из них были мужчины. Полный симптомокомплекс автор наблюдал редко. Как правило, встречались один — два симптома. Полностью развившийся синдром характеризовался: сухим кератоконъюнктивитом, ксеростомией, сухим ринитом, фарингитом, ларингитом и хроническим полиартритом. У женщин отмечалась сухость слизистой оболочки половых органов. В 1925 г. сухой синдром был описан Н. Gougerot и в настоящее время носит имя двух авторов.
Н. Sjogren, изучая морфологию и патогенез, считал, что причиной синдрома являются инфекция или недостаточность витамина А, нарушение функции эндокринных органов, так как чаще болеют женщины в климактерическом периоде. В последнее десятилетие широкое изучение аутоиммунных и ревматических заболеваний позволило выявить у ряда больных хроническим активным гепатитом, тиреоидитом Хашимото, системной красной волчанкой, системной склеродермией, ревматоидным полиартритом признаки сухого синдрома Гужеро — Шегрена. В настоящее время больных с указанным симптомоком- плексом делят на две группы. У одной из них заболевание определяют как синдром Шегрена. Это больные, у которых признаки нарушения функции всех желез внешней секреции возникают при системной красной волчанке, системной склеродермии, ревматоидном полиартрите и других аутоиммунных заболеваниях. У больных второй группы заболевание расценивают как болезнь Шегрена. При той же клинической картине поражения внешнесекреторных желез, характерной для сухого синдрома, у них нет других заболеваний, но имеются иммунологические нарушения, ставящие болезнь Шегрена в ряд заболеваний с аутоим-
мунными нарушениями [Васильев В. И., 1981; Симонова М. В., 1982].
Этиология и патогенез болезни (синдрома) Шегрена изучены мало. Считают, что в развитии патологического процесса играют роль инфекция, эндокринные расстройства, нарушение функции вегетативной нервной системы, иммунного статуса. По-видимому, все эти причины, а не одна из них, имеет значение в возникновении и развитии заболевания.
Развитие сухого синдрома мы представляем себе следующим образом. В организме человека, генетически предрасположенном к данному заболеванию, в результате эмоционального стресса нарушаются функции всех эндокринных желез, что приводит к нарушению обмена в тканях. При этом в слюнных железах повышается проницаемость клеточных мембран. Последнее вызывает задержку выделения в протоки железы образовавшегося в клетках ацинусов секрета. Он переполняет клетку и проникает через ее оболочку в интерстициальную ткань. Белок, претерпевший определенные изменения в клетке ацинуса и предназначенный для выделения с секретом слюнной железы через проток в полость рта, попадая в интерстициальную ткань, играет роль антигена и вызывает образование антител против клеток паренхимы железы. Возникший аутоиммунный процесс вызывает реакцию лимфоидной ткани, ее гиперплазию и деструкцию клеточных элементов паренхимы. Гипосиалия обусловливает проникновение инфекции в железу и развитие хронического сиаладенита. Подобные изменения происходят, по-видимому, во всех железах внешней секреции. Если учесть, что слюнные железы обладают и инкреторной функцией, то можно считать, что патологическое состояние организма усугубляется недостаточностью этой функции.
В пользу высказанного предположения об этиологии и патогенезе болезни Шегрена говорят некоторые клинические наблюдения и исследования, описанные в литературе, а также наши данные. Так, о генетической предрасположенности организма к данному заболеванию можно судить по возникновению сходной патологии слюнных желез у родственников (однояйцевые близнецы, братья, сестры, родители и дети). Стрессовые ситуации очень часто предшествуют развитию болезни Шегрена. О нервных потрясениях перед появлением ксеростомии еще в 1890 г. сообщил A. Seifert. Мы обратили на это внимание 15 лет назад. В настоящее время при целенаправленном
опросе в большинстве случаев (около 90%) удается установить различного характера стрессовые ситуации перед появлением первых признаков болезни.
Стрессоры принято делить на кратковременные и длительно действующие. У одних наших больных раздражителем было внезапное сильное воздействие на эмоциональную сферу. Так, на глазах молодой женщины утонул ее муж. Мужчина, недавно севший за руль автомашины, задавил человека и др. Реакция на эти события выражалась в появлении внезапной сухости полости рта и глаз; в дальнейшем симптомы заболевания нарастали. Многие больные длительное время испытывали в семье или на работе неблагоприятное воздействие на психику (безнадежно больной единственный ребенок в семье, конфликтные ситуации на работе или между супругами и др.).
Мы наблюдали девочку 14 лет с признаками сухого синдрома. Она была единственным ребенком, очень любила своих родителей, которые часто ссорились, и на протяжении нескольких лет оставался нерешенным вопрос о разводе. Девочка была в курсе всех семейных неприятностей. Известно, что у одних людей компенсаторные возможности высоки, и даже значительные по силе раз-
 ДРУ-
ДРУ-
дит в нкции
Шег- нару-
количества спермы. В связи с этим больным назначают гормо
нальную терапию. В некоторых случаях она дает положительные результаты.
Все многообразие изменений в организме при болезни Шегрена и связь этих изменений с патологическим процессом в слюнных железах изучены недостаточно. Морфологическое исследование слюнных желез, проведенное Н. Sjogren на ранней стадии заболевания, подтверждает предположение о возможности роли патологии мембраны клеток паренхимы железы в нарушении внешнесекреторной функции.
В дальнейшем морфологическая картина слюнных желез при синдроме Гужеро — Шегрена описана неоднократно. Отмечено, что изменение больших и малых слюнных желез было сходным [Holm S., 1949; Stanworth А., 1951; Seifert G. et al., 1981; Takeda Y., 1980, и др.]. Вопросами морфологии поднижнечелюстных желез занимались А. М. Солнцев и В. С. Колесов (1981).
Использование электронной микроскопии значительно расширило информацию о морфологии слюнных желез при синдроме Шегрена. Установлено, что инфильтрирующие клетки состоят в основном из лимфоцитов малой и средней величины, плазменных клеток и гистиоцитов. Найденные большие лимфоциты рассматриваются как Т-лимфоциты. Обнаружено повреждение клеток паренхимы с нарушением процесса образования и выделения секрета. Некоторые клетки полностью разрушались и их содержимое изливалось в просвет миоэпителиальных клеток, которые были более резистентны к дегенеративным изменениям. В протоках отмечены эпителиальная пролиферация, метаплазия и инфильтрация плазматических клеток и лимфоцитов. Базальные пластинки протоков и долек железы были изменены [Takeda Y., 1980].
Патогномоничным признаком для синдрома Шегрена считают пролиферацию миоэпителия и образование эпи- миоэпителиальных островков на фоне выраженной лимфоидной инфильтрации стромы. С внедрением иммуно- флюоресцентной техники в морфологические исследования появилась возможность идентифицировать природу лимфоцитов, составляющих инфильтрат малых слюнных желез при синдроме Шегрена. Инфильтраты могут состоять как из Т-, так и из В-лимфоцитов [Talal N. et al., 1974].
Повышенная проницаемость мембран * клеток железистой паренхимы и протоков слюнных желез хорошо определяется на сиалограммах, где видно проникновение контрастного вещества за пределы протоков и ацинусов
в интерстициальную ткань. Рассасывание этого контраста можно обнаружить при динамическом рентгенологическом наблюдении за слюнными железами. Повышение проницаемости мембран, по-видимому, действительно играет не последнюю роль в механизме снижения секреторной функции слюнных желез. Это подтверждается нашими клиническими наблюдениями.
По поручению Г. А. Васильева на кафедре пропедевтики хирургической стоматологии ММСИ П. М. Егоровым проведена работа, в которой было предусмотрено при комплексном лечении больных интерстициальным паротитом применение электрофореза с лидазой и ронидазой с целью предупреждения склерозирования ткани железы. При лечении 22 больных отмечена тенденция к снижению функции железы. У 2 больных возникла асиалия; при этом сухость в полос+и рта напоминала состояние при синдроме Гужеро — Шегрена. До лечения функция слюнных желез была нормальной. В дальнейшем, после новокаиновой блокады, функция желез восстановилась полностью. Если учесть, что препараты лидазы и ронидазы повышают проницаемость мембран, то надо полагать, что асиалия, возникшая у больных при их применении, явилась результатом повышения проницаемости клеточных мембран ткани железы. Не исключено, что подобный механизм нарушения слюноотделения имеет место и при сухом синдроме. В подтверждение этого предположения можно привести еще клинические наблюдения за больными с синдромом Шегрена, находившимися на лечении в нашей клинике.
Применение галантамина как препарата, повышающего функцию всех пищеварительных желез, у больных с идиопатической ксеростомией дало положительные результаты. Мы решили применить его у больных с синдромом Шегрена. При неактивном течении процесса, когда сиало- графически не отмечается повышенная проницаемость железы, галантамин дает положительные результаты. Однако у 2 больных с активным течением процесса и высокой проницаемостью ткани в отношении контрастного вещества лечение галантамином привело к осложнениям. У одного больного возникли боли распирающего характера, усиливающиеся во время еды, железы увеличились и уплотнились. При пункции желез получена мутная слюна в большом количестве. У второй больной в о^ ной из желез образовались две кисты, были
удалены хирургическим путем.
Наблюдения позволили нам предположить, что при синдроме Шегрена функция образования секрета в клетках паренхимы нарушается не в первую очередь; вначале нарушается выделительная и эвакуаторная функция железы. Надо полагать, что это происходит вследствие повышения проницаемости клеточных мембран. Возможность образования секрета в клетках ацинусов в начале заболевания синдромом Шегрена длительное время сохраняется. Это подтверждено неоднократно проведенными морфологическими исследованиями, в которых указано на переполнение клеток паренхимы секреторными гранулами.
Изучение ультраструктуры малых слюнных желез [Talal N., 1974] позволило установить расширение межклеточных пространств и выход содержимого ацинарной клетки через базальную часть дольки в просвет миоэпи- телиальной клетки. Под нашим руководством проведена работа [Перминова И. С., 1982], в которой ультраструк- турные изменения в малых слюнных железах изучены в зависимости от стадии процесса и установлено, что в начальной стадии секреторная активность клеток не нарушена и снижение выделения через проток секрета связано с явлениями реабсорбции его, что подтверждается расширением межклеточных пространств и нарушением микроциркуляторного русла.
В настоящее время доказано наличие аутоиммунного процесса в патогенезе сухого синдрома. Аутоиммунные нарушения проявляются повышением титров циркулирующих антител к эпителию слюнных и слезных желез, тиреоглобулина, ревматоидных факторов, а также отложением иммунных комплексов в пораженных тканях, включающих IgM, IgG, С3-компонент комплемента [Denko С., Schearn М., 1971; Anderson L. et al., 1972]. Это положение подтверждается и патоморфологической картиной болезни, основу которой составляет лимфоплазматическая инфильтрация, замещающая в поздней стадии заболевания паренхиму слюнных и слезных желез.
Массивность лимфоидной инфильтрации слюнных желез на фоне лимфаденопатии даже заставляет думать о возможном переходе доброкачественного лимфопролиферативного процесса в лимфомы и в дальнейшем трансформацию в лимфосаркому [Talal N. et al., 1967; Whaley К. et al., 1968; Cummings N. et al., 1971].
Последние исследования, проведенные в Научно-исследовательском институте ревматологии АМН СССР, не только свидетельствуют о наличии аутоиммунного процесса, но и позволяют на основании иммунологического статуса выделить группы больных с различным клиническим течением процесса (болезнь Шегрена, синдром Шегрена, активное течение заболевания).
Клиника. Патологические проявления при болезни (синдроме) Шегрена со стороны слюнных желез многообразны. Это зависит от сочетания изменений слюнных желез с поражением других органов и тканей (органы пищеварения, глаза, эндокринные железы, суставы, соединительная ткань и др.), стадии процесса (начальной, клинически выраженной, поздней), активности клинического течения и лабораторных показателей (активное и неактивное течение).
По нашим данным, в стоматологических клиниках, занимающихся данной патологией, больные с болезнью (синдромом) Шегрена составляют 27% от числа больных с сиалозами различного происхождения. Большинство больных составляли женщины. Более половины было в возрасте старше 50 лет, около одной трети — от 30 до 50 лет; детей было двое. Последние годы мы стали диагностировать болезнь (синдром) Шегрена в более молодом возрасте, что связано с накоплением опыта и совершенствованием методов специального обследования и диагностики заболеваний слюнных желез.
При целенаправленном обследовании больных в клинике Научно-исследовательского института ревматологии АМН СССР М. В. Симоновой выявлены больные с синдромом Шегрена в молодом возрасте. К моменту появления первых признаков заболевания средний возраст больных составил 27'/2 года, к моменту обследования — 361 /2 года. Эти данные говорят о том, что на протяжении многих лет болезнь не была диагностирована, по-видимому, в связи с тем, что первые ее проявления не сильно беспокоили больных и они не обращались к врачу или, обратившись в какую-либо клинику (в зависимости от первых симптомов болезни — в стоматологическую, офтальмологическую, оториноларингологическую, ревматологическую, гинекологическую, терапевтическую и др.), подвергались лечению только по поводу патологических симптомов соответственно профилю учреждения. Общее заболевание оставалось недиагностированным.
В стоматологических лечебных учреждениях у больных преобладали симптомы поражения слюнных желез и полости рта. Больные жаловались на общую слабость, быструю утомляемость, сухость полости рта, периодически
эазвивающееся воспаление околоушных желез. Не всегда заболевание впервые проявлялось сухостью полости рта.
Иногда вначале появлялись сухость глаз, светобоязнь, чувство песка в глазах, а затем увеличение околоушных и редко поднижнечелюстных желез. Иногда больные указывали, что находятся на учете у ревматолога по поводу заболевания суставов, системной красной волчанки или склеродермии.
Сухость полости рта больные не всегда связывали с общим заболеванием, по поводу которого они обратились к врачу; она выявлялась лишь при опросе. Нередко больные говорили о том, что они любят запивать пищу, или отмечали, что в последние годы стали разрушаться зубы, беспокоит чувство жжения слизистой оболочки языка, губ, неба. В дальнейшем при обследовании была установлена ксеростомия в начальной или даже клинически выраженной стадии. У небольшого числа больных жалобы были характерны для паренхиматозного паротита и лишь спустя несколько лет выявлялась болезнь Шегрена. У одной больной, которую мы впервые обследовали в возрасте 8 лет, лишь в 18 лет были установлены все признаки болезни Шегрена. Двух женщин мы длительное время лечили с диагнозом паренхиматозного паротита. Клинически признаки болезни Шегрена проявились лишь через 8—12 лет.
Из перенесенных и сопутствующих заболеваний больше отмечали анацидный и гипацидный гастрит, хронический колит, хронический гепатит, острый и хронический полиартрит, тиреотоксикоз, невроз, неврастению, склероз сосудов мозга, заболевания сердечно-сосудистой и дыхательной систем. У всех больных при обследовании слюнных желез мы обнаружили сиаладенит.
В начальной стадии сиаладенита при болезни (синдроме) Шегрена больные жалуются на незначительное уплотнение, чаще околоушных, реже поднижнечелюстных желез, распирающие ощущения во время еды; они тем сильнее, чем активнее протекает заболевание. При неактивном течении процесса уплотнения в области железы может не быть или оно совсем не беспокоит больного. Лишь изредка появляется обострение, повышается температура тела, появляется разлитая припухлость в области железы, полностью прекращается выделение слюны. Из протока может появиться гной. На протяжении 7—10 дней воспалительные явления постепенно стихают. В период ремиссии припухлость иногда не определяется. У таких больных на основании дополнительных исследований можно диагностировать сиаладенит. Даже если процесс обостряется только в одной железе, в другой обнаруживается скрыто протекающий воспалительный процесс.
При сиалометрии из правой околоушной железы в среднем выделяется 1,9 ±0,4 мл, а из левой 1,7 ±0,2 мл секрета, из поднижнечелюстных — соответственно 2,2 ±0,2 и 1,8 ±0,2 мл. Число функционирующих малых слюнных желез на 4 см2 слизистой оболочки нижней губы 15 ±4. Цитологическое исследование секрета позволило установить повышенное слущивание клеток плоского и цлиндри- ческого эпителия. При раДиосиалографии средние показатели концентрационной способности слюнных желез соответствуют нарушению функции железы I степени (компенсаторная стадия), время МНР и МПР удлинено, процент МПР увеличен.
При сканировании изображение околоушных желез имеет неравномерную штриховку. Поднижнечелюстные железы увеличены. Изображение полости рта четкое, с интенсивной частой штриховкой. Ультразвуковая биолокация произведена нами у больного 72 лет. Околоушные железы на эхограмме были уменьшены, содержали преимущественно плотную ткань, листки капсулы просматривались не везде. При термовизиографии изменения температуры в области слюнных желез не отмечено. При лечении термодинамика также не выявляется.
При сиалографии и пантомосиалографии отмечена повышенная проницаемость протоков для контрастного вещества, в связи с чем изображение паренхимы неравномерное. Контуры протоков нечеткие, вокруг них определяется «облачко» контрастной массы, проникшей в интерстициальную ткань, которое рассасывается на протяжении недели. При биопсии малых слюнных желез нижней губы в концевых отделах обнаруживаются дистрофические процессы (переполнение ацинусов слизью, кистозная перестройка). Лимфоидный инфильтрат представлен небольшими скоплениями клеток или очаговой перидуктальной инфильтрацией. В отдельных внутридольковых протоках имеет место деструкция стенки на фоне инфильтрата [Симонова М. В., 1982].
В клинически выраженной стадии болезни (синдрома) Шегрена больные, находившиеся под нашим наблюдением, жаловались на сухость полости рта, разрушение зубов, припухание околоушных желез, периодически появляющееся обострение сиаладенита. При об- да увеличены лимфатические регионарные узлы; они тоже подвижны и безболезненны. Секрет из протоков не выделяется. При массировании железы может выделиться небольшая слизистая пробка. У большинства больных зубов нет. Они с трудом могут пользоваться съемными протезами, так как слизистая оболочка рта очень ранима. Если больной может привыкнуть к съемному протезу, то он испытывает облегчение и в отношении сухости полости рта.
При сиалометрии из околоушных и поднижнечелюстных протоков слюна через канюли не выделяется. Число малых слюнных желез на нижней губе, по средним данным, равно 12±2. При цитологическом исследовании слизистого отделяемого из протоков определяются бокаловидные клетки, пласты воспалительно измененного эпителия, а также клетки воспалительного экссудата. При радиосиа- лографии можно установить, что слюнные железы не концентрируют радиоактивное вещество.
При сканировании изображения слюнных желез получить не удается в связи с тем, что концентрационная способность паренхимы резко снижена или отсутствует. Сходные изменения определяются на сцинтиграмме (рис. 26).
На эхосиалограмме внутренний листок капсулы определяется не везде. Средние показатели акустически плотной ткани в железе при всех положениях одномерного датчика составляют 59,4 ±3,5%. Отмечено, что склерозируются преимущественно задненижние отделы железы, где определяется 78,5 ± 5,8% акустически плотной ткани (в области передневерхних отделов 36,6 + 5,8%).
При термовизиографии наблюдается значительная гипертермия над увеличенными околоушными железами. У больных без увеличения желез гипертермия выражена в меньшей степени. При сиалографии паренхима железы не контурируется, полостей, характерных для клинически выраженной стадии, нет. Мелкие протоки железы не определяются; протоки I—III порядков и околоушной проток имеют нечеткие контуры, на некоторых участках они не определяются из-за попадания контрастной массы в интерстициальную ткань (рис. 27). При повторной рентгенографии можно проследить рассасывание контрастного вещества, иногда его следы выявляются через 2— 3 нед.
Морфологически определяется очагово-диффузная или диффузная лимфоплазмоклеточная инфильтрация малых
слюнных желез. В одних дольках сильнее выражены процессы склероза, а в других — лимфоидная инфильтрация; при этом архитектоника долек сохраняется. На фоне инфильтрата, заместившего паренхиму, в результате процессов пролиферации эпителия и миоэпителия на месте прекративших существование протоков образуются миоэпите- лиальные островки.
Диагностика поражения слюнных желез при болезни и синдроме Шегрена основывается на местных характерных клинических признаках: припухании железы, снижении функции, сиалографических симптомах хронического паренхиматозного паротита. При этом отмечается повышение проницаемости протоков для контрастного вещества. Мы наблюдали симптом увеличения парной околоушной железы в ответ на сиалографию, произведенную с противоположной стороны, и рассматриваем его как характерный для активного течения болезни и синдома Шегрена.
Помимо местного обследования, для подтверждения диагноза необходимо произвести исследование внутренних органов. При болезни Шегрена поражаются глаза. По данным Ю. В. Юдиной (1975), в начальной стадии заболевания отмечены явления блефароконъюнктивита и снижение секреции слезных желез первой степени (основной секреции на 2—3 мг, общей — на 5—6 мг при норме: основная секреция правого глаза 12,0 ±0,6, левого глаза 13,0±0,6 мг, общая 28,0±1,0 мг). В клинически выра
Болезнь (синдром) Микулича. Сочетанное увеличение слезных и всех слюнных желез называют болезнью Микулича, а если оно наблюдается при лейкозе, лимфогранулематозе, туберкулезе, сифилисе, эндокринкых нарушениях, то синдромом Микулича.
J. Miculicz в 1892 г. описал заболевание, которое ему пришлось наблюдать в 1888 г. на протяжении 14 мес у крестьянина 42 лет. Основные клинические признаки заключались в увеличении слезных и всех слюнных желез.
Заболевание началось около полугода назад с нрипухания слезных желез. Глазная щель сузилась, и стало трудно смотреть. Никаких других субъективных ощущений не было. Вскоре увеличилгсь поднижнечелюстные, что мешало при разговоре и во время еды, а в дальнейшем и околоушные железы.
При обследовании больного отклонений от нормы не обнаружено. Слезные железы резко увеличены, плотны, бугристы, безболезненны. Зрение не нарушено. Все слюнные железы, большие и малые, также значительно увеличены, имели плотноэластическую консистенцию, безболезненны, умеренно подвижны. Слюны в полости рта много, слизистая оболочка не изменена. Произведено частичное удаление слезных желез, но вскоре они вновь увеличились до прежних размеров. Лишь после полного удаления слезных и поднижнечелюстных желез крестьянин мог возвратиться к своему труду и чувствовал себя хорошо. Однако через 2 мес он заболел и на 9-й день умер от перитонита. Околоушные и малые слюнные железы, несколько увеличившиеся после операции, перед смертью стали быстро уменьшаться и припухлость почти полностью исчезла.
J. Miculicz произвел патологоанатомическое исследование поднижнечелюстных желез. Вся увеличенная железа имела нормальное строение; ее можно было разделить на дольки и доли. На разрезе ткань железы отличалась от нормальной бедностью сосудов, имела бледно-красноватожелтый цвет. Железа была мягкой консистенции, имела сальную проз рачную поверхность. Микроскопически неизмененные ацинусы были раздвинуты круглоклеточной тканью, клетки которой имели различные размеры. Между ними располагалась тонкая эндоплазматическая сеть. В более крупных клетках можно было распознать митозы. Сходная картина наблюдалась в слезных железах.
Автор отмечает, что у этого больного увеличение всех слюнных и слезных желез протекало без признаков воспаления, без выявляемого участия всего организма. Микроскопическое исследование позволило установить, что собственно паренхима желез играет пассивную роль. Увеличение размеров желез обусловлено лишь массивной мелкоклеточной инфильтрацией интерстициальной соединительной ткани, которая скорее всего соответствует лимфа- деноидной ткани. J. Miculicz считает, что заболевание слезных желез не только является самым постоянным, но и возникает раньше других патологических факторов. Общность процесса в слюнных и слезных железах автор объясняет наличием патологического разрастания лимфоидной интерстициальной ткани, которая имеется в тех и других железах. По мнению автора, в описанном наблюдении речь может идти об инфекционном или паразитарном процессе.
В последующие годы в литературе многократно было описано заболевание под названием «болезнь Микулича», при котором основным симптомом было увеличение слюнных и реже слезных желез. Известны случаи заболевания с поражением лимфатического аппарата, селезенки, печени. Заболевание получило ряд новых названий: «синдром Микулича», «симптомокомплекс Микулича», «аллергический ретикулоэпителиальный сиалоз Микулича», «лимфо- миелоидный сиалоз», «лимфоцитарная опухоль» и др. Заболевание стали определять как результат поражения всего лимфатического аппарата, в том числе слюнных и слезных желез, по типу алейкемического (реже лейкеми- ческого) лимфоматоза. Таким образом, этиология и патогенез болезни остаются неизвестными, клиника мало изучена. В настоящее время наиболее вероятной причиной заболевания считают нейротрофические и эндокринные аутоиммунные расстройства.
Клиническая картина заболевания слюнных желез характерна. Припухшие железы плотны, безболезненны, кожа, покрывающая их, в цвете не изменена. Локализация

Рис. 21. Фотографии больной с болезнью Шегрена в клинически выраженной стадии. Определяется увеличение околоушных желез.
следовании околоушных желез в период ремиссии они часто были увеличены, плотны, бугристы, безболезненны (рис. 21). Обычно поражались обе парные железы. Иногда отмечалось увеличение лимфатических узлов, причем больных беспокоил только сам этот факт. Припухлость периодически уменьшалась и увеличивалась; увеличение сопровождалось ухудшением общего самочувствия. Обострение протекало тяжело, с высокой температурой тела, сильными болями, слизисто-гнойным отделяемым из протока. После стихания процесса железы оставались плотными, бугристыми. Обострение чаще наблюдалось с одной стороны. При сиалометрии из околоушных желез справа и слева в среднем получено по 0,6 ±0,2 мл слюны, из поднижнечелюстных — соответственно 0,7 мл справа и 0,3 мл слева. Число функционирующих малых слюнных желез на нижней губе равно 16 ±2. Цитологическое исследование секрета позволило отметить в препаратах клетки слюнных трубок и кубический эпителий.
При радиосиалографии средние показатели концентрационной способности слюнных желез соответствуют нарушению функции II степени (стадия декомпенсации), время МНР укорочено, процент МПР уменьшен. На сканограмме нет четкого изображения околоушных и поднижнечелюстных желез, их изображения сливаются. О площади желез можно судить только при суммарном подсчете изображения обеих желез соответствующей стороны. Контуры желез четкие, но неровные. Штриховка равномерная, иногда с участками выпадения радиоактивности. Нет четкого

Рис. 22. Термовизиограмма той же больной, что на рис. 21, в правой и левой боковых (а, в) и прямой (б) проекциях видны участки гипертермии над околоушными и поднижнечелюстными железами (отчетливо выражен белый цвет). Особенно хорошо они определяются на боковой проекции.
отграничения околоушных и поднижнечелюстных желез от участка повышенной интенсивности изображения в центре (полость рта). В подобных случаях на сканограмме в боковой проекции иногда получается раздельное изображение околоушных и поднижнечелюстных желез, по которому можно определить их площадь.
На эхограмме хорошо определяются листки капсулы, ткань железы акустически неоднородная, с плотными включениями. На термовизиограмме у всех наших больных отмечена гипертермия над околоушными железами (рис. 22). Температура была тем выше, чем более выражено припухание железы. После лечения температура снижалась, но не до нормы.
При сиалографии в железе определяются полости различных размеров, контуры их нечеткие, изображение паренхимы не определяется. Мелкие протоки железы прерывисты, выявляются не везде. Околоушные и поднижнечелюстные протоки имеют неровные, нечеткие контуры (рис. 23, 24). Симптом повышенной проницаемости протоков выражен тем сильнее, чем активнее протекает процесс. На основании сиалограмм можно сделать вывод, что хронический сиаладенит при болезни и синдроме Шегрена протекает как паренхиматозный.
При морфологическом исследовании биоптатов малых

Рис. 23. Сиалограмма левой околоушной железы в боковой проекции больной с болезнью Шегрена в клинически выраженной стадии. Контуры протоков неровные и нечеткие. Контрастная масса проникла через стенки протоков и определяется в виде нечетких, неправильной формы участков за пределами протоков.

Рис. 24. Сиалограмма правой поднижнечелюстной железы той же больной, что на рис. 23. Изменения в поднижнечелюстной железе сходны с таковыми в околоушной.


слюнных желез нижней губы отмечена очагово-диффузная лимфоплазмоклеточная инфильтрация. Концевые отделы дистрофичны, часть из них по периферии содержит слизь; ацинусы вблизи инфильтрата кистозно расширены. Пролиферированный эпителий и миоэпителий нередко закрывают просвет протоков. На фоне лимфоидной инфильтрации часто определяется нарушение целостности базальной мебраны. В некоторых протоках клетки инфильтрата проникают в стенку протока с ее деструкцией. Можно предположить, что указанные морфологические нарушения являются причиной повышения проницаемости стенок протоков для контрастного вещества.
В поздней стадии хронического сиаладенита при болезни и синдроме Шегрена припухлость слюнных желез часто бывает огромной (рис. 25). Больных беспокоит частое обострение сиаладенита. Слизистая оболочка полости рта сухая. В период ремиссии железы плотны, подвижны, безболезненны, кожа над ними истончена. Иног-

Рис. 26. Сцинтиграмма слюнных желез больного с болезнью Шегрена в поздней стадии. В области околоушных и поднижнечелюстных желез в боковых (а, в) и прямой (б) проекциях снижение накопления радионуклида, радиоактивность мало отличаются от фоновой.

Рис. 27. Пантомосиалограмма околоушных желез больной с болезнью Шегрена в поздней стадии. Паренхима и мелкие протоки в железе не определяются. Протоки I порядка и околоушной проток имеют неровные, нечеткие контуры. Контрастная масса выходит за пределы протоков.
протоков вследствие сдавления их лимфоидной тканью на сиалограмме, кроме больших размеров железы, можно выявить нечеткость тени паренхимы. Протоки очень узкие, имеют ровные контуры. Указанные признаки со временем прогрессируют и может наступить период, когда тень паренхимы железы по периферии не будет определяться, поскольку железистые зоны не заполняются контрастным веществом. Контуры протоков железы при этом остаются ровными, но просвет их настолько узок, что на сиалограмме их ход можно проследить лишь с помощью лупы. Описанная рентгенологическая картина слюнной железы при болезни Микулича соответствует тем патологоанатомическим изменениям, которые находят при микроскопическом исследовании слюнных желез.
При генерализованном поражении лимфоидного аппарата, в том числе слезных и слюнных желез, клиническое проявление болезни и результаты специального общего обследования больного позволяют установить признаки лимфогранулематоза. При этом заболевание диагностируют как синдром Микулича. Фактически это опухолевое перерождение лимфоретикулярной системы.
Лечение болезни Микулича представляет большие трудности. Применение, как предлагают некоторые авторы, препаратов мышьяка и калия йодида не приводит к прекращению процесса. Отмечается лишь некоторое улучшение состояния больных. Хорошие результаты дает рентгенотерапия: припухлость желез резко уменьшается или полностью исчезает. Однако эффект лечения нестойкий, часто наступают рецидивы. Мы рекомендуем проведение новокаиновой блокады, применение галантамина, что улучшает трофику тканей и стимулирует секреторную функцию слюнных желез. В случаях хронического воспаления желез, осложняющего течение основного заболевания, следует провести противовоспалительное лечение (введение в протоки железы бактериофага, антибиотиков, компресс с димексидом и др.). В комплекс лечебных мероприятий следует включать также препараты, повышающие неспецифическую резистентность организма: витамины, натрия нуклеинат и др. Кроме того, при лечении больных с синдромом Микулича применяют стероидные препараты. Эти больные должны находиться под наблюдением ревматолога, стоматолога, окулиста, онколога, гематолога и терапевта.
Болезнпь (синдром) Гужеро — Шегрена. Снонимы: ксеродерматоз, синдром Предтеченского — Гужеро —
Шегрена, сухой синдром, синдром Съегрена, болезнь (синдром) Шегрена — заболевание неясной этиологии, характеризующееся сочетанием признаков недостаточности желез внешней секреции: слезных, слюнных, потовых, сальных, слизистых и др.
В 1933 г. Н. Sjogren дал описание симптомокомплекса у 19 больных с сухим кератоконъюнктивитом, а в 1940 г. — у 50 больных. Он отметил жалобы на чувство песка в глазах, светобоязнь, уменьшение секреции слез (даже когда больной плачет, глаза остаются сухими). Кроме того, больных беспокоила сухость слизистой оболочки носа, глотки, гортани. Отмечались разрушение зубов, ахилия, повышение СОЭ, лимфоцитоз. У 80% больных наблюдался полиартрит. Большинство больных составляли женщины, лишь двое из них были мужчины. Полный симптомокомплекс автор наблюдал редко. Как правило, встречались один — два симптома. Полностью развившийся синдром характеризовался: сухим кератоконъюнктивитом, ксеростомией, сухим ринитом, фарингитом, ларингитом и хроническим полиартритом. У женщин отмечалась сухость слизистой оболочки половых органов. В 1925 г. сухой синдром был описан Н. Gougerot и в настоящее время носит имя двух авторов.
Н. Sjogren, изучая морфологию и патогенез, считал, что причиной синдрома являются инфекция или недостаточность витамина А, нарушение функции эндокринных органов, так как чаще болеют женщины в климактерическом периоде. В последнее десятилетие широкое изучение аутоиммунных и ревматических заболеваний позволило выявить у ряда больных хроническим активным гепатитом, тиреоидитом Хашимото, системной красной волчанкой, системной склеродермией, ревматоидным полиартритом признаки сухого синдрома Гужеро — Шегрена. В настоящее время больных с указанным симптомоком- плексом делят на две группы. У одной из них заболевание определяют как синдром Шегрена. Это больные, у которых признаки нарушения функции всех желез внешней секреции возникают при системной красной волчанке, системной склеродермии, ревматоидном полиартрите и других аутоиммунных заболеваниях. У больных второй группы заболевание расценивают как болезнь Шегрена. При той же клинической картине поражения внешнесекреторных желез, характерной для сухого синдрома, у них нет других заболеваний, но имеются иммунологические нарушения, ставящие болезнь Шегрена в ряд заболеваний с аутоим-
мунными нарушениями [Васильев В. И., 1981; Симонова М. В., 1982].
Этиология и патогенез болезни (синдрома) Шегрена изучены мало. Считают, что в развитии патологического процесса играют роль инфекция, эндокринные расстройства, нарушение функции вегетативной нервной системы, иммунного статуса. По-видимому, все эти причины, а не одна из них, имеет значение в возникновении и развитии заболевания.
Развитие сухого синдрома мы представляем себе следующим образом. В организме человека, генетически предрасположенном к данному заболеванию, в результате эмоционального стресса нарушаются функции всех эндокринных желез, что приводит к нарушению обмена в тканях. При этом в слюнных железах повышается проницаемость клеточных мембран. Последнее вызывает задержку выделения в протоки железы образовавшегося в клетках ацинусов секрета. Он переполняет клетку и проникает через ее оболочку в интерстициальную ткань. Белок, претерпевший определенные изменения в клетке ацинуса и предназначенный для выделения с секретом слюнной железы через проток в полость рта, попадая в интерстициальную ткань, играет роль антигена и вызывает образование антител против клеток паренхимы железы. Возникший аутоиммунный процесс вызывает реакцию лимфоидной ткани, ее гиперплазию и деструкцию клеточных элементов паренхимы. Гипосиалия обусловливает проникновение инфекции в железу и развитие хронического сиаладенита. Подобные изменения происходят, по-видимому, во всех железах внешней секреции. Если учесть, что слюнные железы обладают и инкреторной функцией, то можно считать, что патологическое состояние организма усугубляется недостаточностью этой функции.
В пользу высказанного предположения об этиологии и патогенезе болезни Шегрена говорят некоторые клинические наблюдения и исследования, описанные в литературе, а также наши данные. Так, о генетической предрасположенности организма к данному заболеванию можно судить по возникновению сходной патологии слюнных желез у родственников (однояйцевые близнецы, братья, сестры, родители и дети). Стрессовые ситуации очень часто предшествуют развитию болезни Шегрена. О нервных потрясениях перед появлением ксеростомии еще в 1890 г. сообщил A. Seifert. Мы обратили на это внимание 15 лет назад. В настоящее время при целенаправленном
опросе в большинстве случаев (около 90%) удается установить различного характера стрессовые ситуации перед появлением первых признаков болезни.
Стрессоры принято делить на кратковременные и длительно действующие. У одних наших больных раздражителем было внезапное сильное воздействие на эмоциональную сферу. Так, на глазах молодой женщины утонул ее муж. Мужчина, недавно севший за руль автомашины, задавил человека и др. Реакция на эти события выражалась в появлении внезапной сухости полости рта и глаз; в дальнейшем симптомы заболевания нарастали. Многие больные длительное время испытывали в семье или на работе неблагоприятное воздействие на психику (безнадежно больной единственный ребенок в семье, конфликтные ситуации на работе или между супругами и др.).
Мы наблюдали девочку 14 лет с признаками сухого синдрома. Она была единственным ребенком, очень любила своих родителей, которые часто ссорились, и на протяжении нескольких лет оставался нерешенным вопрос о разводе. Девочка была в курсе всех семейных неприятностей. Известно, что у одних людей компенсаторные возможности высоки, и даже значительные по силе раз-
 ДРУ-
ДРУ-
дит в нкции
Шег- нару-
количества спермы. В связи с этим больным назначают гормо
нальную терапию. В некоторых случаях она дает положительные результаты.
Все многообразие изменений в организме при болезни Шегрена и связь этих изменений с патологическим процессом в слюнных железах изучены недостаточно. Морфологическое исследование слюнных желез, проведенное Н. Sjogren на ранней стадии заболевания, подтверждает предположение о возможности роли патологии мембраны клеток паренхимы железы в нарушении внешнесекреторной функции.
В дальнейшем морфологическая картина слюнных желез при синдроме Гужеро — Шегрена описана неоднократно. Отмечено, что изменение больших и малых слюнных желез было сходным [Holm S., 1949; Stanworth А., 1951; Seifert G. et al., 1981; Takeda Y., 1980, и др.]. Вопросами морфологии поднижнечелюстных желез занимались А. М. Солнцев и В. С. Колесов (1981).
Использование электронной микроскопии значительно расширило информацию о морфологии слюнных желез при синдроме Шегрена. Установлено, что инфильтрирующие клетки состоят в основном из лимфоцитов малой и средней величины, плазменных клеток и гистиоцитов. Найденные большие лимфоциты рассматриваются как Т-лимфоциты. Обнаружено повреждение клеток паренхимы с нарушением процесса образования и выделения секрета. Некоторые клетки полностью разрушались и их содержимое изливалось в просвет миоэпителиальных клеток, которые были более резистентны к дегенеративным изменениям. В протоках отмечены эпителиальная пролиферация, метаплазия и инфильтрация плазматических клеток и лимфоцитов. Базальные пластинки протоков и долек железы были изменены [Takeda Y., 1980].
Патогномоничным признаком для синдрома Шегрена считают пролиферацию миоэпителия и образование эпи- миоэпителиальных островков на фоне выраженной лимфоидной инфильтрации стромы. С внедрением иммуно- флюоресцентной техники в морфологические исследования появилась возможность идентифицировать природу лимфоцитов, составляющих инфильтрат малых слюнных желез при синдроме Шегрена. Инфильтраты могут состоять как из Т-, так и из В-лимфоцитов [Talal N. et al., 1974].
Повышенная проницаемость мембран * клеток железистой паренхимы и протоков слюнных желез хорошо определяется на сиалограммах, где видно проникновение контрастного вещества за пределы протоков и ацинусов
в интерстициальную ткань. Рассасывание этого контраста можно обнаружить при динамическом рентгенологическом наблюдении за слюнными железами. Повышение проницаемости мембран, по-видимому, действительно играет не последнюю роль в механизме снижения секреторной функции слюнных желез. Это подтверждается нашими клиническими наблюдениями.
По поручению Г. А. Васильева на кафедре пропедевтики хирургической стоматологии ММСИ П. М. Егоровым проведена работа, в которой было предусмотрено при комплексном лечении больных интерстициальным паротитом применение электрофореза с лидазой и ронидазой с целью предупреждения склерозирования ткани железы. При лечении 22 больных отмечена тенденция к снижению функции железы. У 2 больных возникла асиалия; при этом сухость в полос+и рта напоминала состояние при синдроме Гужеро — Шегрена. До лечения функция слюнных желез была нормальной. В дальнейшем, после новокаиновой блокады, функция желез восстановилась полностью. Если учесть, что препараты лидазы и ронидазы повышают проницаемость мембран, то надо полагать, что асиалия, возникшая у больных при их применении, явилась результатом повышения проницаемости клеточных мембран ткани железы. Не исключено, что подобный механизм нарушения слюноотделения имеет место и при сухом синдроме. В подтверждение этого предположения можно привести еще клинические наблюдения за больными с синдромом Шегрена, находившимися на лечении в нашей клинике.
Применение галантамина как препарата, повышающего функцию всех пищеварительных желез, у больных с идиопатической ксеростомией дало положительные результаты. Мы решили применить его у больных с синдромом Шегрена. При неактивном течении процесса, когда сиало- графически не отмечается повышенная проницаемость железы, галантамин дает положительные результаты. Однако у 2 больных с активным течением процесса и высокой проницаемостью ткани в отношении контрастного вещества лечение галантамином привело к осложнениям. У одного больного возникли боли распирающего характера, усиливающиеся во время еды, железы увеличились и уплотнились. При пункции желез получена мутная слюна в большом количестве. У второй больной в о^ ной из желез образовались две кисты, были
удалены хирургическим путем.
Наблюдения позволили нам предположить, что при синдроме Шегрена функция образования секрета в клетках паренхимы нарушается не в первую очередь; вначале нарушается выделительная и эвакуаторная функция железы. Надо полагать, что это происходит вследствие повышения проницаемости клеточных мембран. Возможность образования секрета в клетках ацинусов в начале заболевания синдромом Шегрена длительное время сохраняется. Это подтверждено неоднократно проведенными морфологическими исследованиями, в которых указано на переполнение клеток паренхимы секреторными гранулами.
Изучение ультраструктуры малых слюнных желез [Talal N., 1974] позволило установить расширение межклеточных пространств и выход содержимого ацинарной клетки через базальную часть дольки в просвет миоэпи- телиальной клетки. Под нашим руководством проведена работа [Перминова И. С., 1982], в которой ультраструк- турные изменения в малых слюнных железах изучены в зависимости от стадии процесса и установлено, что в начальной стадии секреторная активность клеток не нарушена и снижение выделения через проток секрета связано с явлениями реабсорбции его, что подтверждается расширением межклеточных пространств и нарушением микроциркуляторного русла.
В настоящее время доказано наличие аутоиммунного процесса в патогенезе сухого синдрома. Аутоиммунные нарушения проявляются повышением титров циркулирующих антител к эпителию слюнных и слезных желез, тиреоглобулина, ревматоидных факторов, а также отложением иммунных комплексов в пораженных тканях, включающих IgM, IgG, С3-компонент комплемента [Denko С., Schearn М., 1971; Anderson L. et al., 1972]. Это положение подтверждается и патоморфологической картиной болезни, основу которой составляет лимфоплазматическая инфильтрация, замещающая в поздней стадии заболевания паренхиму слюнных и слезных желез.
Массивность лимфоидной инфильтрации слюнных желез на фоне лимфаденопатии даже заставляет думать о возможном переходе доброкачественного лимфопролиферативного процесса в лимфомы и в дальнейшем трансформацию в лимфосаркому [Talal N. et al., 1967; Whaley К. et al., 1968; Cummings N. et al., 1971].
Последние исследования, проведенные в Научно-исследовательском институте ревматологии АМН СССР, не только свидетельствуют о наличии аутоиммунного процесса, но и позволяют на основании иммунологического статуса выделить группы больных с различным клиническим течением процесса (болезнь Шегрена, синдром Шегрена, активное течение заболевания).
Клиника. Патологические проявления при болезни (синдроме) Шегрена со стороны слюнных желез многообразны. Это зависит от сочетания изменений слюнных желез с поражением других органов и тканей (органы пищеварения, глаза, эндокринные железы, суставы, соединительная ткань и др.), стадии процесса (начальной, клинически выраженной, поздней), активности клинического течения и лабораторных показателей (активное и неактивное течение).
По нашим данным, в стоматологических клиниках, занимающихся данной патологией, больные с болезнью (синдромом) Шегрена составляют 27% от числа больных с сиалозами различного происхождения. Большинство больных составляли женщины. Более половины было в возрасте старше 50 лет, около одной трети — от 30 до 50 лет; детей было двое. Последние годы мы стали диагностировать болезнь (синдром) Шегрена в более молодом возрасте, что связано с накоплением опыта и совершенствованием методов специального обследования и диагностики заболеваний слюнных желез.
При целенаправленном обследовании больных в клинике Научно-исследовательского института ревматологии АМН СССР М. В. Симоновой выявлены больные с синдромом Шегрена в молодом возрасте. К моменту появления первых признаков заболевания средний возраст больных составил 27'/2 года, к моменту обследования — 361 /2 года. Эти данные говорят о том, что на протяжении многих лет болезнь не была диагностирована, по-видимому, в связи с тем, что первые ее проявления не сильно беспокоили больных и они не обращались к врачу или, обратившись в какую-либо клинику (в зависимости от первых симптомов болезни — в стоматологическую, офтальмологическую, оториноларингологическую, ревматологическую, гинекологическую, терапевтическую и др.), подвергались лечению только по поводу патологических симптомов соответственно профилю учреждения. Общее заболевание оставалось недиагностированным.
В стоматологических лечебных учреждениях у больных преобладали симптомы поражения слюнных желез и полости рта. Больные жаловались на общую слабость, быструю утомляемость, сухость полости рта, периодически
эазвивающееся воспаление околоушных желез. Не всегда заболевание впервые проявлялось сухостью полости рта.
Иногда вначале появлялись сухость глаз, светобоязнь, чувство песка в глазах, а затем увеличение околоушных и редко поднижнечелюстных желез. Иногда больные указывали, что находятся на учете у ревматолога по поводу заболевания суставов, системной красной волчанки или склеродермии.
Сухость полости рта больные не всегда связывали с общим заболеванием, по поводу которого они обратились к врачу; она выявлялась лишь при опросе. Нередко больные говорили о том, что они любят запивать пищу, или отмечали, что в последние годы стали разрушаться зубы, беспокоит чувство жжения слизистой оболочки языка, губ, неба. В дальнейшем при обследовании была установлена ксеростомия в начальной или даже клинически выраженной стадии. У небольшого числа больных жалобы были характерны для паренхиматозного паротита и лишь спустя несколько лет выявлялась болезнь Шегрена. У одной больной, которую мы впервые обследовали в возрасте 8 лет, лишь в 18 лет были установлены все признаки болезни Шегрена. Двух женщин мы длительное время лечили с диагнозом паренхиматозного паротита. Клинически признаки болезни Шегрена проявились лишь через 8—12 лет.
Из перенесенных и сопутствующих заболеваний больше отмечали анацидный и гипацидный гастрит, хронический колит, хронический гепатит, острый и хронический полиартрит, тиреотоксикоз, невроз, неврастению, склероз сосудов мозга, заболевания сердечно-сосудистой и дыхательной систем. У всех больных при обследовании слюнных желез мы обнаружили сиаладенит.
В начальной стадии сиаладенита при болезни (синдроме) Шегрена больные жалуются на незначительное уплотнение, чаще околоушных, реже поднижнечелюстных желез, распирающие ощущения во время еды; они тем сильнее, чем активнее протекает заболевание. При неактивном течении процесса уплотнения в области железы может не быть или оно совсем не беспокоит больного. Лишь изредка появляется обострение, повышается температура тела, появляется разлитая припухлость в области железы, полностью прекращается выделение слюны. Из протока может появиться гной. На протяжении 7—10 дней воспалительные явления постепенно стихают. В период ремиссии припухлость иногда не определяется. У таких больных на основании дополнительных исследований можно диагностировать сиаладенит. Даже если процесс обостряется только в одной железе, в другой обнаруживается скрыто протекающий воспалительный процесс.
При сиалометрии из правой околоушной железы в среднем выделяется 1,9 ±0,4 мл, а из левой 1,7 ±0,2 мл секрета, из поднижнечелюстных — соответственно 2,2 ±0,2 и 1,8 ±0,2 мл. Число функционирующих малых слюнных желез на 4 см2 слизистой оболочки нижней губы 15 ±4. Цитологическое исследование секрета позволило установить повышенное слущивание клеток плоского и цлиндри- ческого эпителия. При раДиосиалографии средние показатели концентрационной способности слюнных желез соответствуют нарушению функции железы I степени (компенсаторная стадия), время МНР и МПР удлинено, процент МПР увеличен.
При сканировании изображение околоушных желез имеет неравномерную штриховку. Поднижнечелюстные железы увеличены. Изображение полости рта четкое, с интенсивной частой штриховкой. Ультразвуковая биолокация произведена нами у больного 72 лет. Околоушные железы на эхограмме были уменьшены, содержали преимущественно плотную ткань, листки капсулы просматривались не везде. При термовизиографии изменения температуры в области слюнных желез не отмечено. При лечении термодинамика также не выявляется.
При сиалографии и пантомосиалографии отмечена повышенная проницаемость протоков для контрастного вещества, в связи с чем изображение паренхимы неравномерное. Контуры протоков нечеткие, вокруг них определяется «облачко» контрастной массы, проникшей в интерстициальную ткань, которое рассасывается на протяжении недели. При биопсии малых слюнных желез нижней губы в концевых отделах обнаруживаются дистрофические процессы (переполнение ацинусов слизью, кистозная перестройка). Лимфоидный инфильтрат представлен небольшими скоплениями клеток или очаговой перидуктальной инфильтрацией. В отдельных внутридольковых протоках имеет место деструкция стенки на фоне инфильтрата [Симонова М. В., 1982].
В клинически выраженной стадии болезни (синдрома) Шегрена больные, находившиеся под нашим наблюдением, жаловались на сухость полости рта, разрушение зубов, припухание околоушных желез, периодически появляющееся обострение сиаладенита. При об- да увеличены лимфатические регионарные узлы; они тоже подвижны и безболезненны. Секрет из протоков не выделяется. При массировании железы может выделиться небольшая слизистая пробка. У большинства больных зубов нет. Они с трудом могут пользоваться съемными протезами, так как слизистая оболочка рта очень ранима. Если больной может привыкнуть к съемному протезу, то он испытывает облегчение и в отношении сухости полости рта.
При сиалометрии из околоушных и поднижнечелюстных протоков слюна через канюли не выделяется. Число малых слюнных желез на нижней губе, по средним данным, равно 12±2. При цитологическом исследовании слизистого отделяемого из протоков определяются бокаловидные клетки, пласты воспалительно измененного эпителия, а также клетки воспалительного экссудата. При радиосиа- лографии можно установить, что слюнные железы не концентрируют радиоактивное вещество.
При сканировании изображения слюнных желез получить не удается в связи с тем, что концентрационная способность паренхимы резко снижена или отсутствует. Сходные изменения определяются на сцинтиграмме (рис. 26).
На эхосиалограмме внутренний листок капсулы определяется не везде. Средние показатели акустически плотной ткани в железе при всех положениях одномерного датчика составляют 59,4 ±3,5%. Отмечено, что склерозируются преимущественно задненижние отделы железы, где определяется 78,5 ± 5,8% акустически плотной ткани (в области передневерхних отделов 36,6 + 5,8%).
При термовизиографии наблюдается значительная гипертермия над увеличенными околоушными железами. У больных без увеличения желез гипертермия выражена в меньшей степени. При сиалографии паренхима железы не контурируется, полостей, характерных для клинически выраженной стадии, нет. Мелкие протоки железы не определяются; протоки I—III порядков и околоушной проток имеют нечеткие контуры, на некоторых участках они не определяются из-за попадания контрастной массы в интерстициальную ткань (рис. 27). При повторной рентгенографии можно проследить рассасывание контрастного вещества, иногда его следы выявляются через 2— 3 нед.
Морфологически определяется очагово-диффузная или диффузная лимфоплазмоклеточная инфильтрация малых
слюнных желез. В одних дольках сильнее выражены процессы склероза, а в других — лимфоидная инфильтрация; при этом архитектоника долек сохраняется. На фоне инфильтрата, заместившего паренхиму, в результате процессов пролиферации эпителия и миоэпителия на месте прекративших существование протоков образуются миоэпите- лиальные островки.
Диагностика поражения слюнных желез при болезни и синдроме Шегрена основывается на местных характерных клинических признаках: припухании железы, снижении функции, сиалографических симптомах хронического паренхиматозного паротита. При этом отмечается повышение проницаемости протоков для контрастного вещества. Мы наблюдали симптом увеличения парной околоушной железы в ответ на сиалографию, произведенную с противоположной стороны, и рассматриваем его как характерный для активного течения болезни и синдома Шегрена.
Помимо местного обследования, для подтверждения диагноза необходимо произвести исследование внутренних органов. При болезни Шегрена поражаются глаза. По данным Ю. В. Юдиной (1975), в начальной стадии заболевания отмечены явления блефароконъюнктивита и снижение секреции слезных желез первой степени (основной секреции на 2—3 мг, общей — на 5—6 мг при норме: основная секреция правого глаза 12,0 ±0,6, левого глаза 13,0±0,6 мг, общая 28,0±1,0 мг). В клинически выра
