ВНУТРЕННЯЯ РЕГУЛЯЦИЯ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
В 70—80-е годы В. Д. Беляковым с сотрудниками при изучении антропонозов были впервые описаны механизмы внутренней регуляции эпидемического процесса. На этой основе обобщены многочисленные материалы, накопленные к тому времени в науках, изучающих инфекционную патологию, и разработана теория саморегуляции паразитарных систем.
Значение теории для эпидемиологии состоит не только в том, что и в этой науке была сформулирована концепция саморазвития. Наиболее существенным является вскрытие механизмов саморегуляции. В теории выделены четыре положения, объясняющие эти механизмы:
1) генотипическая и фенотипическая гетерогенность популяций паразита и хозяина по признакам отношения друг к другу;
2) взаимообусловленная изменчивость биологических свойств взаимодействующих популяций;
3) фазовая самоперестройка популяций паразита, определяющая неравномерность развития эпидемического процесса;
4) регулирующая роль социальных и природных условий в фазовых преобразованиях эпидемического процесса.
Гетерогенность популяций паразита и хозяина. Универсальным свойством всех живых существ является их генотипическая и фенотипическая гетерогенность, т. е. внутрипопуляционная качественная неоднородность особей.
Внутрипопуляционная вариабельность свойств популяций возбудителей выявляется при их сопоставлении между субпопуляциями, в том числе между
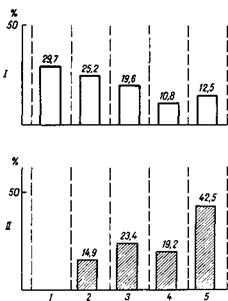
Рис. 8. Доля людей с различной частотой ОРЗ (I) и доля случаев заболеваний в выделенных группах (II) [Беляков В. Д., 1976].
1 — не болели; 2 — болели 1 раз; 3 — болели 2 раза; 4 — болели 3 раза; 5 — болели 4 и более раз.
 клонами, штаммами, изолятами. Фенотипические различия генотипически детерминированы, «поскольку степень и направление допустимой пластичности фенотипа определяются генотипическими факторами» (Майр, 1974). В эпидемиологии неоднородность популяций паразита и хозяина анализируется в пределах свойств, в наибольшей степени отражающих отношение друг к другу. Мерой патогенности является вирулентность. В естественных условиях вирулентность субпопуляций определяется тяжестью течения заболеваний. В лабораторных условиях она измеряется действием на подопытных животных и культуры ткани или по специально отобранным признакам, корреляция которых с вирулентностью установлена заранее. Выявлена неоднородность популяций возбудителей также по признакам контагиозности и иммуногенности. Наиболее доступными для анализа гетерогенности популяций микроорганизмов являются признаки, обнаруживаемые в лабораторных условиях. Это нашло отражение в выделении вариантов циркулирующих микроорганизмов (серовар, фаговар, антибиотиковар, хемовар и т. д.).
клонами, штаммами, изолятами. Фенотипические различия генотипически детерминированы, «поскольку степень и направление допустимой пластичности фенотипа определяются генотипическими факторами» (Майр, 1974). В эпидемиологии неоднородность популяций паразита и хозяина анализируется в пределах свойств, в наибольшей степени отражающих отношение друг к другу. Мерой патогенности является вирулентность. В естественных условиях вирулентность субпопуляций определяется тяжестью течения заболеваний. В лабораторных условиях она измеряется действием на подопытных животных и культуры ткани или по специально отобранным признакам, корреляция которых с вирулентностью установлена заранее. Выявлена неоднородность популяций возбудителей также по признакам контагиозности и иммуногенности. Наиболее доступными для анализа гетерогенности популяций микроорганизмов являются признаки, обнаруживаемые в лабораторных условиях. Это нашло отражение в выделении вариантов циркулирующих микроорганизмов (серовар, фаговар, антибиотиковар, хемовар и т. д.).
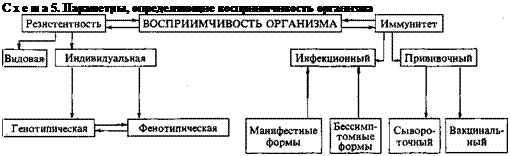
В эпидемиологии длительное время бытовало неверное представление о всеобщей универсальной восприимчивости населения к отдельным возбудителям. В действительности же имеет место вариабельность степени восприимчивости к заболеванию у отдельных индивидуумов. Она выражается, в частности, в характерном распределении часто и редко болеющих людей (рис. 8). Степень восприимчивости определяется резистентностью и иммунитетом (схема 5).
Резистентность (лат. гез181еге — сопротивляться) характеризует степень восприимчивости отдельного организма, не имевшего до того встречи с возбудителем; она наследственно детерминирована и носит генотипический ха
рактер. Распределение индивидуумов популяции по степени резистентности к отдельным возбудителям достаточно стандартно. Оно закреплено в генофонде популяции хозяина, причем организм, высоковосприимчивый к одному возбудителю, может оказаться достаточно резистентным к другому. Таким образом, экологическая ниша каждого конкретного возбудителя-паразита определяется не только его тропностью к определенным органам и тканям, но и приуроченностью к определенным особям гетерогенной популяции хозяина.
Генетически закрепленные характеристики резистентности людей к возбудителям инфекционных заболеваний уточняются в процессе развития организма в связи как с возрастными изменениями, так и под влиянием факторов внешней среды. Следовательно, фактическое распределение популяций людей по признаку резистентности является не только генотипическим, но и фенотипическим.
Фенотипический вклад в фактическое распределение популяции людей по степени восприимчивости к возбудителям инфекционных заболеваний усиливается за счет процессов иммунизации. При этом следует иметь в виду, что способность организма к выработке иммунитета также генотипически детерминирована. В организме одних людей наблюдается выработка напряженного и длительно сохраняющегося иммунитета. В организме других людей вырабатывается менее напряженный и непродолжительный иммунитет. Относительно специализированный характер распределения людей по способности вырабатывать иммунитет проявляется в том, что при прививках ассоциированными вакцинами нередко наблюдается высокий иммунизационный эффект к одному антигену и слабый к другому, причем распределение ответов неодинаково у разных людей.
Целесообразно дифференцировать диапазон, степень и характер гетерогенности популяций паразита и хозяина по каждому из анализируемых признаков (табл. 20).
Таблица 20. Показатели гетерогенности популяций и их содержание
|
Разные популяции возбудителей антропонозов, приуроченные к определенным территориям, социальным, бытовым и возрастным группам людей, в каждый данный момент неодинаковы по степени и характеру гетерогенности. В соответствии с этим можно говорить о втором уровне гетерогенности, который в отличие от внутрипопуляционной гетерогенности является межпопуляционным. Он характеризует пространственную гетерогенность популяций вида.
 |
Изменчивость популяций паразита и хозяина при их взаимодействии. В микробиологии постепенно накапливались факты об изменчивости микроорганизмов в лабораторных условиях их изучения. Наряду с этим в различной эпидемической обстановке от больных и носителей выделяли измененные формы микроорганизмов, которые получили название «атипичных штаммов». Результаты иммунологических исследований не согласовывались с эпидемиологическими представлениями о «всеобщей восприимчивости населения» к возбудителям инфекционных болезней. Клинические наблюдения свидетельствовали об изменениях тяжести течения заболеваний в ходе эпидемии. Все эти наблюдения требовали нового эпидемиологического объяснения.
При исходном рассмотрении эпидемического процесса как популяционного взаимодействия паразита и хозяина стало ясно, что генотипическая и фенотипическая неоднородность популяций хозяина по степени восприимчивости к возбудителям инфекционных заболеваний определяет неодинаковые условия жизнедеятельности возбудителей в организме отдельных индивидуумов. Генотипическая и фенотипическая неоднородность популяций паразитов-возбудителей — приспособительный признак, обеспечивающий их адаптацию к разнообразным условиям среды обитания. В целом же генотипическая и фенотипическая неоднородность популяций паразита и хозяина— материальная основа эволюционно сформировавшейся саморегуляции паразитарных систем.
В адаптации паразитов как сформировавшихся биологических видов к среде обитания принимают участие те же типы отбора, что и в эволюционном процессе видообразования. Из трех типов отбора наибольшее значение имеет направленный и стабилизирующий отбор. Действию направленного отбора предшествует генерация гетерогенности относительно гомогенной до того популяции возбудителя на начальных этапах изменения среды обитания.
Для микропопуляции возбудителя такие условия создаются в ходе инфекционного процесса, заканчивающегося выздоровлением больного и развитием постинфекционного иммунитета (рис. 9). В разгар инфекционного процесса по мере формирования иммунитета в организме больного начинает увеличиваться гетерогенность микропопуляции возбудителя, состоящей до того из вирулентных вариантов. В организме реконвалесцента происходит постепенное освобождение иммунного организма от вирулентного возбудителя и отбор из гетерогенной микропопуляции маловирулентных вариантов (дифференциальное выживание). Последние закрепляются стабилизирующим отбором в условиях новой среды обитания. Соответственно наступает относительная гомогенизация микропопуляции возбудителя в иммунном организме, характеризующемся носительством.
Фактические материалы, иллюстрирующие процесс изменчивости стрептококка группы А в эпидемическом процессе, показаны на рис. 10. Обследование коллектива, где изучался эпидемический процесс, было начато через 10 дней после его формирования. Через месяц после формирования коллектива, в течение которого увеличивалась вирулентность стрептококка и отбирался ведущий серовар, появились первые больные. Число их постепенно нарастало параллельно с нарастанием вирулентности возбудителя, а затем и массивно-
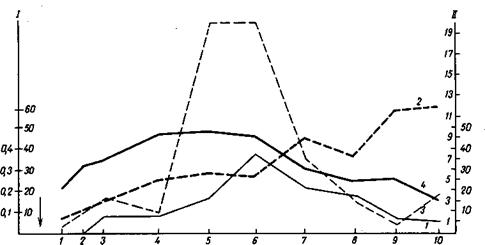
Рис. 10. Изменение вирулентности стрептококка группы А в ходе эпидемического процесса [Ходырев А. П., Беляков В. Д., 1988]. На оси абсцисс — очередность обследования в период с 10.11 по 11.05 (стрелкой указано время формирования коллектива); на оси ординат — шкала I: слева — показатели уровня заболеваемости ангиной (1), справа — доля носителей стрептококков группы А (2); шкала II: слева — медиана величины стрептококковых очагов у носителей в тысячах колониеобразующих единиц (3), справа — средняя вирулентность стрептококков по величине частично очищенного М-белка в микрограммах на 109 стрептококков (4). |
сти очагов в организме носителей. Характерно, что снижение вирулентности стрептококка в циркулирующей популяции началось раньше пика заболеваемости, т. е. в период нарастания иммунной прослойки. Это предопределило снижение заболеваемости и постепенное формирование маловирулентного варианта возбудителя в организме носителей с относительно небольшой величиной микробных очагов. Количество таких носителей постепенно возрастало.
До установления факта снижения вирулентности возбудителей под действием иммунологического процесса угасание эпидемии до исчерпания прослойки восприимчивых при действующем механизме передачи возбудителя считалось «эпидемиологическим парадоксом». Выявленная изменчивость возбудителя под влиянием меняющейся среды обитания в организме хозяина объясняет это явление.
Фазовая самоперестройка популяций паразита. Неравномерность проявлений эпидемического процесса в отдельных территориальных, социальных, возрастных и бытовых группах населения объясняется относительной автоном-
 |
Рис. 12. Динамика основных характеристик эпидемического процесса менингококковой инфекции в организованных коллективах [Ефимов Е. И., 1988].
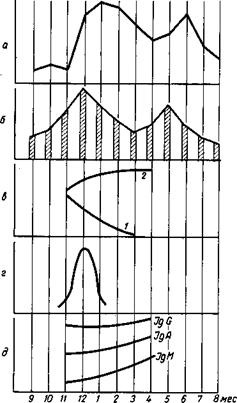 а — заболеваемость (анализ 1400 историй болезни); б — тяжесть течения заболеваний (% тяжелых и средних форм); в — серологическая структура менингококков (в %): 1 — группа А; 2 — политипажные; г — биохимическая активность менингококков (в %); д — концентрация иммуноглобулинов, мг/100 мл.
а — заболеваемость (анализ 1400 историй болезни); б — тяжесть течения заболеваний (% тяжелых и средних форм); в — серологическая структура менингококков (в %): 1 — группа А; 2 — политипажные; г — биохимическая активность менингококков (в %); д — концентрация иммуноглобулинов, мг/100 мл.
ностью его развития, а неравномерность проявлений во времени, характеризующаяся сменой эпидемических и межэпидемических периодов, — внутренними преобразованиями в паразитарной системе. Схематически в жизненном цикле популяции возбудителя можно выделить четыре фазы: 1) резервации, 2) эпидемического преобразования, 3) эпидемического распространения и 4) резерваци- онного преобразования. Качественные и количественные характеристики популяции возбудителей на разных фазах их жизненного цикла не совпадают полностью с фазами развития эпидемического процесса. Фазовые преобразования в популяции возбудителя опережают эпидемиологические проявления. На примере инфекций, вызываемых возбудителями, фазовая самоперестройка которых определяется инфекционноиммунологическими взаимоотношениями, принципиальная схема происходящих изменений показана на табл. 21 и рис. 11. При каждой нозологической форме инфекционной болезни действительные фазовые преобразования в системе имеют те или иные отклонения от принципиальной схемы. Они строго индивидуальны и определяются эволюционно выработанными и заложенными в генофонде взаимодействующих популяций потенциями.
На рис. 12 представлены материалы, иллюстрирующие фазность развития менингококковой инфекции. При анализе заболеваемости генерализованными формами менингококковой инфекции в организованных коллективах взрослых было выявлено, что первые случаи болезни появлялись, как правило, через 1—2 мес после формирования коллективов и заболеваемость стремительно нарастала в последующие 3-й и 4-й месяцы. Максимум тяжелых форм регистрировался за 1 мес до пика сезонных эпидемий. В это время отмечалась наивысшая ферментативная активность менингококков и высокая доля менингококков серогруппы А. Затем наблюдалось стремительное снижение менингококков серогруппы А и рост полиагглютинабельных менингококков, которые ферментативной активностью не обладали. Заболевания связывались только с менингококком группы А. Увеличение доли полиагглютинабельных, лишенных ферментативной активности менингококков, сопровождавшееся снижением тяжести течения заболеваний, а затем и уменьшением заболеваемости, происходило на фоне нарастающего коллективного иммунитета. Фазность развития эпидемического процесса за счет внутренних регуляторных механизмов подтверждается и тем, что заболевания генерализованны-
| Фаза | Среда обитания | Соответствие среде обитания | Степень
гетерогенности |
| Резервация | Иммунные организмы хозяина
V |
Соответствует | Относительная гомогенность |
| Эпидемическое преобразование | Пассаж (начало) через восприимчивые особи хозяина. Иммунологический след | Не соответствует | Г енерация гетерогенности с последующей гомогенизацией |
| Эпидемическое распространение | Восприимчивые организмы. Нарастание коллективного иммунитета | Соответствует | Относительная гомогенность |
| Резервационное преобразование | Пассаж через иммунные особи | Не соответствует | Генерация гетерогенности с последующей гомогенизацией |
ми формами менингококковой инфекции с этиологическим участием менингококков серогруппы А возникали в периоды, когда циркуляцию этой серогруппы не обнаружили в течение времени, превышающего продолжительность инкубационного периода в 5 — 6 раз, а занос возбудителя извне полностью исключался условиями существования коллектива.
Регулирующая роль социальных и природных условий в фазовых преобразованиях эпидемического процесса. Фазность развития эпидемического процесса -»результат эволюционно приобретенных внутренних перестроек популяций паразита и хозяина в меняющихся социальны^ и природных условиях их взаимодействия. Многообразие выработанных экологических связей разных видов возбудителей предполагает и многообразие конкретных социальных и природных условий, регулирующих фазовые преобразования паразитарных систем. При инфекциях, регулируемых инфекционно-иммунологическими взаимоотношениями, общим фактором, определяюйцим переход фазы резервации к фазе становления эпидемического варианта возбудителя, является ослабление популяционного иммунитета в цепи циркуляции возбудителя, а от фазы эпидемического распространения к фазе становления резервационного варианта — нарастание популяционного иммунитета.
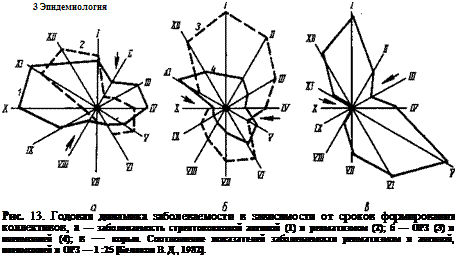
Социальные и природные условия, определяющие фазность развития эпидемического процесса при этих инфекциях, можно объединить в три обобщающие группы: а) факторы, определяющие различные формы /«перемешивания» людей: формирование коллективов, естественные и искусственные миграции (рис. 13); б) факторы, определяющие активизацию механизма передачи возбудителя (рис. 14); в) факторы, снижающие иммунитет и резистентность (рис. 15). Любые из перечисленных условий приводят в конечном счете к возрастанию прослойки высоковосприимчивых организмов в цепи циркуляции возбудителя, что является сигналом к перестройке внутренней организации его популяции. С другой стороны, иммунизация коллектива и проведение мероприятий, снижающих активность механизма передачи возбудителя, уменьшают прослойку высоковосприимчивых организмов в цепи циркуляции возбудителя и являются условием формирования резервационного варианта возбудителя.
| Тип отбора | Вирулентность | Численность | Проявление эпидемического процесса |
| Стабилизи
рующий |
Низкая | Низкая, стабильная | Конец эпидемического (сезонного) спада заболеваемости и основная часть межэпидемического (межсезонного) периода |
| Направлен
ный |
Нарастающая | Увеличивающаяся (дифференциальное выживание) | Предэпидемический (предсезонный) период |
| Стабилизи
рующий |
Высокая | Высокая,, увеличивающаяся | Эпидемический (сезонный) подъем заболеваемости |
| Направлен
ный |
Снижающаяся | Уменьшающаяся (дифференциальная гибель) после достижения максимальной численности | Вершина эпидемического сезонного подъема и период спада заболеваемости |
|
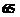
|
||
Основными факторами, определяющими скорость формирования эпидемического варианта возбудителя и его вирулентный потенциал, являются численность вновь сформировавшегося коллектива и активность механизма передачи возбудителя, т. е. в конечном счете количество восприимчивых лиц в цепи циркуляции возбудителя за единицу времени. В результате интенсивные показатели заболеваемости неодинаковы в коллективах разной численности: заболеваемость выше в коллективах большей численности (рис. 16). Большие спальные комнаты в общежитиях, пионерских лагерях и других оз-
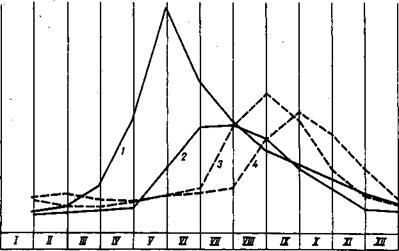
Рис. 14. Годовая динамика заболеваемости дизентерией Флекснера (средние данные за 1958-1964 гг.) 1 — в Ашхабаде; 2 — в Самарканде; 3 — в Караганде; 4 — в Ленинграде [Беляков В. Д., 1976]. |
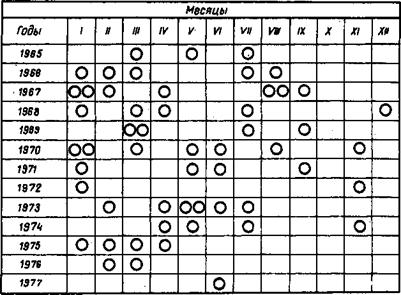
Рис. 15. Вспышки ОРЗ среди участников советских антарктических экспедиций (по материалам ВНИИ гриппа М3 СССР), Светлыми кружками обозначены вспышки заболеваний, связанные с внешними контактами, красными — вспышки заболеваний в период полной изоляции. |
доровительных учреждениях — один из основных неблагоприятных эпидемиологических факторов.
При других группах инфекций5 эволюционно сформировались иные пусковые механизмы фазовых преобразований популяций. Однако любая саморегуляция — это ответная реакция на регуляцию. Эпидемии развиваются там и тогда, где и когда создаются сначала социальные и (или) природные усло-
бб
Рис. 16. Уровни заболеваемости ангиной при различной численности формируемых коллективов (при равных условиях размещения) [Беляков В. Д., Ходырев А. П., 1987].
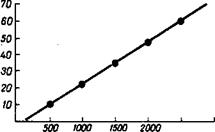 На оси ординат — уровень заболеваемости в условных единицах, на оси абсцисс — численность формируемых коллективов.
На оси ординат — уровень заболеваемости в условных единицах, на оси абсцисс — численность формируемых коллективов.
вия, стимулирующие переход от фазы резервации возбудителя к фазе эпидемического распространения за счет внутренних механизмов саморегуляции, а затем условия, способствующие распространению вирулентного возбудителя. Подлинная профилактика эпидемий основывается на знании границ адаптационной изменчивости популяций возбудителя, резервов саморегуляции на управляющие воздействия.
Познание внутренних механизмов развития эпидемического процесса позволяет предвидеть возможные эпидемиологические последствия тех или иных социальных и природных изменений и, что особенно важно, найти в сложной цепи причинно-следственных отношений такие звенья, на которые можно повлиять имеющимися средствами профилактики и тем самым предотвратить возможные неблагоприятные последствия социальных и природных явлений: не допустить внутренних перестроек популяции возбудителя с формированием вирулентного варианта и его распространения.
Универсальность положений теории саморегуляции паразитарных систем. Основные положения теории саморегуляции паразитарных систем являются универсальными независимо от вида хозяина и природы возбудителя-паразита. Поэтому они в равной мере применимы при рассмотрении не только проблем эпидемиологии, но и проблем эпизоотологии, а также инфекционной фитопатологии. Конкретные механизмы саморегуляции строго индивидуальны. Они вскрыты при антропонозных инфекциях, эпидемический процесс при которых регулируется инфекционно-иммунологическими взаимоотношениями популяций паразита и хозяина. Холерный же вибрион резервируется, очевидно, во внешней среде.
Медицинское значение имеют проблемы саморегуляции эпизоотического процесса, в котором участвуют возбудители, опасные для человека. Фазность развития эпизоотического процесса обеспечивает сохранение возбудителей зоонозов как биологических видов и в то же время определяет их эпидемиологическое значение. Заражение людей происходит при их контакте с очагами в фазу эпизоотического распространения возбудителя, когда он характеризуется наиболее выраженной вирулентностью. Следовательно, механизм развития эпидемического процесса при зоонозах связан с механизмом развития эпизоотического процесса, определяющего резервуар возбудителя и его эпидемиологический потенциал, а также социальными условиями, определяющими контакт людей с очагами заболеваний.
Фазовые преобразования популяций сапронозов происходят при смене са- профитической и паразитической фаз жизнедеятельности. Здесь также обнаружено существование эпидемических и резервационных вариантов возбудителя.
Вопросы для самостоятельной работы.
1. - Изложите эволюцию взглядов на механизм развития эпидемического процесса. Какие совре- менные теоретические обобщения эпидемиологии используются для раскрытия механизма развития эпидемического процесса? 1
2. Дайте определение понятиям «механизм передачи», «стадии механизма передачи», «факторы передачи», «пути передачи», «источник инфекции», «резервуар инфекции». Иллюстрируйте ответ примерами.
3. На конкретных примерах укажите, как первичные факторы передачи сопряжены с первой ста
дией механизма передачи, а конечные факторы — с третьей стадией механизма передачи. Какие, по Вашему мнению, факторы передачи могут выполнять роль одновременно первичных, промежуточных и конечных, а какие не могут? Как Вы понимаете отнесение факторов передачи к специфическим и неспецифическим? Сопоставьте с понятиями «специфический и неспецифический хозяин» паразита.
4. Сформулируйте основной закон механизма передачи возбудителей. Дайте объяснение пяти ти
пам механизма передачи. При ответе на вопрос используйте рис. 7. Приведите характерные примеры.
5. Дайте определение понятию «природная очаговость инфекционных болезней человека». Опишите основные этапы развития учения о природной очаговости.
6. Изучите данные табл. 19. Раскройте содержание современного этапа изучения инфекционных болезней, когда основные положения теории природной очаговости распространяются на все инфекционные болезни с внечеловеческим резервуаром возбудителя. Используйте при ответе материалы табл. 16.
7. Используйте терию механизма передачи возбудителя для характеристики зоонозных инфекций. При ответе руководствуйтесь классификацией инфекционных болезней, приведенной на схеме 2.
8. Обдумайте вопрос о причине незаразительности больных людей при большинстве зоонозных инфекций и невозможности закрепления в организме людей тех возбудителей зоонозов, которые передаются от человека к человеку.
9. Сформулируйте основные положения теории саморегуляции паразитарных систем, раскрывающей механизмы внутренней регуляции эпидемического процесса. Почему, по Вашему мнению, они были сформулированы в конце 70-х — 80-е годы.
10. Изучите содержание рис. 8. Объясните представленное на рисунке распределение заболеваемости в коллективах. Используйте также материалы схемы 5.
11. Изучите содержание табл. 20. В чем разница в понятиях «диапазон», «степень» и «характер» гетерогенности?
12. Почему, по Вашему мнению, в табл. 21, где говорится о перераспределении степени и характера гетерогенности, не упоминается термин «диапазон гетерогенности» (см. табл. 20).
13. Рассмотрите рис. 9, 10, 12. Опишите механизм изменений вирулентности стрептококка группы А и менингококка.
14. Пользуясь данными табл. 21 и рис. 11, укажите узловые моменты фазовых изменений паразита. Отметьте общее и различное в понятиях «межэпидемический период» и «фаза резервации возбудителя». Как Вы представляете предэпидемический период?
15. Пользуясь данными рис. 13, 14, 15, 16, сформулируйте Ваше понимание механизмов внутренней регуляции эпидемического процесса.
Источник: Беляков В. Д., Яфаев Р. X., «Эпидемиология: Учебник» 1989
А так же в разделе «ВНУТРЕННЯЯ РЕГУЛЯЦИЯ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА »
- РАЗДЕЛЫ УЧЕНИЯ ОБ ЭПИДЕМИЧЕСКОМ ПРОЦЕССЕ
- СУЩНОСТЬ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
- ПРИРОДА СПЕЦИФИЧНОСТИ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
- СОЦИАЛЬНЫЕ И ПРИРОДНЫЕ ФАКТОРЫ В РАЗВИТИИ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
- Глава 5 МЕХАНИЗМ РАЗВИТИЯ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
- МЕХАНИЗМ ПЕРЕДАЧИ ИНФЕКЦИИ
- ПРИРОДНАЯ ОЧАГОВОСТЬ ОТДЕЛЬНЫХ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ ЧЕЛОВЕКА