Субэпителиальная соединительная ткань содержит большое количество макрофагов, которые выступают здесь в качестве одного из ведущих факторов неспецифической защиты от патогена.
Иепь событий с участием макрофагов представляется следующим образом. Патоген, преодолевший эпителиальный барьер, сталкивается с фагоцитирующими мононуклеарами, которые экспрессируют на своей поверхности рецепторы к наиболее общим компонентам клеточной стенки микроорганизмов. Среди них — рецепторы к липополисахариду и маннозе. Взаимодействие патогена с макрофагами приводит к поглощению микробной клетки посредством фагоцитоза и ее последующему разрушению в фаго- лиэосомах.
Следствием взаимодействия тканевых макрофагов с патогеном является также секреция различных цитокинов фагоцитирующими клетками. Возможно, что в индукции секреции цитокинов участвуют те же самые рецепторы, что и при взаимодействии с патогеном. Продукция цитокинов сама по себе является важнейшим фактором, направленным на мобилизацию в зону проникновения патогена дополнительных клеток и гуморальных веществ, совместное действие которых создает д ля него мощный заслон.
И, наконец, еще одно свойство макрофагов в зоне проникновения патогена — это подготовка антигенов микроорганизмов к индукции специфического иммунного ответа.
Активация альтернативного пути развития системы комплемента и поглощение макрофагами преодолевших эпителиальный барьер микроорганизмов представляют собой наиболее раннюю реакцию врожденного, неспецифического иммунитета, которая встречается в первые часы после заражения. Если же микроорганизм все-таки ускользает от постоянно присутствующих факторов ранней, немедленной защиты, то мобилизуются клеточные и гуморальные механизмы, которые характеризуют собой ранний индукционный ответ. Импульсом к развитию такого ответа является факт распознавания антигенов микроорганизмов, которые по своей природе являются наиболее общими для них, например упоминавшийся выше липополисахарид. Понятно, что тонкая антиген- распознающая специфичность, свойственная адаптивному иммунитету, в данном случае отсутствует.Более того, природа факторов, включенных в ранний индукционный ответ, такова, что не создает памяти от первичного контакта с антигеном, столь свойственной специфическому иммунитету. Следует помнить, что именно на неспецифическом этапе развития противоинфекционного иммунитета закладываются основы для формирования специфического ответа. Этот преадаптационный процесс связан в первую очередь с переработкой антигенов микроорганизмов в их индуци- 324
бсльную (иммуногенную) форму для клеточных элементов специфической защиты.
Как отмечалось, одно из проявлений активности макрофагов в ранний индукционный период состоит в интенсивной продукции семейства цитокинов (монокинов). Основные из них: интерлейкины-1,6,8,12 (ИЛ-1,6,8,12) и фактор некроза опухолей а (ФНО-а). Эти цитокины обладают местным и системным эффектами (табл. 13.4). Главным из них является ФНО-а, основное предназначение которого состоит в формировании очага воспаления.
Таблица 13.4
Функциональная активность цитокинов (монокинов), секретнруе- мых активированными макрофагами
Воспалительный ответ в месте проникновения патогена характеризуется локальным образованием вздутия, покраснением, болью, повышением температуры. Все эти патологические нарушения есть результат двух основных событий, связанных с ФНО-а. Прежде всего, под влиянием ФНО-а увеличивается диаметр сосудов в очаге инфекции, что приводит к локальному усилению кровотока и, как следствие, к местному покраснению и повышению температуры. Кроме того, усиливается проницаемость сосудов, влекущая за собой локальное накопление жидкости, которая определяет формирование припухлости и возникновение болевых ощущений. Увеличение проницаемости сосудов и локальное накопление жидкости обеспечивает концентрацию в очаге проникновения инфекции иммуноглобулинов, комплемента и других функционально значимых белков.
Второе событие состоит в экспрессии под влиянием ФНО-а адгезивных молекул на эндотелиальных клетках, в результате усиливается приток фагоцитов в очаг воспаления, что крайне важно для локализации инфекции.
Процесс миграции лейкоцитов в очаг воспаления делится на четыре этапа. На первом этапе под влиянием ФНО-а происходит экспрессия Р- и Е-селектинов на эпителиальных клетках сосудов. Селектины распознают углеводные радикалы на гликопротеино- вых рецепторах циркулирующих в кровеносном русле лейкоцитов. Однако такое распознавание проходит при низкой аффинности. Лейкоциты, проходя мимо эпителиальных клеток с Р- и Е-селек- тинами, лишь замедляют движение, но не образуют прочных кон- стактных связей.
Под влиянием ФНО-а индуцируются не только селектины, но и адгезивные молекулы суперсемейства иммуноглобулинов ICAM-1, которые также экспрессируются на эпителиальных клетках. Взаимодействие ICAM-1 со своим лигандом LFA-1, представленным на фагоцитирующих клетках, как и в предыдущем случае, низкоаффинно. На этом фоне в процесс клеточного взаимодействия вступают молекулы ИЛ-8, продукция которых обеспечена активированными макрофагами инфекционного очага. Взаимодействие ИЛ-8 со своим рецептором на поверхности фагоцитов приводит к такому конформационному изменению LFA-1, которое значительно повышает эффективность связи с ICAM-1. В результате всех этих клеточно-молекулярных событий наступает важный момент в миграционном процессе — остановка движения фагоцитов по кровеносному руслу, что и характеризует второй этап.
Рис. 13.2. Этапы проникновения фагоцитирующих лейкоцитов из кровяного русла в очаг воспаления.
После установления достаточно прочной связи между фагоцитами и эндотелиальными клетками разворачивается третий этап
На четвертом, заключительном, этапе проникшие через эндотелиальную стенку фагоциты мигрируют непосредственно в очаг воспаления, перемещаясь по градиенту плотности , создаваемому ИЛ-8.
Помимо ФНО-а, значительная роль в формировании защитных механизмов при местной инфекции принадлежит хемокинам
Основные свойства различных хемокинов
Таблица 13.5
Существенную роль в формировании антибактериальной защиты играют цитокины Ш1-1 и ИЛ-6. Их особое значение, помимо всего прочего, состоит в том, что они, с одной стороны, являясь эндогенными пирогенами, инициируют повышение температуры тела, а с другой, стимулируют продукцию белков острой фазы (С-реактивный белок, или белок, связывающий маннозу). Спектр биологической активности ИЛ-1 и ИЛ-6 представлен в табл. 13.6.
Таблица 13.6
Биологическая активность цитокинов интерлейкина-1
и интепрлейкина-б
При развитии инфекции повышение температуры тела имеет вполне положительное значение, так как препятствует размножению микроорганизмов и спосбствует формированию специфического иммунного ответа.
Благодаря усиленной продукции ИЛ-6 активированными макрофагами инициируется синтез белков острой фазы. Один из них — С-реактивный белок, взаимодействуя с фосфорилхолином бактериальной стенки, выступает и как опсонин, и как индуктор классического пути активации системы комплемента. Другой белок острофазного ответа связывает маннозу. Его структура напоминает С1-компонент комплемента. В противоинфекционном ответе он выполняет две функции: выступает в качестве опсонина, взаимодействуя с маннозой бактериальных стенок, и активирует протеолитический белковы^ комплекс, который расщепляет С4 и
С2-компоненты комплемента с тем, чтобы инициировать развитие классическогго пути активации системы комплеменнта.
Таким образом, макрофаги, столкнувшись с патогеном, инициируют целую цепь событий, направленных на подавление развития инфекции. Активность фагоцитирующих мононуклеаров проявляется не только во внутриклеточном переваривании и уничтожении микроорганизма, но и в инициации секреции набора цитокинов с различной функциональной активностью. Все разнообразие биологического действия цитокинов (монокинов), секрети- руемых макрофагами, направлено на нейтрализацию и уничтожение патогена от инициации белков острой фазы, активации системы комплемента до привлечения в зону проникновения патогена дополнительных фагоцитирующих клеток.
Иепь событий с участием макрофагов представляется следующим образом. Патоген, преодолевший эпителиальный барьер, сталкивается с фагоцитирующими мононуклеарами, которые экспрессируют на своей поверхности рецепторы к наиболее общим компонентам клеточной стенки микроорганизмов. Среди них — рецепторы к липополисахариду и маннозе. Взаимодействие патогена с макрофагами приводит к поглощению микробной клетки посредством фагоцитоза и ее последующему разрушению в фаго- лиэосомах.
Следствием взаимодействия тканевых макрофагов с патогеном является также секреция различных цитокинов фагоцитирующими клетками. Возможно, что в индукции секреции цитокинов участвуют те же самые рецепторы, что и при взаимодействии с патогеном. Продукция цитокинов сама по себе является важнейшим фактором, направленным на мобилизацию в зону проникновения патогена дополнительных клеток и гуморальных веществ, совместное действие которых создает д ля него мощный заслон.
И, наконец, еще одно свойство макрофагов в зоне проникновения патогена — это подготовка антигенов микроорганизмов к индукции специфического иммунного ответа.
Активация альтернативного пути развития системы комплемента и поглощение макрофагами преодолевших эпителиальный барьер микроорганизмов представляют собой наиболее раннюю реакцию врожденного, неспецифического иммунитета, которая встречается в первые часы после заражения. Если же микроорганизм все-таки ускользает от постоянно присутствующих факторов ранней, немедленной защиты, то мобилизуются клеточные и гуморальные механизмы, которые характеризуют собой ранний индукционный ответ. Импульсом к развитию такого ответа является факт распознавания антигенов микроорганизмов, которые по своей природе являются наиболее общими для них, например упоминавшийся выше липополисахарид. Понятно, что тонкая антиген- распознающая специфичность, свойственная адаптивному иммунитету, в данном случае отсутствует.Более того, природа факторов, включенных в ранний индукционный ответ, такова, что не создает памяти от первичного контакта с антигеном, столь свойственной специфическому иммунитету. Следует помнить, что именно на неспецифическом этапе развития противоинфекционного иммунитета закладываются основы для формирования специфического ответа. Этот преадаптационный процесс связан в первую очередь с переработкой антигенов микроорганизмов в их индуци- 324
бсльную (иммуногенную) форму для клеточных элементов специфической защиты.
Как отмечалось, одно из проявлений активности макрофагов в ранний индукционный период состоит в интенсивной продукции семейства цитокинов (монокинов). Основные из них: интерлейкины-1,6,8,12 (ИЛ-1,6,8,12) и фактор некроза опухолей а (ФНО-а). Эти цитокины обладают местным и системным эффектами (табл. 13.4). Главным из них является ФНО-а, основное предназначение которого состоит в формировании очага воспаления.
Таблица 13.4
Функциональная активность цитокинов (монокинов), секретнруе- мых активированными макрофагами
|
Цитокин |
Локальные эффекты |
Системные эффекты |
|
Интерлейкин-1 |
активация сосудистого эндотелия; активация лимфоцитов; усиление прохождения эффектор ных клеток через эндотелий; локальное разрушение тканей |
лихорадка, пирогенный эффект, инициация продукции ИЛ-6 |
|
Интерлейкин-6 Интерлейкин-Й |
активация лимфоцитов хемоггаксический фактор для лейкоцитов; усиление прохождения эф- фекторных клеток через эндотелий |
повышение температуры тела |
|
Интерлейкин-12 |
увеличение продукции антител |
индукция белков острой фазы |
|
ФНО-а |
активация сосудистого эндотелия и повышение проницаемости сосудов, что обеспечивает увеличение поступления IgG, комплемента и клеток в зону проникновения патогена; усиливает ток лимфы через лимфатические уалы |
повышение температуры тела; мобилизация метаболитов; инициация шока |
Воспалительный ответ в месте проникновения патогена характеризуется локальным образованием вздутия, покраснением, болью, повышением температуры. Все эти патологические нарушения есть результат двух основных событий, связанных с ФНО-а. Прежде всего, под влиянием ФНО-а увеличивается диаметр сосудов в очаге инфекции, что приводит к локальному усилению кровотока и, как следствие, к местному покраснению и повышению температуры. Кроме того, усиливается проницаемость сосудов, влекущая за собой локальное накопление жидкости, которая определяет формирование припухлости и возникновение болевых ощущений. Увеличение проницаемости сосудов и локальное накопление жидкости обеспечивает концентрацию в очаге проникновения инфекции иммуноглобулинов, комплемента и других функционально значимых белков.
Второе событие состоит в экспрессии под влиянием ФНО-а адгезивных молекул на эндотелиальных клетках, в результате усиливается приток фагоцитов в очаг воспаления, что крайне важно для локализации инфекции.
Процесс миграции лейкоцитов в очаг воспаления делится на четыре этапа. На первом этапе под влиянием ФНО-а происходит экспрессия Р- и Е-селектинов на эпителиальных клетках сосудов. Селектины распознают углеводные радикалы на гликопротеино- вых рецепторах циркулирующих в кровеносном русле лейкоцитов. Однако такое распознавание проходит при низкой аффинности. Лейкоциты, проходя мимо эпителиальных клеток с Р- и Е-селек- тинами, лишь замедляют движение, но не образуют прочных кон- стактных связей.
Под влиянием ФНО-а индуцируются не только селектины, но и адгезивные молекулы суперсемейства иммуноглобулинов ICAM-1, которые также экспрессируются на эпителиальных клетках. Взаимодействие ICAM-1 со своим лигандом LFA-1, представленным на фагоцитирующих клетках, как и в предыдущем случае, низкоаффинно. На этом фоне в процесс клеточного взаимодействия вступают молекулы ИЛ-8, продукция которых обеспечена активированными макрофагами инфекционного очага. Взаимодействие ИЛ-8 со своим рецептором на поверхности фагоцитов приводит к такому конформационному изменению LFA-1, которое значительно повышает эффективность связи с ICAM-1. В результате всех этих клеточно-молекулярных событий наступает важный момент в миграционном процессе — остановка движения фагоцитов по кровеносному руслу, что и характеризует второй этап.
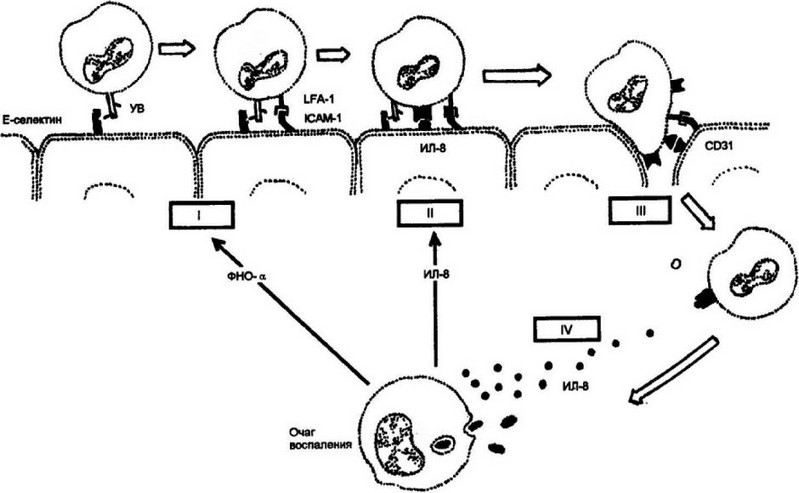
Рис. 13.2. Этапы проникновения фагоцитирующих лейкоцитов из кровяного русла в очаг воспаления.
- этап. Низкоаффинное взаимодействие адгезинов эндотелиальных клеток с лигандами лейкоцитов. Под влиянием ФНО-а, продуцируемого поглотившими антиген макрофагами в очаге воспаления, экспрессируется адгезивный белок Е- селектин на эндотелиальных клетках. Он взаимодействует при низком уровне аффинности с углеводными радикалами (УВ) поверхности лейкоцитов. Индуцируемый ФНО-а адгезии ICAM-1 вступает во взаимодействие с LFA-1 лейкоцитов. Данная форма взаимодействия также ниэкоаффинна. При подобных формах взаимодействия лейкоциты замедляют свое движение вдоль эндотелия, но не прекращают его полностью.
- этап. Остановка движения лейкоцитов. ИЛ-8, продуцируемый активированными макрофагами, взаимодействует со своим рецептором на поверхности лейкоцитов, усиливая тем самым аффинность взаимодействия ICAM-1:LFA-1, что и является причиной остановки движения.
- этап. Диапедез. Остановившийся лейкоцит проходит между эндотелиальными клетками с помощью рецепторов CD31 и ICAM-l:LFA-l.
- этап. Миграция в очаг воспаления. Лейкоцит, оказавшийся в субэндотелиальной области, перемещается против градиента плотности ИЛ-8 в зону воспаления

После установления достаточно прочной связи между фагоцитами и эндотелиальными клетками разворачивается третий этап
- проход клеток через эндотелиальную стенку сосудов. Проникновение реализуется через взаимодействие тех же молекул LFA-1 и дополнительных иммуноглобулиноподобных молекул CD31, экспрессирующихся как на лейкоцитах, так и на эпителиальных клетках в местах плотного соединения клеток. Именно эти молекулы обеспечивают диапетез фагоцитов — проход через эпителиальную стенку в район развития воспалительной реакции.
На четвертом, заключительном, этапе проникшие через эндотелиальную стенку фагоциты мигрируют непосредственно в очаг воспаления, перемещаясь по градиенту плотности , создаваемому ИЛ-8.
Помимо ФНО-а, значительная роль в формировании защитных механизмов при местной инфекции принадлежит хемокинам
- низкомолекулярным белкам, секретируемым различными типами клеток в очаге проникновеения патогена. Все хемокины делятся на две группы: аир. Хемокины а являются хемоаттрактантами для нейтрофилов. К этой группе хемокинов относится, в частности, ИЛ-8. Хемокины р способствуют миграции моноцитов, которые, достигнув очага инфекции, дифференцируются в тканевые макрофаги. Одним из активных р-хемокинов является MCAF (сокр. от “англ, macrophage chemoattractant and activating factor”). Другие хемокины привлекают в зону инфекции иные клеточные типы. Свойства хемокинов двух групп суммированы в табл. 13.5.
Основные свойства различных хемокинов
Таблица 13.5
|
|
Суб- |
Клетки- |
|
Влияние на |
|
|
Хемокин |
класс |
продуценты |
Т-клетки |
Моноциты |
Нейтро филы |
|
ИЛ-8 PBP/jl TG/ |
а а |
моноциты, макрофаги, фибробласты, кератиноциты тромбоциты |
|
|
активация миграции активация миграции и дегрануля- цнн |
|
MIP-Ib |
Р |
моноциты, макрофаги, нейтрофилы, эндотслиоциты |
активация миграции CDS Т-кл. |
|
активация миграции |
|
MCAF |
р |
моноциты, макрофаги, фиброласть], кератиноциты |
активация миграции Т- кл. памяти |
активация миграции |
|
|
RANTES |
р |
Т-клетки |
активация миграции CD4 Т-кл. памяти |
активация миграции |
|
Существенную роль в формировании антибактериальной защиты играют цитокины Ш1-1 и ИЛ-6. Их особое значение, помимо всего прочего, состоит в том, что они, с одной стороны, являясь эндогенными пирогенами, инициируют повышение температуры тела, а с другой, стимулируют продукцию белков острой фазы (С-реактивный белок, или белок, связывающий маннозу). Спектр биологической активности ИЛ-1 и ИЛ-6 представлен в табл. 13.6.
Таблица 13.6
Биологическая активность цитокинов интерлейкина-1
и интепрлейкина-б
|
Мишень |
Функциональное действие |
Конечный результат |
|
Печень |
индукция синтеза белков острой |
активация комплемента, |
|
|
фазы (С-реактивного белка, сывороточного амилоидного белка, фибриногена, белка, связывающего маннозу) мобилизация нейтрофилов |
опсониэация |
|
Эндотелий |
|
усиление фагоцитарного |
|
костного мозга |
|
ответа |
|
Гипоталамус |
повышение температуры тела |
подавление размножения бактерий и вирусов; усиление презентации антигена в иммуногенной форме; усиление специфического иммунного ответа |
|
Жировая ткань, |
мобилизация белков и энергии, |
то же |
|
мышцы |
приводящие к повышению температуры тела |
|
|
Т- и В-лимфоциты |
увеличение активности |
то же |
При развитии инфекции повышение температуры тела имеет вполне положительное значение, так как препятствует размножению микроорганизмов и спосбствует формированию специфического иммунного ответа.
Благодаря усиленной продукции ИЛ-6 активированными макрофагами инициируется синтез белков острой фазы. Один из них — С-реактивный белок, взаимодействуя с фосфорилхолином бактериальной стенки, выступает и как опсонин, и как индуктор классического пути активации системы комплемента. Другой белок острофазного ответа связывает маннозу. Его структура напоминает С1-компонент комплемента. В противоинфекционном ответе он выполняет две функции: выступает в качестве опсонина, взаимодействуя с маннозой бактериальных стенок, и активирует протеолитический белковы^ комплекс, который расщепляет С4 и
С2-компоненты комплемента с тем, чтобы инициировать развитие классическогго пути активации системы комплеменнта.
Таким образом, макрофаги, столкнувшись с патогеном, инициируют целую цепь событий, направленных на подавление развития инфекции. Активность фагоцитирующих мононуклеаров проявляется не только во внутриклеточном переваривании и уничтожении микроорганизма, но и в инициации секреции набора цитокинов с различной функциональной активностью. Все разнообразие биологического действия цитокинов (монокинов), секрети- руемых макрофагами, направлено на нейтрализацию и уничтожение патогена от инициации белков острой фазы, активации системы комплемента до привлечения в зону проникновения патогена дополнительных фагоцитирующих клеток.
