ЭНДОКРИННАЯ СИСТЕМА
Эндокринная система желудочно-кишечного тракта включает эндокринные (энтероэндокрин- ные) клетки слизистой оболочки и желёз пищеварительной трубки. Сюда же относят некоторые нейроны энтеральной нервной системы, секретирующие гормоны (в ряде случаев те же, что и энтероэндокринные клетки). По этой причине эндокринную систему ЖКТ часто называют нейроэндокринной системой. Наконец, с функциональной точки зрения к этой же системе можно отнести гистамин, простагландины и другие биологически активные вещества, выделяющиеся из разных клеточных источников. Традиционно эндокринные клетки островков Лангер- ханса поджелудочной железы рассматривают в разделе «Пищеварительная система».
- Островки Лангерханса. Эндокринная часть поджелудочной железы — совокупность островков Лангерханса (около I млн). Каждый островок имеет диаметр до 0,2 мм и содержит несколько сотен и даже тысяч эндокринных клеток, окружённых тонкой сетью ретикулиновых волокон и многочисленными кровеносными капиллярами с фенестрированным эндотелием. Островковые клетки синтезируют и секретируют пептидные гормоны, отсюда — хорошее развитие гранулярной эндоплазматической сети, аппарата Голь- джи, наличие секреторных гранул. Различают несколько типов эндокринных клеток, синтезирующих и секретирующих в просвет капилляров следующие пептидные гормоны (рис. 12-12): инсулин (р-клетки), глюкагон (а-клетки), соматостатин (8-клетки), панкреатический полипептид (РР-клетки) и у детей младшего возраста — гастрин (G-клетки). Идентификацию типов клеток осуществляют при помощи специальных методов окраски, точная идентификация — иммуноцитохимическая.
а. а-Клетки составляют около 15% островковых клеток, расположены преимущественно по периферии островка, имеют неправильной формы ядро, в цитоплазме содержат гранулы глюкагона.
- Глюкагон
(а) Ген GCG (138030, 2q36-q37) содержит последовательности, кодирующие глюкагон, а также глюкагоноподобные пептиды I и 2.
Мутация гена GCG приводит к выраженной гипогликемии.
Lys-Ala-Pro-Ser-Gly-Arg-Met-Ser-Ile-Val-Lys-Asn-Leu-Gln-Asn-Leu-Asp
H2NPhe-Asp-Met-Trp-Gly-Met-Tyr-Asp-Arg-Asp-Ser-lle-Arg-His-Ser-Pro
|_| Холецистокинин
3
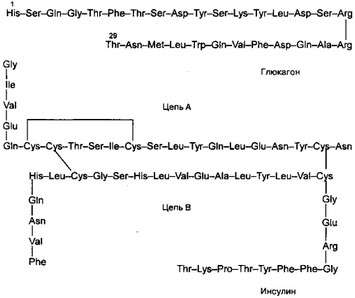
Рис. 12-12. Структура некоторых гормонов ЖКТ [по Merck Index, 12 издание, 1996]
(б) Структура (рис. 12-12). Глюкагон — пептид, содержащий 29 аминокислотных остатков. Время полужизни глюкагона в крови — около 5 минут.
(в) Секрецию глюкагона подавляет глюкоза.
(г) Мишени. Основные мишени глюкагона — гепатоциты и адипоциты.
(д) Рецептор глюкагона (ген GCGR, 138033, 17q25) расположен в плазмолемме клеток-мишеней, связывает только глюкагон и посредством G-белков активирует аденилатциклазу.
Мутация гена GCGR (GLY40 -gt; SER) приводит к развитию одной из форм инсулин-независимого сахарного диабета.
(е) Функции. Глюкагон расценивают как антагонист инсулина, этот гормон стимулирует гликогенолиз и липолиз, что ведёт к быстрой мобилизации источников энергии (глюкоза и жирные кислоты).
- Глюкагоноподобный пептид I (GLP-I)
(а) Ген глюкагона GCG кодирует последовательность глюкагоноподобного пептида I (138032, GLP-1, пептид 7-37). Глюкагоноподобный пептид I секретируют L-клетки слизистой оболочки ЖКТ. Неизвестно, экспрессируют ли а-клетки островков Лангерханса GLP-I.
(б) Секрецию GLP-I, как и глюкагона, подавляет глюкоза.
(г) Мишени. Главная мишень GLP-I — секретирующие инсулин р-клетки островков Лангерханса.
(д) Рецептор GLP-I (ген GLP1R, 6р21) специфически связывает GLP-I (но не глюкагон) и активирует аденилатциклазу.
(е) Функции. Глюкагоноподобный пептид I — самый мощный стимулятор вызванной глюкозой секреции инсулина. GLP-I также подавляет желудочную секрецию.
б. р-Клетки составляют до 70% эндокринных клеток островка, расположены преимущественно в его центральных частях, содержат крупное округлое ядро и гранулы инсулина.
- Инсулин
(а) Ген INS (176730, 11р15.5) кодирует транслируемый проинсулин, преобразуемый в инсулин и С-пептид.
Мутации. Известно до 10 мутаций гена INS, приводящих к трансляции дефектных инсулинов (гиперпроинсулинемия и гиперинсулинемия).
(б) Структура (рис. 12-12). Инсулин — димер, состоящий из двух цепей, связанных дисульфидными группами. В крови практически полностью деградирует в течение 5 минут.
(в) Регуляция
- Стимуляция
Гиперкалиемия. Повышение содержания K+ во внутренней среде организма. Глюкоза. Повышение содержания глюкозы в крови.
Ацетилхолин из блуждающего нерва (здесь не всё ясно, т.к. классический антагонист атропин не влияет на стимулирующий эффект ацетилхолина). Гастрин-рилизинг гормон, выделяющийся из блуждающего нерва. Глюкагоноподобный пептид I (GLP-1). Мощный стимулятор секреции инсулина. Производные сульфонилмочевины (например, толбутамид)
- Торможение Соматостатин
Адреналин и норадреналин (через а-адренорецепторы) подавляют секрецию инсулина. Через Р-адренорецепторы эти агонисты стимулируют секрецию инсулина, но в островках Лангерханса преобладают а-адренорецепторы; суммарный эффект — угнетение секреции инсулина.
(г) Мишени. Главные мишени — печень, скелетные мышцы, адипоциты.
(д) Рецептор инсулина [рецепторная тирозин киназа, см. главу 21В 2 а (2) (a) (J)) — тетрамер (рис. 9-1), его субъединицы кодирует один ген (ген INSR, 147670,19р13.2). Мутации. Известно не менее 30 мутаций гена INSR, приводящих к развитию
полной или частичной нечувствительности мишеней к эффектам инсулина (сахарный диабет типа II).
(е) Функции инсулина разнообразны (регуляция обмена углеводов, липидов и белков). Инсулин — главный регулятор гомеостаза глюкозы. Мембранный транспорт глюкозы — стимуляция.
Гликолиз — стимуляция.
Липогенез — стимуляция.
Синтез белка — стимуляция.
Пролиферация клеток — стимуляция.
- Сахарный диабет (diabetes mellitus) — гетерогенная группа состояний, синдром, складывающийся из метаболических нарушений (гипергликемия, дислипи- демия, расстройства энергетического обмена), поражения мелких сосудов (ретинопатии, нефропатии), поражения крупных сосудов (атеросклероз) и периферической невропатии. Гипергликемия и другие метаболические нарушения при сахарном диабете имеют одну причину — неадекватное действие инсулина на мишени гормона вследствие уменьшения секреции инсулина или резистентности мишеней к его действию.
(а) Инсулин-зависимый сахарный диабет (тип I, юношеский диабет). Тяжёлый сахарный диабет, аутоиммунное заболевание, быстрое развитие в возрасте до 20 лет (этой формой диабета страдает I из 250); происходит опосредованная Т-лимфоцитами гибель р-клеток островков Лангерханса поджелудочной железы (наблюдается экспрессия р-клетками т.н. суперантигена — ретровируса?); клинически: жажда, полиурия, повышенный аппетит, потеря массы, низкое содержание инсулина в крови, инсулино- терапия и диета обязательны.
- Этиология неясна. Патологический процесс, приводящий к гибели р-клеток
островков Лангерханса, связывают с рядом генетических, аутоиммунных факторов и факторов окружающей среды.
- Генетические факторы
Наблюдается повышенная частота экспрессии некоторых Ar MHC (HLA OR3 и DR4). При одновременном наследовании DR3 и DR4 риск развития диабета удваивается.
Среди ближайших родственников больного риск заболевания повышен; страдает 2-5% сибсов и их потомков.
Конкордантность для однояйцовых близнецов — 50%.
- Аутоиммунные факторы. Аутоиммунную природу заболевания подтверждает наличие циркулирующих AT к р-клеткам в сыворотке 85% пациентов со свежим диабетом типа I и повышенная частота ассоциированности с аутоиммунными заболеваниями.
- Факторы окружающей среды. Менее ясно значение факторов окружающей среды. Роль вирусов при развитии инсулин-зависимого сахарного диабета обсуждается давно. Маловероятно, что за возникновение всех вариантов болезни ответственен один и тот же вирус.
- Патогенез
- При разрушении 90% р-клеток снижение секреции инсулина становится клинически значимым. Без инсулина обменные процессы смещаются в сторону катаболизма (сниженное потребление глюкозы и повышенное образование глюкозы путём глюконеогенеза и гликогенолиза), что приводит к гипергликемии.
- Если содержание глюкозы в плазме крови превышает почечный порог реабсорбции (более 180 мг%, или 10,2 ммоль/л), развивается глюкозурия, приводящая к осмотическому диурезу, повышающему выделение мочи и потребление жидкости. При резко выраженном дефиците инсулина в большом количестве образуются кетоны. Без инсулинотерапии развивается диабетический кето- ацидоз (метаболический синдром, характеризующийся гипергликемией, мета-
болическим ацидозом, дегидратацией и сонливостью). Кетоацитоз может привести к развитию комы и смерти.
(б) Инсулин-независимый сахарный диабет (тип II, диабет взрослых). Умеренно выраженный сахарный диабет с постепенным началом, обычно в возрасте свыше 35 лет у лиц полного телосложения (этой формой диабета страдает каждый двадцатый); абсолютное содержание инсулина в крови — от нормы до высоких значений, в соотношении с сахаром крови повышение содержания инсулина незначительно; поддаётся терапии диетой и/или гипогликемическими препаратами per os; могут развиться дегенеративные поражения органов.
Этиология
- Генетические факторы ещё более значимы при диабете II типа. Уровень конкордантности среди идентичных близнецов достигает 100%.
- Ожирение. У 80% больных диабетом II типа масса превышает идеальную на 15% и более. Ожирение сочетается с резистентностью к действию инсулина как у больных диабетом, так и у здоровых; эта резистентность может быть вызвана уменьшением числа рецепторов инсулина, их дефектами и событиями, происходящими после взаимодействия инсулина и его рецептора.
в. 5-Клетки секретируют соматостатин (см. главу 9 II Д I и рис. 9-10).
г. РР-клетки (F-клетки, согласно другой терминологии) секретируют панкреатический полипептид.
Панкреатический полипептид расценивают как один из регуляторов пищевого режима.
(а) Ген PNP (167780, I7ql2-q21).
(б) Структура. Полипептид из 36 аминокислот.
(в) Стимуляторы секреции
- Богатая белком пища
- Гипогликемия
- Голодание
- Физическая нагрузка
(г) Функция. Угнетает секрецию экзокринной части поджелудочной железы.
(д) Недостаточность секреции панкреатического полипептида наблюдается у детей с синдромом Прадер-Вйлли.
д. G-клетки (D-клетки, согласно другой терминологии) секретируют гастрин в ранних возрастных группах в островках Лангерханса и постоянно — в слизистой оболочке желудка (преимущественно в антральном отделе).
Гастрин
(а) Ген 64,54137250, 17q21) кодирует несколько идентичных последовательностей, известных под разными именами (гастрин I, гастрин П, минигастрин и т.д.).
(б) Структура. Пептид из 17 аминокислот.
(в) Стимулятор секреции — гастрин освобождающий гормон (GRP).
(г) Рецептор гастрина/холецистокинина (ген CCKBR, 118445, 11р15.5-р15.4) обнаружен в ЦНС и слизистой оболочке желудка.
(д) Функция. Стимулирует секрецию соляной кислоты в желудке.
(е) Синдром ЗоААИнгера-Эллисона. Большое количество гастрина вырабатывают опухоли островковых клеток поджелудочной железы.
е. Регенерация островковых эндокринных клеток не показана. В этом отношении эпителиальные островковые клетки представляют исключение из общего правила: эпителиальные клетки способны к регенерации.
- Энтероэндокринные клетки находятся в слизистой оболочке кишечного типа, главным образом среди эпителиальных клеток крипт в кишечнике, в железах желудка, а
также в собственном слое слизистой оболочки желудка и кишечника, они особенно многочисленны в двенадцатиперстной кишке. Клетки слюнных и бруннеровых желёз двенадцатиперстной кишки секретируют эпидермальный фактор роста (EGF)1 урогастрон. Регуляция активности. При поступлении пищи в просвет ЖКТ различные эндокринные клетки под действием растяжения стенки, под влиянием самой пищи или изменения pH в просвете пищеварительного канала начинают выделять гормоны в ткани и в кровь. Активность энтероэндокринных клеток находится под контролем вегетативной нервной системы.
Вегетативная нервная система
(а) Парасимпатический отдел. Стимуляция блуждающего нерва способствует высвобождению гормонов, усиливающих пищеварение (табл. 12-3 и 12-4).
(б) Симпатический отдел. Повышение активности чревных нервов оказывает противоположный эффект.
- Нейроны. Из окончаний нервных волокон секретируется гастрин-рилизинг гормон; из окончаний нервных волокон, из крови и из собственных (интрамуральных) нейронов пищеварительного тракта поступают пептидные гормоны: нейропептид Y (секретируется вместе с норадреналином), относящийся к кальцитониновому гену пептид.
- Другие источники гормонов. Гистамин секретируют главным образом тучные клетки. Наконец, из разных источников поступают серотонин, брадикинин, простагландин E (табл. 12-5).
- Функции биологически активных веществ в пищеварительном тракте
а. Адреналин и норадреналин подавляют перистальтику кишечника и моторику желудка, сужают просвет кровеносных сосудов.
б. Ацетилхолин стимулирует все виды секреции в желудке, двенадцатиперстной кишке, поджелудочной железе, а также моторику желудка и перистальтику кишечника.
в. Брадикинин стимулирует моторику желудка. Вазодилататор.
г. VIP стимулирует моторику и секрецию в желудке, перистальтику и секрецию в кишечнике. Мощный вазодилататор. Выделяется в ответ на стимуляцию блуждающего нерва.
Таблица 12-3. Влияние различных отделов вегетативной нервной системы на секрецию в пищеварительном тракте
|
|
Блуждающий нерв |
Чревные нервы |
|
HCI |
+ |
- |
|
Соыатостатин |
- |
- |
|
Гастрин |
+ |
- |
|
Холецистокинин |
+ |
- |
*+* — усиление секреции, «-» — её подавление
Таблица 12-4. Нейрогуморальная регуляция секреции холецистокииина
|
Прогестерон |
+ |
|
Блуждающий нерв |
+ |
|
Чревные нервы |
- |
|
Эстрогены -» окситоцин -gt; блуждающий нерв |
+ |
«+» — усиление секреции,«-* — её подавление
Таблица 12-5. Источники биологически активных веществ в пищеварительном тракте
|
Гормон |
Эндокринные клетки |
Элементы энтеральной нервной системы |
|
Вещество P |
+ |
+ |
|
Гастрнн |
+ |
+ |
|
Гастрин-рилизинг гормон |
+ |
+ |
|
Гнстамин |
+ |
|
|
Глюкагон |
+ |
|
|
Желудочный ингибирующий пептид (GIP) |
+ |
|
|
Инсулин |
+ |
|
|
Метионин-энкефалик |
+ |
+ |
|
Мотилин |
+ |
|
|
Нейропептид Y |
+ |
+ |
|
Нейротензин |
+ |
+ |
|
Относящийся х кальцитоннновому гену пептид |
+ |
+ |
|
Секретин |
+ |
+ |
|
Серотонин |
+ |
|
|
Соматостатин |
+ |
|
|
Холецистокинин |
+ |
|
|
VIP |
+ |
|
Знаком «+* отмечены гормоны, вырабатываемые указанными структурами
д. Вещество P вызывает незначительную деполяризацию нейронов в ганглиях меж- мышечного сплетения, сокращение ГМК.
е. Гастрин стимулирует секрецию слизи, бикарбоната, ферментов, соляной кислоты в желудке, подавляет эвакуацию из желудка, стимулирует перистальтику кишечника и секрецию инсулина, стимулирует рост клеток в слизистой оболочке.
ж. Гастрин-рилизинг гормон стимулирует секрецию гастрина и гормонов поджелудочной железы.
з. Гистамин стимулирует секрецию в железах желудка и перистальтику.
и. Глюкагон стимулирует секрецию слизи и бикарбоната, подавляет перистальтику кишечника.
к. Желудочный ингибирующий пептид подавляет желудочную секрецию и моторику желудка, л. Мотилин стимулирует моторику желудка.
м. Нейропептид Y подавляет моторику желудка и перистальтику кишечника, усиливает вазоконстрикторный эффект норадреналина во многих сосудах, включая чревные,
и. Пептид, связанный с кальцитониновым геном, подавляет секрецию в желудг ке, вазодилататор.
о. Простагландин E стимулирует секрецию слизи и бикарбоната в желудке, п. Секретин подавляет перистальтику кишечника, активирует эвакуацию из желудка, стимулирует секрецию сока поджелудочной железы, р. Серотонин стимулирует перистальтику.
с. Соматостатин подавляет все процессы в пищеварительном тракте, т. Холецистокинин стимулирует перистальтику кишечника, но подавляет моторику желудка; стимулирует поступление жёлчи в кишечник и секрецию в поджелудочной железе, усиливает высвобождение инсулина. Холецистокинин имеет значение для процесса медленной эвакуации содержимого желудка, расслабления сфинктера Одди. у. Эпидермальный фактор роста (EGF) стимулирует регенерацию клеток эпителия в слизистой оболочке желудка и кишечника.
- Влияние гормонов на основные процессы в пищеварительном тракте
а. Секреция слизи и бикарбоната в желудке. Стимулируют: гастрин, гастрин- рилизинг гормон, глюкагон, простагландин Е, эпидермальный фактор роста (EGF). Подавляет соматостатин.
б. Секреция пепсина и соляной кислоты в желудке. Стимулируют ацетилхолин, гистамин, гастрин. Подавляют соматостатин и желудочный ингибирующий пептид.
в. Моторика желудка. Стимулируют ацетилхолин, мотилин, VIP. Подавляют соматостатин, холецистокинин, адреналин, норадреналин, желудочный ингибирующий пептид.
г. Перистальтика кишечника. Стимулируют ацетилхолин, гистамин, гастрин (подавляет эвакуацию из желудка), холецистокинин, серотонин, брадикинин, VIP. Подавляют соматостатин, секретин, адреналин, норадреналин.
д. Секреция сока поджелудочной железы. Стимулируют ацетилхолин, холецистокинин, секретин. Подавляет соматостатин.
е. Секреция инсулина. Стимулируют ацетилхолин, гастрин-рилизинг гормон, холецистокинин, VIP, увеличение концентрации глюкозы. Подавляют соматостатин, адреналин, норадреналин.
ж. Желчеотделение. Стимулируют гастрин, холецистокинин.
Источник: Под ред. Э.Г. Улумбекова, Ю.А. Челышева, «Гистология (введение в патологию)» 1997
А так же в разделе «ЭНДОКРИННАЯ СИСТЕМА »
- ИСТОЧНИКИ И РАЗВИТИЕ
- ПЛАН СТРОЕНИЯ ПИЩЕВАРИТЕЛЬНОГО ТРАКТА
- НЕРВНЫЙ АППАРАТ
- V РОТОВАЯ ПОЛОСТЬ
- ПИЩЕВОД
- ЖЕЛУДОК
- IX ТОНКИЙ КИШЕЧНИК
- ТОЛСТЫЙ КИШЕЧНИК
- ЖЕЛЕЗЫ ПИЩЕВАРИТЕЛЬНОГО ТРАКТА
- ПРЕПАРАТЫ
- ОТВЕТЫ И ПОЯСНЕНИЯ
- 13 Дыхательная система
- ПРЕПАРАТЫ
- ОТВЕТЫ И ПОЯСНЕНИЯ
- 14 Мочевыделительная система
- ПРЕПАРАТЫ
- ОТВЕТЫ И ПОЯСНЕНИЯ