Успехи в осуществлении анализа генетических основ тканевой несовместимости и трансплантационного иммунитета были связаны с использованием генетически чистых линий мышей и следовали за достижениями в изучении локусов гистосовместимости, прежде всего MHC (см. раздел 3.2.2.1). Дж. Снелл (G.D. Snell) — один из сооткрывателей MHC — сформулировал генетические законы трансплантации. Приведем здесь первые четыре из них, наиболее важные для иммунологии трансплантаций (см. также рис. 4.7):
- сингенные трансплантаты (внутри генетически чистой линии или между однояйцовыми близнецами) приживаются;
- аллогенные трансплантаты (между мышами разных линий) отторгаются;
- трансплантаты от мышей родительской линии приживаются у гибридов первого поколения (F1) с мышами другой линии;
- трансплантаты от гибридов F1 приживаются у F1, но отторгаются у мышей обеих родительских линий.
Законы трансплантации соответствуют представлениям о кодоминантной природе наследования антигенов гистосовместимости, т.е. экспрессии обоих аллелей в условиях гетерозиготности.
Тогда же сложилась современная номенклатура трансплантологии. Ткани от генетически идентичных доноров называют сингенными, от генетически неидентичных доноров того же вида — аллогенными, от представителей другого вида — ксеногенными. Пересадка тканей в пределах одного организма называют аутотрансплантацией, между разными организмами одного вида — аллотрансплантацией, между разными видами — ксенотрансплан- тацией. Антигены, отражающие генетический полиморфизм внутри вида, обозначают как аллоантигены. Наиболее известные их разновидности — антигены MHC, а также антигены групп крови.
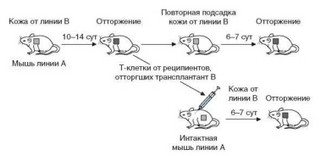
Рис. 4.7. Доказательства иммунологической природы отторжения аллотрансплантата: наличие вторичного иммунного ответа и возможность переноса иммунитета с клетками. Два главных доказательства иммунологической (клеточной) природы отторжения аллотрансплантата состоят в возможности индуцировать иммунологическую память и вторичный иммунный ответ и перенести память интактным сингенным реципиентам с лимфоцитами мышей, ранее отторгших ткань того же донора
Известно много (у мышей — 30—40) генетических локусов, обусловливающих тканевую совместимость, или гистосовместимость. Однако с различиями только по одному локусу — MHC (у мышей — Н-2, у человека — HLA) связано развитие сильной трансплантационной реакции, релизуемой в пределах двух недель. Наибольшую роль в развитии реакции отторжения играют различия по антигенам MHC-II, вызывающие преимущественно Т-клеточный иммунный ответ. Влияние на судьбу трансплантата определило название данного генетического комплекса как главного локуса гистосовместимости. Этот генетический комплекс детально рассмотрен ранее (см. раздел 3.2.2.1). Отметим, что его открытие и первоначальное изучение было связано именно с анализом генетических основ несовместимости тканей, а не с изучением роли молекул MHC в презентации антигенов Т-клеткам, которая была установлена значительно позже. С этим связано и название локуса, не соответствующее современным представлениям о функциях закодированных в нем молекул, но сохраненное в соответствии со сложившейся традицией.
Различия по другим (слабым) локусам гистосовместимости обусловливают медленное отторжение, растягивающееся на месяцы.
