ГЕНИТАЛЬНЫЙ ЭНДОМЕТРИОЗ
Эндометриоз — патологический процесс, формирующийся на фоне нарушенных гормонального и иммунного гомеостазов и характеризующийся ростом и развитием ткани, идентичной по структуре и функции с эндометрием, за пределами границ нормальной локализации слизистой оболочки тела матки.
Гистологическое строение эндометриоза во многом напоминает строение эндометрия (сочетание железистого эндометриоподобного эпителия и цитогенной стромы). Однако, в отличие от неизменной слизистой тела матки, эндометриоидная ткань менее подвержена циклическим превращениям — в частности, под влиянием прогестерона в очагах эндометриоза не происходит полноценной секреторной трансформации и, в целом, эндометриоз достаточно слабо реагирует на воздействие экзогенных гормонов.
Макроскопически эндометриоз может иметь форму узлов, инфильтратов или кистозных образований, полость которых заполнена геморрагическим содержимым (густая коричневая жидкость, по внешнему виду напоминающая горячий шоколад). Узлы эндометриоза формируются в результате проникновения в ткани окружающих фокусы эндометриоза менструальноподобных кровянистых выделений, протеолитических и липолитических ферментов, выделяемых патологическими имплантатами, а также продуктов деструкции тканей, образующихся в зоне эндометриоза. Подобное развитие эндометриоидных узлов определяет особенность их строения, а именно, отсутствие в них окружающей соединительнотканной капсулы.
Следует отметить, что эндометриоз обладает способностью к инфильтрирующему росту в окружающие ткани и органы с деструкцией последних. Более того, эндометриоз способен распространяться по кровеносным и лимфатическим сосудам, а также диссеминироваться в результате нарушения целостности стенок его кистозных форм. Иначе
говоря, эндометриоз обладает метастатическими свойствами.
Итак, отсутствие окружающей соединительнотканной капсулы, способность к инфильтрирующему росту и мета- стазированию — в совокупности сближают эндометриоз с опухолевым процессом. В то же время, в отличие от истинной опухоли, цдя эндометриоза не является характерным: а) клеточный атипизм; б) прогрессивный автономный рост; в) отсутствие взаимосвязи между клиническими проявлениями и состоянием менструальной функции. Помимо указанного, имеются существенные различия и во взаимоотношениях с беременностью. Как известно, беременность стимулирует экспансивный рост раковой опухоли. Напротив, для больных эндометриозом физиологическое течение беременности представляет благоприятствующий фактор — длительное воздействие гормонов желтого тела и плаценты на очаги эндометриоза обусловливает их инактивацию.
В связи с изложенным, необходимо дополнить определение «эндометриоз» — дисгормональный опухолевидный процесс, обладающий способностью к инфильтративному росту и, в редких случаях, к метастазированию.
Онкологический аспект эндометриоза до настоящего времени представляет одну из наиболее важных и дискуссионных проблем. Необходимо уточнить, что не обсуждается непосредственно возможность малигнизации заболевания, так как данный факт не вызывает сомнений. Основу разногласий по этой проблеме составляют сведения о частоте злокачественной трансформации эндометриоза, которая варьирует от 0,1—0,9 до 11—24%. Б. И. Железнов полагает, что появление сведений о высокой частоте злокачественной трансформации внутреннего эндометриоза вызвано неточностями в терминологии. Так, в понятие «стромальный эндометриоз» иногда ошибочно включают различные патологические процессы, в том числе стромальную эндометриальную саркому. Однако в подобной ситуации источником злокачественной опухоли является не эндометриоз, а эндометриальная строма.
В отношении терминологии особого внимания заслуживает диагноз «эндометриоидная карцинома». Этот термин может дезориентировать отношение к эндометриозу. На
самом деле «эндометриоидная карцинома» (согласно пояснительным замечаниям ВОЗ к гистологической классификации опухолей яичников) подчеркивает лишь гистологическую идентичность этих опухолей с поражениями эндометрия.
С учетом изложенного возникает закономерный вопрос: какова онкологическая настороженность генитального эндометриоза? На наш взгляд, не следует излишне преувеличивать степень малигнизации эндометриоза. Вероятным подтверждением подобного высказывания является отсутствие (или крайне редкое наблюдение) злокачественного перерождения эндометриоза шейки матки, маточных труб, влагалища, позадишеечной области.
Классификация. В настоящее время принято выделять генитальный (локализация патологического процесса во внутренних и наружных половых органах) и экстрагенитальный эндометриоз (развитие эндометриоидных имплантатов в других органах и системах организма женщины). В свою очередь генитальный эндометриоз подразделяют на внутренний (тело матки, ее перешеек, интерстициальные отделы маточных труб) и наружный (наружные половые органы, влагалище и влагалищная часть шейки матки, ретроцервикальная область, яичники, маточные трубы, брюшина, выстилающая углубления малого таза). Наружный генитальный эндометриоз классифицируют по отношению к брюшине: 1) внутрибрюшинный (перитонеальный) эндометриоз (яичники, маточные трубы, брюшина, выстилающая углубления малого таза) и 2) экстраперитонеальный эндометриоз (наружные половые органы, влагалище, влагалищная часть шейки матки, ретроцервикальная область). К внутрибрюшииному эндометриозу поражение яичников отнесено по двум причинам: во-первых, из-за приемлемости классификации (все органы, расположенные в брюшной полости); во-вторых, зародышевый эпителий яичников имеет общее онтогенетическое происхождение с мезотели- ем брюшины.
Эпидемиология. Эндометриоз — диагноз гистологический. Поэтому его частоту целесообразно рассматривать не в обшей популяции, а среди оперирированных гинекологических больных. В структуре показаний к хирургическо-
му лечению на долю эндометриоза приходится 0,7—0,9%. Тем не менее, в последние годы отмечена стойкая тенденция к возрастанию частоты генитального эндометриоза, в частности, за период 1960—1990 гг. в среднем на 1—7% в общей популяции.
Этиопатогенез. Общепризнанными этиологическими факторами, определяющими возникновение эндометриоза, являются: а) возраст, б) социально-экономическое положение, в) наследственность, г) гормональные и д) иммунологические нарушения. К менее вероятным этиологическим факторам эндометриоза относят ожирение, позднее начало половой жизни и поздние роды, осложненные роды, аборты, позднее наступление менархе.
С момента первых научных сообщений, посвященных проблеме эндометриоза (Н. Muller, 1854; Van Rokitansky, 1860), предложены многочисленные теории, объясняющие его происхождение и развитие.
В современном представлении выделяют следующие теории патогенеза эндометриоза: транспортную (имплантационную, трансплантационную, иммиграционную, лимфогенной, гематогенной и ятрогенной диссеминации), целомической метаплазии, эмбриональную.
Наибольшее распространение получила имплантационная теория (или теория ретроградной менструации), впервые предложенная J. A. Sampson и обоснованная в серии его работ. Согласно этой теории формирование очагов эндометриоза происходит в результате ретроградного заброса в брюшную полость клеток эндометрия, отторгнувшихся во время менструации, и дальнейшей их имплантации на окружающих органах и брюшине (естественно, при условии проходимости маточных труб).
В пользу гипотезы J. A. Sampson свидетельствуют следующие факты:
вблизи отверстий маточных труб и, следовательно, наиболее подверженные воздействию менструальной крови;
Вместе с тем, по мнению противников иммиграционной теории, результаты ряда исследований не соответствуют представлениям о подобном происхождении эндометриоза. Так, регургитация менструальной крови имеет место у 90% женщин с проходимыми маточными трубами, что существенным образом не коррелирует с частотой генитального эндометриоза в общей популяции. Однако, по-видимому, для внедрения и дальнейшего развития элементов эндометрия на брюшине и/или других структур таза необходимо наличие не только живых и способных к имплан-
тации клеток, но и факторов и условий, обеспечивающих формирование эндометриоза. Анализируя возможные причины, благоприятно воздействующие на процессы имплантации ретроградных элементов эндометрия, следует констатировать:
Теории лимфогенной, гематогенной и ятрогенной дис- семинации и ретроградной менструации по существу представляют различные концепции транспортной гипотезы происхождения эндометриоза, так как отличает их лишь способ переноса клеток эндометрия за пределы его физиологической локализации.
Теория целомической метаплазии представляет наиболее спорный аспект в патогенезе эндометриоза. В соответствии с этой гипотезой, впервые выдвинутой Н. С. Ивановым в 1887 г. и разработанной R. Meyer (1903), развитие эндометриоза происходит вследствие перерождения (метаплазии) мезотелия брюшины, в результате которого образуются фокусы эндометриоподобных желез и стромы. С точки зрения теории целомической метаплазии сторонники ее объясняют обнаружение признаков эндометриоза у жен-
щин с агенезией мюллерового протока, отсутствием матки или ее гипоплазией, дисгенезией гонад, а также случаи выявления эндометриоза у мужчин.
По мнению Robert Meyer, в отличие от зрелого мезоте- лия брюшины, элементы эмбрионального целомического покрова, вкрапленные между зрелыми клетками мезотелия, могут трансформироваться в маточно-трубный эпителий. Данная гипотеза поддерживается с позиций гистогенеза опухолей яичников: известно, что в гистогенетическом отношении эпителиальные новообразования яичников рассматриваются как опухоли парамезонефроидного (мюлле- рового) происхождения. И, несмотря на то, что яичники развиваются не из мюллерового протока (дающего начало матке и маточным трубам), источником этих опухолей является поверхностный (зародышевый) эпителий гонад, развивающийся из целомического эпителия. Последний, как известно, дает начало парамезонефральным протокам, из которых формируется трубный, эндоцервикальный и эндометриальный эпителий. Все это говорит том, что целомический эпителий гонад обладает способностью к превращению (метаплазии) в эпителий различного вида, в том числе, и эндометриального типа.
Однако, если транспортная теория происхождения эндометриоза доказана в экспериментальных условиях, то гипотеза целомической метаплазии до настоящего времени не получила подобного подтверждения. Кроме этого ряд научно не опровергнутых аспектов, представленных ниже, противоречит данной гипотезе:
Таким образом, анализируя изложенные выше сведения о патогенезе эндометриоза, необходимо констатировать, что до настоящего времени механизм происхождения и развития эндометриоза окончательно не изучен. Ни одна из известных теорий в полной мере не отвечает современным представлением об этом заболевании. Даже гипотеза «комбинации» имплантационной и метапластической теорий, согласно которой эндометриоз представляет не что иное, как метапластическую реакцию эпителия в ответ на раздражающее действие трансплантированной эндометриальной ткани, не в полной мере объясняет пути формирования и развития эктопических участков эндометриоподобных желез и стромы.
Определенный научный интерес представляет концепция этиопатогенеза, разработанная R. W. Shaw (рис. 10). Ученый попытался объединить известные гипотезы этиопатогенеза эндометриоза в единую стройную систему. Вместе с тем, многолетний опыт собственных исследований, основанный на изучении большого клинического материала, убеждает, что в отдельных наблюдениях клиническое течение эндометриоза, а также структура его очагов имеют существенные различия. Данное обстоятельство позволяет высказать предположение: происхождение (а в последую-
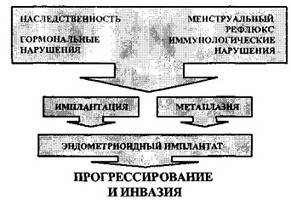
Рис. 10. Схема патогенеза эндометриоза по Я. XV Бпаш
щем и развитие) эндометриоидных фокусов, отличающихся между собой как клиническим течением, так и гистологическим строением, имеет различную патогенетическую основу.
Гистологическое строение эндометриоза во многом напоминает строение эндометрия (сочетание железистого эндометриоподобного эпителия и цитогенной стромы). Однако, в отличие от неизменной слизистой тела матки, эндометриоидная ткань менее подвержена циклическим превращениям — в частности, под влиянием прогестерона в очагах эндометриоза не происходит полноценной секреторной трансформации и, в целом, эндометриоз достаточно слабо реагирует на воздействие экзогенных гормонов.
Макроскопически эндометриоз может иметь форму узлов, инфильтратов или кистозных образований, полость которых заполнена геморрагическим содержимым (густая коричневая жидкость, по внешнему виду напоминающая горячий шоколад). Узлы эндометриоза формируются в результате проникновения в ткани окружающих фокусы эндометриоза менструальноподобных кровянистых выделений, протеолитических и липолитических ферментов, выделяемых патологическими имплантатами, а также продуктов деструкции тканей, образующихся в зоне эндометриоза. Подобное развитие эндометриоидных узлов определяет особенность их строения, а именно, отсутствие в них окружающей соединительнотканной капсулы.
Следует отметить, что эндометриоз обладает способностью к инфильтрирующему росту в окружающие ткани и органы с деструкцией последних. Более того, эндометриоз способен распространяться по кровеносным и лимфатическим сосудам, а также диссеминироваться в результате нарушения целостности стенок его кистозных форм. Иначе
говоря, эндометриоз обладает метастатическими свойствами.
Итак, отсутствие окружающей соединительнотканной капсулы, способность к инфильтрирующему росту и мета- стазированию — в совокупности сближают эндометриоз с опухолевым процессом. В то же время, в отличие от истинной опухоли, цдя эндометриоза не является характерным: а) клеточный атипизм; б) прогрессивный автономный рост; в) отсутствие взаимосвязи между клиническими проявлениями и состоянием менструальной функции. Помимо указанного, имеются существенные различия и во взаимоотношениях с беременностью. Как известно, беременность стимулирует экспансивный рост раковой опухоли. Напротив, для больных эндометриозом физиологическое течение беременности представляет благоприятствующий фактор — длительное воздействие гормонов желтого тела и плаценты на очаги эндометриоза обусловливает их инактивацию.
В связи с изложенным, необходимо дополнить определение «эндометриоз» — дисгормональный опухолевидный процесс, обладающий способностью к инфильтративному росту и, в редких случаях, к метастазированию.
Онкологический аспект эндометриоза до настоящего времени представляет одну из наиболее важных и дискуссионных проблем. Необходимо уточнить, что не обсуждается непосредственно возможность малигнизации заболевания, так как данный факт не вызывает сомнений. Основу разногласий по этой проблеме составляют сведения о частоте злокачественной трансформации эндометриоза, которая варьирует от 0,1—0,9 до 11—24%. Б. И. Железнов полагает, что появление сведений о высокой частоте злокачественной трансформации внутреннего эндометриоза вызвано неточностями в терминологии. Так, в понятие «стромальный эндометриоз» иногда ошибочно включают различные патологические процессы, в том числе стромальную эндометриальную саркому. Однако в подобной ситуации источником злокачественной опухоли является не эндометриоз, а эндометриальная строма.
В отношении терминологии особого внимания заслуживает диагноз «эндометриоидная карцинома». Этот термин может дезориентировать отношение к эндометриозу. На
самом деле «эндометриоидная карцинома» (согласно пояснительным замечаниям ВОЗ к гистологической классификации опухолей яичников) подчеркивает лишь гистологическую идентичность этих опухолей с поражениями эндометрия.
С учетом изложенного возникает закономерный вопрос: какова онкологическая настороженность генитального эндометриоза? На наш взгляд, не следует излишне преувеличивать степень малигнизации эндометриоза. Вероятным подтверждением подобного высказывания является отсутствие (или крайне редкое наблюдение) злокачественного перерождения эндометриоза шейки матки, маточных труб, влагалища, позадишеечной области.
Классификация. В настоящее время принято выделять генитальный (локализация патологического процесса во внутренних и наружных половых органах) и экстрагенитальный эндометриоз (развитие эндометриоидных имплантатов в других органах и системах организма женщины). В свою очередь генитальный эндометриоз подразделяют на внутренний (тело матки, ее перешеек, интерстициальные отделы маточных труб) и наружный (наружные половые органы, влагалище и влагалищная часть шейки матки, ретроцервикальная область, яичники, маточные трубы, брюшина, выстилающая углубления малого таза). Наружный генитальный эндометриоз классифицируют по отношению к брюшине: 1) внутрибрюшинный (перитонеальный) эндометриоз (яичники, маточные трубы, брюшина, выстилающая углубления малого таза) и 2) экстраперитонеальный эндометриоз (наружные половые органы, влагалище, влагалищная часть шейки матки, ретроцервикальная область). К внутрибрюшииному эндометриозу поражение яичников отнесено по двум причинам: во-первых, из-за приемлемости классификации (все органы, расположенные в брюшной полости); во-вторых, зародышевый эпителий яичников имеет общее онтогенетическое происхождение с мезотели- ем брюшины.
Эпидемиология. Эндометриоз — диагноз гистологический. Поэтому его частоту целесообразно рассматривать не в обшей популяции, а среди оперирированных гинекологических больных. В структуре показаний к хирургическо-
му лечению на долю эндометриоза приходится 0,7—0,9%. Тем не менее, в последние годы отмечена стойкая тенденция к возрастанию частоты генитального эндометриоза, в частности, за период 1960—1990 гг. в среднем на 1—7% в общей популяции.
Этиопатогенез. Общепризнанными этиологическими факторами, определяющими возникновение эндометриоза, являются: а) возраст, б) социально-экономическое положение, в) наследственность, г) гормональные и д) иммунологические нарушения. К менее вероятным этиологическим факторам эндометриоза относят ожирение, позднее начало половой жизни и поздние роды, осложненные роды, аборты, позднее наступление менархе.
С момента первых научных сообщений, посвященных проблеме эндометриоза (Н. Muller, 1854; Van Rokitansky, 1860), предложены многочисленные теории, объясняющие его происхождение и развитие.
В современном представлении выделяют следующие теории патогенеза эндометриоза: транспортную (имплантационную, трансплантационную, иммиграционную, лимфогенной, гематогенной и ятрогенной диссеминации), целомической метаплазии, эмбриональную.
Наибольшее распространение получила имплантационная теория (или теория ретроградной менструации), впервые предложенная J. A. Sampson и обоснованная в серии его работ. Согласно этой теории формирование очагов эндометриоза происходит в результате ретроградного заброса в брюшную полость клеток эндометрия, отторгнувшихся во время менструации, и дальнейшей их имплантации на окружающих органах и брюшине (естественно, при условии проходимости маточных труб).
В пользу гипотезы J. A. Sampson свидетельствуют следующие факты:
- присутствие в ретроградной менструальной крови живых и способных к имплантации в окружающие ткани клеток энлометрия;
- преимущественной локализацией эндометриоидных гетеротопий являются крестцово-маточные связки, брюшина прямокишечно-маточного углубления и задние листки широкой связки матки, т. е. поверхности, расположенные
вблизи отверстий маточных труб и, следовательно, наиболее подверженные воздействию менструальной крови;
- в соответствии с законом всемирного тяготения клетки эндометрия, проникшие в брюшную полость через маточные трубы, оседают (и в последующем внедряются) на брюшине и органах малого таза, в связи с чем эндометриоз верхних отделов брюшной полости встречается крайне редко;
- имплантация клеток эндометрия осуществляется, главным образом, на неподвижных структурах малого таза, так как для полного ее завершения требуется определенное время; данное положение подтверждает относительно низкая частота эндометриоза мобильных органов (маточных труб, различных отделов тонкого кишечника);
- процесс внедрения клеток эндометрия в окружающие органы и ткани определяется характером их кровоснабжения: как известно, брюшина, покрывающая органы малого таза, васкуляризирована в значительной степени выше в сравнении с мезотелием, покрывающим верхние отделы живота;
- немаловажным фактором, свидетельствующим в пользу имплантационной теории патогенеза эндометриоза, является высокая частота поражения эндометриозом яичников, так как яичники представляют идеальную зону для имплантации эндометриальных клеток. В частности, этому способствует продуцирование гонадами эстрогенов, их локализация (близость к брюшному отверстию маточных труб), неровная поверхность, высокая васкуляризация и периодическое повреждение целостности зародышевого эпителия во время овуляции.
Вместе с тем, по мнению противников иммиграционной теории, результаты ряда исследований не соответствуют представлениям о подобном происхождении эндометриоза. Так, регургитация менструальной крови имеет место у 90% женщин с проходимыми маточными трубами, что существенным образом не коррелирует с частотой генитального эндометриоза в общей популяции. Однако, по-видимому, для внедрения и дальнейшего развития элементов эндометрия на брюшине и/или других структур таза необходимо наличие не только живых и способных к имплан-
тации клеток, но и факторов и условий, обеспечивающих формирование эндометриоза. Анализируя возможные причины, благоприятно воздействующие на процессы имплантации ретроградных элементов эндометрия, следует констатировать:
- лишь отдельные жизнеспособные клетки эндометрия, проникшие в результате ретроградной менструации в брюшную полость, обладают способностью к внедрению в окружающие ткани; в экспериментальных исследованиях обнаружено, что большие железистые фрагменты эндометрия не обладают способностью к имплантации;
- в норме в перитонеальной жидкости содержится высокая концентрация половых стероидных гормонов, в частности, прогестерона, значительно превышающая ее уровень в плазме крови и обеспечивающая инактивацию эндометриальных клеток, поступающих в брюшную полость;
- в генезе эндометриоза немаловажная роль отводится объему менструальной крови, забрасываемой в брюшную полость; факторами, определяющими количество ретроградной менструальной крови, являются: а) длительность менструального кровотечения; б) состояние шеечного канала — при его сужении или атрезии объем ретроградной крови резко возрастает; в) состояние маточно-трубного просвета.
Теории лимфогенной, гематогенной и ятрогенной дис- семинации и ретроградной менструации по существу представляют различные концепции транспортной гипотезы происхождения эндометриоза, так как отличает их лишь способ переноса клеток эндометрия за пределы его физиологической локализации.
Теория целомической метаплазии представляет наиболее спорный аспект в патогенезе эндометриоза. В соответствии с этой гипотезой, впервые выдвинутой Н. С. Ивановым в 1887 г. и разработанной R. Meyer (1903), развитие эндометриоза происходит вследствие перерождения (метаплазии) мезотелия брюшины, в результате которого образуются фокусы эндометриоподобных желез и стромы. С точки зрения теории целомической метаплазии сторонники ее объясняют обнаружение признаков эндометриоза у жен-
щин с агенезией мюллерового протока, отсутствием матки или ее гипоплазией, дисгенезией гонад, а также случаи выявления эндометриоза у мужчин.
По мнению Robert Meyer, в отличие от зрелого мезоте- лия брюшины, элементы эмбрионального целомического покрова, вкрапленные между зрелыми клетками мезотелия, могут трансформироваться в маточно-трубный эпителий. Данная гипотеза поддерживается с позиций гистогенеза опухолей яичников: известно, что в гистогенетическом отношении эпителиальные новообразования яичников рассматриваются как опухоли парамезонефроидного (мюлле- рового) происхождения. И, несмотря на то, что яичники развиваются не из мюллерового протока (дающего начало матке и маточным трубам), источником этих опухолей является поверхностный (зародышевый) эпителий гонад, развивающийся из целомического эпителия. Последний, как известно, дает начало парамезонефральным протокам, из которых формируется трубный, эндоцервикальный и эндометриальный эпителий. Все это говорит том, что целомический эпителий гонад обладает способностью к превращению (метаплазии) в эпителий различного вида, в том числе, и эндометриального типа.
Однако, если транспортная теория происхождения эндометриоза доказана в экспериментальных условиях, то гипотеза целомической метаплазии до настоящего времени не получила подобного подтверждения. Кроме этого ряд научно не опровергнутых аспектов, представленных ниже, противоречит данной гипотезе:
- если эпителий брюшины обладает высокой потенциальной способностью к метаплазии, то следовало бы ожидать высокую частоту распространения эндометриоза у мужчин; вместе с тем, науке известны лишь четыре случая обнаружения так называемого эндометриоза у мужчин, причем во всех наблюдениях имело место наличие рака предстательной железы, лечение которого проводилось высокими дозами эстрогенсодержащих препаратов, а признаки эндометриоза (точнее, отдельные железистые фрагменты) установлены в ткани предстательной маточки, являющейся у мужчин остатком мюллерова протока;
- с позиций теории целомической метаплазии эндометриоидные фокусы брюшины должны были бы характеризоваться однородностью гистологической структуры, что не соответствует действительности;
- согласно гипотезе целомической метаплазии эндомет- риоподобному превращению с одинаковой частотой должен подвергаться весь целомический эпителий, выстилающий как брюшную, так и грудную полости; однако эндометриоз органов грудной клетки встречается крайне редко;
- по теории целомической метаплазии возраст пациенток и частота выявления эндометриоза должны находиться в прямо пропорциональной зависимости, т. е. пик заболеваемости эндометриоза должен бы соответствовать постменопаузальному периоду, а, как известно, в подавляющем большинстве наблюдений эндометриозом болеют женщины репродуктивного возраста.
Таким образом, анализируя изложенные выше сведения о патогенезе эндометриоза, необходимо констатировать, что до настоящего времени механизм происхождения и развития эндометриоза окончательно не изучен. Ни одна из известных теорий в полной мере не отвечает современным представлением об этом заболевании. Даже гипотеза «комбинации» имплантационной и метапластической теорий, согласно которой эндометриоз представляет не что иное, как метапластическую реакцию эпителия в ответ на раздражающее действие трансплантированной эндометриальной ткани, не в полной мере объясняет пути формирования и развития эктопических участков эндометриоподобных желез и стромы.
Определенный научный интерес представляет концепция этиопатогенеза, разработанная R. W. Shaw (рис. 10). Ученый попытался объединить известные гипотезы этиопатогенеза эндометриоза в единую стройную систему. Вместе с тем, многолетний опыт собственных исследований, основанный на изучении большого клинического материала, убеждает, что в отдельных наблюдениях клиническое течение эндометриоза, а также структура его очагов имеют существенные различия. Данное обстоятельство позволяет высказать предположение: происхождение (а в последую-

Рис. 10. Схема патогенеза эндометриоза по Я. XV Бпаш
щем и развитие) эндометриоидных фокусов, отличающихся между собой как клиническим течением, так и гистологическим строением, имеет различную патогенетическую основу.
А так же в разделе « ГЕНИТАЛЬНЫЙ ЭНДОМЕТРИОЗ »
- Методы оценки сердечной деятельности плода
- Определение биофизического профиля плода.
- Инвазивные методы пренатальной диагностики.
- ГЕСТОЗЫ
- ДЕКОМПЕНСИРОВАННАЯ ФОРМА ПЛАЦЕНТАРНОЙ НЕДОСТАТОЧНОСТИ
- ВРОЖДЕННЫЕ ПОРОКИ РАЗВИТИЯ ПЛОДА
- КЛИНИЧЕСКИ УЗКИЙ ТАЗ
- АКУШЕРСКАЯ ТАКТИКА, ИНТЕНСИВНАЯ ТЕРАПИЯ И ПРОФИЛАКТИКА КРОВОТЕЧЕНИЯ В ПОСЛЕДОВОМ И РАННЕМ ПОСЛЕРОДОВОМ ПЕРИОДАХ
- ЭФФЕРЕНТНЫЕ МЕТОДЫ ЛЕЧЕНИЯ В АКУШЕРСТВЕ
- Эфферентные методы в лечении гестозов у беременных
- Эфферентные методы в лечении гнойных септических заболеваний
- Эфферентные методы лечения при вирусных инфекциях у беременных
- Эфферентные методы лечения при иммунологическом конфликте
- Эфферентные методы при антифосфолипидном синдроме в акушерстве
- ВНУТРИУТРОБНЫЕ ИНФЕКЦИИ
- Особенности отдельных нозологических форм внутриутробных инфекций
- КЕСАРЕВО СЕЧЕНИЕ В СОВРЕМЕННОМ АКУШЕРСТВЕ
- СЕПТИЧЕСКИЕ ОСЛОЖНЕНИЯ КЕСАРЕВА СЕЧЕНИЯ
- НЕЙРОГУМОРАЛЬНАЯ РЕГУЛЯЦИЯ МЕНСТРУАЛЬНОГО ЦИКЛА
- ФИЗИОЛОГИЯ репродуктивной системы
- Нейрогуморальная регуляция менструального цикла
- Роль простагландинов в регуляции репродуктивной системы
- ГНОЙНЫЕ ВОСПАЛИТЕЛЬНЫЕ ЗАБОЛЕВАНИЯ ПРИДАТКОВ МАТКИ
- Патогенетические механизмы инфицирования внутренних половых органов.
- Этиологическая структура гнойных воспалительных заболеваний придатков матки.
- Патогенез гнойных воспалительных заболеваний придатков матки.
- Принципы и методы лечения гнойных воспалительных заболеваний придатков матки.
- Иммунокорригирующая терапия.
- ЗАБОЛЕВАНИЯ, ПЕРЕДАВАЕМЫЕ ПОЛОВЫМ ПУТЕМ (ЗППП)
- ГИПЕРПЛАСТИЧЕСКИЕ ПРОЦЕССЫ ЭНДОМЕТРИЯ
- МИОМА МАТКИ
- Патогенез миомы матки
- Классификация.
- Клиника.
- Осложнения.
- Онкологическая настороженность.
- Основные критерии.
- Дифференциальная диагностика.