Особенности анестезиологического обеспечения
Современные оперативные вмешательства в челюстно-лицевой области характеризуются значительной кро- вопотерей, продолжительной анестезией, травматич- ностью и резкими сдвигами гомеостаза. Любое оперативное вмешательство сопровождается ответной реакцией на анестезию и операционную травму. В связи с анатомотопографическим единством и одинаковой локализацией патологического процесса, но различным генезом хирургических заболеваний челюстно-лицевой области, необходим индивидуальный методический подход к анестезии при каждой нозологической группе. Возникновение адаптационной реакции на хирургическую агрессию приводит к развитию симптомокомплекса, характерного для каждой отдельно взятой группы больных, и сопровождается метаболическими сдвигами, связанными с реакцией систем организма (кровообращения, газообмена), белковой недостаточностью, нарушением водно-электролитного баланса, жирового и углеводного обмена.
В последние годы расширены показания к выполнению оперативных вмешательств у онкологических больных, у которых опухоли локализуются в области головы и шеи. Как правило, у таких больных отмечаются метаболическая нестабильность, ограниченные резервы системы кровообращения и дыхания, особенно после курса лучевого лечения и химиотерапии. Значительно возрос удельный вес операций с применением микрохирургической техники. Продолжительными и травматичными остаются костно-реконструктивные операции в области головы с внутричерепным доступом к орбитам (гипертелоризм).
Все это ограничивает возможность выполнения подобных оперативных вмешательств, требующих высокого профессионального уровня анестезиологической службы, мониторинга.
Увеличение масштабности операций способствовало широкому внедрению в стоматологическую практику современного обезболивания, основные разработки которого были «заимствованы» из общехирургической анестезиологии. В то же время при выполнении оперативных вмешательств в черепно-лицевой области предъявляются особые требования к анестезиологическому обеспечению. Обезболивание у таких больных до сих пор является одним из наиболее сложных для анестезиологической бригады, несмотря на более чем вековую историю его существования: 16 октября 1846 г., в день открытия эфирного наркоза, были выполнены операции по поводу сосудистой опухоли подчелюстной области и анкилоза височно-нижне- челюстного сустава. Технические трудности, с которыми сталкивались хирурги и анестезиологи в прошлые годы, как наследство остаются последующим поколениям специалистов, использующих общее обезболивание у больных с патологией челюстно-лицевой области. Анатомотопографические особенности челюстно-лицевой области предопределили развитие специальных методов анестезии, способствовали поиску и разработке мероприятий, не только защищающих больного от хирургической агрессии, но и позволяющих хирургу расширять показания к операциям и производить их в иной, более благоприятной обстановке. Возникающие трудности обусловлены особенностями выполнения оперативных вмешательств в области костей черепа, остеотомий орбит со стороны мозгового черепа, остеотомий верхней челюсти и в полости рта.
Основными анестезиологическими проблемами следует считать: интубацию трахеи в тех случаях, когда ограничено открывание рта и не представляется возможным выполнить классическую ларингоскопию для введения трубки в трахею; подведение ингаляционных анестетиков к верхним дыхательным путям и обеспечение эффективной защиты дыхательных путей от аспирации; создание свободного от различных приспособлений, переходников, трубок и коннекторов операционного поля в челюстно
лицевой области. Практически неустранимым является препятствие к поддержанию адекватного газообмена и свободному прохождению воздуха по верхним дыхательным путям больного во время пробуждения и в послеоперационном периоде после экстубации трахеи. Актуальной задачей остается обеспечение оптимального уровня анестезии во время операции «метаболического ухода», т.е. своевременная и оптимальная коррекция возможных обменных сдвигов во время и после операции. Не менее важной задачей является поддержание оптимальных параметров системы кровообращения и газообмена ва всех этапах анестезии. Величина операционной кровопотери во многом определяет течение наркоза и послеоперационного периода, особенно при таких заболеваниях, как нейрофиб- роматоз (болезнь Реклингхаузена) и ангиоматоз.
Этапы анестезин. Перед наркозом всем больвым проводят премедикацию, задача которой — обеспечение седативного и потенцирующего эффектов. Схема премедикации должна быть индивидуальной и в целом мало отличаться от общеанестезиологических принципов премедикации в любой области медицины. Причинами резкого эмоционального напряжения больных, а нередко и психической травмы являются волнение перед операцией, боязнь боли, возможных последствий операции и др. Это отражается на деятельности всех систем организма и объясняется возбуждением центральной нервной системы, усиленной деятельностью эндокринных желез с выбросом в кровь больших количеств адренергических веществ, стимуляцией различных отделов вегетативной нервной системы. Выраженная эмоциональная реакция способствует истощению компенсаторных механизмов и ухудшению течения анестезии. Для достижения седативного эффекта можно использовать барбитураты (люминал, нембутал), небарбитуровые снотворные (ноксирон), нейро- плегики (дипразин), нейролептики (дроперидол), седативные средства (седуксен, элениум). С большой осторожностью следует использовать для премедикации опиаты (морфин, промедол), вызывающие депрессию дыхания и кровообращения.
В период подготовки к анестезии следует предусмотреть применение препаратов, тормозящих нежелательные
рефлекторные реакции, в частности холинолитиков (атропин). В связи с тем, что атропин дает выраженный ваго- литический эффект, он является важным компонентом премедикации. Анестезиолог использует способность атропина ослаблять вагусные реакции сердца, предотвращать развитие брадикардии и асистолии синусового происхождения во вводной фазе анестезии. Ценным качеством атропина является его бронходилатирующий эффект, используемый для того, чтобы ослабить и предупредить бронхоспазм при интубации трахеи. Атропин уменьшает секрецию слизи и слюны.
Вводный период наркоза — это промежуток времени от начала анестезии до достижения хирургической стадии наркоза. Различают введение в наркоз при сохраненном самостоятельном дыхании и при общей анестезии с использованием миорелаксантов и последующей интубации трахеи. Наиболее распространенный метод вводного наркоза — применение препаратов барбитуровой кислоты. Комбинированные схемы вводного наркоза могут включать препараты, оказывающие снотворное и антигиста- минное действие. Большое распространение получила ата- ралгезия с использованием вводного наркоза седуксеном. Введение в наркоз осуществляют с помощью ингаляционных или газообразных наркотических средств, вводимых через маску наркозного аппарата или назофарингеальным способом, через аналгейзер. С этой целью используют фто- ротан, метоксифлоран, циклопропан, анекотан и др.
Интубация трахен. Особый характер патологических изменений в челюстно-лицевой области обусловливает возникновение препятствия при оказании анестезиологического пособия и во многом определяет особенности одного из ответственных этапов наркоза — интубации трахеи. Интубация трахеи — надежный способ поддержания свободной проходимости дыхательных путей, она позволяет производить отсасывание секрета из трахеи и бронхов с помощью катетеров. Патофизиологические изменения, возникающие в ответ на интубацию трахеи, имеют не меньшее значение, чем механические повреждения. Обычно применяемые методы контроля за состоянием больного не позволяют выявить быстротечные изменения в различных системах организма. В то время как для здорового челове
ка возникающие в этот период патологические изменения не имеют существенного значения, при наличии сопутствующих заболеваний они нередко представляют серьезную опасность.
Основные патофизиологические изменения, возникающие в ответ на интубацию трахеи в сердечно-сосудистой системе — это нарушение ритма и гипертензия в системе органов дыхания, гипоксия, гиперкапния, повышение сопротивления на вдохе, ларингоспазм, бронхоспазм в центральной нервной системе, повышение внутричерепного давления, в системе пищеварения — регургитация и аспирация содержимого желудка.
Изменения, происходящие в сердечно-сосудистой системе во время интубации трахеи, возникают в ответ как на ларингоскопию, так и непосредственно на введение трубки в трахею. Изменения наблюдаются даже при быстрой атравматичной интубации, не сопровождающейся кашлем. Имеется множество сообщений о нарушениях ритма и функции сердечно-сосудистой системы в ответ на интубацию трахеи. Частота нарушений ритма, по данным литературы, колеблется от 0 до 90%; такой разброс объясняется, вероятно, различным контингентом больных, характером применяемого анестетика, различиями в определении нарушения ритма (рис. 22).
Интубацию трахеи чаще всего выполняют с помощью ларингоскопа, но она может быть произведена и вслепую. Для осуществления интубации трахеи больных обычно укладывают на спину, но в некоторых ситуациях, например при компрессионном переломе позвоночника со сдавлением спинного мозга, она может быть выполнена в положении на боку и даже на животе.
Правильное положение головы облегчает интубацию трахеи. Известны два положения головы при интубации: классическое и «улучшенное*. При классическом положении головы шея резко разгибается в атланто-окципиталь- ном сочленении и затылок приводится возможно ближе к шейным позвонкам. В этом случае линия, проведенная от верхних резцов через глотку и гортань к трахее, почти полностью выпрямляется. В «улучшенном» положении по Джексону голову больного приподнимают на подушке на 10—12 см от плоскости стола, в результате чего оси горта-
Среди АД ЧСС
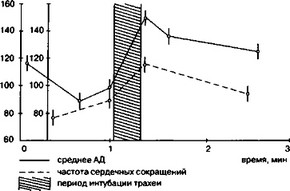
Рис 22 Динамика артериального давления и частоты сердечных сокращений при ларингоскопии и интубации трахеи
ни, глотки и полости рта сливаются в одну линию и интубация не вызывает затруднений.
При осмотре полости рта убеждаются в отсутствии в ней инородных предметов и рвотных масс, а затем вводят клинок ларингоскопа до задней стенки глотки и продвигают его в направлении голосовой щели. Прямым клинком ларингоскопа приподнимают надгортанник, обнаруживают голосовую щель, через которую проводят эндотрахе- альную трубку, а ларингоскоп извлекают. В последующем раздувают манжетку к трубке и выполняют тампонаду полости рта для создания герметичности при проведении искусственного дыхания.
Анатомо-топографические особенности челюстно- лицевой области редко бывают единичными; как правило, они представляют собой патологический комплекс, степень выраженности которого зависит от причины и длительности заболевания, размеров поражения, возраста больного, количества предшествовавших операций и многих других факторов. Все анатомические изменения черепно-лицевой области тесно связаны с деформацией
костного скелета и мягких тканей лица и шеи. Чаще всего встречаются сочетания костных и мягкокостных изменений, которые тесно взаимосвязаны и приводят к ограничению открывания рта или полному его закрытию. Нарушение анатомических взаимоотношений необходимо учитывать при оказании анестезиологического пособия во время операции.
При интубации трахеи применяют три основные методики: 1) назотрахеальную, т.е. интубацию трахеи с проведением трубки через нос; 2) оротрахеальную, классическую методику с визуальным контролем, при которой трубку направляют в трахею с помощью прямого или изогнутого клинка ларингоскопа либо вслепую; 3) интубацию трахеи через предварительно сделанное отверстие в трахее (трахеостома).
Назотрахеальную интубацию применяют у 80 % стоматологических больных, которым производят интубацию трахеи. Введение интубационной трубки через нос осуществляют с помощью прямой ларингоскопии, вслепую, под контролем дыхания, с обработкой слизистой оболочки аппликационными анестезирующими средствами.
В недалеком прошлом у больных с полностью закрытым ртом интубацию трахеи производили по проводнику или с помощью боковой рентгеноскопии шеи, при которой основные анатомические ориентиры приходилось наблюдать на экране рентгеновской установки. Наиболее эффективной и наименее травматичной считают интубацию трахеи с помощью современных волоконных эндоскопов типа «Олимпус*. Эту методику интубации применяют у больных, у которых имеются аномалии развития, врожденные или травматические дефекты челюстей или окружающих мягких тканей (анкилозы височно-нижнечелюстного сустава, рубцовые контрактуры, микрогения и др.), препятствующие применению обычных методик интубации трахеи. В успешном осуществлении любой модификации назотрахеальной интубации большое значение имеют подготовка интубационной трубки, выбор соответствующего носового хода, знание анатомических взаимоотношений верхних дыхательных путей. Применение эндоскопов предполагает знание технических возможностей приборов с волоконной оптикой и особенностей анатомо-топографи-
ческих соотношений в этой области, что позволяет анестезиологу предвидеть возникновение препятствий по ходу интубации.
Оротрахеальная интубация (через рот) у больных с деформацией челюстей или травмой имеет ограниченное применение, так как не позволяет по ходу операции сопоставить отломки костей в правильном положении. Интубацию через рот целесообразно производить в тех случаях, когда оперативное вмешательство выполняют в основном на мягких тканях нижней зоны лица и шеи или невозможно провести интубационную трубку через носовой ход.
Показания к выполнению трахеостомии с целью интубации должны быть строго ограничены в связи с тем, что правильный выбор одной из указанных методик (оро- или назотрахеальной) позволяет произвести ее практически при любых патологических изменениях челюстно-лицевой области. Исключения составляют превентивные трахеостомии, выполняемые до операции и в случае необходимости обеспечения свободной проходимости верхних дыхательных путей при иммобилизации челюстей у больных с тяжелой черепно-мозговой травмой. Трудновыполнимые интубации трахеи у таких больных приводят к значительным изменениям функции кровообращения и газообмена, свидетельствующим об ухудшении сократительной способности сердечной мышцы, гипоксии и гиперкапнии. Степень выраженности этих изменений находится в прямой зависимости от травматичности и продолжительности интубации, качества анестезии и вентиляции легких в период вводного наркоза (рис.23).
Частота осложнений при интубации зависит от степени подготовки анестезиолога и особенностей деформации челюстно-лицевой области. При интубации возможны повреждения передних зубов, губ, задней стенки глотки и голосовых складок, которые нередко возникают при грубых манипуляциях. Не составляет труда выполнение интубации у лиц обычной конституции, но у тучных пациентов с короткой шеей или имеющих ограничения подвижности в шейном отделе позвоночника интубация часто затруднена. В этих случаях применяют ларингоскоп с изогнутым клинком, i згиб которого повторяет анатомический изгиб полости рт*. и глотки, чем обеспечивает более свободную

Рис 23 Транстрахеальная интубация трахеи
интубацию. Тактильную интубацию по методу Кюна производят следующим образом. Располагаясь справа от больного, анестезиолог вытягивает его язык. Двумя пальцами, введенными глубоко в ротовую полость, ощупывает корень языка и надгортанник. Захватывает надгортанник и отодвигает его вперед вместе с корнем языка, в результате чего вход в трахею становится свободным для введения эндотрахеальной трубки.
Период поддержания общей анестезии. При выполнении оперативного вмешательства и для поддержания общей анестезии можно использовать любой препарат, обеспечивающий адекватную защиту организма от операционной агрессии, или комбинацию таких препаратов. С этой целью при комбинированном эндотрахеальном наркозе в качестве основного анестетика чаще всего используют фторотан, метоксифлоран, эфир, препараты НЛА. В период поддержания наркоза необходимо разумное управление компонентами анестезии. Применение фармакологически разнонаправленных средств (анальгетик
обеспечивает аналгезию, наркотик — сон во время операции, миорелаксанты расслабление мускулатуры и возможность управления газообменом) позволяет обеспечит!, комбинированное общее обезболивание.
В последние два десятилетия для поддержания анестезии у больных с заболеваниями челюстно-лицевой области чаще всего использовали нейролеитаналгезию. При некоторых реконструктивных операциях на мягких тканях лица, сравнительно непродолжительных и малотравматичных, целесообразно сохранение спонтанного дыхания. В настоящее время для поддержания анестезии широко применяют электроанестезию.
Оценку адекватности анестезии проводят на основе результатов анализа: частоты сердечных сокращений, артериального давления, га job крови, кислотно-щелочного состояния, ЭЭГ, ЭКГ. Одной из новых методик оценки адекватности наркоза является вариационная пульсо- метрия — метод математического анализа ритма сердца. С этой целью проводят также определение концентрации адреналина и норадреналина. Критериями оценки адекватности анестезии считают данные, полученные при интегральной реографии и многоканальной электротермометрии.
Заключительный этап общей анестезии. Проведение этого этапа планируется задолго до окончания операции. К этому времени анестезиолог восстанавливает у больного основные показатели гомеостаза: газообмен, дыхание, кровообращение, объем циркулирующей крови (ОЦК). У больных с послеоперационным перемещением тканей в челюстно-лицевой области не всегда удается добиться адекватного дыхания сразу после окончания операции. В этих случаях экстубацию выполняют в палате интенсивной терапии спустя 6—8 ч., осуществляя при этом продленную искусственную вентиляцию легких.
После прекращения анестезии могут возникнуть рвота, регургитация (пассивное затекание содержимого желудка в трахею), ларинго- и бронхоспазм. В этот период анестезиолог должен находиться рядом с больным до тех пор, пока окончательно не стабилизируется состояние и больной не будет переведен в палату интенсивной терапии.
Источник: Грицук С.Ф., «Анестезия в стоматологии» 1998
А так же в разделе « Особенности анестезиологического обеспечения »
- Анестезия в хирургии опухолей челюстно-лицевой области
- Анестезия у больных с деформациями черепно-лицевой области
- Анестезиологическое обеспечение реконструктивных и пластических операций с применением микрохирургической техники
- Обезболивание у больных с воспалительными заболеваниями челюстно-лицевой области
- Анестезиологическое обеспечение операций у больных пожилого и старческого возраста
- Хирургический стресс. Концепция адекватности анестезии и метаболической защиты пациента при реконструктивных операциях на лицевом и мозговом черепе
- ПОСЛЕОПЕРАЦИОННАЯ ИНТЕНСИВНАЯ ТЕРАПИЯ
- Профилактика и лечение дыхательной недостаточности
- Поддержание эффективной гемодинамики
- Метаболическая коррекция (трансфузионная терапия, парентеральное и энтеральное питание)
- Интенсивная терапия у больных с острыми воспалительными заболеваниями челюстно-лицевой области
- Принципы трансфузионной терапии больных с флегмонами челюстно-лицевой области