9.2. Восприимчивый организм
Из вышесказанного можно заключить, что вероятность включения в ц куляцию паразита третьего звена — реципиента или восприимчивого ор низма — зависит как от состояния самого организма, так и от мощно источника инфекции и эффективности механизма передачи. Иначе го ря, вероятность образования третьего звена и, соответственно, завер]
ния формирования элементарной ячейки эпидемического процесса — это интегральный показатель участия всех трех звеньев.
Справедливость этого положения можно оценить, в частности, по приведенным выше данным об опасности источников в зависимости от тяжести течения болезни: чем дольше выделяется паразит и чем выше его концентрация в выделениях, тем больше вероятность получения достаточной дозы для возникновения инфекционного процесса у восприимчивых людей.
Вполне логичное представление о том, что вероятность формирования третьего звена и, соответственно, развития эпидемического процесса зависит от возможностей передачи паразита, может быть подтверждено множеством наблюдений. Так, более всего население страдает от так называемых неуправляемых (отсутствуют средства специфической профилактики) воздушно-капельных инфекций; высока заболеваемость кишечными инфекциями среди населения, которое не обеспечено доброкачественной водой и т. д. и т. п. В частности, значение 2-го звена можно проследить на примере возникновения и распространения инфекций дыхательных путей, при которых инфекционный процесс может протекать как в виде болезни, так и первичного носительства. Для нозоформ с воздушно-капельным механизмом передачи (считается, что он чрезвычайно эффективный, как бы эталон высокой мощности — в очагах заражается практически 100% людей) определен индекс манифестности (прежнее название — индекс контагиозности), как избирательный показатель восприимчивости (заражаются все, а заболевают только восприимчивые). Эти индексы были определены во времена, когда не проводилось прививок и не существовало антибиотиков. Так, для кори он равен 1 (все заразившиеся, у которых отсутствует иммунитет, переносят инфекцию в манифестной форме), и соответственно, вывод: восприимчивость к вирусу кори всеобщая (100%). Для скарлатины индекс манифестности равен 0,4 (среди достоверно заразившихся токсигенным штаммом гемолитического стрептококка заболевает 40%, у остальных, возможно, имеет место первичное посительство возбудителя) — восприимчивость, следовательно, равна 40%. При дифтерии такой индекс равен 0,2 (восприимчивость — 20%), и так были определены, а иногда рассчитаны без должной объективной оценки, индексы для целого ряда нозоформ. Для кори, скарлатины и дифтерии индексы были получены на основании оценки характера развития эпидемического процесса на достаточно значительных, изолированных от общения с внешним миром популяциях (жители острова Фиджи и Фарерских островов, которые не имели иммунитета против возбудителей указанных болезней) и могут считаться достоверными. Между тем уже давние наблюдения свидетельствовали о сомнительности узверждения, что индекс характеризует только степень восприимчивости (и ничего более). Так, в допрививочное время в Англии было установлено (Frost, 1928), что при общении с больными дифтерией в домашних условиях соотношение носители : больной составило 6:1 (1 больной в результате 7 эффективных заражений), в школах 47:1 (1 больной при 48 эффективных заражениях), т. е. в первом случае вероятность заболеть у восприимчивых детей была примерно в 8 раз выше, чем во втором, когда теснота общения для большинства была выражена меньше. Во втором случае при всей активности механизма передачи он не смог обеспечить доставку возбудителя в дозе, которая вызвала болезнь, с той же вероятностью, что имела место в первом случае. Иначе говоря, приведенные материалы о достоверно вычисленных индексах манифестности при дифтерии и скарлатине отражают среднестатистическую вероятность встречи с дозами, ведущими к развитию манифестных форм инфекции, в достаточно большой популяции неиммунных людей. В отдельных очагах в зависимости от тесноты общения ситуация, очевидно, имела определенные отличия. Таким образом, даже при воздушно-капельных инфекциях мы видим значимость механизма передачи для формирования третьего звена.
Итак, возможность формирования третьего звена определяется прежде всего степенью видовой восприимчивости к различным паразитам, которая характеризуется дозой, вызывающей заболевание или носительст- во. Например, при брюшном тифе доза, вызывающая болезнь у 50% зараженных добровольцев, равна 107 микробных клеток вирулентного штамма, при дизентерии — 0,5x103—0,5x104 микробных клеток, при туляремии люди заболевают при введении им 25—50 микробных клеток вирулентного штамма Shu. Однако на фоне видовой восприимчивости имеют значение также следующие переменные величины:
• совокупная мощность источника инфекции и механизма передачи, которая обеспечивает доставку необходимой для инфицирования дозы паразита;
• вирулентность возбудителя (чем выше вирулентность, тем меньше инфицирующая доза) — см. табл. 8.2;
• индивидуальные характеристики восприимчивости людей, подвергающихся заражению;
• возможные фенотипные трансформации восприимчивости, связанные с внутренними (например, сопутствующие заболевания) или внешними (облучение и т. д.) факторами.
После перенесения инфекции, как известно, развивается иммунитет. Если формируется одна элементарная ячейка, то иммунными станут только два человека (бывший источник инфекции и заразившийся от него), но с развитием эпидемического процесса иммунитет будет развиваться у множества людей, причем число иммунных находится в прямой зависимости от размаха эпидемического процесса. Таким образом, эпидемический процесс ведет к развитию не индивидуального, а популяционного иммунитета.
Как уже сказано, человек болеет в результате заражения паразитами животных. Это возможно потому, что ряд паразитов животных не имеет закрепленной в эволюции строгой адаптации к жизни в организме какого-то определенного вида хозяина, поскольку популяции многих животных достаточно разрежены и существование паразитических видов за их счет практически не реально. Некоторое биологическое сходство с животными, прежде всего с теплокровными, привело к тому, что от подобных возбудителей может пострадать человек. В таких случаях говорят о зоонозах. При зоонозах эпизоотический процесс, если в циркуляцию возбудителя вовлекаются люди, формирует эпидемический процесс. Схема такой трансформации может выглядеть так, как представлено на рис. 9.3.
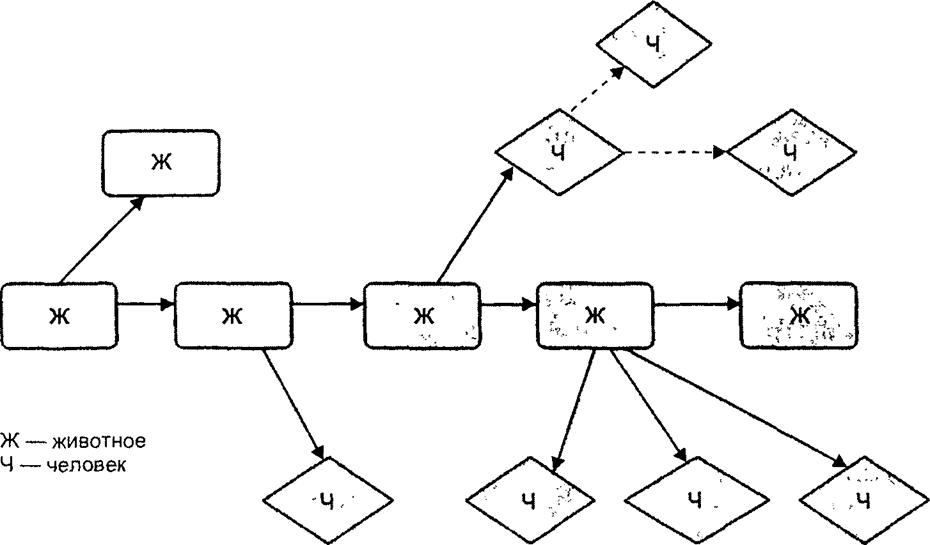
Рис. 9.3. Формирование эпидемического процесса при зоонозах |
В тех случаях, когда эпизоотический процесс развивается среди домашних животных (включая птиц), говорят об антропургических очагах. К антропургическим должны быть отнесены также очаги, которые формируются за счет так называемых синантропных животных, т. е. не одомашненных, но живущих около человека — в его домах или населенных пунктах (крысы, домовая мышь, голуби, воробьи и т. д.).
Наличие эпизоотий среди диких животных свидетельствует о существовании природно-очаговых инфекций, которые могут быть опасны для человека. Суммируя множество своих экспедиционных исследований в различных регионах СССР и на территории Ирана, а также обобщая данные мировой науки Е. Н. Павловский сформулировал теорию природной очаговости многих заболеваний. Согласно этому учению, природные очаги заболеваний образовались в определенных климатических и ландшафтных условиях ввиду исторически сложившихся биоционотических взаимоотношений между различными обитателями, приспособившимися жить в этих условиях (дикие животные, в том числе в ряде случаев птицы, пресмыкающиеся, земноводные, рыбы, моллюски, членистоногие и др.). К указанным биоционотическим взаимоотношениям в эволюции приспособились различные паразитические виды, которые, по существу, стали одним из составляющих компонентов указанных биоционотических связей
Возбудители природно-очаговых заболеваний могут вызвать образование вторичных антропургических очагов, включая в циркуляцию си- нантропных (например, голуби, воробьи, которые формируют очаги японского энцефалита среди городских жителей) и домашних (собаки при бешенстве) животных.
Среди животных возбудители инфекций перемещаются соответственно общему закону о единой системе — локализация возбудителя в организме и механизм передачи, однако нередко из-за невозможности существования паразита за счет одного механизма передачи эпизоотический процесс поддерживается с помощью нескольких локализаций и, следовательно, нескольких механизмов передачи. Не исключено, что в этой сумме имеется основной механизм, но в разных ситуациях, как показывают наблюдения, значимость основного и дополнительного может измениться. Так, туляремия существует в природных очагах несомненно за счет трансмиссивного механизма передачи (иксодовые клещи), но в некоторых конкретных ситуациях эпизоотический процесс среди грызунов поддерживается при передаче возбудителя пищевым и водным путем.
Заражение человека осуществляется в одних случаях в соответствии с механизмом передачи, который сложился в естественных условиях среди животных, в других — оно может происходить иным путем. Так, сибирская язва животных — это типичная кишечная инфекция, сибирская язва у людей в 98—99% случаев развивается в виде кожной формы, т. е. заражение чаще всего реализуется контактным путем (уход за животными, непрямой контакт за счет объектов животного происхождения — кожи, шкур, шерсти и др.).
Человек при зоонозных инфекциях чаще всего является биологическим тупиком — дальнейшее существование паразита становится невозможным. Это связано с тем, что человек в роли источника инфекции, как правило, не может конкурировать по опасности для окружающих с зараженными животными. В условиях общества, т. е. в условиях общения среди людей, не может реализовываться тот механизм передачи, который проявляется в животном мире. Наконец, хотя это нуждается в дальнейшем изучении, допускается мысль о том, что при пассировании через организм человека возможно снижение вирулентности возбудителя
Лишь в очень редких случаях (на рис. 9.3 это отображено не связующей линией, а в виде пунктира) опасность человека становится реальной. С очевидностью это прослежено при некоторых тропических заболеваниях — желтой лихорадке («желтая лихорадка городов») и болезни денге. Описаны также случаи заражения от людей, больных крымской геморрагической лихорадкой (заболевание регистрируется на юге страны в равнинных и предгорных местах, расположенных между Черным и Каспийским морями) Кровь больных, у которых возможны кровоизлияния и кровотечения, содержит вирус, поэтому при уходе и оказании помощи больным, а также при различных лечебных манипуляциях возможно заражение окружающих, в частности медицинского персонала. Но, конечно, эти эпизолы не могут обеспечить сохранение возбудителя в природе.
Как уже говорилось, человек может пострадать при заражении факультативными паразитами, для которых основной средой обитания является внешняя среда. Такие нозоформы получили не совсем удачный термин — сапронозы, отражающий определенную непоследовательность выбора. Хотя всем этим агентам свойственен сапрофитический способ питания (они существуют за счет утилизации неживых органических субстратов), вряд ли правильно было брать этот признак за основу, поскольку две другие группы (антропонозы, зоонозы) названы по месту основного обитания Кроме того, надо иметь в виду, что целый ряд облигатных паразитов также обладает сапрофитическим способом питания (многие обитатели кожных покровов и просвета кишечника).
При сапронозах формирование эпидемического процесса можно представить в виде схемы (рис 9 4).
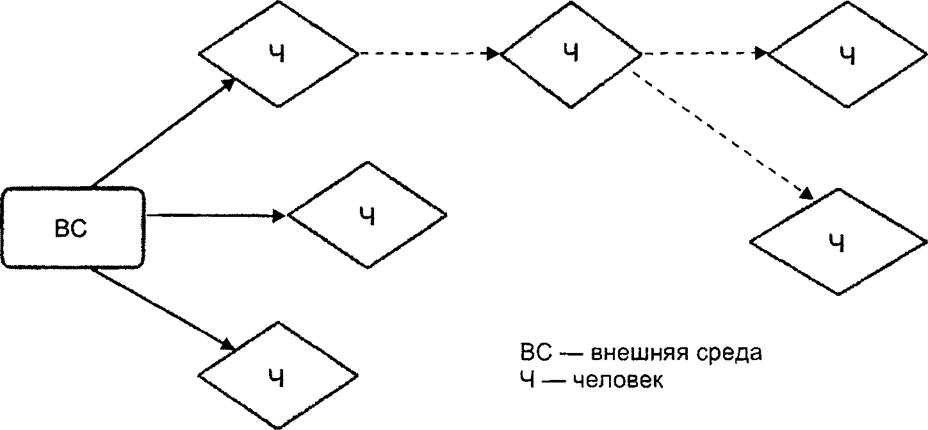
Рис 9.4. Формирование эпидемического процесса при сапронозах |
На рис 9.4 видно, что люди заражаются при попадании возбудителя из внешней среды (например, возбудителями газовой гангрены и столбняка, которые проникают в раны из почвы), однако иногда возможно заражение от человека (в стационарах регистрируются вспышки, вызванные свободноживущей во внешней среде синегнойной палочкой, которые оказываются результатом заражения пациентов друг от друга из-за нарушений правил асептики и антисептики при медицинских манипуляциях).
Завершая описание трех групп инфекций, необходимо указать на некоторую терминологическую непоследовательность, которая нередко встречается в литературе. Речь идет о том, что зоонозные инфекции предлагают называть зооантропонозами или даже антропозоонозами, поскольку эти болезни опасны для человека и население от них страдает (в отличие от инфекций только животных, т е. истинно зоонозных) Эволюционный подход, однако, имеет в виду обозначать группы по признаку не случайного поражения человека, а по основному хозяину, который
обеспечивает существование и сохранение паразитического вида. Если для дифференциации использовать случайные явления, то можно дойти до абсурда. Так, например, чуму пришлось бы обозначить как сапрозоо- антропоноз, поскольку, по современным данным, возбудитель чумы, как и другие иерсинии, обитает в основном во внешней среде, т. е. он, по-видимому, должен быть отнесен не к облигатным, а к факультативным паразитам (подробнее см. в разделе «Частная эпидемиология»). Или, скажем, сальмонеллы, которые могут вызвать крупные пищевые токсикоин- фекции за счет размножения и накопления в пищевом продукте, должны быть отнесены к возбудителям зоосапроантропонозов. Из этого правила можно выделить одно исключение; для ряда биогельминтов (лентец широкий и некоторые другие) основными хозяевами могут быть люди и животные (кошки и др ), т е. эволюция паразита привела к приспособленности к жизни параллельно как в организме человека, так и животных Иначе говоря, ио-видимому, это истинные зооантропонозы.
Источник: Л. П. Зуева, Р. X. Яфаев, «ЭПИДЕМИОЛОГИЯ» 2005
А так же в разделе «9.2. Восприимчивый организм »
- Глава 8 ОПРЕДЕЛЕНИЕ ЭПИДЕМИЧЕСКОГО ПРОЦЕСС
- 8.1. Характеристика паразитов
- Характеристика макроорганизма (хозяина)
- Глава 9 СОСТАВНЫЕ ЧАСТИ (ВНУТРЕННЯЯ СТРУКТУРА) ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
- 9.1. Источник инфекции
- 9.2. Механизм передачи
- Глава 10 ПОПУЛЯЦИОННЫЙ ИММУНИТЕТ И ТЕОРИЯ САМОРЕГУЛЯЦИИ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
- Теория саморегуляции эпидемического процесса
- Глава 11 КЛАССИФИКАЦИЯ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ
- Глава 19 ХАРАКТЕРИСТИКА ПРОЯВЛЕНИЙ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
- Глава 13 ФАКТОРЫ ЭПИДЕМИЧЕСКОГО ПРОЦЕССА
- Глава 14 ЭПИДЕМИОЛОГИЧЕСКИЙ НАДЗОР
- 14,1. Оперативный анализ
- 14.2. Ретроспективный анализ
- Глава 15 ПРОФИЛАКТИЧЕСКИЕ И ПРОТИВОЭПИДЕМИЧЕСКИЕ МЕРОПРИЯТИЯ
- 1.5.1. Общая структура профилактических и противоэпидемических мероприятий
- Дезинфекция 15,2. Дезинфекция (обеззараживание)
- 15.2.2, Дезинсекция
- 15.2.3. Дератизация
- 15.3. Специфическая профилактика инфекционных заболеваний