Синдром Бругада
Данное заболевание характеризуется наличием высокого риска возникновения полиморфной (пируэт) желудочковой тахикардии, фибрилляции желудочков и внезапной смерти.
Генетические исследования показали, что синдром Бругада является аллельным заболеванием по отношению к третьему типу синдрома Романо- Ворд'а, при котором наблюдается мутация гена, кодирующего функцию натриевого канала (SCN 5А). Заболевание передается по аутосомно-доминан- тному типу. Недавно С. Bezzine с соавт. описали вариант мутации данного гена, при котором у больных одновременно возникают клинические проявления и ЭКГ-данные, характерные для синдрома Бругада и синдрома удлиненного QT (LQT 3). Три варианта мутации гена SCN 5А могут быть выявлены у больных с синдромом Бругада, которые характеризуются наличием: 1) недостаточности транспортной функции натриевых каналов; 2) снижения тока в результате сдвига в вольтаж-зависимой и время-зависимой активации тока натрия; 3) снижения вклада тока натрия в раннюю фазу потенциала действия в результате ускоренной инактивации натриевых каналов.
Результаты исследований, проведенные с Antzelevitch с сотр., позволяют предположить, что электрофизиологические нарушения при синдроме Бругада обусловлены изменениями ионного тока, возникающего в фазу 1 потенциала действия в эпикардиальном слое правого желудочка. В результате в этой фазе исчезает куполообразный подъем потенциала действия только в эпикардиальных клетках, что приводит к выраженной трансмуральной дисперсии в реполяризации и рефрактерности и к возникновению уязвимого окна, в течение которого возникшая экстрасистола может спровоцировать развитие ри-энтри тахикардии.
В настоящее время в клинике пока недостаточно данных, позволяющих выделить факторы, которые провоцируют возникновение жизнеопасной аритмии. Но, исходя из теоретических предпосылок, у таких больных следует избегать использования препаратов, значительно тормозящих транспорт через клеточную мембрану ионов натрия, кальция или усиливающих выход из клетки калия и хлора. Возникновение ишемии миокарда увеличивает вероятность появления аритмогенного участка у таких больных и развитие полиморфной желудочковой тахикардии (типа пируэт) с очень большой частотой ритма, что затрудняет дифференциацию её с фибрилляцией желудочков.
Критерии диагностики:
- Повышение сегмента ST (спонтанное или индуцированное) в Va-V3 на 1 мм и более, которое может изменяться в течение нескольких дней (рис. 31).
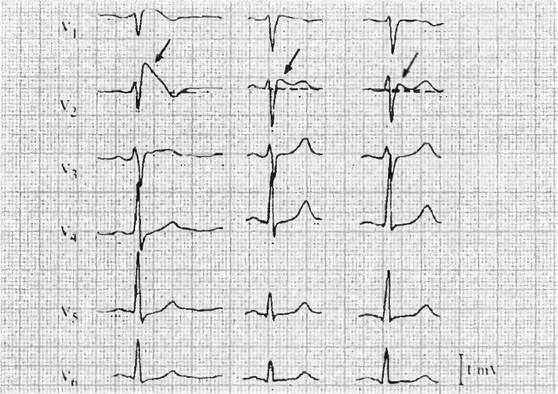
Рис. 31. Три варианта ЭКГ у больных синдромом Бругада.
В правых грудных отведениях сегмент ST в различной степени приподнят и имеет форму седла
- Блокада правой ножки (полная или неполная) пучка Гиса.
- Обморочные состояния, желудочковая тахикардия, фибрилляция желудочков (внезапная смерть).
Изменения на ЭКГ могут носить непостоянный характер. Но их проявления индуцируются с помощью введения препаратов I класса (в частности, новокаи- намида). С.А. Remme с сотр., используя лекарственную пробу (флекаинид, но- вокаинамид) среди 37 реанимированных в связи с идиопатической фибрилляцией желудочков у 9 больных выявили синдром Бругада. С этой целью новока- инамид вводился в дозе 1000 мг внутривенно со скоростью 50 мг в минуту.
Чувствительность и специфичность предложенных критериев диагностики пока не изучены. В частности, остается неясной информативность, например, наличия лишь подъема сегмента ST, в т.ч. провоцируемого препаратами класса I. В некоторых случаях изменения на ЭКГ становятся более отчетливыми после смещения электродов V1—V3 на 1 межреберье выше. Поэтому распространенность данного заболевания в общей популяции неизвестна.
Клинические данные. Заболевание проявляется преимущественно в молодом возрасте (в среднем 38 лет), но встречается и в пожилом - 70 лет и старше.
Характерными симптомами являются обмороки и пароксизмы полиморфной желудочковой тахикардии. Внезапная остановка кровообращения и внезапная смерть чаще регистрируются среди мужчин. Их причиной может быть возникновение пароксизма полиморфной желудочковой тахикардии или развития фибрилляции желудочков.
При проведении внутрисердечной программированной кардиостимуляции после реанимации у большинства больных (около 70%) удается вызвать желудочковую тахикардию или фибрилляцию желудочков при нанесении экстрастимулов в правом желудочке. Но имеются указания, что электрокардиостимуляция, выполненная из коронарного синуса вызывает пароксизм аритмии даже в тех случаях, когда она не провоцируется при эндо- кардиальной стимуляции (J. Carlsson с соавт.).
Описаны случаи внезапной смерти среди таких больных, возникавшей на фоне повышения температуры тела. Среди имеющих данное заболевание ежегодно у 10% регистрируются случаи возникновения жизнеопасной аритмии.
При обследовании этих больных не удается выявить наличие каких-либо структурных изменений со стороны сердца.
Группу высокого риска летального исхода составляют реанимированные больные, больные с желудочковой тахикардией, с отягощенным семейным анамнезом, а также больные с обмороками.
Лечение. Наиболее безопасным методом для купирования полиморфной желудочковой тахикардии является электроимпульсная терапия. Для профилактики жизнеопасных аритмий, несмотря на отсутствие соответствующих исследований, рекомендуется осуществлять имплантацию кардиовер- тера-дефибриллятора. В частности, их следует устанавливать больным, выжившим после реанимации, а также больным с обмороками в анамнезе или после пароксизма полиморфной желудочковой тахикардии, или при наличии в семье случаев внезапной кардиальной смерти в молодом возрасте.
Целесообразность использования данного метода профилактики внезапной смерти у остальных больных считается сомнительной.
Эффективность и безопасность антиаритмических препаратов в профилактике жизнеопасных нарушений желудочкового ритма сердца у больных с синдромом Бругада не установлена. Высказываются предположения, что использование препаратов, которые угнетают транспорт ионов натрия и кальция или увеличивают выход из клетки ионов калия и хлора может оказать проаритмическое действие. Более того, отрицательное влияние могут оказывать жирные кислоты, тормозящие транспорт натрия, а также препараты активирующие циклическую ГМФ (например, нитраты).
Источник: Мазур Н.А., «ПАРОКСИЗМАЛЬНЫЕ ТАХИКАРДИИ» 2005
А так же в разделе «Синдром Бругада »
- Предисловие
- Механизм возникновения аритмий
- Общие клинические методы обследования больных с подозрением на наличие пароксизмальной тахикардии
- Пароксизмальные наджелудочковые тахикардии
- Синусовая спонтанная тахикардия
- Синусоваяузловая реципрокная пароксизмальная тахикардия
- Фокальная (эктопическая) предсердная тахикардия
- Предсердная макро-ри-энтри тахикардия
- Предсердно-желудочковая узловая тахикардия
- Эктопическая (фокальная) тахикардия из атриовентрикулярного соединения
- Непароксизмальная реципрокная тахикардия из атриовентрикулярного соединения
- Пароксизмальная предсердно-желудочковая реципрокная тахикардия
- Фибрилляция и трепетание предсердий
- Желудочковые тахикардии
- Желудочковая тахикардия у больных без органического поражения сердца
- Синдром удлиненного QT (LQT)
- Синдром укороченного QT
- Аритмогенная правожелудочковая кардиомиопатия
- Трепетание и фибрилляция желудочков
- Внезапная смерть и ее профилактика
- Факторы риска возникновения фибрилляции желудочков у больных ИБС
- Профилактика ВСС у больных ИБС
- Гипертрофическая кардиомиопатия и риск ВСС
- Дилатационная кардиомиопатия, сердечная недостаточность и риск ВСС
- Клапанные пороки и риск внезапной смерти
- Аномалии отхождения коронарных артерий, мышечные мостики и риск внезапной смерти
- Нарушение функции проводящей системы сердца
- Внезапная смерть после аблации предсердно-желудочкового узла и после имплантации водителя ритма
- ВСС у людей со «здоровым» сердцем
- Реанимация в амбулаторных условиях
- Антиаритмические препараты
- Выбор антиаритмической терапии, её безопасность и эффективность при длительном лечении
- Литература
- Приложение Алгоритмы дифференциальной диагностики и выбора терапии