17.2. Коклюш
Определение
Коклюш — острая антропонозная инфекция, вызываемая бактериями коклюша (Bordetella pertussis), сопровождаемая катаральными явлениями в верхних дыхательных путях и приступообразным спазматическим кашлем.
Стандартное определение случая заболевания (Центр контроля за заболеваниями, США):
Клиническое определение случая:
Кашлевое заболевание, длящееся минимум 2 нед, сопровождающееся одним из следующих признаков: приступы кашля, шумный вдох в конце приступа, рвота после кашля.
Лабораторные критерии:
Выделение Bordetella pertussis из клинических проб.
гв5
Классификация мучая:
Вероятный — отвечает клиническому определению случая, не подтвержден лабораторно и не имеет эпидемиологической связи с лабораторно подтвержденным случаем.
Подтвержденный — клинически похожее заболевание, лабораторно подтверждено и/или имеет эпидемиологическую связь с лабораторно подтвержденным случаем.
История
Первое описание этой болезни было сделано в 1578 г. Гийомом де Байю во время эпидемии коклюша в Париже, сопровождавшейся высокой летальностью. В России коклюш впервые описан М. Максимович-Амбо- диком (1784 г.) и более подробно — педиатром Хотовицким (1847 г.). Первые статистические сведения были опубликованы в конце XIX в. Согласно им, коклюш в те годы занимал среди основных детских инфекционных заболеваний четвертое место по смертности детей до 5 лет, уступая первые три места кори, скарлатине и дифтерии.
Возбудитель
Возбудителем коклюша является палочка Bordetella pertussis, относящаяся по современной классификации к роду Bordetella, включающему в себя В. pertussis, В. parapertussis и др. Для бактерий этого рода характерен тканевой тропизм к цилиарному эпителию респираторного тракта соответствующего хозяина. Паразитами для человека являются В. pertussis и В. parapertussis (возбудитель паракоклюша).
Популяции коклюшных бактерий характеризуются гетерогенностью. Различают 4 серологические фазы, от больных возбудители выделяются в вирулентной форме (1 фаза), но на простых питательных средах быстро трансформируются, теряя поэтапно вирулентность (II—IV фазы).
Наиболее важным признаком бордетелл с точки зрения идентификации возбудителя, патогенеза инфекции и формирования иммунитета является содержание фимбриальных видоспецифических агглютиногенов. В настоящее время выделяют 4 разновидности (серотипа) коклюшного микроба: 1.2.3; 1.2.0; 1.0.3 и 1.0.0. Указанные разновидности выделяются повсеместно, но их соотношения неодинаковы на разных территориях и на одной территории в разное время (рис. 17.14).
В многолетней динамике наблюдается смена ведущих антигенных вариантов возбудителя. Имеются данные, что наиболее вирулентна разновидность, содержащая антиген 2, особенно вариант 1.2.0. Вирулентность циркулирующих штаммов подвергается постоянному изменению. В настоящее время под воздействием увеличения охвата иммунизацией детей преобладают культуры со сниженной вирулентностью (см. рис. 17.14), хотя у непривитых и сейчас могут развиться тяжелые формы болезни и выделяться вирулентные культуры.
Качественно новым этапом в развитии представлений о коклюше стало появление концепции о доминирующей роли экзотоксина коклюшного микроба в патогенезе инфекции и формировании иммунитета. Кок- гее
Часть It. ЭПИДЕМИОЛОГИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИИ
люшный токсин является основным фактором патогенности коклюшного микроба, В организме хозяина он вызывает лимфоцитоз, сенсибилизацию к гистамину, большинство системных поражений и одновременно обладает высокой иммуногенностью.
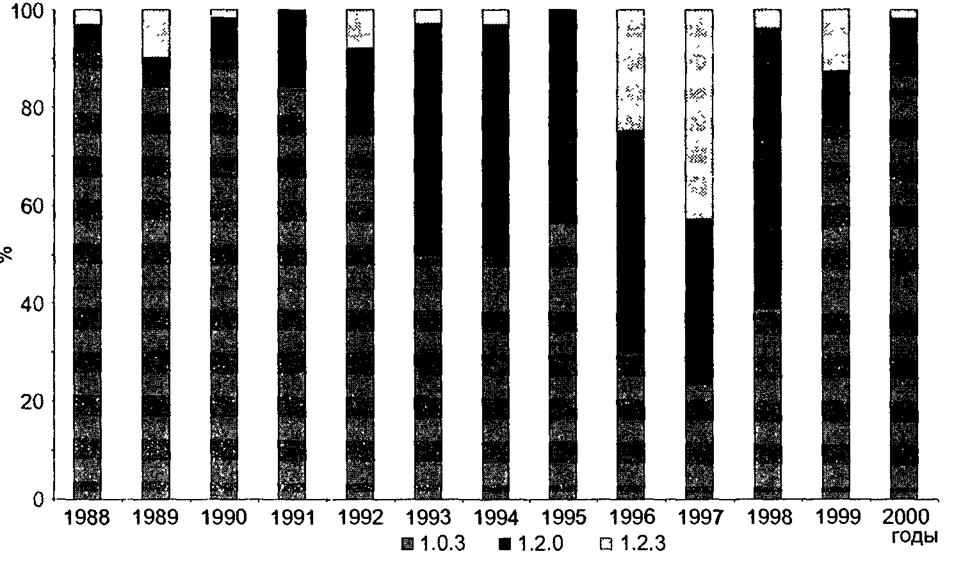 |
Рис. 17.14. Удельный вес различных серотипов возбудителя коклюша в Кировском районе Санкт-Петербурга в 1988-2000 гг.
В. pertussis продуцирует несколько биологически активных субстанций, играющих определенную роль в развитии болезни и формировании защиты от нее, — это филаментозный гемагглютинин, пертактин, трахеальный токсин, а также аденилатциклаза, которая подавляет вместе с токсином антибактериальные антитоксические функции нейтрофилов, моноцитов и естественных киллеров.
Возбудитель паракоклюша, по-видимому, также имеет значение в патологии, вызывая заболевания клинически сходные с коклюшем, однако в последние годы заболеваемость паракоклюшем значительно снизилась. Существует мнение, что В. parapertussis — это нетоксигенный вариант коклюшной палочки. Коклюшная палочка вне организма человека быстро погибает (действие ультрафиолетового облучения, кислорода воздуха и т, п.).
Механизм развития эпидемического процесса
Источник инфекции
Источниками инфекции являются больные клинически выраженными формами коклюша, больные стертыми формами и бактерионосители.
Коклюш характеризуется цикличностью течения. Выделяют инкубационный период длительностью от 3 до 14 дней (в среднем 7—8 дней), катаральный период — от 3 до 14 дней (в среднем 7—10 дней), период спаз
матического или судорожного кашля — от 2-3 до 6—8 нед и более и период реконвалесценции — 2—4 нед, иногда до 6 мес.
В катаральный период больной представляет наибольшую опасность для окружающих. В стадию судорожного кашля больной еще заразен, но чаще всего не более двух недель. Общая заразительность больного длится 4 нед, причем в конце этого срока опасность, исходящая от больного, уже невелика.
Наряду с ярко выраженными типичными формами инфекции встречаются легкие, атипичные формы болезни (абортивная и стертая) и бессимптомные формы — носительство (главным образом у взрослых, чаще у матерей больных детей и у работающих в детских дошкольных учреждениях — до 10% по отношению к больным).
Принимая во внимание неблагополучную эпидемическую ситуацию во многих регионах России, преобладание стертых форм инфекции среди больных, трудности клинического распознавания болезни в течение наиболее заразного периода, лабораторная диагностика является важным звеном в выявлении инфекции и системе противоэпидемических мероприятий. Таким образом, в современных условиях нельзя ориентироваться только на клиническую диагностику.
Механизм передачи
Возбудитель передается воздушно-капельным путем, причем заражение возможно только при непосредственном общении.
Восприимчивость
Различие восприимчивости населения обусловлено генетическими особенностями людей, характером формируемого иммунитета в результате прививок, а также особенностями в вирулентности возбудителя и величине заражающих доз. После перенесения коклюша в клинически выраженной форме развивается достаточно напряженный иммунитет, если в формировании его принимали участие все составные части коклюшного возбудителя, особенно типовые антигены. Но повторные случаи заболевания наблюдались даже в допрививочное время.
Проявления эпидемического процесса
Интенсивность
По данным ВОЗ, ежегодно в мире заболевают коклюшем 50 млн человек, умирает от него 0,5~1 млн человек. Заболевание распространено повсеместно, однако в разных странах и континентах уровень заболеваемости имеет существенные колебания. Даже в Европейском регионе выделяются 3 группы стран с разными уровнями заболеваемости (от единиц до 100 на 100 тыс. населения), которые зависят от национальных программ вакцинации и непосредственно связаны со степенью привитости населения.
В России в допрививочный период заболеваемость коклюшем составляла 400—800 на 100 тыс. населения и занимала 2-е место после кори. Коклюш был ведущим фактором смертности детей до 1 года.
Часть И. ЭПИДЕМИОЛОГИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИИ
После введения в широкую практику вакцинации наступило существенное снижение заболеваемости, затем ее уровень стабилизировался на показателях 10—20 и даже выше (в 1994 г. заболеваемость составила 32,9 на 100 тыс. населения). Этот средний уровень по стране складывается из весьма неодинаковых показателей на разных территориях, которые зависят от степени привитости детского населения. Так, в некоторых регионах заболеваемость коклюшем в 1994 г. составляла 100—140 на 100 тыс. населения. В 2001—2003 гг., вследствие энергично проведенных мероприятий по иммунизации детей, после подъема в 1994 г., заболеваемость коклюшем в стране снизилась до показателей 3,8—8,7 на 100 тыс. населения.
Динамика
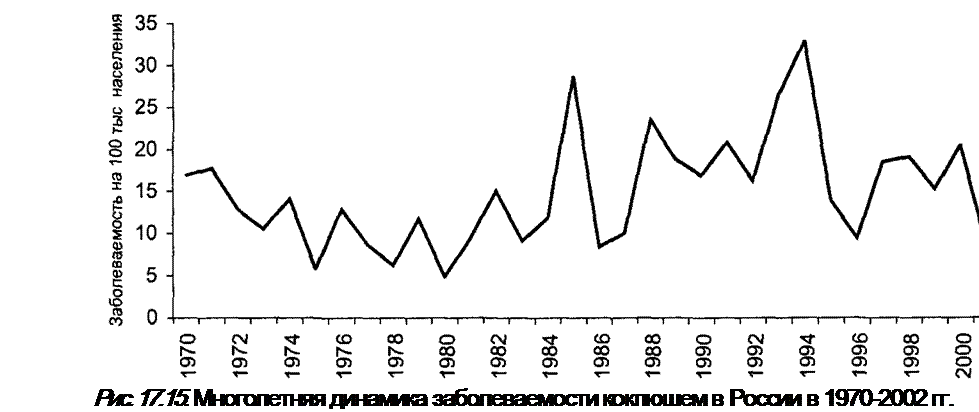
В многолетней динамике заболеваемости отмечается цикличность — чаще всего подъем заболеваемости наступает через 3—4 года (рис. 17.15).
Цикличность объясняется изменением вирулентности циркулирующих возбудителей, усиление которой неизбежно при возрастании частоты пассажей среди людей с повышенной восприимчивостью, вследствие высокого процента непривитых детей.
Сезонность при коклюше достаточно характерна, но имеет некоторые отличия от сезонности при других воздушно-капельных инфекциях. Подъем начинается уже летом — в июне-августе и достигает максимума в осенне-зимний период.
Структура
Эпидемическому процессу коклюшной инфекции свойственны выраженные различия в возрастной структуре заболеваемости. Максимальные уровни отмечаются у детей первого года жизни и 3—6 лет. В последние годы растет заболеваемость школьников и взрослых, у которых коклюш часто протекает в атипичной форме. С эпидемиологических позиций опасны заболевшие взрослые лица, работающие с детьми в детских дошкольных учреждениях, детских летних и зимних оздоровительных уч-
ЮЗак "846
реждениях, начальных классах школ, закрытых детских учреждениях, родильных домах, санаториях.
Многолетнее использование в практике здравоохранения АКДС-вак- цины в рамках календаря прививок привело к значительным изменениям в характере эпидемического процесса и клиническом течении этой инфекции. Коклюш стал протекать более легко, значительно снизилась заболеваемость, а также летальность и смертность. Однако начиная с середины 1980-х гг. в некоторых регионах России (см. рис. 17.15) имели место подъемы заболеваемости коклюшем с утяжелением клинических проявлений инфекции, формированием очагов с большим количеством случаев заболевания. Активизация эпидемического процесса определялась заболеваемостью непривитых детей 3~6 лет и младшего школьного возраста при высоком уровне заболеваемости детей первого года жизни.
Факторы риска
Основным фактором риска является недостаточная иммунологическая защищенность детей вследствие низкого охвата прививками, нарушения схемы и сроков вакцинации, широкого применения необоснованных медицинских отводов.
Эпидемиологический надзор
Эпидемиологический надзор предусматривает:
♦ Слежение за заболеваемостью коклюшем с выделением групп, территорий, времени и объектов риска.
♦ Оценку иммунологического статуса детского населения (постоянный контроль степени привитости детей, контроль за охватом прививками, изучение обоснованности медицинских отводов и т. д.). Не менее значимой является проблема разработки отечественных диагностических систем для качественной и количественной оценки противококлюш- ного иммунитета, так как используемые для этих целей реакция агглютинации и РПГА не дают адекватного представления о направленности антител к различным компонентам коклюшного микроба и о реальной протективной активности этих антител. Для этих целей перспективен метод иммуноферментного анализа (ИФА).
♦ Слежение за циркуляцией возбудителя коклюша среди населения. Применяется классический метод бактериологического исследования с выделением чистой культуры возбудителя, с использованием для получения материала заднеглоточного тампона. Однако в реальных условиях результативность бактериологического подтверждения у больных коклюшем не превышает 20—30%. Неудачи при выделении возбудителя обусловлены особенностями микроорганизма и его медленным ростом, сроками бактериологического обследования (лучшая высеваемость достигается при обследовании больных в течение первых двух недель от начала болезни), нарушением правил взятия материала, кратности обследования, сроков и условий доставки материала в лабо-
гэо
раторию, качества питательных сред и др. Учитывая изложенное выше, рекомендуются в качестве дополнительных методов:
• иммунофлюоресцентный — определение антигенов возбудителя в слизи с задней стенки глотки;
• латексной агглютинации — определение антигенов коклюшной палочки в слизи с задней стенки глотки;
• иммуноферментного анализа (ИФА) — определение антигенов
5. pertussis в слизи зева;
• молекулярный метод — ПЦР (полимеразная цепная реакция) — позволяющий определить минимальное количество возбудителя, в том числе в поздние сроки и на фоне антибактериальной терапии.
♦ Слежение за профилем протективных антигенов в вакцине и использование для производства вакцины штаммов с актуальным набором антигенов (прерогатива исследовательских центров).
Противоэпидемические и профилактические мероприятия
При возникновении заболеваний коклюшем больные дети подлежат изоляции из детских учреждений. Допуск в коллектив осуществляется после проведения курса этиотропной терапии. Остальные группы населения из числа больных изолируются по клиническим показаниям.
В отношении общавшихся с больным коклюшем детей до 7 лет предусмотрен карантин сроком на 14 дней. Контактные с больным дети до 7 лет, а также работники родильных домов, детских больниц, санаториев и воспитатели детских учреждений подлежат наблюдению и бактериологическому обследованию на коклюш.
В современных условиях профилактика коклюша обеспечивается активной иммунизацией. В России специфическая профилактика осуществляется с помощью ассоциированного препарата — адсорбированной коклюшно-дифтерийно-столбнячной (АКДС) вакцины. Прививки проводятся с трехмесячного возраста трехкратным введением препарата с интервалом 1,5 мес. В 18 мес проводится однократная ревакцинация.
Коклюшный компонент вакцины АКДС обладает достаточной реак- тогенностью; после прививок наблюдаются как местные, так и общие реакции. Зарегистрированы реакции неврологического характера, которые являются прямым следствием прививок. Данные обстоятельства привели к тому, что педиатры с большой осторожностью подходят к проведению прививок АКДС-вакциной, этим объясняется большое количество необоснованных медицинских отводов.
Реактогенность убитой вакцины привела к тому, что в некоторых странах (Япония, Швеция, Великобритания) вообще отказались от прививок, что сразу же привело к резкому подъему заболеваемости. В это же время в мире появилось много новых научных данных, значительно расширивших обшее представление о коклюшной инфекции и ее возбудителе, в частности о роли и значении отдельных антигенов в формировании защиты против коклюша. Была предложена концепция о ведущей роли
коклюшного токсина в патогенезе инфекции. Не последняя роль в формировании защиты против коклюша принадлежит филаментозному гем- агглютинину, агглютиногенам 2, 3, белку 69КДе (пертактину). В конце XX в. в разных точках земного шара (Австралия, Северная Америка, Западная Европа) зафиксирован рост заболеваемости коклюшем на фоне массового применения АКДС-вакцины, при этом выявлен дрейф протек- тивных антигенов В. pertussis (пертактина, S\ и субъединицы коклюшного токсина). По мнению специалистов, дрейф обусловлен влиянием поствакцинального иммунитета, а возникающие изменения протективных антигенов у новых штаммов столь существенны, что вакцины из «старых» штаммов оказываются не эффективными. В связи с этим необходимо постоянное слежение за циркулирующими штаммами.
Учитывая новую концепцию, сначала в Японии, а затем в США и Швеции была создана и введена бесклеточная коклюшная вакцина, на основе коклюшного токсина и новых факторов зашиты. В России также ведутся работы по созданию бесклеточной коклюшной вакцины.
Источник: Л. П. Зуева, Р. X. Яфаев, «ЭПИДЕМИОЛОГИЯ» 2005
А так же в разделе «17.2. Коклюш »
- Глава 16 ОБЩАЯ ХАРАКТЕРИСТИКА ИНФЕКЦИЙ С ФЕКАЛЬНО-ОРАЛЬНЫМ МЕХАНИЗМОМ ПЕРЕДАЧИ
- 16.1. Шигеллезы
- 16.2. Кишечные эшерихиозы
- 16.2. Брюшной тиф и паратифы А и В
- Холера
- 16.4. Ротавирусный гастроэнтерит
- 16.4. Полиомиелит
- 16.7. Энтеровирусные неполиомиелитные инфекции
- 16.4. Вирусный гепатит А (ВГА)
- 16.9. Вирусный гепатит Е
- 16.9. Протозойные кишечные инвазии
- 16.10.1. Амебиаз
- 16.10.2. Балантидиаз
- Криптоспоридиоз
- 16.10.3. Лямблиоз
- 16.9. Кишечные гельминтозы
- 16,12. Перкутанные гельминтозы
- Глава 17 ОБЩАЯ ХАРАКТЕРИСТИКА ИНФЕКЦИЙ С ВОЗДУШНО-КАПЕЛЬНЫМ МЕХАНИЗМОМ ПЕРЕДАЧИ
- 17.1. Дифтерия
- 17. 3. Стрептококковые инфекции (стрептококкоз)
- 17.4. Менингококковая инфекция
- 17.5. Туберкулез
- 17.5. Грипп и острые респираторные заболевания (ОРЗ)
- 17.6.1. Парагриппозная инфекция
- 17.6.2. RS-инфекция
- 17.6.3. Коронавирусные инфекции
- 17.6.5. Аденовирусная инфекция
- 17.6.6 Микоплазмоз
- 17.6.7. Грипп
- 17.5. Корь
- 17.8. Эпидемический паротит
- 17.9. Инфекция, вызываемая вирусом варицелла-зостер: ветряная оспа и опоясывающий лишай
- 17.10. Краснуха
- Глава 18 ОБЩАЯ ХАРАКТЕРИСТИКА ИНФЕКЦИЙ С КОНТАКТНЫМ МЕХАНИЗМОМ ПЕРЕДАЧИ
- 18.1. ВИЧ-инфекция — СПИД
- 18.2. Вирусные гепатиты с контактным механизмом передачи
- 18.2.1. Вирусный гепатит В
- 18.2.2. Дельта-гепатит
- 18.2.3. Вирусный гепатит С
- 18.2.4. Вирусный гепатитС
- 18. 2. 5. Другие (предполагаемые) вирусные гепатиты