ИКД используются для восстановления синусового ритма в случае развития ЖТ или ФЖ во время обычной жизненной активности пациентов (рисунки 132, 133, 134, таблица 53). Для восстановления синусового ритма используется антитахикардитическая электрокардиостимуляция и двухфазный электрический разряд, более эффективный и требующий меньшей энергии.
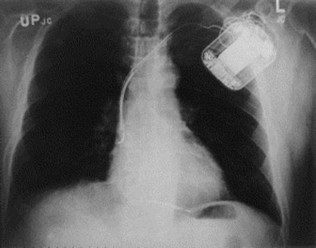
Рис. 132. Имплантируемый кардиовертер-дефибриллятор.
Для купирования реципрокной ЖТ используется электрокардиостимуляция, способная прекратить движение волны по кругу reentry. Низкоэнергетический разряд (1-5 дж) восстанавливает синусовый ритм в 8093% случаев ЖТ. При стойкой ЖТ и ФЖ может потребоваться высокоэнергетический разряд (29-37 дж). После прекращения ЖТ нередко развивается выраженная брадикардия, и в этой ситуации устройство работает как обычный ЭКС.
Рис. 133. Различные кардиовертеры-дефибрилляторы.
Основной режим работы выбирают во время имплантации устройства. Несколько раз вызывается и прерывается ЖТ и ФЖ. При ЖТ обычно используется ярусная терапия, при которой сначала аппарат дает несколько учащающих стимулов, при неудаче - низкоэнергетический разряд, а при повторной неудаче - высокоэнергетический разряд.

Рис. 134. Восстановление синусового ритма при ФЖ разрядом ИКД. ЭГвж - внутрижелудочковая электрограмма.
Таблица 53
Показания для ИКД-терапии (ACC/AHA/HRS, 2008; ВНОА, 2011)
I класс (доказана эффективность)
- После внезапной остановки кровообращения, развившейся вследствие ФЖ или ЖТ, если доказано что их причина не носила обратимый характер.
- Пациентам со структурной патологией сердца и спонтанной устойчивой ЖТ, как гемодинамически нестабильной, так и гемодинамически стабильной.
- Обмороки неясного генеза, которые клинически соответствуют гемо- динами-чески значимой ЖТ или ФЖ, индуцированными во время электрофизиологического исследования.
- Дисфункция левого желудочка (ФВЛЖ lt;35%) и сердечная недостаточность II-III ФК вследствие перенесенного gt;40 дней назад инфаркта миокарда.
- Неишемическая дилятационная кардиомиопатия, дисфункция левого желудочка (ФВЛЖ lt;35%) и сердечная недостаточность II-III ФК.
- Дисфункция левого желудочка (ФВЛЖ lt;30%) и сердечная недостаточность I ФК вследствие перенесенного gt;40 дней назад инфаркта миокарда.
- Неустойчивая ЖТ вследствие перенесенного инфаркта миокарда с дисфункцией левого желудочка (ФВЛЖ lt;40%) и индуцируемой устойчивой ЖТ или ФЖ при проведении электрофизиологического исследования.
11а класс (больше данных в пользу эффективности)
- Рецидивирующие устойчивые ЖТ вследствие инфаркта миокарда с нормальной функцией левого желудочка.
- Рецидивирующие устойчивые некоронарогенные ЖТ, когда их невозможно устранить радикально с помощью катетерной абляции.
- Обмороки неясного генеза, значимая дисфункция левого желудочка и дилятационная кардиомиопатия.
- Гипертрофическая кардиомиопатия при наличии одного или более факторов риска ВСС ( перенесенный эпизод остановки кровообращения, спонтанная устойчивая ЖТ, спонтанная неустойчивая ЖТ, ВСС в
семейном анамнезе, обмороки, толщина межжелудочковой перегородки более 30 мм , неадекватное изменение АД в ответ на нагрузку).
- Предупреждение ВСС у пациентов с аритмогенной дисплазией (кардиомиопатией) правого желудочка, при наличии одного или более факторов риска ВСС (перенесенная остановка кровообращения, ЖТ с потерей сознания, полиморфная ЖТ, доказанное выраженное поражение миокарда правого желудочка, аневризма правого желудочка, вовлечение в процесс левого желудочка).
- Предупреждение ВСС у пациентов с синдромом удлиненного интервала QT, при наличии ЖТ и/или обмороков, которые возникают несмотря на постоянный прием бета-блокаторов.
- Синдром Бругада с обмороками и/или ЖТ, при наличии документированного эпизода ЖТ.
- Катехоламинергическая полиморфная ЖТ, при наличии документированных эпизодов ЖТ, которые возникают несмотря на постоянный прием бета-блокаторов.
- Пациенты, ожидающие трансплантацию сердца вне клиники.
- Пациенты страдающие саркоидозом сердца, гигантоклеточным миокардитом, болезнью Чагаса.
Отметим, что наряду с ИКД, пациентам с высоким риском внезапной смерти дополнительно назначают антиаритмические препараты (амиода- рон, соталол, бета-блокаторы).
Если необходимо отключить ИКД, то можно поднести к устройству сильный магнит. В этом случае функция водителя ритма сохраняется.
Сильные электрические и магнитные поля способны воздействовать на работу кардиовертера-дефибриллятора. Пациентам рекомендуется находиться на расстоянии gt;30 см от стереоприемников, магнитных пропускников в аэропорту, инструментов с батарейками без шнура (дрели, отвертки), генераторы. Сотовые телефоны не нужно подносить к устройству ближе, чем на 15 см.
Во время операции при электрокоагуляции индифферентный электрод нужно стараться держать как можно дальше от кардиовертера- дефибриллятора. Диатермию проводят на максимальном удалении от устройства. Во время радиотерапии устройство следует защитить. Пока недостаточно информации относительно риска при литотрипсии. Противопоказана магнито-резонансная томография.
Госпитальная летальность при неторакотомической имплантации кардиовертера-дефибриллятора составляет 0,2%, а торакотомической и неторакотомической имплантации - 2,7%, и обусловлена в основном тяжестью заболевания сердца (van Rees J.B., et al., 2011). Частота пери- операционных осложнений по данным National ICD Registry за 2006-2008 годы составила 3,4% (Hammill S.C., et al., 2009). В большинстве случаев отмечали дислокацию электрода (1,1%), гематому (1,0%) и ге- мо/пневоторакс (0,6%). Среди катастрофических осложнений зарегистрированы смерть в лаборатории (0,02%), перфорация сердца (0,08%) и транзиторная ишемическая атака (0,06%). В последние годы возрастает частота инфекции, связанной с имплантируемыми электрическими
устройствами - с 1,5% в 2004 году до 2,4% в 2008 году (Greenspon A.J., et al., 2011).
По данным базы данных ИКД в Онтарио большие осложнения после имплантации устройства встречались у 3,8% пациентов, которым проводилась первичная профилактика аритмогенной смерти, и у 4,8% - в случаях вторичной профилактики (Lee D.S., et al., 2010). Только малая часть осложнений (0,8%) развивалась в госпитале. Регистрировали механические (дислокация электрода, перфорация сердца, пневмо/гемоторакс, инфекция, гематома, расслоение коронарной вены, стимуляция диафрагмы) или клинические (отек легких, гипотензия, инсульт, смерть) осложнения.
Разработанные модели двухкамерных ИКД показали более высокий уровень госпитальной летальности (+45%) и осложнений (+40%), по сравнению с традиционными однокамерными моделями (Dewland T.A., et al., 2011).
Стоимость аппарата составляет около 700000-900000 рублей, что значительно ограничивает широту применения этого устройства. Срок службы ИКД зависит от частоты разрядов, зависимости от ЭКС, других программируемых режимов и обычно составляет 5-9 лет.
Первичная профилактика
При разработке превентивных мероприятий выделяют методы первичной профилактики внезапной аритмической смерти у пациентов без анамнеза жизнеопасных желудочковых аритмий, и методы вторичной профилактики для пациентов, перенесших остановку сердца или ЖТ сочетавшуюся с обмороком или артериальной гипотензией.
